胰腺疾病相关消化不良的诊治
王晓乙, 傅德良
复旦大学附属华山医院胰腺外科, 上海 200040
胰腺是仅次于肝脏的人体第二大外分泌器官,兼具有内、外分泌两大功能[1]。胰腺的内分泌功能表现为通过胰岛内的A 细胞、B 细胞、D 细胞和PP 细胞发挥调节糖代谢的作用[2];胰腺的外分泌功能表现为由胰酶介导的消化功能。胰腺的外分泌部占胰腺的80%~85%,由腺泡、导管和间质3 个部分组成,其中腺泡是合成、储存和分泌胰酶的部位,导管的主要功能是分泌水和电解质,也是输送胰液的通道。胰腺分泌人体所需90%以上的消化酶和100%的脂肪酶,因此胰腺外分泌功能不全(pancreatic exocrine insufficiency,PEI)是胰腺疾病相关消化不良的主要原因[3-4]。
1 PEI相关消化不良的病因
1.1 PEI与消化不良 消化不良是指一组表现为上腹部疼痛或烧灼感、餐后上腹饱胀和早饱感的综合征,可伴食欲不振、嗳气、恶心或呕吐等。消化不良经常被临床医师和患者自身忽略,全球范围内未被临床诊断的消化不良患者约占20.8%(95%CI:17.8%~23.9%)[5]。
正常的消化需要经过完整的物理性消化和由消化酶介导的化学性消化,因此消化不良从病因上被分为器质性(机械性)消化不良和功能性(化学性)消化不良[6]。消化不良症状的产生与胃肠疾病有关,也可由胰、胆、肝脏疾病等引起。PEI是指由于各种原因引起的胰酶分泌量绝对下降,或胰酶激活环境改变造成胰酶不完全激活而导致胰酶相对不足,进而引起消化系统异常的疾病[7]。各种胰腺疾病均可引起PEI,是导致化学性消化不良的主要原因。
1.2 PEI的病理生理机制及发生率
任何胰腺疾病以及对胰腺疾病的治疗干预均可能导致胰酶绝对分泌量下降或是胰酶分泌不同步,常见于胰腺实质细胞损伤(慢性胰腺炎)、胰管阻塞(胰腺、十二指肠肿瘤)、胰腺分泌刺激降低(乳糜泻/麸质过敏)[8]以及胃肠道pH值改变导致胰酶不完全激活/失活(胰腺术后)[9-10]。临床上,PEI的发病机制可能由以上一种或多种因素造成。
1.2.1 慢性胰腺炎 慢性胰腺炎是PEI的主要病因,其病理改变为胰腺实质腺泡发生不可逆损伤。据统计[7],慢性胰腺炎患者确诊时的PEI发病率约为36%,5年后约为60%;晚期患者PEI发生率为100%。
1.2.2 急性胰腺炎 急性胰腺炎发生水肿渗出时,可见胰酶分泌量下降合并有组织水肿造成的胰管堵塞。重症坏死性胰腺炎伴有大面积胰腺组织坏死,可能造成胰腺功能永久性损伤,进而导致不可逆的PEI[11]。
1.2.3 胰腺肿瘤及胰腺术后状态 无论良、恶性胰腺肿瘤均可能导致PEI,其机制在于胰腺肿瘤占位效应引起的胰腺分泌量减少以及肿瘤阻塞胰管引起的胰酶流出梗阻;胰腺恶性肿瘤还可能合并慢性胰腺炎,进一步影响胰腺实质功能。临床上,胰头肿瘤确诊时的PEI 发病率约为66%,2 个月后超过90%[3,12]。PEI 为胰腺肿瘤术后的常见并发症,其发生率与肿瘤良恶性和手术方式相关,发病原因在于胰腺体积减小,胰酶分泌量下降;消化道重建后,胃肠道pH 值下降导致胰酶激活不同步/不完全激活。因此,术后剩余胰腺体积大,残余胰腺功能好,则PEI 发病率低。PEI发生率在全胰切除术后为100%,胰十二指肠切除术后为73%,胰体尾切除术后为10%~42%,胰腺中段切除术后为10%[13-14]。
1.2.4 糖尿病 糖尿病与胰腺内外分泌功能在解剖和生理上相互关联、影响。糖尿病患者可见胰腺形态、组织学和功能改变。PEI 发生率在1 型糖尿病患者中约为40%,在2型糖尿病患者中约为27%。我国成年人总糖尿病患病率和糖尿病前期患病率分别为9.7%和15.5%,糖尿病相关PEI患者超过1 000万,但糖尿病相关PEI引起的消化不良在临床上却极易被忽视[4,15]。
1.3 PEI的临床表现及危害 PEI的临床表现主要由碳水化合物、蛋白质和脂肪三大营养物质的不完全消化吸收所引发:碳水化合物不完全消化,食物残渣被胃肠道内细菌分解,产生过多肠道气体,造成腹胀(92.7%)、腹痛(71.7%)、胀气(91.1%);蛋白质与脂肪不完全消化可导致脂肪泻(52.4%)。消化不良可导致营养不良、体质量下降、脂溶性维生素吸收障碍并缺乏等严重临床后果,易增加围手术期并发症风险,降低患者生活质量,降低恶性肿瘤患者的治疗耐受性,最终影响患者生存期[7,16-20](图1)。
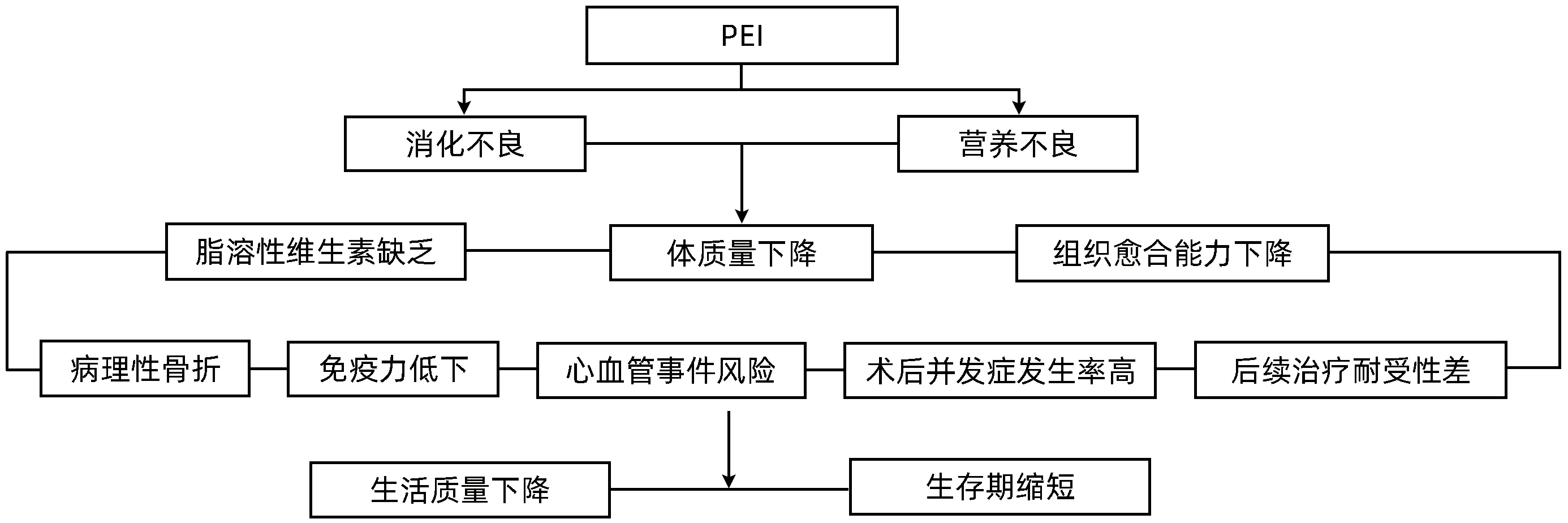
图1 PEI的临床危害Figure 1 Clinical outcome of PEI
2 PEI的诊断
临床上,胰腺相关疾病引发的消化不良大多存在PEI。相反的,胰腺具有代偿功能,仅有部分PEI 患者可见明显的消化不良症状。早期PEI 可无任何临床表现,当胰腺分泌脂肪酶降至正常水平的10%以下时才出现脂肪泻[4]。因此,不能将临床症状(如脂肪泻)作为PEI的诊断依据。
目前,诊断PEI 的实验室检查主要为胰腺外分泌功能检测,以明确是否存在胰液分泌量减少。胰腺外分泌功能测定包括直接检测和间接检测。直接检测为胆囊收缩素激发试验,需行内镜逆行胰胆管造影,直接收集胰管中的胰液,操作复杂且有创,目前已基本不在临床使用[21]。超声内镜检查可一定程度上提供形态学判断依据[22]。间接检测主要包括脂肪吸收系数(coefficient of fat absorption,CFA)测定、粪弹性蛋白酶检测和13C-MTG 呼吸试验,前者同样也是诊断脂肪消化不良的“金标准”。CFA检测要求患者在5天内严格控制饮食(每天进食含100 g脂肪的饮食),在最后3天收集排泄的所有粪便,并在72 h 粪便脂肪定量分析的基础上计算出CFA。年龄>6个月的患者,排泄脂肪>摄入脂肪的7%即为阳性。但该方法受限于患者依从性因素,较难实施[7];粪弹性蛋白酶检测较为简便,仅需1次大便样本,正常值为>200 µg/g[23];13C-MTG呼吸试验无须粪便标本,检测方法是将250 mg 的13C-MTG 掺入含有16 g 脂肪的固态试验餐中,受试者服下后脂肪由胰酶水解,释放出13C 标记的底物,经肝代谢释放出13CO2并随呼出气排出体外,收集并分析呼气样本,重收集率<29%表示存在脂肪消化不良,该方法在慢性胰腺炎中检测脂肪消化不良的敏感度和特异度均>90%[7,24-25]。然而,13C-MTG 呼吸试验目前仅在少数实验室开展。
临床上更常用的诊断指标为反映营养状态的血生化指标,如血清白蛋白、总蛋白、微量元素等。此外,胰酶替代治疗(pancreatic enzyme replacement therapy,PERT)有效即可证实PEI相关消化不良的存在[4]。
3 胰腺相关消化不良的治疗
对于胰腺疾病引起的消化不良,首要治疗原则为祛除病因。对于急性胰腺炎,应积极控制炎症,尽可能减少胰腺组织坏死面积;对于慢性胰腺炎,虽然胰腺实质已存在不可逆的病理变化,但仍需积极去除高危因素(如长期饮酒),以延缓疾病进程。对于已明确存在PEI 的患者,尤其是胰腺术后PEI 患者,PERT 是首选治疗方法。
PERT 的原则为早期、及时、长期、足量[25]。治疗时机为确诊或怀疑PEI 时即开始治疗通过在进食时补充胰酶,帮助营养物质消化,以改善患者消化道症状、提高生活质量、纠正营养不良。为提高胰酶的效价,必须随餐服用,使胰酶与食糜充分混合。各大指南[4,23,25]的推荐剂量略有差别,原则上推荐的起始剂量为25 000~40 000 PhU 脂肪酶/正餐,且可以根据实际情况逐渐加量,最大剂量为75 000~120 000 PhU脂肪酶/正餐。胰酶摄入量不足可导致症状持续存在,使患者依从性降低。足量、长期PERT 不仅可以改善症状,提高患者生活质量[26],还能够提高胰腺癌患者对标准治疗的耐受性,延长总生存期[24]。
既往观念认为PEI 患者需要限制脂肪的摄入,但考虑到胰腺具有代偿功能,通过限制饮食改善脂肪泻可能会掩盖营养不良的存在,当前的认识正逐步转变为不限制饮食并足量补充胰酶。对于消化道重建后胃肠道pH 下降的患者,可应用胰酶联合质子泵抑制剂,以提高胰酶的效用[7]。
4 小结
目前,聚焦于胰腺疾病相关消化不良的学术讨论尚少,《临床肝胆病杂志》2024 年第12 期“胰腺病相关消化不良诊治”重点号专刊将着眼于慢性胰腺炎、胰腺肿瘤、胰腺术后相关消化不良的诊断和治疗等方面开展深入总结及阐述,以期进一步加强对胰腺疾病相关消化不良的认识,提升其临床诊断和治疗率。
利益冲突声明:本文不存在任何利益冲突。
作者贡献声明:王晓乙负责查阅文献,撰写论文;傅德良负责拟定文章思路,修改并最终定稿。

