团簇MMoS4(M=Ni、Co、Fe)催化性质密度泛函研究
宋 嘉 方志刚 王智瑶 宋静丽 吴庭慧
(辽宁科技大学化学工程学院, 鞍山 114051)
引 言
近年来,随着化石原料的不断开采和大量利用,环境污染、能源短缺等问题日益受到人们关注,因此迫切需要找到一种清洁、绿色、来源丰富的可替代能源。 氢作为一种产热高、原料丰富、绿色环保的清洁能源[1-2],可用于替代不可再生能源。 在工业生产中,氢气的制备需要催化剂的参与[3],贵金属催化剂具有高效的催化性能,但其价格高昂、资源短缺,不能满足实际生产的需要。 MMoS4(M=Ni、Co、Fe)作为非晶态合金类催化剂具有短程有序、长程无序等特点,相较于贵金属催化剂,其价格低廉、容易获取、性能优异,在电子材料[4]、催化剂[5]、生物医学[6]、能源[7]等领域具有广阔的应用前景。
MMoS4体系是非晶态合金应用于催化材料的热门体系,已有较多学者对其催化性能进行了研究[8-17]。 Leyral 等[8]研究了离子液体的存在和用量对NiMoS 催化性能的影响,结果表明,在离子液体存在下制备的NiMoS 催化剂具有更高的催化活性和对碳氢化合物更大的选择性,在n(NiMoS)∶n(离子液体) =1∶100 下制备的催化剂的活性是在n(NiMoS)∶n(离子液体) =1∶0下制备的催化剂的3 倍。 Wang 等[9]通过水热法和简单的硫化工艺,在Ti 网格上合成了新型的分层珊瑚状Ni-Mo硫化物(HC-NiMoS/Ti)双功能催化剂,这种催化剂在多组分反应中具有良好的协同效应,展现出优异的催化活性和很强的稳定性。 Lee 等[10]利用两步水热法制备了多孔NiMoSx包裹的Zn-Ni 层状双氢氧化物(Zn-Ni LDH@NiMoSx),这是一种具有纳米结构的超级电容器,其独特的结构具有许多优点,如高导电性、快速电子转移性和优异的氧化还原反应性。 Liang 等[11]提出了一种通过结晶多金属氧酸酯(POM)前驱体来研究加氢脱硫(HDS)催化剂活性相形成机制的新方法,POM 前驱体在硫化过程中对NiMoS 活性相结构具有结构导向效应(structure-directing effects),该效应使得NiMoS 活性相的含量更高,分散性更好,为合理设计和可控制备高性能的NiMoS 催化剂提供了思路。 Li 等[12]采用浸渍法制备了不同原子数比的CoMoS/ZrO2催化剂,在实验中发现当Co 与Mo 的原子数比为0.3 时,加氢脱氧反应的活性最高。Ren 等[15]通过水热法合成了非晶态FeMoS4纳米棒催化剂,该催化剂表现出优异的催化活性和强大的长期电化学耐久性。 目前,对MMoS4体系的研究主要集中在宏观实验方面,而缺少从微观角度进行的研究。 团簇是通过一定作用力组成的相对稳定的微观聚集体,团簇模型研究方法的主要特点在于采用局域化的原子基团模型模拟整个晶体,是在微观层面上研究非晶态材料性质的有效方法。本文以密度泛函理论为基础,利用活性能级差、费米能级、态密度、能量最高占据轨道(HOMO)和能量最低未占据轨道(LUMO)以及库普曼斯定理对团簇MMoS4进行了微观理论分析,研究了其得失电子能力、亲电指数、电负性和催化活性等性质,本文的结果可以为相关研究提供理论参考。
1 模型设计与计算方法
采用Gaussian 09 程序[18],依据密度泛函理论[19],参考本课题组之前的研究方法[20-25]设计出团簇MMoS4在一、二、三、四重态下的36 种初始构型,并采用B3LYP 和def2tzvp 基组对团簇MMoS4的所有初始构型进行全参数优化计算,最大作用力小于0.000 45,均方根作用力小于0.000 30,最大位移小于0.001 80,均方根位移小于0.001 20,对S 加极化函数。 以上所有的运行及计算均在计算机HPZ440 上完成。
2 结果与讨论
2.1 团簇MMoS4的稳定构型
本文设计的团簇MMoS4的初始构型主要为平面型、四角双锥型以及五棱锥型这3 种构型,通过改变不同原子的相对位置,最终确定了36 种可能存在的构型。 在排除相同构型和因虚频而不能稳定存在的构型后,最终得到8 种稳定构型,其中四重态构型1 种、三重态构型3 种,一、二重态构型各2 种。 以能量最低的构型作为基准(0 kJ/mol),依据相对能量的高低,分别对NiMoS4、CoMoS4和FeMoS4这3 种体系的稳定构型进行排序,结果如图1 所示,其中上角标括号内的数字代表重态,构型后括号内的数字表示相对能量。
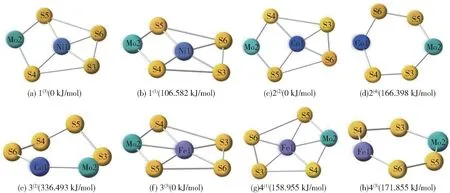
图1 团簇MMoS4的优化构型图Fig.1 Optimized configuration diagrams of the MMoS4 cluster
由图1 可以看出,团簇MMoS4的稳定构型有平面型和类平面型两种,平面型为主要构型。 其中,构型2(4)、4(3)为平面六边形,构型1(3)、1(1)、2(2)、3(3)、4(1)为中心带一个原子的平面五边形,只有构型3(2)为类平面型。 不难看出,大部分构型在优化后都以平面型存在,说明平面型更为稳定。
2.2 团簇MMoS4的活性能级差、费米能级、态密度图
能级差(Egap)表示金属在超导态时基态与最低激发态之间的能量差,可以用HOMO 能级(EHOMO)与LUMO 能级(ELUMO)的差值来表示(Egap=ELUMO-EHOMO)。 物质的能级差越大,电子从占据轨道向空轨道的跃迁能力越小,物质的活性越小;能级差越小,电子从占据轨道向空轨道的跃迁能力越大,物质的活性就越大。 团簇MMoS4各稳定构型的能级差列在表1 中。 可以看出:在团簇NiMoS4中,构型1(1)的能级差较小(74.455 kJ/mol),构型1(3)的能级差较大(115.040 kJ/mol),说明构型1(1)的催化性能较好;在团簇CoMoS4中,构型2(4)的能级差最小(120.078 kJ/mol),构型3(2)的能级差最大(221.056 kJ/mol),说明在构型2(2)、2(4)、3(2)中构型2(4)的催化性能最好;在团簇FeMoS4中,构型4(3)的能级差最小(145.289 kJ/mol),说明在构型3(3)、4(1)、4(3)中4(3)的催化性能最好。 从整体上可以看出,在这8 种稳定构型中团簇NiMoS4的构型1(1)的能级差最小,催化性能最优;团簇NiMoS4的能级差小于团簇CoMoS4和FeMoS4的能级差,表明其具有较好的催化性能。
费米能级(EFermi)也可以表示物质催化性能的大小,其计算式为:EFermi=(EHOMO+ELUMO)/2,计算得到的团簇MMoS4各稳定构型的费米能级列于表1中。 本文采用Multiwfn 软件计算了团簇MMoS4各稳定构型的态密度,并将得到的态密度绘制成态密度曲线,结果如图2 所示,其中虚线部分表示费米能级。 态密度可以反映电子云密度,分析费米能级周围的电子云密度大小,可以看出各构型催化活性的强弱,电子云密度越小,构型的催化活性越弱。 费米能级右侧电子云密度的分布情况可以反映物质接受电子的能力,费米能级左侧电子云密度的分布情况可以反映物质提供电子的能力。 费米能级两侧最高峰距费米能级的直线距离可以反映物质得失电子的能力:费米能级左侧最高峰距费米能级的距离小于右侧最高峰距费米能级的距离,说明在催化反应中物质具有较强的提供电子能力,反之具有较强的接受电子能力。 无论是接受电子能力还是提供电子能力,都可以反映物质催化活性的大小。

图2 团簇MMoS4各稳定构型的态密度图Fig.2 State density diagrams for the stable configurations of the MMoS4 cluster
由图2 可以观察到,在团簇NiMoS4、CoMoS4和FeMoS4中,费米能级左侧最高峰距费米能级的直线距离都小于右侧最高峰距费米能级的直线距离,表明这3 种团簇的各稳定构型在化学反应中均具有很好的提供电子能力。 进一步观察可以看出,构型3(2)和4(3)的左侧最高峰距费米能级的距离小于右侧最高峰距费米能级的距离更加明显,表明这两种构型的提供电子能力优于其他6 种构型。 还可以发现,这8 种稳定构型的右侧电子云密度明显大于左侧电子云密度,左侧峰的面积远远小于右侧峰的面积,并且这些稳定构型的最高峰均在费米能级的右侧,说明费米能级右侧的峰对催化活性也有一定的影响,团簇MMoS4也具有较强的接受电子能力。 整体来看,团簇MMoS4具有一定的接受电子和提供电子能力,说明其具有一定强度的催化活性。
2.3 团簇MMoS4的HOMO 图和LUMO 图
前线轨道的HOMO 图和LUMO 图可以用于判断物质得失电子的能力,也可以作为判断物质反应活性的依据。 图3 为团簇MMoS4各稳定构型的HOMO图与LUMO 图,其中黑色区域面积代表轨道波函数的负相位,白色区域面积代表轨道波函数的正相位,HOMO 图的面积大小表示构型提供电子的能力,LUMO 图的面积大小表示构型接受电子的能力。 由图3 可以看到,每个稳定构型的HOMO 和LUMO 轨道中各原子附近都存在不规则区域,电子在该区域出现时其波函数形成离域空间,离域空间中电子出现的概率越大,电子的流动越剧烈,物质的化学活性与此相关。 总体上看,在团簇MMoS4中8 种稳定构型的HOMO 图与LUMO 图的面积相差较小,说明团簇MMoS4的提供电子能力与接受电子能力相当。

图3 团簇MMoS4各稳定构型的HOMO 图和LUMO 图Fig.3 HOMO and LUMO diagrams for the stable configurations of the MMoS4 cluster
此外还可以看出,团簇NiMoS4的构型1(3)、1(1)的HOMO 图和LUMO 图的面积略大于其他构型,每个原子形成的轨道波函数正相位与负相位重叠的面积也较大,说明这两种构型的得失电子能力强于其他构型,其催化活性也更高。 构型4(3)的LUMO 图的面积略小于其他构型,原子周围出现电子的概率也略小,说明其接受电子的能力弱于其他构型。 整体上看,在NiMoS4、CoMoS4和FeMoS4中团簇NiMoS4的催化性能相对较好。
2.4 团簇MMoS4活性的库普曼斯定理分析
物质催化活性的大小可以通过电离势(EI)、电子亲和能(EEA)、电负性(χ)和亲电指数(ω)来判断。 电离势越小,物质的化学反应活性越好;电子亲和能越小,物质的化学反应活性越差;电负性表示物质在反应中提供电子的能力,电负性越大,物质的催化活性越好;亲电指数表示物质在化学反应中得到电子的能力,与电负性类似,亲电指数越大,物质的催化活性越好。 依据库普曼斯定理[26],可以得到这4 个物理量的计算公式。
表2 为团簇MMoS4各稳定构型的EI、EEA、χ和ω计算结果。 在团簇NiMoS4的构型1(3)和1(1)中,ω、EI、EEA、χ的最大值与最小值的差值(极值差)分别为708.865、46.41、5.824、26.117 kJ/mol,其中亲电指数ω的极值差最大,远大于其他3 个物理量的极值差; 在团簇 CoMoS4中,ω的极值差最大(753.579 kJ/mol),远大于其他3 个物理量的极值差;同样,在团簇FeMoS4中,ω的极值差最大(162.188 kJ/mol),远大于其他3 个物理量的极值差。 上述结果表明,亲电指数ω对物质的催化活性有较大影响。 总体上看,构型1(1)的亲电指数ω远大于其他构型,虽然构型1(1)的电负性χ不是最大,但是与其他构型的电负性相差较小。 因此综合来看,相比其他构型,团簇NiMoS4的构型1(1)具有较好的得失电子能力和催化性能,这与前文通过能级差、HOMO 图和LUMO 图得到的结论是一致的。
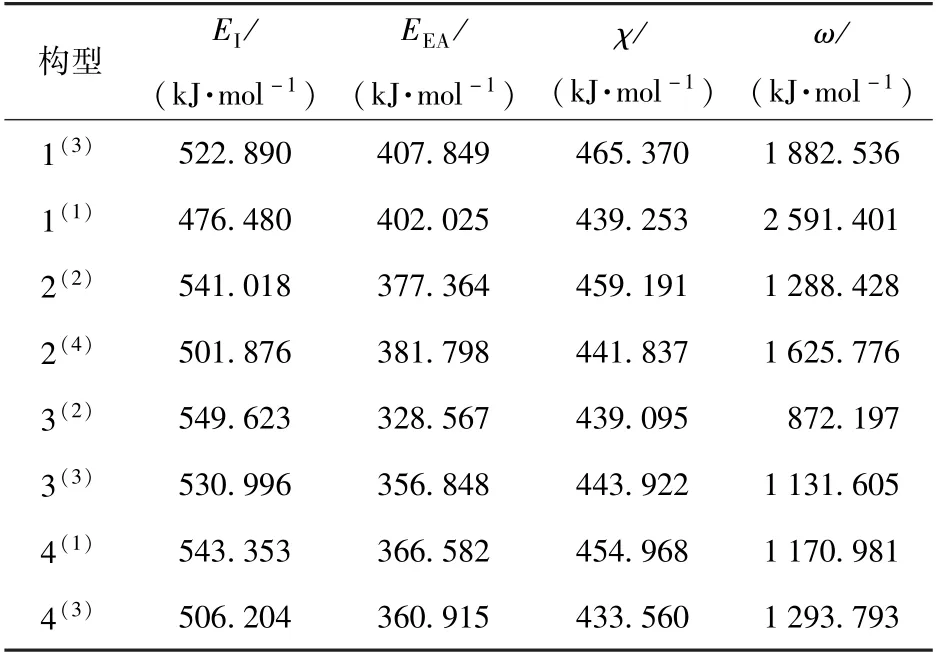
表2 团簇MMoS4各稳定构型的反应活性参数Table 2 Reactivity parameters of the stable configurations of the MMoS4 cluster
3 结论
通过能级差和库普曼斯定理分析得出,在团簇MMoS4中,NiMoS4的构型1(1)的能级差最小,亲电指数最大,说明构型1(1)具有比其他构型更好的得失电子能力和更强的催化活性。 通过对HOMO 图、LUMO 图以及态密度图分析可得,团簇MMoS4的接受电子和提供电子的强度相当,说明其具有一定强度的催化活性,并且团簇NiMoS4的催化性能略好于团簇CoMoS4和FeMoS4。

