鼻咽癌同步放化疗患者发生营养不良的相关影响因素
江琴,鲁卉,符楚楚,李艳婷(通信作者)
1 江西省肿瘤医院 (江西南昌 330029); 2 南昌大学第一附属医院 (江西南昌 330006)
鼻咽癌(naso pharyngeal carcinoma,NPC)作为临床常见的头颈部恶性肿瘤,其病因涉及人类疱疹病毒4 型感染、遗传等多因素,具有起病隐匿的特点,大部分患者就诊时肿瘤已发展至中晚期[1]。目前,临床多采用同步放化疗治疗NPC,以杀伤肿瘤细胞,预防肿瘤远处转移,提高患者生存率[2]。但放化疗不良反应易引发消化道症状、损伤患者口腔黏膜,从而影响进食,以及肿瘤细胞增殖会消耗营养物质,从而导致患者发生营养不良[3]。而机体营养不良会影响组织修复能力,降低免疫功能,增加感染风险,并影响放化疗耐受性,降低整体治疗效果,从而导致患者预后不良[4]。相关研究指出,20%~50%的肿瘤患者预后不良与机体营养状况有关[5]。基于此,本研究旨在分析NPC 同步放化疗患者发生营养不良的相关影响因素,为临床制定护理方案提供参考依据,现报道如下。
1 资料与方法
1.1 一般资料
选取2022 年1 月至2023 年2 月我院收治的107 例NPC 同步放化疗患者为研究对象。
纳入标准:NPC 符合相关诊断标准[6],且经病理组织活检确诊;年龄≥18 岁;卡氏评分≥70 分,体力状况评分<2 分;行同步放化疗治疗;预期生存时间≥1 年。排除标准:肿瘤远处转移;合并胃肠道疾病;合并感染性疾病;合并营养代谢障碍或吸收障碍性疾病;合并脏器原发性病变;合并其他部位恶性肿瘤;入组前6 个月接受营养支持治疗;精神、视听障碍,交流异常;处于哺乳期或妊娠期。
本研究经医院医学伦理委员会批准,患者及家属均签署知情同意书。
1.2 方法
(1)资料收集:设计一般资料调查表,包括患者性别(男、女)、年龄(<60 岁、≥60 岁)、肿瘤分期(Ⅰ~Ⅱ期、Ⅲ~Ⅳ期)、肿瘤位置(侧壁、后上壁、下壁)、消化道症状(≤3 个、>3 个)、手术治疗(是、否)、味觉障碍(是、否)、合并基础疾病(糖尿病、慢性阻塞性肺疾病、高血压、高脂血症等)、焦虑抑郁[采用医院焦虑抑郁量表(hospital anxiety and depression,HAD)[7]评 估,量表内容包括焦虑情绪、抑郁情绪2 项,均包括7 个条目,每个条目0~3 分,评分越高表明焦虑、抑郁情绪越严重;其中任意1 项评分>7 分,则判定为焦虑抑郁]、疲乏程度[采用piper 疲乏调查量表[8]评价,共计22 个条目,每个条目0~10 分,总分0~220 分,评分越高表明疲乏程度越高;评分轻度<88 分,88~132 分,重度>132 分]。(2)营养不良评估:采用主观整体营养状况评估量表 (patient-generated subjective global assessment,PG-SGA)[9]评估,量表内容包括体质量丢失、症状表现、活动与身体功能、摄食情况、代谢需要、疾病与营养需求的关系、体格检查7 项,其中前4 项由患者自评,其他项由护理人员评价,评分越高表明营养状况越差。根据PG-SGA 评分,营养状况可分为良好(0~1 分)、疑似营养不良(2~3 分)、中度营养不良(4~8 分)、重度营养不良(≥9 分),参照既往研究,将PG-SGA 得分≥4 分判定为发生营养不良[10]。
1.3 观察指标
比较发生营养不良、未发生NPC 同步放化疗患者的相关资料,经Logistic回归分析NPC 同步放化疗患者发生营养不良的相关影响因素。
1.4 统计学处理
采用SPSS 23.0 统计软件进行数据分析。计量资料以±s表示,采用t检验。计数资料以率表示,采用χ2检验。采用Logistic回归分析探讨NPC同步放化疗患者发生营养不良的相关影响因素。P<0.05 为差异有统计学意义。
2 结果
2.1 NPC 同步放化疗患者发生营养不良情况
107 例NPC 同步放化疗患者中52 例发生营养不良,发生率为48.60%。
2.2 NPC 同步放化疗患者发生营养不良的单因素分析
单因素分析显示,发生、未发生营养不良的NPC 同步放化疗患者肿瘤分期、消化道症状、味觉障碍、焦虑抑郁、疲乏程度比较,差异有统计学意义(P<0.05);发生、未发生营养不良的NPC 同步放化疗患者其他资料比较,差异无统计学意义(P>0.05),见表1。
2.3 NPC 同步放化疗患者发生营养不良的影响因素Logistic 回归分析
将经单因素分析差异有统计学意义的变量作为自变量(见表2),将NPC 同步放化疗患者发生营养不良状况作为因变量(发生=1,未发生=0),经Logistic回归分析显示,肿瘤分期Ⅲ~Ⅳ期、消化道症状>3 个、味觉障碍、焦虑抑郁、中重度疲乏是NPC 同步放化疗患者发生营养不良的影响因素(OR>1,P<0.05),见表3。

表2 自变量说明
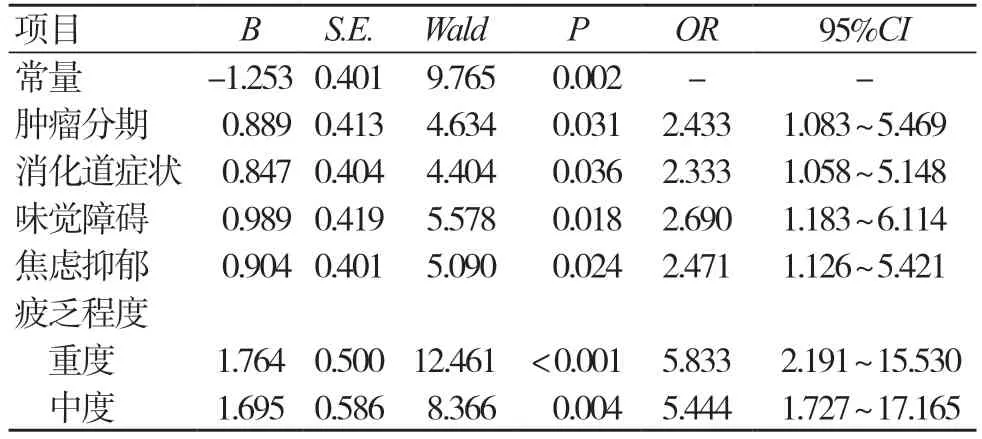
表3 NPC 同步放化疗患者发生营养不良的影响因素Logistic 回归分析
3 讨论
同步放化疗作为NPC 患者的主要治疗方案之一,其疗效确切,可提高局部肿瘤控制率,减少肿瘤转移风险,但易引发恶心呕吐、味觉下降等不良反应,导致患者进食减少,发生营养不良[11]。而NPC 患者发生营养不良会降低放化疗耐受性,影响预后。调查显示,肿瘤患者营养不良发生率约30%~80%[12]。本研究结果显示,107 例NPC 同步放化疗患者中48.60%发生营养不良,与上述研究结果相近,提示临床应积极采取干预措施,以改善患者的营养状况。
本研究经Logistic回归分析显示,肿瘤分期Ⅲ~Ⅳ期、消化道症状>3 个、味觉障碍、焦虑抑郁、中重度疲乏是NPC 同步放化疗患者发生营养不良的影响因素,分析原因如下。(1)肿瘤分期:晚期肿瘤患者机体肿瘤细胞数量较多,细胞增殖时消耗机体大量营养物质,日常营养物质、能量需求较高,同时患者体内炎性因子较多,加速蛋白质降解,造成肌瘤质量丢失,导致患者食欲减退,从而增加营养不良发生的风险[13]。(2)消化道症状:约70%以上的放化疗患者多伴有恶心、食欲不振等消化道症状,直接导致患者进食量减少,引发机体电解质失衡,体质量下降,并影响营养物质吸收,从而增加营养不良发生风险[14]。(3)味觉障碍:放射治疗期间放射线会损伤味觉细胞、口腔黏膜等,导致患者味觉障碍,影响食欲,且患者因口腔不适,可能大量饮水,增加饱腹感,减少食物摄入量,导致营养不良发生[15]。(4)焦虑抑郁:肿瘤患者受疾病、放化疗不良反应影响,易出现焦虑抑郁情绪,降低治疗积极性,且患者脑内神经递质、血清素、色氨酸等水平降低,导致食欲下降,影响进食[16]。同时,伴有焦虑抑郁情绪的患者会放大疼痛感知,影响进食舒适感知,从而减少进食量,增加营养不良发生风险。(5)疲乏程度:疲乏是肿瘤患者的常见症状,中重度疲乏患者易抑制免疫活性,降低放化疗耐受性,采取消极应对策略,并降低机体活动能力,影响食欲,从而增加营养不良发生风险[17]。建议未来重点关注中晚期NPC 同步放化疗患者营养状况,早期采取营养干预措施,如使用药物减轻放化疗不良反应,增加中医干预方案缓解味觉障碍、消化道症状等;加强心理支持,积极排解患者焦虑、抑郁情绪,减轻其疲乏感,进而改善患者的营养状况。
综上所述,NPC 同步放化疗患者发生营养不良高风险,受肿瘤分期、消化道症状、味觉障碍、焦虑抑郁、疲乏程度影响,可据此制订个体化护理方案,预防患者营养不良发生。但本研究为单中心样本量研究,纳入样本量较少,且更多影响因素尚待明确,未来仍需进一步探讨。

