神经肌肉电刺激联合感知觉适度刺激干预对脑出血术后患者康复进程的影响
王立华,季玉洁,武利凤
天津医科大学第二医院 (天津 300211)
脑出血是指颅内血管在多种因素共同作用下出现破裂出血而引发的一类神经系统病变[1]。患者临床表现为突发性四肢或面部感知觉障碍、恶心呕吐及语言功能障碍等[2]。外科手术清除出血灶是早期治疗脑出血的手段,但患者在疾病、麻醉及手术创伤应激影响下,其言语、运动及神经功能均可能出现障碍,加之需长期对肢体实施制动,易引发偏瘫,临床预后效果往往与预期水平差之甚远[3]。故寻找一种积极、有效的康复措施对改善患者预后具有重要意义。感知觉适度刺激干预是指通过视、听、触觉等康复训练发挥促醒作用,在康复护理领域得到广泛应用。神经肌肉电刺激(neuromuscular electrical stimulation,NMES)作为新型康复干预手段,已在医学领域得到广泛应用。鉴于此,本研究分析NMES 联合感知觉适度刺激干预对脑出血患者术后康复进程的效果,现报道如下。
1 资料与方法
1.1 一般资料
选取2020 年2 月至2023 年2 月我院收治的91 例脑出血术后患者为研究对象,以电脑随机编号法分为试验组(45 例)与对照组(46 例)。试验组男28 例,女17 例;年龄44~75 岁,平均(60.02±4.10)岁。对照组男30 例,女16 例;年龄43~76 岁,平均(60.14±4.15)岁。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会批准,患者及家属均签署知情同意书。
纳入标准:所有患者均经颅脑CT 或MRI 检查确诊为脑出血;均为首次发病;符合手术治疗指征;年龄>18 周岁。排除标准:心、肝、肺等脏器功能严重受损;神志异常;伴有严重感染、免疫性疾病或恶性肿瘤。
1.2 方法
对照组予以感知觉适度刺激干预。(1)组建干预小组:成员包括1 名神经科医师,2 名主管护师,1 名康复治疗师,6 名责任护师;开展干预前,组织小组成员参与培训,内容包括疾病病因、临床表现、治疗方案、预后效果与注意事项等;采用头脑风暴法分析康复重点、难点,制订可行性方案。(2)视觉刺激:在距离患者可视物清晰处20 cm 处放置颜色不同的卡片或(和)小球,指导患者视线随卡片或(和)小球进行上下左右移动,5 ~10 min/ 次;上述刺激结束后,用手电筒对患者瞳孔实施反复光刺激,时机以6:00、22:00 为宜,3~5 次/min,共施行3~5 min。(2)听觉刺激:根据患者个人喜好于音频资料库内选取3~5 首歌曲,之后协助其佩戴耳机,音量以20~30 dB 为宜;每天早、中、晚循环播放歌曲3 次,10~15 min/次;护理人员遵医嘱进行注射、生命体征监测及清洁卫生等操作前,主动与患者交流沟通,告知其操作的作用和具体步骤,以通俗易懂的语言为患者解读脑出血相关知识。(3)语言刺激:正确指导患者按照口令完成舌、咽功能训练,如最大限度伸展舌体,持续3~5 s 后收回,10~15 次/组;以舌尖垂直于上颚最大限度伸展,持续3~5 s 后收回,10~15 次/组;指导其进行吮吸、深呼吸及鼓腮等训练,10~15 次/组;一对一指导患者进行发音动作、口形及唇、舌、齿摆放位置训练,根据循序渐进的原则,从最简单的单个汉字开始,逐渐过渡到词组、短句、长句。(4)运动刺激:术后24 h 内协助患者完成上肢、下肢各关节部位的被动康复运动,包括趾关节背伸放松、踝关节逆时针旋转、膝关节屈伸、下肢高抬、髋关节外展内敛、手指关节握拳、肩关节外展、高举等;25 ~30 min/次,2 ~3 次/d;根据患者病情康复及运动耐力恢复等情况,指导其开展早期创伤桥式运动、早期下床活动、行走、慢跑等;运动过程中至少有1 名照护者或护理人员陪同。
试验组在对照组基础上加用NMES 干预:选用NMES 治疗仪(日本株式会社好玛公司,型号:Tens-21)完成操作,将电极板分别贴于患者患侧肌肉两端,设置刺激强度为20 ~30 mA,脉宽为300 μs,刺激频率为30 Hz,选择单向方波,间歇时间为10~15 s,干预时间15 min/次,2 次/d。
两组均持续干预30 d。
1.3 观察指标
(1)康复进程:采用修订版昏迷恢复量表(coma recovery scale-revised,CRS-R)[4]及神经功能缺损程度评分(neurological functtion impairment,NFI)[5]进行评估。修订版昏迷恢复量表内容包括言语、听觉、触觉、视觉、运动及觉醒6 个方面,最高分23 分,评分越高表明意识恢复越好。神经功能缺损程度评分包括步行能力、语言、面谈、肌力及意识5 个方面,最高分45 分,评分越高表明神经功能缺损越严重。(2)运动功能:采用Fugl-Meyer 运动功能评定量表(Fugl-Meyer assessment scale,FMA)[6]评估,包括上肢与下肢2 个分量表,最高分分别为66 分、34 分,评分越高表明运动功能越强。(3)并发症:包括感染、静脉血栓形成、跌倒及呛咳等。(4)凝血功能指标及股静脉、腘静脉血流速度:干预前及干预10 d 后,检测患者凝血功能指标及股静脉、腘静脉血流速度;凝血功能指标包括纤维蛋白原(fibrinogen,FIB)与D-二聚体(D-dimer,D-D)。
1.4 统计学处理
采用SPSS 24.0 统计软件进行数据分析。计量资料以±s表示,采用t检验。计数资料以率表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组康复进程比较
干预30 d 后两组CRS-R 及NFI 评分较干预前均有改善,且试验组CRS-R 评分高于对照组,NFI评分低于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组CRS-R 及NFI 评分比较(分,±s)
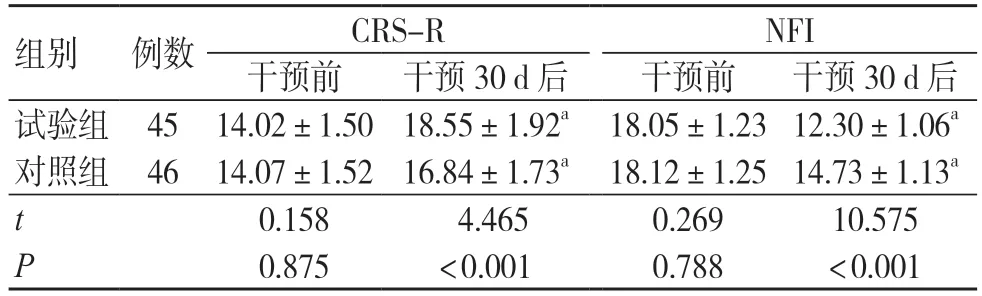
表1 两组CRS-R 及NFI 评分比较(分,±s)
注:与同组干预前比较,aP<0.05;CRS-R 为修订版昏迷恢复量表,NFI 为神经功能缺损程度评分
组别 例数 CRS-R NFI干预前 干预30 d 后 干预前 干预30 d 后试验组 45 14.02±1.50 18.55±1.92a 18.05±1.23 12.30±1.06a对照组 46 14.07±1.52 16.84±1.73a 18.12±1.25 14.73±1.13a t 0.158 4.465 0.269 10.575 P 0.875 <0.001 0.788 <0.001
2.2 两组运动功能比较
干预30 d 后两组上肢、下肢FMA 评分均高于干预前,且试验组高于对照组,差异均有统计学意义(P<0.05),见表2。
表2 两组FMA 评分比较(分,±s)
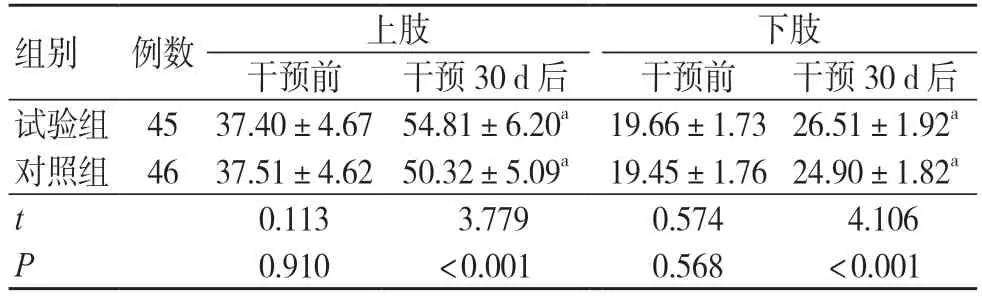
表2 两组FMA 评分比较(分,±s)
注:与同组干预前比较,aP<0.05;Fugl-Meyer 为 运动功能评定量表
组别 例数 上肢 下肢干预前 干预30 d 后 干预前 干预30 d 后试验组 45 37.40±4.67 54.81±6.20a 19.66±1.73 26.51±1.92a对照组 46 37.51±4.62 50.32±5.09a 19.45±1.76 24.90±1.82a t 0.113 3.779 0.574 4.106 P 0.910 <0.001 0.568 <0.001
2.3 两组术后并发症比较
术后试验组并发症发生率低于对照组,差异有统计学意义(P<0.05),见表3。
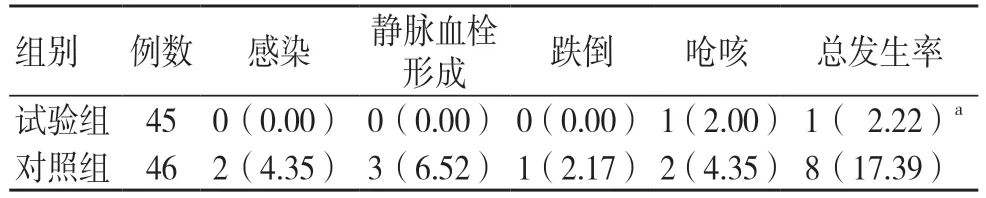
表3 两组术后并发症发生率比较[例(%)]
2.4 两组凝血功能指标及股静脉、腘静脉血流速度比较
干预30 d 后两组FIB、D-D 均低于干预前,且试验组低于对照组,差异均有统计学意义(P<0.05);干预30 d 后股静脉、腘静脉血流速度均高于干预前,且试验组高于对照组,差异均有统计学意义(P<0.05),见表4。
表4 两组凝血功能指标及股静脉、腘静脉血流速度比较(±s)
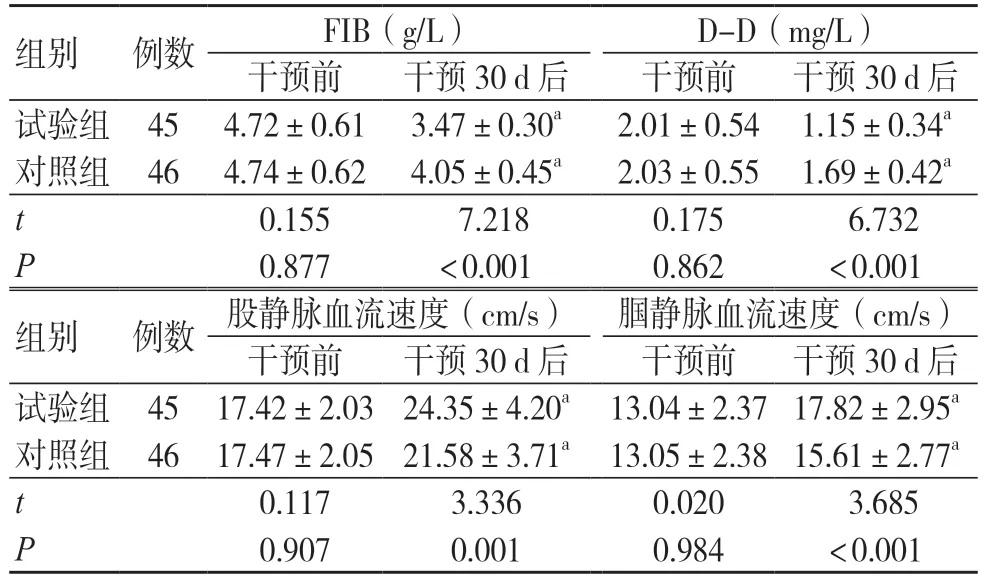
表4 两组凝血功能指标及股静脉、腘静脉血流速度比较(±s)
注:与同组干预前比较,aP<0.05;FIB 为纤维蛋白原;D-D为D-二聚体
组别 例数 FIB(g/L) D-D(mg/L)干预前 干预30 d 后 干预前 干预30 d 后试验组 45 4.72±0.61 3.47±0.30a 2.01±0.54 1.15±0.34a对照组 46 4.74±0.62 4.05±0.45a 2.03±0.55 1.69±0.42a t 0.155 7.218 0.175 6.732 P 0.877 <0.001 0.862 <0.001组别 例数 股静脉血流速度(cm/s) 腘静脉血流速度(cm/s)干预前 干预30 d 后 干预前 干预30 d 后试验组 45 17.42±2.03 24.35±4.20a 13.04±2.37 17.82±2.95a对照组 46 17.47±2.05 21.58±3.71a 13.05±2.38 15.61±2.77a t 0.117 3.336 0.020 3.685 P 0.907 0.001 0.984 <0.001
3 讨论
随着人们生活水平的不断提高,以及膳食结构与生活作息的持续改变,脑出血发病率呈逐年升高趋势,具有发病急、病情进展迅速且致残率、致死率高等特点[7-8]。患者经手术治疗后往往处于昏迷状态,为后续干预带来较大难度,严重影响预后。因此,有效促进患者快速觉醒,对病情康复及预后转归具有积极作用。研究表明,高血压患者术后普遍存在不同程度的意识、神经或肢体功能障碍,如不予以及时、有效的干预,可能出现深静脉血栓、感染及跌倒等并发症[9-10]。由此可见,开展积极、有效的康复治疗尤为重要。
本研究结果显示,干预30 d 后两组CRS-R 及NFI 评分较干预前均有改善,且试验组CRS-R 评分高于对照组,NFI 评分低于对照组,提示NMES联合感知觉适度刺激干预促进脑出血术后患者康复进程的效果明显。其原因为,感知觉适度刺激干预主要是在术后早期予以患者多层次促醒刺激,从而有效增强患者器官反应能力,促进大脑神经皮质修复,促进术后康复[11]。NMES 可直接作用于周围神经与肌肉,促使肌肉节律性收缩,增强肌肉功能及中枢系统运动调控能力;同时有利于血肿吸收,促进神经系统功能恢复,改善血液循环,有助于患者术后康复[12]。两者联用可发挥协同作用,对患者病情康复及神经功能恢复起到积极作用。此外,干预30 d 后两组上肢、下肢FMA 评分均高于干预前,且试验组高于对照组,表明试验组干预方案可促进脑出血患者术后运动功能恢复。其原因为,NMES可通过对肢体大肌群进行有效电刺激,刺激肌肉收缩运动,对患者肢体功能进行有效锻炼,进而促进运动功能恢复[13]。本研究结果显示,试验组并发症发生率低于对照组,表明试验组干预方案可降低脑出血术后并发症发生率。其原因为,NMES 可通过电流反复刺激高级运动中枢,进而促进神经系统通路重建,改善运动、吞咽、言语等功能,对相关并发症起到预防作用[14]。本研究结果还显示,干预30 d 后两组FIB、D-D 及股静脉、腘静脉血流速度较干预前均有改善,且试验组改善幅度大于对照组。其原因为,NMES 可通过电极发射脉冲电刺激促进肌肉收缩,并通过刺激支配肌肉群的神经增强肌肉泵血功能,促进静脉与淋巴回流,有助于局部循环改善,提升静脉血流速度。同时,改善局部循环可减少促凝物质聚集,抑制血小板黏附,促进D-D代谢,改善凝血功能。叶思思等[15]的研究证实,NMES 可改善急性期脑出血患者的凝血功能,加快下肢深静脉血流速度,与本研究结果相似。
综上所述,NMES 联合感知觉适度刺激干预可加速脑出血患者术后康复进程,降低术后并发症发生风险,改善凝血功能指标及股静脉、腘静脉血流速度。

