抗结核固定剂量复合剂(FDC)治疗糖尿病合并肺结核的效果及安全性
顾玉虹 张雅惠 何 刚 伍小英
1.广州市胸科医院二分所 (广东 广州 510000)
2.呼吸疾病国家重点实验室 (广东 广州 510000)
结核病(TB)是全球第二大传染病杀手。根据世界卫生组织(WHO)的数据,2021年全球约有1060万结核病患者,有160万死于结核病,据统计,90% 的患者是成年人,其中中国在全球结核病发病率最高的国家中排名第三,仅次于印度和印度尼西亚[1]。当前,对于活动性肺结核的治疗主要以抗结核药物治疗为主,常用的一线抗结核药物包括异烟肼(isoniazid,INH)、利福平(rifampin,RFP)、吡嗪酰胺(pyrazinamide,PZA)、乙胺丁醇(ethambutol,EMB)等,必要时需采取多药联合的方案,导致其用法复杂,直接影响患者服药依从性,并降低其整体疗效[2]。而抗结核固定剂量复合剂(FDC)作为近年来临床广泛推广的复合型制剂,在结核治疗中发挥重要作用。此外,该药包含2种或2种以上不同的药物,并按一定剂量制备而成,有效简化了药物处方,便于患者服用,最大程度提高患者配合治疗的积极性,同时可预防处方错误、减轻患者药丸负担和提高依从性,在一定程度上降低了患者的耐药性,最终达到增强疗效的目的[3-4]。糖尿病(DM) 是世界上增长最快的慢性病之一,预计到2040年患病率将超过6.4亿。两项大型研究和一项荟萃分析表明,与非糖尿病患者相比,糖尿病患者患结核病的风险高出3倍以上[5-6]。此外,糖尿病与结核病患者治疗失败、死亡和复发的风险增加有关[7]。 这可能是由于免疫活性降低,包括糖尿病患者的吞噬细胞和T细胞功能,这增加了结核病等感染的风险,以及对感染的早期协调免疫反应较差,导致更高的细菌负担[8]。相应地,结核病会使糖尿病患者的血糖控制恶化,这可能会进一步增加感染的严重程度[9]。FDC和ST在糖尿病合并肺结核的这一特殊人群中的治疗效果及安全性的研究相对较少,本研究的目的是比较FDC和SF抗结核药物在初治菌阳糖尿病合并肺结核患者的疗效及安全性。
1 资料与方法
1.1 临床资料 按回顾性分析法将广州市胸科医院2020年1月至2021年12月收治108例初治菌阳的糖尿病合并肺结核患者。从病案系统、检验系统、影像学系统记录中收集患者相关资料。
纳入标准:符合初治菌阳肺结核诊断;有糖尿病病史,符合2型糖尿病诊断标准;年龄≥18周岁;配合治疗。排除标准:合并妊娠、慢性性肝炎、肾功能不全、HIV、癌症或感染了对INH、RFP、PZA 或EMB具有耐药性的结核分枝杆菌;依从性差以及不能耐受方案的患者。两组患者的年龄、性别、体重指数(BMI)、治疗前的糖化血红蛋白等临床资料并无统计差异(P>0.05)。本试验经医院伦理委员会批准。
1.2 方法 患者每天一次口服抗结核药物。用药剂量根据患者的体重计算。FDC组以FDC 开展治疗。强化期,选择固定剂量复合剂异烟肼+利福平+吡嗪酰胺+乙胺丁醇(HRZE,规格:INH 37.5 mg、RFP 75mg、PZA 200mg和EMB 137.5mg/片),口服,体重≤37kg 4片/次,体重在38~54kg,6片/次,体重≥54kg,8片/次,治疗2月末,若患者痰菌检查仍显示为阳性,则延长强化期1个月,用药剂量不变。巩固期,服用固定剂量复合剂 HR [规格:(H150 mg+R300 mg)/粒],1 次/d,2 粒/次。ST组以常规抗结核药物方案开展治疗,强化期,选择抗结核药:INH(剂量:0.30g),PZA(剂量:1.50g),RFP (剂量:体重<50 kg 0.45 g,≥50kg 服用 0.60g),EMB (剂量:体重<50kg 0.75g,体重≥50 kg 1.0 g),口服,治疗2月末,若患者痰菌检查仍显示为阳性,则延长强化期1个月,用药剂量不变。
巩固期,INH(剂量:0.30g),RFP(剂量:体重<50 kg 0.45g,体重≥50 kg 0.60 g)。患者通过口服降糖药和/或胰岛素以及定期空腹血糖监测了解糖尿病控制情况。
1.3 观察指标及评估标准(1)记录两组患者治疗第2、5、6个月的痰菌检查结果,判定方式:获取患者痰液标本,通过痰涂片及痰培养分枝杆菌检查,观察结果是否转阴;(2)病灶吸收情况:以复诊时间为准,在患者治疗2、5、6个月末时进行X线胸片检查,依据病灶吸收情况分为显著吸收(病灶吸收≥原病灶的1/2);吸收(1/3<原病灶<1/2);无变化(吸收≤原病灶的1/3或增大<原病灶的1/3);恶化(病灶明显变大≥原来病灶的1/3)。总吸收率=显著吸收率+吸收率;(3)统计用药期间的不良反应,包含肝损伤、胃肠反应、高尿酸血症、神经系统症状、视觉异常。药物性肝损害(ATBDILI)的定义符合指南[10]。 胃肠不良反应,包括恶心、呕吐或上腹痛和腹痛。高尿酸血症定义为任何高于420μmmo/L的尿酸水平。当患者报告视觉不良事件时,包括视力模糊、色盲或眼痛。
1.4 统计分析计量资料以(±s)表示,采用独立样本t检验进行组间比较,计数资料以率(%)表示,组间比较采检验,P<0.05差异提示统计学意义。所有统计分析均采用 SPSS 25.0 统计学软件进行分析和处理。
2 结 果
2.1 两组菌阳转阴率比较两组治疗2、5、6 个月时均有菌阳转阴,FDC组治疗 2、5、6个月菌阳转阴率均较ST组升高,尤其是治疗2月的菌阳转阴率存在统计差异(P<0.05),两组治疗5、6月的转阴率并无统计差别(P>0.05)。见表1。
2.2 两组病变部位病灶吸收情况比较治疗后FDC组病灶总吸收率较ST组更高(P<0.05),见表2。

表2 两组病变部位病灶吸收情况比较[例(%)]
2.3 不良反应治疗期间2组均出现一系列不良反应,虽然FDC组不良反应的发生率稍低于ST组,但差异无显著性(P>0.05),见表3。
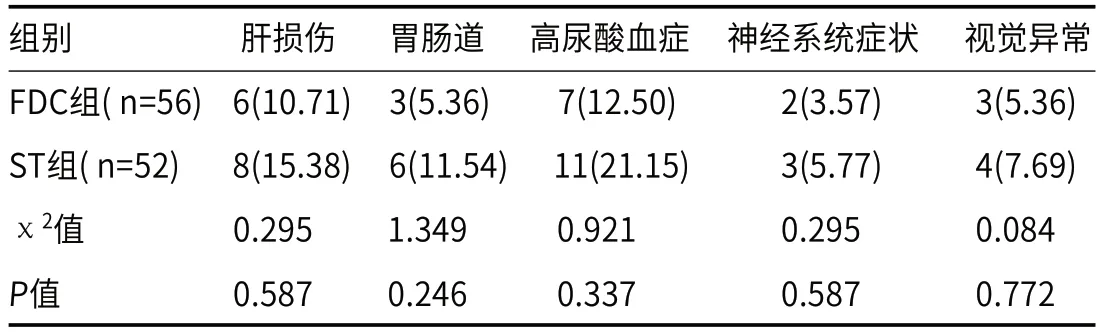
表3 两组不良反应比较[例(%)]
3 讨 论
这是一项比较四种药物 FDC和ST方案对初治菌阳糖尿病合并肺结核病人的治疗的有效性和安全性的研究。两种方案都显示出不同的临床疗效和安全性。通过治疗期间痰菌阳转阴的时间、病灶吸收的程度观察疗效,并根据结核病药物常见的不良事件出现的概率来评估安全性。在我们的研究中,与ST剂量相比,初治菌阳糖尿病合并肺结核的患者中,FDC治疗与ST治疗相比较,抗结核治疗2月后痰菌阳性转阴的比例更高。这结果与Jacqueline Mui Lan Lai及Al-Shaer MH等[11-12]研究结果一致。可能促成这一结果的因素之一是与ST方案(12~14片/天)相比,FDC 的药丸负担较低(4~8片/天) 相关,糖尿病患者容易出现包括胃轻瘫在内的胃肠道问题[13],因此他们很容易出现药物吸收延迟或吸收不良,较少的药丸摄入极大地减少了患者胃肠的负担,从而在一定程度上提高了药物的吸收,快速杀灭结核菌,达到较快的转阴效果。然而有部分研究提示在FDC组和ST方案组中,达到痰AFB阴性的平均时间没有统计学差异[14],笔者认为导致结果不一致的原因是研究人群的差异。
本研究同时表明,在促进病灶吸收方面,FDC组合制剂,亦能让这类糖尿病的患者受益,郑军[15]等研究结果表明,糖尿病合并肺结核常牵连多个肺叶受损,且病变分布范围较宽泛,通常集中于上叶前段,极易引起空洞或坏死、干酪样病变,抗结核固定剂量复合处方时更严格按照患者体重进行个性化给药,处方相对简单,患者治疗依从性得到提高,还能避免忘记服药、错误服药等问题[16], 对病灶的吸收有帮助。本次FDC治疗组病灶吸收率为 96.4%和ST组的 82.7%比较差异显著;同时两组患者在接受治疗的过程中,均发生不同程度不良反应,其中以高尿酸血症及肝损伤的发生例数较多,但FDC组的使用未增加不良反应,而且还与肺部病灶的总吸收率,患者从经济上、治疗效果上更受益。
综上所述:FDC在初治菌阳糖尿病合并肺结核的治疗中发挥积极作用,且在促进痰菌快速阳转阴、病灶吸收效果方面受益明显,用药不良反应发生率未增加;因此,值得在此类病人中应用及推广。

