血管内超声显像在冠状动脉药物洗脱支架植入术治疗冠心病左主干病变患者中的应用效果
杨嵘斌,叶胜义(通信作者)
1 福建省晋江市医院晋南分院 (福建晋江 362241);2 福建省晋江市医院 (福建晋江 362200)
冠心病左主干病变(left main coronary artery disease,LMCAD)病情凶险,临床病死率较高。LMCAD 若治疗不及时,左主干分叉长期狭窄会使其支配的左心室心肌逐渐出现缺血缺氧,甚至造成急性心肌梗死、心源性休克、室颤或猝死等严重后果[1-2]。既往临床以血运重建为首选策略,但预后较差。研究表明,在经皮冠状动脉介入(percutaneous coronary intervention,PCI)基础上采用冠状动脉药物洗脱支架植入术治疗LMCAD 患者可在一定程度上解决血管狭窄问题,提高远期血管通畅率[3-5]。但PCI 难度较大,加上支架置入操作复杂、精细,易导致急性或濒临闭塞,需术中准确判断左主干、前降支、回旋支三者之间的解剖关系,最终制定合适的手术方案[6]。冠状动脉造影为临床评估LMCAD 的常见方法,可直观显示冠状动脉形态,便于医师了解血管有无狭窄病灶存在,但在左主干病变造影方面存在一定局限性,对血管壁的显示效果较差,无法精准评估血管直径、病变长度、斑块性质及分布[7-8]。血管内超声显像的原理是将超声换能器置入血管腔,经成像系统完整显示心血管横断面,相较于冠状动脉造影,可直接显示血管壁病变,凭借组织穿透力强、精准度高等优点成为介入诊疗的重要辅助手段[9-10]。基于此,本研究探讨血管内超声显像在冠状动脉药物洗脱支架植入术治疗LMCAD 患者中的应用效果,现报道如下。
1 资料与方法
1.1 一般资料
选取2020 年2 月至2022 年2 月于我院行冠状动脉药物洗脱支架植入术的106 例LMCAD 患者作为研究对象,根据术中引导方式不同分为对照组(42 例)与试验组(64 例)。对照组男25 例,女17 例;平均年龄(60.33±5.97)岁;平均病变长度(9.22±1.38)mm;病变位置:开口12 例,体部16 例,尾体部14 例;合并基础疾病:高血压23 例,高血脂25 例,糖尿病28 例。试验组男38 例,女26 例;平均年龄(61.45±6.12)岁;平均病变长度(9.18±1.40)mm。病变位置:开口20 例,体部22 例,尾体部22 例;合并基础疾病:高血压25 例,高血脂28 例,糖尿病30 例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究已获得医院医学伦理委员会审核批准。
纳人标准:符合LMCAD 相关诊断标准[11];接受冠状动脉药物洗脱支架植入术治疗;无血管内超声显像与冠状动脉造影禁忌证;无介入治疗禁忌证;随访资料完整,并已签署研究知情同意书。排除标准:合并心肌梗死;对造影剂及介入术中溶栓药物过敏;重要脏器功能障碍;凝血功能障碍;严重心脏瓣膜疾病;既往接受过介入术治疗;恶性肿瘤;严重精神认知障碍导致其无法接受相关调查及随访;因个人原因中途退出或失访。
1.2 方法
两组均行冠状动脉药物洗脱支架植入术,术前完善相关检查,排除相关禁忌证。
对照组行冠状动脉造影,常规消毒桡动脉及股动脉穿刺区域,选择正位(后前位)或左前斜位,首先注入6 000 U 肝素钠,以桡骨茎突上约一横指处为穿刺点,采用Seldinger 穿刺法于皮下打一皮丘,再进针;未见血液流出即可推注利多卡因,针尖斜面朝上沿血管走形缓慢进针,进针完成后缓慢撤除穿刺外鞘,待回血良好送入直导丝,可在X 线引导下观察导丝走向;多体位充分展露冠脉各节段情况,选择主动脉根部平面为感兴趣区,注射 370 mg I/ml 碘普罗胺对比剂80 ml 后,停滞10 s,观察并测量相关指标,根据具体数值置入适宜的药物洗脱支架。
试验组穿刺、置入等步骤同对照组,推注肝素6 000 U,并根据血压数值向冠状动脉内注射硝酸甘油。不同的是更换为血管内超声显像评估左主干病变程度、直径、狭窄程度等,其超声导管插入方法同PCI,在X 线透视引导下将导丝随导管伸入病变远段,撤回超声导管至开口处;连接主机后利用超声探头仔细观察,显示各部位的高清图像。若图像显示分界不清可注入适当造影剂或0.9%氯化钠注射液;根据数据及图像置入适宜的支架,确保支架贴壁良好、扩张充分、展开均匀和完全覆盖。
1.3 观察指标
(1)比较两组PCI 指标,包括支架直径、支架长度、后扩张次数、后扩张球囊直径及后扩张球囊压力。(2)比较两组手术指标,包括X 线曝光时间、对比剂用量及手术时间。(3)预后情况:记录6 个月内两组心肌梗死、二次血运重建、病死等并发症发生情况。
1.4 统计学处理
2 结果
2.1 两组PCI 指标比较
试验组支架直径大于对照组,支架长度长于对照组,后扩张次数少于对照组,后扩张球囊直径、后扩张球囊压力均小于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组PCI 指标比较(±s)
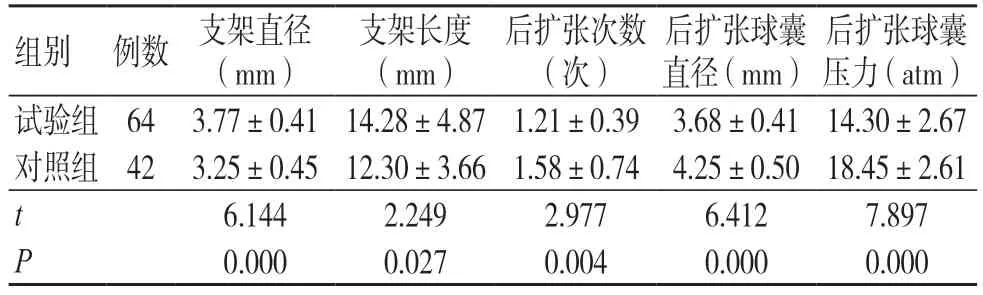
表1 两组PCI 指标比较(±s)
注:PCI 为经皮冠状动脉介入
后扩张次数(次)组别 例数 支架直径(mm)支架长度(mm)后扩张球囊直径(mm)后扩张球囊压力(atm)试验组 64 3.77±0.41 14.28±4.87 1.21±0.39 3.68±0.41 14.30±2.67对照组 42 3.25±0.45 12.30±3.66 1.58±0.74 4.25±0.50 18.45±2.61 t 6.144 2.249 2.977 6.412 7.897 P 0.000 0.027 0.004 0.000 0.000
2.2 两组手术指标比较
两组X 线曝光时间、对比剂用量及手术时间比较,差异无统计学意义(P>0.05),见表2。
表2 两组手术指标比较(±s)
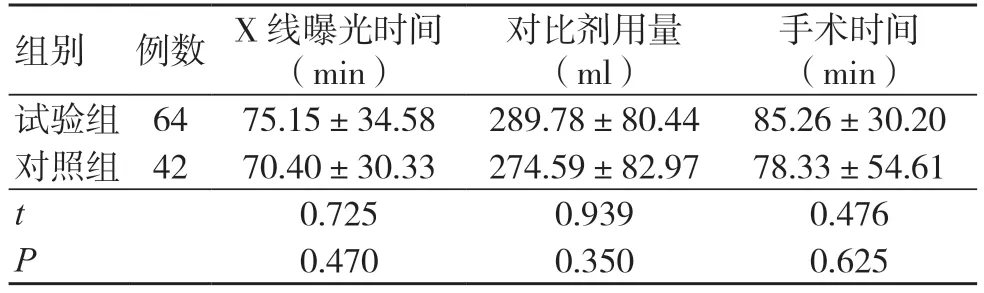
表2 两组手术指标比较(±s)
手术时间(min)试验组 64 75.15±34.58 289.78±80.44 85.26±30.20对照组 42 70.40±30.33 274.59±82.97 78.33±54.61 t 0.725 0.939 0.476 P 0.470 0.350 0.625组别 例数 X 线曝光时间(min)对比剂用量(ml)
2.3 两组预后情况比较
两组均出现心肌梗死、二次血运重建、病死等并发症,试验组并发症发生率低于对照组,差异有统计学意义(P<0.05),见表3。
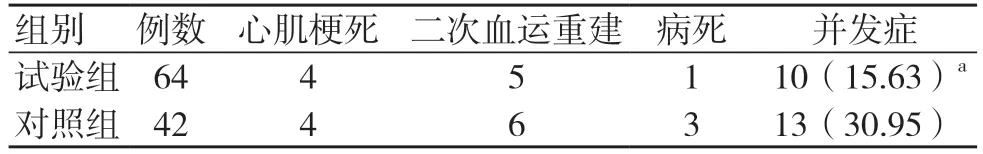
表3 两组预后情况比较[例(%)]
3 讨论
在冠状动脉病变中,LMCAD 发病最急促、危险度最高、病情最复杂凶险,且发生心源性休克的风险较大[12]。因此,须尽早采取措施治疗该病患者,开通血管、恢复血流,抑制梗死扩散。临床常借助PCI 减少心肌坏死面积,在对LMCAD 患者施行手术前需准确判断左主干、开口、体部、尾部之间的解剖关系,评估病变及狭窄程度以选择合适的支架,提高手术安全性及效果[13]。冠状动脉造影为常用的辅助诊疗手段,通过评估狭窄程度可为药物洗脱球囊置入术提供指导,提高临床生存率[14]。但冠状动脉造影在显示血管管腔图像时易受血管走向及投照体位的影响,加上左主干解剖结构较为复杂,无法精准评估血管直径、病变长度等信息,在临床实际应用中表现出许多不足之处[15]。血管内超声显像的工作原理与传统B 超类似,即通过微型超声探头可全方位观察血管壁内部情况,准确定量狭窄率。此外,其所获取的血管管腔、斑块、形态、钙化程度、血管重构等信息还可辅以选择适宜的支架,指导临床制定最佳的介入策略。因此,血管内超声显像已成为临床用于左主干介入治疗指导支架植入的重要方法[16-17]。
本研究结果显示,试验组支架直径大于对照组,支架长度长于对照组,后扩张次数少于对照组,后扩张球囊直径、后扩张球囊压力均小于对照组,并发症发生率低于对照组,提示血管内超声在冠状动脉药物洗脱支架植入术治疗LMCAD 患者中可发挥较好的临床效果,利于辅助医师识别狭窄原因,选择植入支架。其原因为,血管内超声显像巧妙结合了无创超声技术与有创导管技术,通过将高频微型超声探头导入血管腔内,可准确显示血管的几何形态及解剖信息,用于左主干可直接获取血管横截面病变部位、范围、严重程度等信息,准确测量管腔及粥样斑块或纤维斑块的大小。此外,粥样斑块面积增大,冠状动脉呈代偿性扩张,管腔面积可无狭窄,冠状动脉造影可能无法观察到此变化,但血管内超声显像可予以弥补,因此,血管内超声显像在临床诊断及治疗复杂病变时可发挥优势[18]。
综上所述,血管内超声显像在冠状动脉药物洗脱支架植入术治疗LMCAD 患者中可发挥较好的临床效果,提高支架植入效果,利于手术顺利进行,并可降低并发症发生风险。

