玻璃体腔注射康柏西普与阿柏西普治疗厚脉络膜新生血管病变的疗效比较
王晓宇,刘 渊,侯静文,詹 添,王爱媛
0 引言
厚脉络膜新生血管病变(pachychoroid neovasculopathy,PNV)在临床表现为与脉络膜增厚和/或Haller血管扩张相关的1型新生血管的生成,但不伴有典型的玻璃膜疣等年龄相关性黄斑变性特征的厚脉络膜谱系疾病[1]。依据Warrow和Freund最早提出的厚脉络膜疾病概念,因在厚脉络膜色素上皮病变的眼底观察到1型新生血管的形成,并由此提出了PNV[2-3]。PNV被认为是由厚脉络膜表型所引发的病理生理机制改变,该病介于中心性浆液性脉络膜视网膜病变(presence of central serous chorioretinopathy,CSCR)、脉络膜色素上皮病变(pigment epitheliopathy,PPE)和息肉样脉络膜血管病变(polypoidal choroidal vasculopathy,PCV)之间,其可能在长期CSCR和PPE后形成,并在最终进展成为PCV。抗血管内皮生长因子(vascular endothelial growth factor, VEGF)药物作为该疾病的首选治疗方法,既往已有很多研究报道了阿柏西普对PNV的治疗起到了一定效果[4-5],康柏西普作为一种多靶点作用的重组融合蛋白,在临床对于新生血管类疾病发挥了良好表现,当前已报道的关于阿柏西普及康柏西普对比治疗研究多集中在糖尿病视网膜病变及湿性年龄相关性黄斑变性等疾病[6-7],在PNV方面的尚未见报道。本研究将首次对接受康柏西普与阿柏西普治疗的PNV患者进行回顾性观察,随访6mo内患者的最佳矫正视力(best corrected visual acuity, BCVA)、黄斑中心凹下脉络膜厚度(subfoveal choroidal thickness,SFCT)、黄斑中心凹视网膜厚度(central macular thickness, CMT)及注药次数,探讨玻璃体腔注射康柏西普在治疗PNV上的安全性及有效性。
1 对象和方法
1.1对象选取2018-02/2022-10于中国医科大学附属盛京医院确诊为PNV并进行玻璃体腔注射阿柏西普或康柏西普的患者33例35眼,其中男18例20眼,女15例15眼;平均年龄50.8±6.2岁。根据不同给药方案将患者分为A组(康柏西普组)和B组(阿柏西普组)。纳入标准:(1)Ⅰ型CNV;(2)双眼SFCT≥300μm[8];(3)存在CSCR或PPE(包括RPE异常、脉络膜血管扩张以及既往CSCR病史)。排除标准:(1)合并其他眼底疾病;(2)合并视神经病变及影响屈光间质疾病干扰眼底疾病诊断的患者;(3)既往接受过激光光凝、光动力治疗(PDT)或抗VEGF治疗等任何眼内手术治疗的患者(非复杂的白内障手术除外);(4)既往有其他严重的全身疾病,包括脑卒中、心肌梗死、恶性肿瘤等;(5)怀孕及哺乳期妇女;(6)临床资料不全或其他不能配合完成研究的患者。本研究遵循《赫尔辛基宣言》原则,并经伦理委员会审核批准。所有患者治疗前均签署知情同意书。
1.2方法
1.2.1检查方法所有患者治疗前均进行全面的眼科检查,包括BCVA、眼压、裂隙灯检查、眼底照相、OCT和眼底血管造影(全身状况不允许的患者需有OCT血管成像)。BCVA采用标准对数视力表测得,统计分析时转换为最小分辨角对数视力[LogMAR视力,转换公式LogMAR=lg(1/小数视力)]。CMT、SFCT采用OCT自动测量并进行数据记录。
1.2.2治疗方法术前常规使用抗生素滴眼液,玻璃体腔注射均在无菌层流手术室内进行,眼周消毒、铺巾、开睑器开睑后使用聚维酮碘及生理盐水冲洗结膜囊,随后采用30G注射针头在距角巩膜缘3.5~4mm的睫状体平坦部垂直进针,注入药物康柏西普(0.5mg/0.05mL)或阿柏西普(2mg/0.05mL),拔出后使用消毒棉签压迫进针处30s。患者遵循在首诊注射后采用按需治疗(pro re nata,PRN)的方式,即1+PRN方案。若复查时出现视力减退、CMT增高、OCT结果可见层间积液其中的两项,则重复进行注射抗新生血管药物。
1.2.3观察指标所有患者均于术前,术后1、3、6mo进行BCVA、OCT检查,比较患者治疗前后BCVA、CMT及SFCT变化。记录患者在6mo内的注药次数,观察治疗后是否出现并发症及药物不良反应。

2 结果
2.1治疗前两组基线资料的比较A组14例14眼,B组19例21眼。治疗前两组患者年龄、性别、BCVA、CMT、SFCT比较,差异均无统计学意义(P>0.05),见表1。
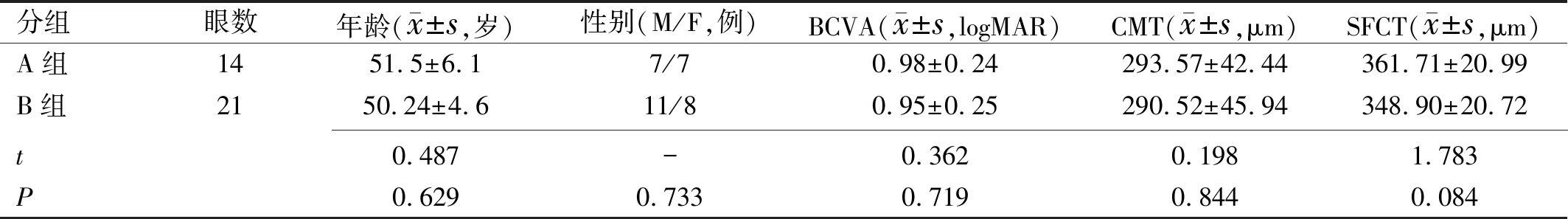
表1 两组患者治疗前视力和解剖参数比较
2.2治疗效果
2.2.1两组患者治疗前后视力和解剖参数比较在初次玻璃体腔注射药物后,随着时间的推移,治疗后1、3、6mo,两组患者BCVA均较治疗前有了明显改善(均P<0.001),但两组间视力改善方面的差异无统计学意义(均P>0.05)。同时,治疗前后两组患者CMT及SFCT随时间推移显著降低,差异具有统计学意义(均P<0.001),但两组间上述观察指标改善情况的差异无统计学意义(均P>0.05),见表2。典型病例的临床表现及治疗前后对比见图1~3。
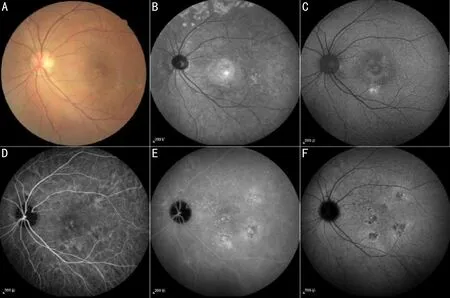
图1 眼底图片 A:眼底照相可见黄斑区色素不均,但未见玻璃膜疣(drusen);B:红外照相可见与眼底照相病灶对应区域的脉络膜深层病损;C:自发荧光可见黄斑区斑片状增强病灶区域;D~F:吲哚菁绿血管造影(IA)早期可见点状病灶,随着时间推移相应病灶处点片状荧光素渗漏,随着背景荧光减弱晚期可见5处点状荧光染色病灶。

图3 治疗前后对比可发现RPE层逐渐趋于平伏,视网膜下液逐渐减少及SFCT明显降低。

表2 两组患者治疗前后视力和解剖参数比较
2.2.2两组患者玻璃体腔注药次数比较在初次治疗后随访观察的6mo内,康柏西普组注药次数为2(2,3)次,阿柏西普组注药次数为2(1.5,2)次,两组间的注药次数比较差异无统计学意义(Z=-0.802,P=0.423)。
2.3两组患者并发症发生情况在所有治疗过程中,康柏西普及阿柏西普各出现结膜下出血1例1眼,两组患者均未见严重的与手术相关的并发症,如并发性白内障、视网膜脱离、眼内炎等。
3 讨论
PNV是由Ⅰ型CNV发展而来的厚脉络膜病变,其疾病的发生机制是与厚脉络膜的形成密切相关,具体包含脉络膜大血管扩张和通透性增高[1]。Ⅰ型新生血管的形成是PNV的特征性改变,其在空间上的分布或出现的位置常常对应局部脉络膜血管增厚、脉络膜毛细血管层变薄和RPE异常,在临床上通常将此认为是PPE及CSCR的晚期并发症。当前在临床上,PNV的鉴别诊断仍是一个难点。在本次回顾性研究中我们发现,有相当数量的PNV在临床上被误诊断为年龄相关性黄斑变性(age-related macular degeneration,ARMD)。该病区别于新生血管性ARMD的关键特征在于发病年龄小、OCT可见新生血管区对应的脉络膜增厚且无或仅有少量的软性玻璃膜疣[9]。Pang和Freund提出,在缺乏特征性ARMD或退行性改变的情况下,当出现Ⅰ型新生血管形成和脉络膜增厚特征时应优先考虑PNV[1,10]。Hata等[11]通过研究眼内VEGF浓度发现在PNV患者中,其VEGF浓度显著低于新生血管ARMD患者的VEGF浓度。因此,PNV患者需要的玻璃体腔注药次数通常少于ARMD患者。虽然当前临床对于上述疾病的主流治疗方式均为抗VEGF药物,但其治疗效果往往具有很大差异。因此,准确的诊断疾病并给予适当的治疗至关重要。
当前PNV的发病机制尚不明确,既往研究结果表明阿柏西普作为多靶点的抗VEGF药物在治疗亚洲人群的厚脉络膜疾病中具有良好表现。部分报告指出在减少脉络膜厚度方面,多靶点的阿柏西普显著优于单靶点药物[4]。阿柏西普通过抑制VEGF及其受体信号传递来降低眼内VEGF的水平,同时在VEGFR1/2/3、KIT、PDGFRB等多个靶点发挥作用,从而显著抑制新生血管,减轻血管渗漏;同样康柏西普作为我国自主研发生产的多靶点药物,是一种人源化的VEGF受体抗体,属于重组融合蛋白,具有很强的亲和力,可以与VEGF-1各亚型及VEGF-B、胎盘生长因子(placental growth factor,PIGF)等结合,起到抗VEGF-A、VEGF-B的作用,此外还能通过改善脉络膜微循环,激活色素上皮酶来促进营养物质的输送,进一步使得感光细胞功能得到修复[12]。当前认为脉络膜厚度调节机制为当病理条件下脉络膜毛细血管异常时,脉络膜基质中的高渗透性大分子积聚,从而引起水分子向脉络膜血管内积聚,导致脉络膜厚度增加。此外,液体也可从视网膜流经病变的RPE而逆流至脉络膜[13]。而康柏西普与阿柏西普可能就是通过上述机制减轻了脉络膜厚度,促进了视力的恢复。本研究对玻璃体腔注射康柏西普与阿柏西普治疗PNV患者进行了回顾性分析。我们发现,两组患者在治疗后1、2、3mo视力逐渐改善,且相较于治疗前其BCVA均显著改善,差异均有统计学意义(P<0.001),同时,CMT及SFCT均显著降低,两种药物均表现良好,上述数据在两组间的差异无统计学意义(均P>0.05)。通过进一步对比发现,虽然无论是阿柏西普组还是康柏西普组其BCVA在治疗后均较治疗前有了明显改善,但在治疗后1、3、6mo的结果比较时,并无明显的差别,通过对数据的再次分析发现是因为在A、B两组中分别有5、7眼出现了在第1mo注射药物后,BCVA在之后治疗过程中不见改善,这提示PNV患者在治疗到一定程度时可能会出现停滞的情况,Sartini等[14]提出可以通过PDT的方法改善上述的情况。康柏西普既往在糖尿病视网膜病变、脉络膜新生血管、ARMD等多种疾病中显著抑制了新生血管的生长,因此本研究将其与阿柏西普进行对比研究,结果证明康柏西普及阿柏西普均能在短期内改善视力,同时有效诱导黄斑CMT及SFCT降低,均具有较高的安全性。
本研究存在一定的局限性:(1)该病发生率较低,临床患者数量相对较少,同时少部分患者由于注药次数过多带来的经济及心理负担过重而导致部分失访,可能会对结果产生一定影响;(2)我们研究的人群都是中国东北地区患者,由于地域及种族群体的限制可能会对药物治疗PNV的疗效产生影响,另外在诊断时尚未考虑到脉络膜厚度受到生理及病理因素的影响,生理上眼轴轴长、年龄与黄斑区的脉络膜厚度呈明显负相关[15],在病理情况方面,当发生脉络膜低灌注相关眼病时,如青光眼和慢性肾脏疾病,SFCT变薄;而发生脉络膜高灌注相关的视网膜脉络膜病变,如CSCR、Ⅰ型CNV等,SFCT则明显增加[16-17]。这提示对于PNV的诊断标准可能需要进一步的完善。尽管如此,本研究结果仍表明玻璃体腔注射康柏西普及阿柏西普均可以起到改善厚脉络膜血管病变的解剖结构和视功能。希望在将来有更多的研究着眼于PNV治疗的研究。

