重症脑损伤患者气切导管拔除影响因素的临床分析
华小锋,简崇东,李新洲,覃金艳
(1. 右江民族医学院研究生学院,广西 百色 533000;2.右江民族医学院附属医院神经内科重症监护病房,广西 百色 533000;3. 右江民族医学院附属医院康复医学科,广西 百色 533000)
重症脑损伤(severe brain injury)主要包含严重的创伤性脑损伤、缺血性和出血性卒中及缺血缺氧性脑损伤[1]。文献报道[2],重症脑损伤患者气管切开率为50%~70%,拔管失败率为 2%~25%。目前临床上评价气切导管的拔除因素存在不同认识,没有形成以证据为基础的导管拔除指针。本研究通过对104例重症脑损伤留置气切导管的患者可能影响气切导管拔除的因素进行分析,以期为气切导管的安全拔除提供临床参考。
1 资料与方法
1.1 一般资料 选取2021年1月至2023年3月本院康复医学科住院的重症脑损伤合并留置气切导管[内径为7.5 mm ,对应截面通气S=3.14×(7.5/2)2=44.15 mm2]的成人患者104例为研究对象。
1.2 患者分组 按拔管成功与否分为拔管成功组和拔管失败组。所有患者家属均被告知拔管方案并签署拔管知情同意书。拔管成功组:拔管后患者呼吸平稳(16~20次/分),指脉氧≥94%,未重新插管。拔管失败组:拔管后当即出现呼吸困难(吸气三凹征之一表现),呼吸急促(>25次/分),指脉氧持续低于94%,下降经面罩吸氧症状不改善,重新留置气切导管后呼吸困难解除。
1.3 拔管指征 ①患者体温正常、少痰;②自主呼吸平稳,指脉氧94%以上;③肺部CT提示感染病灶少和颈椎CT平扫提示上气道通畅。
1.4 拔管方法 ①口咽部相对狭窄处横截面面积(口咽狭窄处横截面面积)测量:对患者常规行颈椎CT平扫,对口咽部气道相对狭窄处进行面积测量(注:平扫后图像上传至电脑影像阅片系统后,利用配套的阅片测量工具可自行计算出相应截面的面积);②视情况吸除口咽部分泌物,“开放”颈段气道:先用20~50 mL注射器对气切导管的吸痰管充分负压抽吸,减少气囊近端潴留的痰液,再对气囊管进行充分负压抽吸,使气囊“干瘪”并减少“气囊活瓣”对呼吸影响,达到“开放”颈段气道的目的;③堵管后气促评估:将修剪好的输液器墨菲式管一端套在气切导管处,另一端根据呼吸情况逐步封堵,观察呼吸频率、气促情况,评估经口呼吸能力,过程1~3 d,密切注意呼吸肌耐受能力,指脉氧不低于94%;④拔管:拔管前视情况吸除口咽部分泌物,避免经气切导管吸痰,以免引起剧烈呛咳、气道痉挛、心率/律异常、血压升高等异常情况,减少“医源性心理创伤”。拔管时“右利手”医师立于患者右侧床旁,剪断气切导管的固定绳,右手持气切导管末端,前臂做“旋后”动作,沿其管径弧度方向顺时针方向、轻微用力向外“旋拔”即可拔除气切导管;⑤拔管后处理:常规碘伏消毒气切口周围皮肤,无菌纱布覆盖气切口、胶布固定。予患者高半卧位,经鼻高流量湿化氧疗,利于缓解呼吸肌疲劳[3]。每天换药至气切口愈合。
1.5 拔管前病史资料收集、整理 包括患者基本信息,临床诊断,年龄60岁以上为老年组,50~60岁为中年组,49岁以下为青中年组;气管插管时间7 d以内为短期气管插管,超过7 d为长期插管;气切置管时间<30 d以内为短期插管,30~60 d为长期置管,超过60 d为超长期置管;同时根据APACHE-Ⅱ评分系统及康复功能评估指标综合评估拔管前感染控制指标血液白细胞总数>10×109/L、中性粒细胞百分比>70%提示感染控制不良;营养状况不良指存在中度以上的贫血(血红蛋白<90 g /L)或低蛋白血症(血清白蛋白<30 g /L);堵管后呼吸气促指气切导管堵管试验时呼吸频率>25次/分,呼吸频率16~24次/分表示无气促或不明显;意识水平采用格拉斯哥昏迷量表评分表示(GCS),低于8分为昏迷;咳嗽能力强弱根据咳嗽是否响亮有力,痰液可否部分或全部从气管切口咳出评估;吞咽能力强弱依据可否自主吞咽或被动刺激咽部引起吞咽动作评估;常规颈椎CT平扫观察上气道通畅程度(具体观察舌体有无后坠、鼻咽部软组织有无后坠、测量咽部狭窄处截面面积——利用CT阅片系统配套工具测量)。
1.6 统计学方法 数据采用SPSS 23.0软件包处理。计数资料用频数和率(%)表示,组间比较采用χ2检验或 Fisher’s Exact Test。采用Logistic回归分析探索重症脑损伤气管切开患者拔管成功与否的影响因素。以P<0.05表示差异有统计学意义。
2 结果
2.1 研究对象的人口学资料及临床特征 成人气管切开并留置气切导管(内径7.5 mm)的患者104例,气切导管留置时间18 ~194 d,见表1。
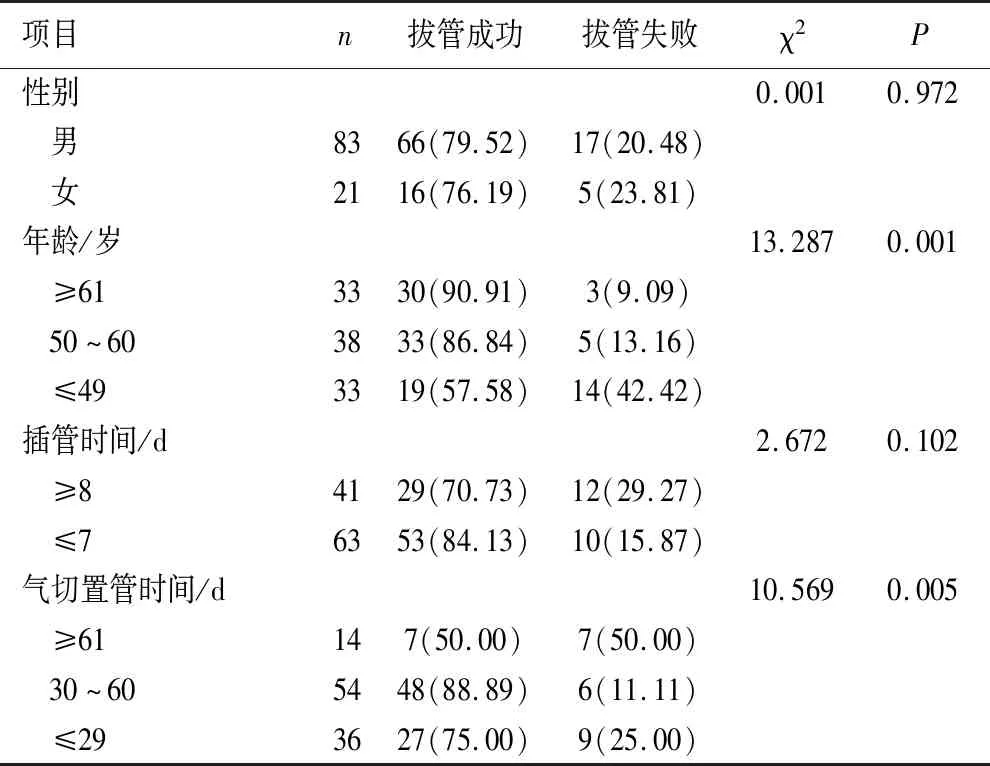
表1 重症脑损伤气管切开患者拔管成功与失败发生率比较
2.2 不同人口学资料和临床特征拔管成功率的比较分析 104例气管切开患者拔管成功82例,拔管失败22例,其中成功率为78.85%。分别比较不同年龄组、不同气切置管时间、有无舌体后坠、有无鼻咽软组织后坠、不同口咽横截面面积、不同吞咽能力、不同意识水平、不同堵管后气促程度、不同血清白蛋白水平等患者间气切导管拔管成功率的差异均有统计学意义(P<0.05),而且不同性别、不同插管时间、不同疾病类型、不同咳嗽能力、不同血液白细胞数水平、不同中性粒细胞百分比水平、不同血红蛋白水平等患者间气切导管拔管成功率的差异均无统计学意义(P>0.05)。见表1。
2.3 重症脑损伤气管切开患者拔管成功与否的多因素分析 以年龄、气切置管时间、舌体后坠、鼻咽软组织后坠、口咽狭窄处横截面面积、吞咽能力、意识水平、堵管后气促程度、白蛋白水平等为自变量,以拔管成功与否为因变量,行Logistic回归分析。变量赋值情况见表2。分析结果显示:口咽狭窄处横截面面积、意识水平、堵管后气促程度是影响重症脑损伤患者气切套管拔管成功率的独立危险因素,见表3。

表2 Logistic回归分析变量赋值
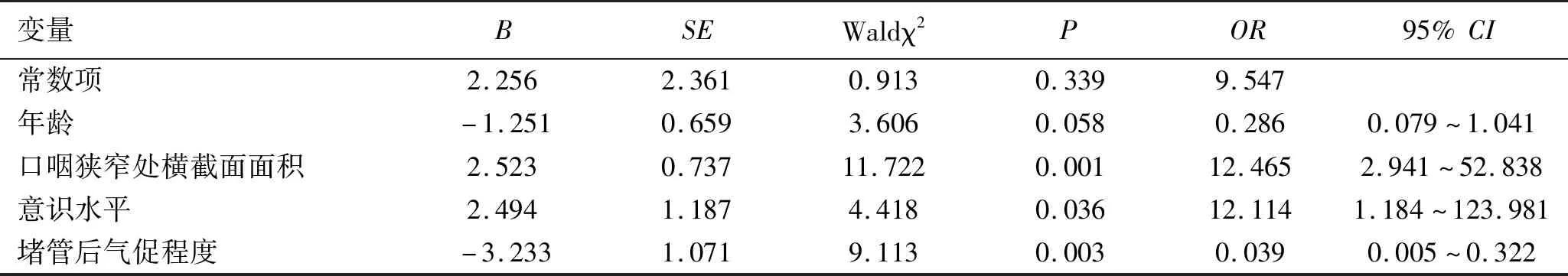
表3 影响重症脑损伤气管切开患者拔管成功与否的多因素Logistic回归分析
3 讨论
重症脑损伤患者的气切导管能否安全拔除,既要考虑自主呼吸情况,又要考虑完整气道的通畅性。研究发现,卒中患者呼吸肌力量只有健康人的50%左右[4]。行机械通气18 h以上的留置气切导管患者即可出现不同程度的呼吸肌和膈肌的萎缩[5]。对于已经脱离呼吸机辅助呼吸的患者,呼吸肌舒缩功能和气切导管的通畅性已能满足日常呼吸的安全性需要。此时,及时拔除气切导管既有助于行呼吸肌反馈训练,改善呼吸功能障碍[6]和减少卒中后呼吸肌无力所致气道分泌物排除困难的不利影响[7],又有助于去除抗生素难以有效杀灭气切导管气囊-管壁周围附着的细菌[8],从而利于减少抗生素的使用。
本研究选取16个可能影响气切导管拔除的因素进行分析,根据单因素分析结果显示,年龄、气切置管时间、舌体后坠、鼻咽后坠、口咽截面面积、吞咽能力、堵管后气促程度、意识水平、白蛋白共 9个因素与气切导管拔管成功与否有。进一步对这9个单因素行多因素Logistic回归分析显示,只有口咽狭窄处横截面面积、堵管后气促程度、意识水平与拔管成功率有关。
3.1 口咽狭窄处横截面面积因素 正常情况下上气道扩张肌(特别是颏舌肌)的有效收缩对保持咽部气道通畅至关重要[9]。重症脑损伤易致颏舌肌无力,患者平躺仰卧时出现舌体、舌根整体后坠,导致咽部气道通畅性下降,严重者完全堵塞。本文根据空气与颈部肌肉、骨骼密度差异性,采用颈椎CT平扫的方法,利用电脑进行矢状位、水平位阅片评估拔管前上气道口咽部是否通畅,筛查除外咽部气道完全堵塞者。在通畅的基础上,进一步分析通畅部位最狭窄处口咽横截面面积大小对拔管的影响,因为这直接决定着咽部气道的通气量大小。在气切导管的气囊充气而人为堵塞颈段气管时,呼吸通道依靠气切导管建立,因此,呼吸气体的出入量与气切导管内径截面面积[即S=π×(内径的半径)2]成正相关。本文患者均为留置内径为7.5 mm的气切导管,故气切导管内径横截面面积经计算为S=3.14×(7.5/2)2=44.15 mm2。据此,理论上咽部气道通畅部位最狭窄处的口咽横截面面积大小为44.15 mm2时也能满足正常呼吸需要。但通过研究发现,口咽横截面面积大小为44.15 mm2时均无法满足正常呼吸,当面积增大至88.30 mm2时,21例患者中只有4例拔管成功(19.05%),17例拔管失败(80.95%),口咽横截面面积大小为88.31~132.45 mm2之间时,20例患者中17例拔管成功,成功率为85.00%,3例失败,失败率为15.00%;当口咽横截面面积大小为132.46~176.6 mm2之间时,20例患者中19例拔管成功,成功率为95.00%,1例失败,失败率为5.00%;当口咽截面面积大小为176.7 mm2以上时,43例患者中42例拔管成功,成功率为97.67%,1例失败,失败率为2.33%,上述结果表明,口咽横截面面积越大,拔管成功率越高。因此,通过本研究数据表明,咽部气道通畅部位最狭窄处口咽横截面面积大小为88.31 mm2以上时拔管成功率明显增高,提示对气切导管的成功拔除具有临床指导意义;口咽横截面面积大小在132.46~176.6 mm2之间与口咽横截面面积大小在176.7 mm2以上时,拔管成功率相当,因此,口咽横截面面积大小在132.46 mm2以上时,认为临床拔管较为安全。而对于口咽横截面面积在88.30 mm2以下时无法满足正常的经口呼吸要求,导致气切导管拔管失败率高的原因可能与吸气过程中胸腔内负压增大,咽部最狭窄处的软组织发生“吸吮”作用,舌根进一步后坠而无法满足通气需求,临床上表现为拔管后患者当即出现明显的吸气困难或“三凹征”表现。
对于正常成人,颈段气管的直径为15~20 mm,对应的气管截面面积为176.6~314 mm2。当气管直径低于正常水平的 50%(即为7.5~10 mm)时会产生呼吸困难的现象[10],对应的气管横截面面积为44.16~78.5 mm2。故本文的结果也与之相符,区别在于颈段气管具有弹性支撑作用,而本文研究对象为咽部的软组织(肌肉等组织),更容易在吸气时胸腔负压增大而发生“吸吮”导致咽部气道狭窄、呼吸困难等情形发生。另外,留置气切导管的横截面面积为44.15 mm2(对应气切导管内径的直径7.5 mm)却能满足正常呼吸,分析的原因为其是硬质导管,不会发生如同软组织的“吸吮”作用,导致横截面面积变小。因此,临床上拔除气切导管前,建议行颈椎CT平扫评估咽部气道是否通畅以及通畅部位最狭窄处的测量口咽横截面面积大小,以提高拔管的安全性,同时也有助于预防清醒患者非计划性拔管所致的不良事件。
3.2 堵管后气促程度评估 本研究中,70例患者堵管后呼吸平稳,其中67例拔管成功(95.71%),3例拔管失败(4.29%)。这3例患者拔管后出现吸气时气切口发生“吸吮”、内陷导致呼吸困难情况,失败的原因分析与留置的气切导管时间长,导致气切口处的气管壁软化、失去弹性支撑引起颈段气道通气不足,造成拔管失败。上述结果表明,对于咽部气道通畅且行气切导管堵管后呼吸平稳的患者,其上气道至气切口处的通畅性能够满足正常呼吸需求,这类患者拔管是安全的。另外,34例患者堵管时出现呼吸费力情形,其中19例(55.88%)患者“剩余通气间隙”较宽却出现堵管后呼吸困难、拔管失败的情形是咽部气道狭窄处横截面面积过小(88.31 mm2以下17例,2例为89.4 mm2和90.2 mm2),而无法满足通气需求所致。另外15例患者中,经测量咽部气道狭窄处口咽横横截面面积大于88.31 mm2,占14例(其中88.31~132.45 mm2有3例,132.46~176.6 mm2有4例,大于176.7 mm2有7例),另外1例口咽横横截面面积为88.2 mm2,这15例(44.12%)拔管均成功,考虑呼吸费力的原因与气管内壁-气切导管外壁之间的“剩余通气间隙”狭窄以及封堵的气切导管堵塞气道导致通气量下降有关,予拔除气切导管后呼吸平稳、拔管成功;另有上述结果表明,堵管时出现呼吸费力情况,既可能与咽部气道狭窄处横截面面积小有关,又可能与留置的气切导管导致颈段气道“狭窄”引起通气量不足有关。因此,临床上仍应当重视评估堵管后气促的情况。相关文献也将堵管试验作为气切导管拔管的主要指标[11],本研究结论与之一致,是拔管的影响因素。
3.3 意识水平 本研究提示,清醒患者的气切导管拔管成功率高于昏迷患者。对比拔管成功组中清醒患者和昏迷患者之间咽部气道狭窄处横截面面积发现,两者之间的均值相当(清醒组为219.36 mm2,昏迷组为228.77 mm2);平均拔管时间清醒组为41.05 d,昏迷组为56.30 d。对比拔管失败组中清醒患者和昏迷患者之间咽部气道狭窄处横截面面积发现,两者之间的均值差异明显(清醒组为59.55 mm2,昏迷组为82.57 mm2);拔管时间对比,清醒组为27.17 d,昏迷组为73.13 d。上述结果一方面提示咽部气道狭窄处横截面面积处于88.31 mm2以下时,拔管难以成功,另一方面也提示了清醒患者的拔管时间短于昏迷患者。换言之,昏迷患者拔管难度较大,拔管失败率(38.10%)高于既往研究(重症脑损伤患者格拉斯哥昏迷评分<8分时,拔管失败率为2%~25%情形)[12]。原因分析考虑与重症脑损伤伴意识障碍时容易出现舌根后坠,引起咽部气道机械性梗阻有关。另有研究也提示部分高血压脑出血患者容易发生舌后坠使肺通气功能下降[13]和卒中疾病因咽部气道塌陷导致低通气,发生阻塞性睡眠呼吸暂停综合征[14]有关。因此,临床上建议尽可能在意识水平恢复情况下拔管较为安全。同时,本研究也提示,昏迷状态并非拔管的禁忌证,只要患者气道分泌物明显减少,咽部狭窄处气道的通气横截面面积大于88.30 mm2、堵管试验无明显气促或者排除留置的气切导管所致“剩余通气间隙”不足引起的呼吸困难,仍可试行拔除气切导管。
4 结论
重症脑损伤患者气切导管的拔除,本研究认为应当遵循优先保证患者安全为主要原则的拔管方案。本研究通过选取16个可能影响重症脑损伤患者拔除气管导管的相关因素进行分析后认为,口咽狭窄处横截面面积、堵管后气促程度、意识水平是相关影响因素,对日后安全拔除气切导管具有一定的临床指导意义。但本文也存在研究样本相对较小,不排除其他因素也参与其中,还有待于通过大样本的数据来进一步分析研究,以期进一步提高临床拔管安全性。

