经胸超声心动图诊断儿童肺动脉异常起源的价值
周 婕, 罗 红
(四川大学华西第二医院 超声科,出生缺陷与相关妇儿疾病教育部重点实验室,四川 成都 610041)
肺动脉异常起源是一类罕见的先天性心血管畸形,主要包括以下3类:肺动脉吊带(pulmonary artery sling, PAS)、单侧肺动脉起源异常(anomalous origin of unilateral pulmonary artery, AOPA)以及先天性单侧肺动脉缺如(unilateral absence of pulmonary artery, UAPA)。此类疾病既可单独发生也可合并其他心内畸形[1-2],因早期临床表现不典型而易被忽视或误诊。尽管计算机体层血管成像(computed tomography angiogrphy,CTA)CTA是影像学诊断肺动脉异常起源的金标准,但其价格相对高昂,且具有辐射,非临床常规选用筛查肺动脉异常起源的检查方式,而超声心动图具有实时、直观、安全及价格相对低廉等优势,常为临床首选。本文旨在总结患儿肺动脉异常起源的经胸超声心动图(transthoracic echocardiography, TTE)特征及分析其误诊原因。
1 资料与方法
1.1 一般资料 回顾性分析2018年1月至 2021年6月在我院经TTE检查诊断为肺动脉异常起源的24例患儿超声心动图表现及CTA检查结果,其中男14例,女10例,年龄1d~12岁。
1.2 仪器与方法 应用Philips EPIQ 7C彩色多普勒超声诊断仪,探头频率2.5~5.6 MHz。患儿在安静状态下取左侧卧位或平卧位,对每例患儿行完整的经胸超声心动图检查,重点观察肺动脉分叉结构,对无正常分叉者多方位多切面仔细检查,仔细探查单侧肺动脉的有无,未见正常左肺动脉者,应着重探查右肺动脉有无多余血管发出及尽量全段显示升主动脉至主动脉弓降部,观察其间有无异常血管发出,以判定单侧肺动脉异常为缺如还是起源位置的异常,并观察有无合并其他心内畸形。
2 结果
2.1 TTE及CTA诊断结果 24例患儿均合并其他心内畸形。24例肺动脉异常起源患儿的TTE及CTA检查结果见表1。24例CTA证实的肺动脉异常起源患儿中,PAS 12例,其中完全型11例(图1),合并气管受压5例;部分型1例(图2)并合并气管受压;AORPA 3例(图3),其中2例起自于升主动脉近端,均并发肺动脉高压,包括Berry综合征1例;1例起自于无名动脉远端,该例在我院产前超声检查中诊断提示;UPAP 9例(图4),其中右肺动脉缺如(RUPAP)5例,右肺动脉缺如(LUPAP)4例。TTE正确诊断21例,诊断符合率87.5%。其中PAS诊断准确率为91.6%,AORPA诊断准确率为100%,UPAP诊断准确率为77.7%。TTE误诊3例,包括2例LUPAP误诊为完全性PAS及1例完全性PAS误诊为LUPAP。
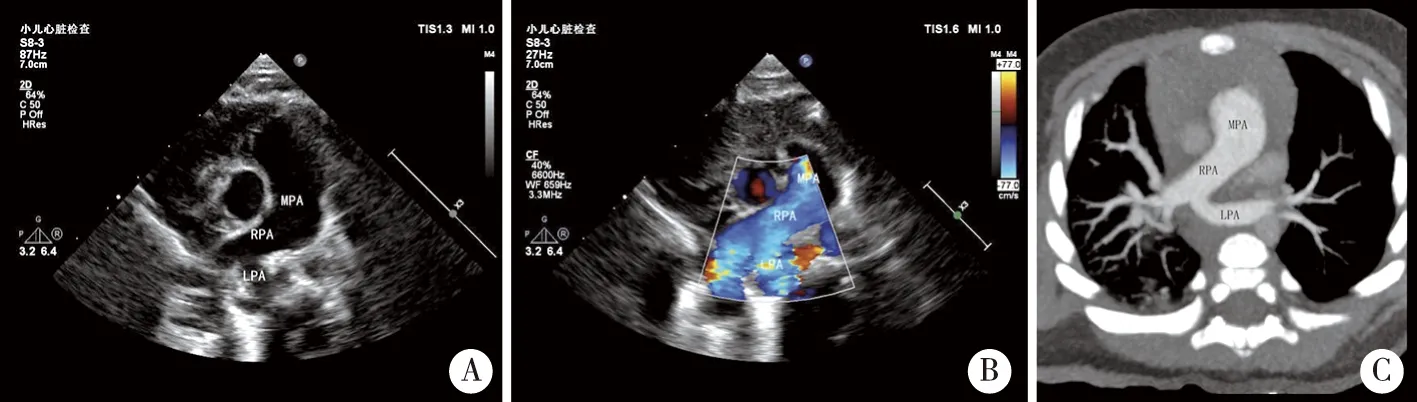
A、B:经胸超声心动图示主肺动脉直接延续为右肺动脉,左肺动脉于右肺动脉后侧方发出,右肺动脉血流进入左肺动脉; C:患儿CTA薄层扫描证实左肺动脉完全起源于右肺动脉。图1 4个月女性患儿完全型肺动脉吊带
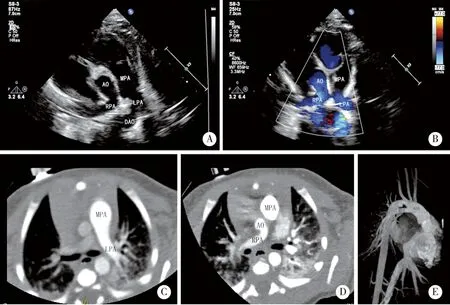
A、B:经胸超声心动图示主肺动脉仅见左肺动脉延续,右肺动脉起源于升主动脉近端; C、D:患儿的CTA薄层扫描分别显示主肺动脉仅见左肺延续及右肺动脉起自升主动脉左后壁; E:患儿的CTA最大密度投影证实右肺动脉起源于升主动脉近端。图3 11 d男性患儿右肺动脉起源于升主动脉
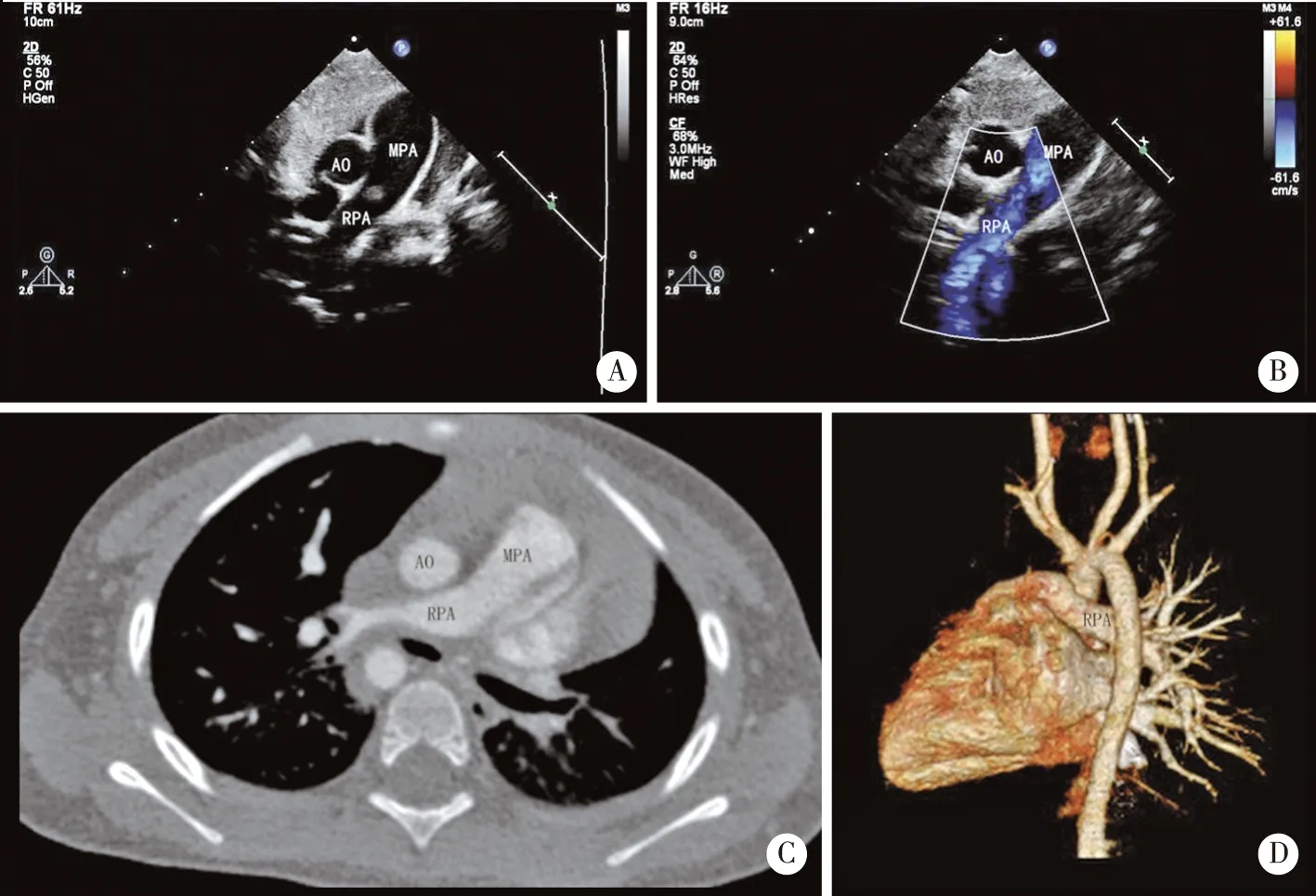
A、B:经胸超声心动图示主肺动脉仅见右肺动脉延续; C、D:分别为该患儿的CTA薄层扫描及CTA三维成像(后面观)证实左肺动脉缺如。图4 1岁女性患儿左肺动脉缺如
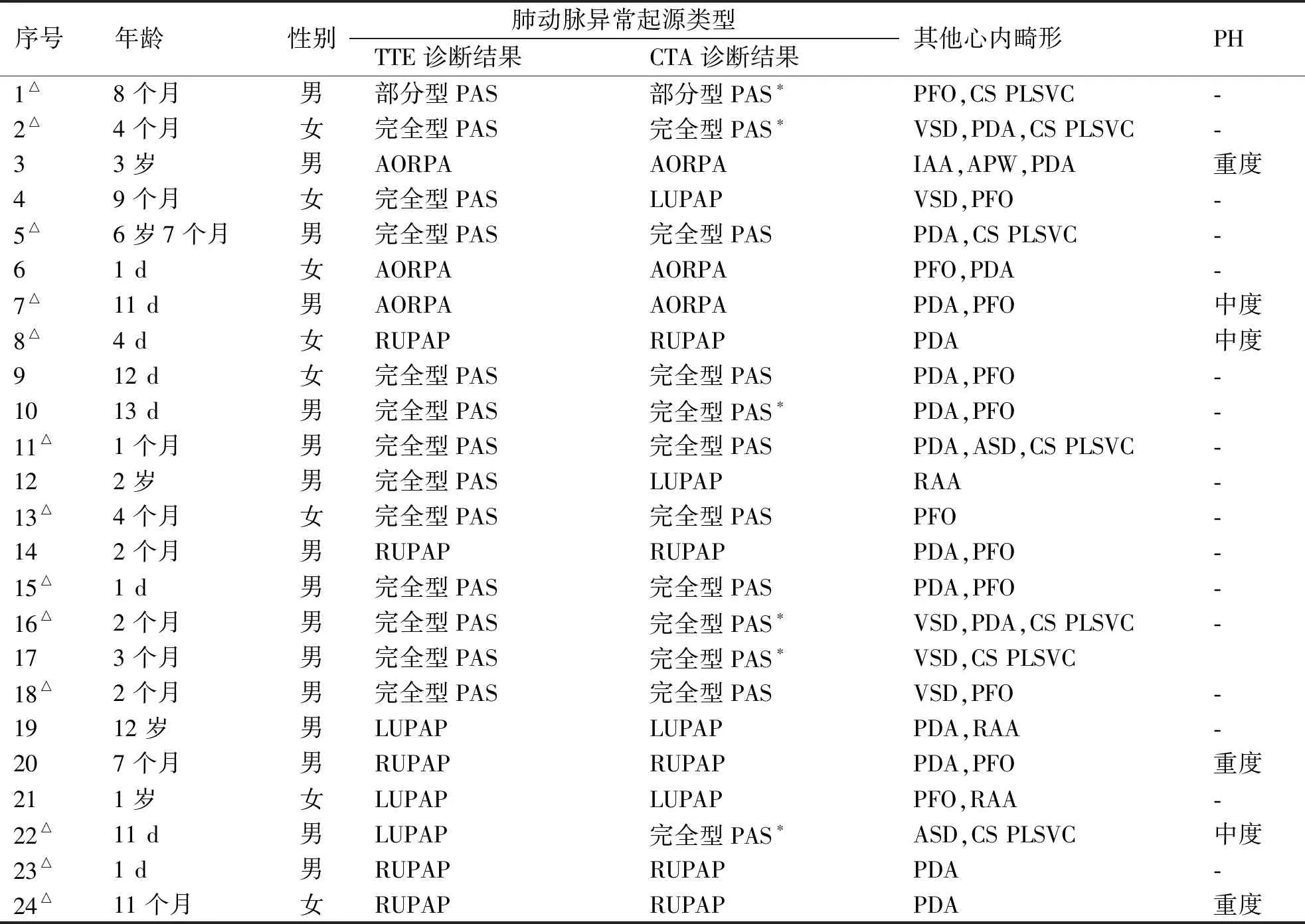
表1 24例肺动脉分支发育异常患儿的TTE及CTA检查结果
2.2 TTE诊断特征 肺动脉异常起源的TTE共同特点如下:(1)具有独立的主、肺动脉瓣;(2)多切面连续扫查无正常肺动脉分叉结构。其中完全型PAS表现为主肺动脉直接延续为右肺动脉,左肺动脉起源于右肺动脉后侧壁,在胸骨上窝切面右肺、左肺动脉呈大小眼征象。而部分型PAS除可见一支动脉起源于肺动脉主干外,还可见一支血管源于右肺动脉,内可探及动脉频谱。AOPA仅见单侧肺动脉分支为主肺动脉的延续,而另一侧肺动脉起源于主动脉且多合并肺动脉高压。UPAP表现为主肺动脉仅与一侧肺动脉相延续;胸骨上窝切面彩色多普勒可显示于主动脉弓及降主动脉起始处可探及侧枝血管向肺动脉缺如侧肺门走行。
3 讨论
肺动脉异常起源主要包括PAS、AOPA及UAPA 3类。它可以单独发生或与其他心内畸形合并发生,由于病理解剖结构不同,手术治疗和预后也不同[2]。TTE为临床诊治心血管疾病的常用手段,在肺动脉异常起源的诊治中起了重要作用。本研究共纳入24例经CTA证实的肺动脉异常起源患儿,TTE整体诊断符合率为87.5%,说明TTE是诊断该类疾病的有效检查手段,但必要时仍需行CTA进一步明确诊断。
PAS解剖表现为左肺动脉起源于右肺动脉,绕行右支气管,向左走行于气管和食道之间,并形成气管周围的部分吊带,从而可能使这些结构受压,可出现咳喘等呼吸道症状[3-4],其受累情况需CTA加以明确。PAS的胚胎学异常被认为是发育期支气管树的尾端毛细血管和来源于右侧第二弓衍生出的支配动脉相连续形成[5]。超声检查通常将其分为完全型和部分型,完全型指左肺动脉主干从右肺动脉发出,而部分型相对少见,指左肺动脉仅部分动脉从右肺发出,以左下肺动脉起源异常多见[6]。本研究12例PAS患儿中11例为完全型,仅1例为部分型,该例即为左下肺动脉异常起源。12例PAS中经CTA检查有6例存在支气管受压表现。研究表明,PAS患者常合并其他心内畸形,未经治疗的PAS具有很高的发病率和死亡率,其中大部分是由于气道和其他相关异常所致而不是异常动脉本身,未合并严重心内畸形的PAS患者术后效果良好[7]。本研究中,所有PAS患儿均合并其他心内畸形,与既往研究报道基本一致。超声心动图可清晰显示主肺动脉及左、右肺动脉近段结构与走行,当发现左肺动脉未显示,而在右肺动脉近端后方发出一呈“之”字形向左方走行的血管时,大多数完全型PAS能明确诊断[8-9]。本研究中PAS诊断准确率为91.6%,仅误诊1例,回顾分析该病例误诊原因为该病例较其他典型完全型PAS而言,其左肺动脉起源于右肺动脉处相对更远,超声心动图未能显示该处,故误诊左肺动脉缺如。另外,就本研究诊断的1例部分型PAS而言,该患儿因“反复咳喘”于我院就诊行超声心动图诊断为部分型PAS。该例患儿既往于外院漏诊PAS,笔者的经验是呼吸道症状是诊断肺动脉吊带的重要信号,即使存在肺动脉分叉结构,但当其分叉走行异常或者单支肺动脉内径异常时,仍需仔细扫查右肺动脉有无异常分支发出,以防漏诊部分型PAS。
AOPA的发生率占所有先心病的0.12%[10],根据其病理解剖改变,可分为AORPA及AOLPA,其中右侧起源异常的发生率高于左侧,为5~6倍[11]。本研究中,3例AOPA均为AORPA。目前认为AOPA是由于胚胎发育时第6主动脉弓发育异常所致[2]。未接受外科修复治疗的AOPA患者1年内死亡率高达70%[10],其主要原因在于该疾病导致的肺动脉高压和不可逆性肺血管疾病[10-11]。AORPA患者常合并其他心脏畸形,以PDA常见,而AOLPA患者常合并主动脉弓发育异常[10]。本组资料的3例病例中,1例新生儿期死亡;1例仅合并PDA以及中度肺高压,行手术治疗后情况良好;1例合并IAA、APW、PDA即为Berry综合征,就诊时年龄已为3岁,合并重度肺高压,该例因病情严重及家庭经济原因放弃治疗,不久后便死亡,也证实了该病未治疗的高死亡率。笔者的经验为肺动脉高压是AOPA的显著特征,典型征象为主肺动脉仅向一侧延续,并同时观察到主动脉有异常血管发出并向对侧肺部走行,内可探及动脉频谱。
UAPA发生率1/300 000~1/200 000[2,12],胚胎发生机制为近端第6主动脉弓的退化和肺动脉远端及第5主动脉弓的远端持续连接造成[12],很少孤立发病,常合并其他心内畸形,包括ASD/PFO、PDA及VSD等[12-13]。有学者研究表明,约45%此类患儿合并肺动脉高压[14]。目前,对UAPA的治疗尚无共识,常综合有无并发症、肺动脉解剖、主肺侧支循环及是否存在肺高压等情况决定治疗方式,预后亦取决于相关的心血管异常和肺高压的程度等情况[15]。本研究中UAPA共计9例,肺动脉高压发生率约33%,合并心内畸形包括PDA、VSD、PFO、CS PLSVC及RAA,与既往报道基本一致。UAPA应主要与PAS相鉴别,本研究中TTE诊断UAPA的准确率为77.7%,2例LUPAP被误诊为完全型PAS。误诊原因为未正确区分右肺动脉旁紧邻血管究竟为侧枝循环还是异常起源的左肺动脉。当未见左肺动脉从主肺动脉延续,而紧邻右肺动脉处又发现异常血管时,应多切面与多角度的以二维为基础,彩色血流为辅助寻找该血管与右肺动脉的真实关系并尽量观察该血管的走行而做出正确的诊断。
综上所述,超声心动图是诊断肺动脉异常起源的重要影像学检查手段,其可明确或提示诊断肺动脉异常起源的具体类型,可作为临床筛查此类疾病常用且便捷的检查方法。
本研究样本量相对较少,需进一步扩大样本量来观察TTE对肺动脉异常起源的诊断效能;未进行术前术后超声心动图随访研究,进一步的深入研究可用于评估超声心动图在临床管理此类疾病的价值。

