自身免疫特征的间质性肺炎肺功能障碍的相关因素研究
赵书山,张春意,岳丽霞
间质性肺病(ILD)是以弥漫性肺实质、肺泡炎症和间质纤维化为病理基本病变,以活动性呼吸困难为临床表现的不同种类疾病群构成的临床-病理实体的总称。ILD 病因复杂,可为特发性。此外,环境因素、职业因素、药物因素以及遗传因素也与ILD的发病有关,继发性ILD最常见的病因是系统性疾病,如结缔组织病(CTD)[1]。特发性ILD 和继发性ILD的临床进程、治疗策略及预后不同[2]。然而,有时CTD-ILD 很难做出明确诊断,因为ILD 可能是某些CTD 的唯一表现,或者CTD 相关症状不明显[3]。在没有明确CTD 的情况下,10%~20%的特发性ILD患者存在与自身免疫相关的症状和血清学异常[4]。为了区分特发性或与“隐性”CTD 相关的ILD,2015年欧洲呼吸学会和美国胸科学会工作组提出了“自身免疫特征的间质性肺炎(IPAF)”的分类标准[5]。IPAF 可能是一种异质性疾病,但关于IPAF 的研究结论存在差异,尚不清楚IPAF是一种独特的临床综合征还是特发性ILD[6],IPAF 的管理仍然知之甚少。目前关于IPAF的研究多为短期、单中心的回顾性研究。因此本研究开展了纵向观察性研究,目的是探讨IPAF患者的临床特征,分析肺功能障碍的危险因素,并评估药物的治疗干预作用,现报道如下。
1 资料与方法
1.1 一般资料 本研究采用纵向观察性研究,收集2021 年1 月至2022 年10 月在绍兴市人民医院就诊的门诊和住院IPAF 患者73 例,所有患者均符合2015 年欧洲呼吸学会和美国胸科学会工作组提出的“IPAF”分类标准[5]。纳入标准:IPAF 的诊断必须满足2 个先决条件:患者必须有肺高分辨率CT(HRCT)成像和/或外科肺活检证实的间质性肺炎证据;排除已知原因引起的间质性肺炎,且不符合CTD的诊断标准。诊断标准包括:(1)临床表现:包括特征性的肺外表现;(2)血清学:包括特征性的自身抗体;(3)形态学:包括特征性的胸部影像特点、肺组织病理特点或生理特点。IPAF 患者必须满足所有先决条件,并且3 个项目诊断标准中应至少具备2 个项目的表现(每个项目至少有1 个特征)。排除标准:(1)既往患有过敏性肺炎、放射性肺炎、尘肺、肺泡蛋白沉积症、结节病、严重感染、肺结核、肿瘤、妊娠或哺乳期妇女;(2)药物引起的ILD 及特发性ILD;(3)有严重心、脑、肾等并发症及合并其他严重原发病、精神病患者。
1.2 方法 主要观察指标:(1)肺功能障碍:定义为用力肺活量(FVC)相对于前一次就诊至少下降5%,在基线和至少每6 个月进行一次肺功能及肺HRCT检查。(2)基线变量:①社会人口特征;②临床特点;③IPAF 分类标准项目;④肺功能检查;⑤ILD 影像分型;⑥治疗用药:IPAF 诊断前3 个月内以及在随访期间使用糖皮质激素,IPAF 诊断前3 个月内以及在随访期间使用改变病情抗风湿药物(DMARDs),传统DMARDs 包括硫唑嘌呤(AZA)、霉酚酸酯(MMF)、甲氨蝶呤(MTX)、来氟米特(LEF)、钙调磷酸酶抑制剂(他克莫司、环孢素)和羟氯喹(HCQ),靶向合成或生物DMARDs 包括TNF抑制剂(TNFi)、利妥昔单抗(RTX)、托珠单抗(TZL)及托法替布等,抗肺纤维化药物包括吡非尼酮或尼达尼布。
1.3 统计方法 采用SPSS 22.0 统计软件进行分析,符合正态分布的计量资料以均数±标准差表示,不符合正态分布的计量资料以M(P25,P75)表示;计数资料采用检验。生存曲线采用Kaplan-Meier 法,并采用Log Rank 检验。随访期间将出现肺功能障碍作为因变量,先将某一自变量与因变量进行单变量Cox回归分析,如果自变量有统计学差异则引入多变量Cox回归分析,用比值比(OR)及95%置信区间(CI)估计临床各变量与出现肺功能障碍的联系强度。P<0.05 表示差异有统计学意义。
2 结果
2.1 IPAF 患者临床表现、血清学和形态学分析IPAF 最常见的临床表现为关节炎(30.1%)、皮疹(23.3%)和雷诺现象(16.4%);最常见的血清学表现为ANA 阳性(84.9%)、抗SSA阳性(27.4%)和RF >2 倍正常值(9.6%);肺CT 最常见的表现为NSIP(47.9%)和UIP(39.7%),见表1。
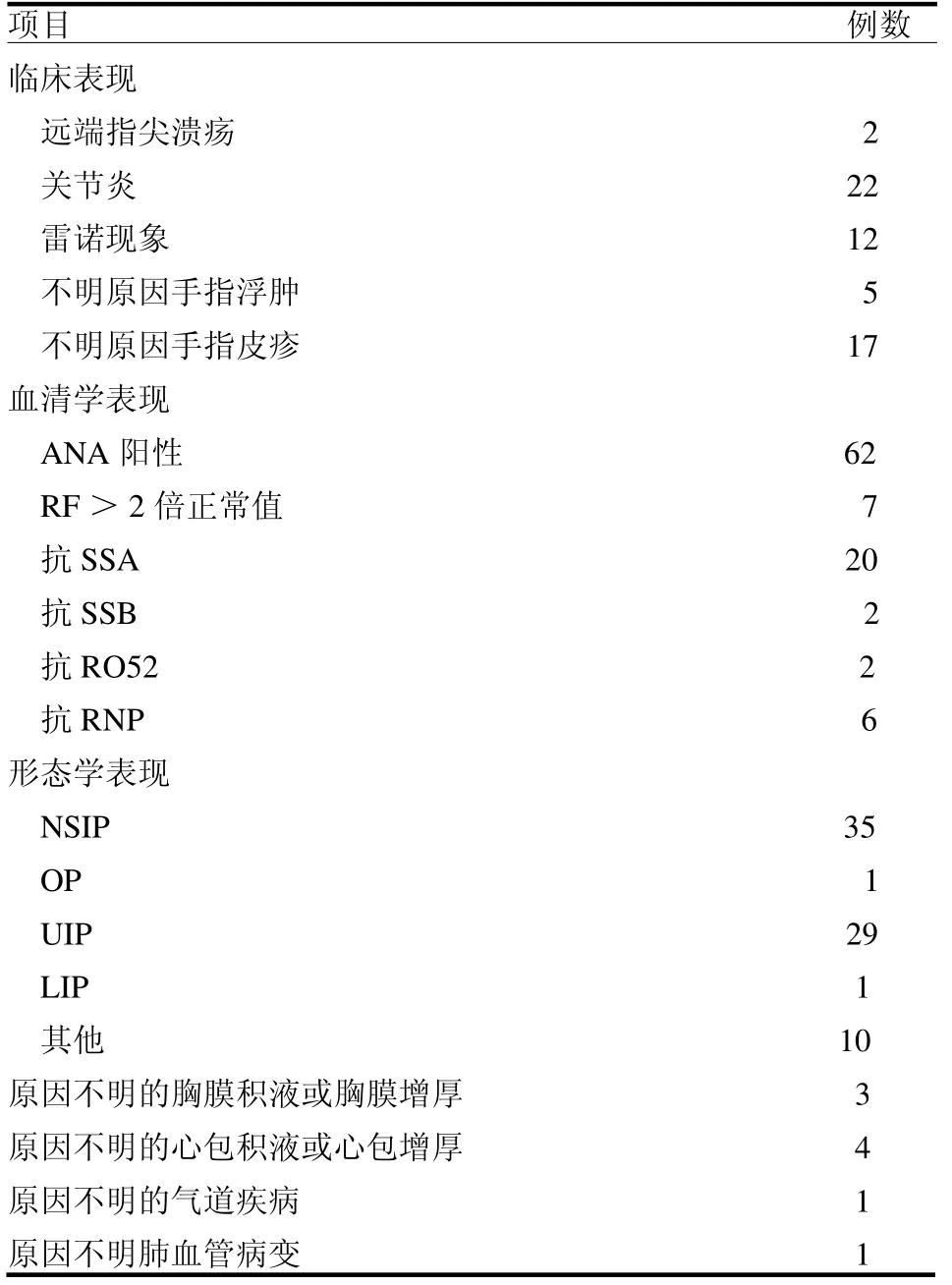
表1 73 例IPAF 患者分类诊断表现
2.2 IPAF 患者用药情况分析 研究期间,64.4%的患者接受糖皮质激素治疗;61.6%的患者应用传统DMARDs(MMF 21 例,钙调磷酸酶抑制剂8 例,HCQ 19 例,LEF 2 例,AZA 2 例);1 例患者使用生物制剂(IL-6R 抑制剂1 例);1 例患者使用靶向合成DMARDs(托法替布1 例);13.7%的患者使用抗肺纤维化药物(吡非尼酮6 例,尼达尼布4 例)。
2.3 ILD 影像分型与肺功能障碍的关系 63%的IPAF 在随访中出现肺功能障碍。Kaplan-Meier 生存分析显示,肺部UIP表现与肺功能障碍有关,差异有统计学意义(=17.538,P <0.05,HR=3.756);而NSIP 与肺功能障碍差异无统计学意义(=0.303,P>0.05,HR=0.846);UIP 肺功能障碍率明显高于NSIP,见图1。

图1 ILD 影像分型与肺功能障碍的关系
2.4 IPAF 患者肺功能障碍危险因素分析 以IPAF患者是否发生肺功能障碍(有=1,无=0)为因变量,纳入年龄、性别、吸烟史、血清学抗体、ILD影像分型及治疗药物进行单因素Cox生存回归分析,结果显示:年龄>60 岁及UIP 为肺功能障碍的危险因素(均P<0.05),抗SSA 抗体、MMF 应用为肺功能障碍的保护性因素(均P <0.05)。多因素Cox 回归分析,仍发现UIP为肺功能障碍的独立危险因素,MMF治疗是肺功能障碍的保护性因素,见表2。

表2 IPAF 患者肺功能障碍与临床变量的多因素Cox 回归分析
3 讨论
IPAF 在其自身的定义中是一种异质性疾病,其用来描述一个同时患有间质性肺炎和从临床、血清学、肺部形态学特征推测存在潜在的自身免疫状况的疾病患者。IPAF 具有其自身特点,不属于某一特定的CTD,也有别于特发性间质性肺炎。本研究发现IPAF最常见的临床表现是关节炎、皮疹和雷诺现象;最常见的血清学表现是ANA 阳性、抗SSA 阳性和RF >2 倍正常值。有研究报道,IPAF 患者以女性为主,年龄通常>60 岁,最常见的临床和血清学表现为关节症状和血清ANA 抗体阳性[7],这与本研究相符。值得注意的是,对症状的评估需要综合病史及专科医师体格检查,而不能仅仅依靠患者主观陈述来判定。
有研究发现HRCT 中NSIP 型占31.9%,外科肺活检的病理类型中NSIP型和OP型分别占22.9%和16.9%[7]。多项研究表明HRCT 最常见的模式均为NSIP 型[8],这与本研究结果相符。诊断标准中HRCT或外科肺活检病理类型均除外UIP 型,而UIP 型是特发性间质性肺炎中最为常见的类型,不少回顾性研究发现形态学表现为UIP 型的IPAF 患者占一定比重,所以有学者建议将UIP 列入形态学诊断标准中,值得商榷。
ILD 以限制性通气障碍为特征,主要表现为FVC 明显下降[9]。在无支气管阻塞或肺气肿的情况下,FVC是限制性通气模式的特异性指标,与纤维化相关。而肺一氧化碳弥散量(DLCO)是肺泡炎、通气血流比例失调、血管受累和纤维化的指标[10]。DLCO特异性较低且可靠变化可能发生非常缓慢,有时需要长达数年的变化。所以本研究选择FVC 作为主要终点更能反应IPAF 患者肺功能变化。在本研究中,63%的IPAF 在随访中出现肺功能障碍。IPAF 在疾病的最初几年出现进展,因为50%的患者在IPAF诊断1 年内出现肺功能障碍。本研究分析了IPAF 出现肺功能障碍的相关危险因素。单因素分析显示,年龄>60 岁及UIP 为肺功能障碍的危险因素。但多因素Cox 回归分析发现UIP 为肺功能障碍的独立危险因素。UIP 模式被认为与IPAF[11]和CTD-ILD[12]的死亡风险增加有关。与CTD-ILD 相似,IPAF 具有显著异质性,可存在不同的亚型,从而预后不同。与特发性ILD 相似,表现为UIP 型的IPAF 患者预后不佳。如果能及早识别异质性和高危因素,对如何管理患者、指导治疗和改善预后有重要的临床价值。
在治疗方面,IPAF 存在明显的个体差异并缺乏标准治疗,通常会使用治疗CTD-ILD的药物和抗纤维化药物。治疗决策需要多学科参与,要综合考虑患者的健康状况、肺外疾病以及ILD的严重程度等。有研究报道了56 例接受治疗的IPAF 患者,其中38例(67.9%)患者接受糖皮质激素治疗,16 例(28.6%)患者接受免疫抑制剂治疗,仅有3 例(5.4%)进行抗纤维化治疗[7]。一项小型观察性研究显示,糖皮质激素和MMF 对IPAF 有益[13]。有临床试验证实抗纤维化药物对IPAF 有积极的治疗作用[2]。本研究发现MMF 治疗是IPAF 肺功能障碍的保护性因素。这表明IPAF 与特发性ILD 相比,自身免疫特征相关的ILD 存在不同的发病机制[14]。有研究也表明MMF可减少IPAF 肺功能障碍进展[7],这与本研究结果相符。有研究认为应该在进展性纤维化表型ILD 患者使用糖皮质激素。但本研究发现糖皮质激素治疗没有影响IPAF 患者的肺功能。本研究也评估了不同抗体对预后的作用,单因素分析显示抗SSA 抗体的存在与肺功能进展风险减少相关,但多因素分析没有发现相关性。
本研究局限性在于样本量偏小。尽管如此,本研究提供了该领域真实世界的研究证据。笔者认为IPAF 患者随着病程的延长会出现肺功能障碍,进而影响患者的预后。UIP 是肺功能障碍的独立危险因素,相对于糖皮质激素,MMF 治疗有利于肺功能。这些结论可能有助于临床医生的日常实践。治疗IPAF 患者应倾向于类似CTD-ILD 的免疫抑制剂疗法,还是特发性肺纤维化的抗纤维化疗法,可能与其形态学特征密切相关。如NSIP 型可能对免疫抑制剂疗法更有效,UIP 型可能更倾向于抗纤维化疗法。关于IPAF 治疗干预仍需要大样本的前瞻性研究。
利益冲突所有作者声明无利益冲突
作者贡献声明赵书山:实施研究、论文撰写;张春意:数据整理、统计学分析;岳丽霞:研究指导、论文修改

