老年髋部骨折围术期营养不良风险综合管理策略研究进展
黄黎银 张颖 曹治东
世界卫生组织数据显示,2019 年,全球60 岁及以上人口达10 亿。到2030 年,这一数字将增至14 亿,到2050 年将增至21 亿[1-2]。随着人口老龄化加剧,我国每年约有100 万人发生髋部骨折,其中大部分为老年人,一旦发生髋部骨折,其致残致死风险极高,严重威胁老年人生命健康[3]。
欧洲肠外肠内营养学会 (European society of parenteral and enteral nutrition,ESPEN) 将营养不良 (malnutrition) 定义为蛋白质、碳水化合物等营养素缺乏或过量,包括营养不足和过剩两个方面。可使用两种标准来判断老年人营养不良,一是表型标准,指非意志性的体重减轻,肌肉质量减少,或低体质量指数 (body mass index,BMI);二是病因学标准,如严重疾病,特别是同时伴随炎症,以及食物摄入量减少和 (或) 吸收不良等情况[4]。相关研究指出,营养不良在发生髋部骨折的老年人中普遍存在,因评估工具差异,其发生率为 7%~70% 不等,与同年龄人群亚组相比,髋部骨折患者在入院前即更可能存在营养不良[5-6]。营养不良可导致老年髋部骨折患者病死率增加、住院时间延长、并发症增多等严重后果,对老年人健康结局和生活质量造成严重不利影响[7]。因此,对于老年髋部骨折患者,应准确识别营养不良风险、及早预防并及时干预。
笔者以“老年人”“髋部骨折”“营养”中文检索词检索中国知网、中华医学期刊全文数据库、万方医学网、医脉通临床指南决策网等中文数据库和网站,以“hip fractures”“aged”“nutrition”英文检索词检索 JBI(joanna briggs institute) 循证卫生保健中心、美国国立临床诊疗指南数据库、BMJ Best Practice、Cochrane library、PubMed 等外文数据库,检索相关研究。基于欧洲临床营养和代谢学会 2022 年老年患者临床营养和水化指南[8]、中国老年患者肠外营养和肠内营养指南[9]、2018 年老年患者围术期管理北京协和医院专家共识[10]、Cochrane 老年人髋部骨折术后营养护理荟萃分析[11]、苏格兰校际指南网(Scottish intercollegiate guidelines network,SIGN) 老年髋部骨折的管理国家临床指南[12]等内容,撰写此综述,目的在于完善老年髋部骨折患者的动态营养评估,识别潜在营养不良风险,通过积极干预规避或降低风险,改善老年髋部骨折患者的预后。
一、营养不良的危险因素
老年营养不良的发生原因尚不明确,多由复合因素引起。近年来,基于大样本的研究和构建预测模型识别营养不良风险成为老年营养学领域研究的热点。笔者主要从生理功能、疾病、社会心理等方面进行危险因素总结。
1.生理学因素:年龄本身就是营养不良一个确定的不可逆的风险因素[8,13]。年龄增大导致的生理变化,如味觉和嗅觉受损、胃顺应性下降、食欲下降等问题都可能会缓慢地引起或加重营养不良。年龄的增长和疾病风险、营养问题的发生呈正相关,所以应重视年龄引起的老年综合征评估[14]。Bardon 等[13]纳入了欧洲、北美等地区社区营养不良老人进行荟萃分析,指出女性由于寿命更长,发生营养不良的风险比男性高 45%。另外还指出,随着年龄增长,引起的食欲下降与抑郁症、认知能力下降、咀嚼及吞咽困难、感官变化等引起营养不良的因素息息相关。
2.疾病因素:Kiess 等[15]将德国四所老年研究中心的数据进行回顾性分析指出,从器官功能方面来说,呼吸系统和消化系统疾病与营养不良关系最密切,主要与疾病引发炎症导致能量需求增加和严重疾病本身引起的能量消耗有关。欧洲知识中心通过对 33 名老年营养专家开展德尔菲访谈,构建了名为 DoMAP 的老年人营养不良决定因素模型,该模型指出任何可引起低摄入、高需求和营养生物利用度受损的因素都是风险因素。一项系统综述探究了口腔健康与营养不良的关系,指出牙齿减少、唾液量少、口腔溃疡、牙周病、口干等问题与营养不良显著相关[16-17]。Torbahn 等[18]则对来自全球的 11 923 名疗养院居民进行调查发现,合并疾病数量、用药种类和数量、自理能力等是营养不良的重要预测因素。癌症与住院患者发生营养不良密切相关,这取决于若干因素,包括肿瘤类型、疾病分期、与治疗有关的副作用和营养治疗不足。此外,心力衰竭或糖尿病等常见疾病,也被报道会增加营养不良的发生率[19]。
3.社会心理因素:Besora 等[20]从社会经济学角度探究了 61 818 名老人发生营养不良的原因,指出独居、丧偶、文化程度低等是重要影响因素。酗酒、吸烟等不良生活习惯是营养不良的常见独立风险因素。心理方面,抑郁、孤独情绪被报道是营养不良的独立影响因素[19]。
探究老年髋部骨折患者发生营养不良的危险因素时,除了关注老年人共性的风险因素外,还应特别注意创伤、手术应激、围术期营养支持的方式和时机、骨折导致的自理能力下降、卧床导致排便障碍、疼痛、药物使用、心理应激等方面的影响[21-22]。老年髋部骨折患者营养不良常由内在危险因素和外在促成因素间相互作用引起,在识别风险因素时,应进行动态、详细、全面的评估。
二、营养不良的筛查与评估
营养筛查评估是识别营养不良、判断是否需要营养干预的重要手段。适用于老年人的筛查工具需要关注老年营养不良的最重要风险因素,以便不仅能诊断明显的营养不良,而且捕捉到发生营养不良的风险。对于老年髋部骨折患者,在围术期及时开展营养评估,可以识别营养不良问题,从而采取科学的营养支持策略。目前,已有多种营养评估筛查工具被报道。各种筛查方法仅在特定患者群体中被证明其有效性和可靠性。笔者主要综述相关研究中用于老年髋部骨折患者营养筛查的三个工具。
1.营养风险筛查量表 (nutrition risk screening,NRS)2002:ESPEN 建议应使用 NRS 2002 筛查所有住院患者营养状况。该量表由疾病相关、营养状态、年龄三个部分的评分构成,≥3 分即说明存在营养不良风险,需要采取有效的营养支持策略 (图1)[4]。该量表将髋部骨折纳入了疾病相关的评分项,同时将 70 岁以上列为了年龄加分项,因此适用于老年髋部骨折患者[23]。但该量表纳入的疾病种类有限,这在一定程度上忽略了老年患者多病共存的实际情况。同时,相关研究也指出,该方法的评估结果和评估者的主观判断显示出强相关性,这就意味着该量表的稳定性、可操作性可能并不优于其它筛查工具[24]。该量表用于老年髋部骨折营养评估时,可能需要具备多学科知识的专业人员进行。
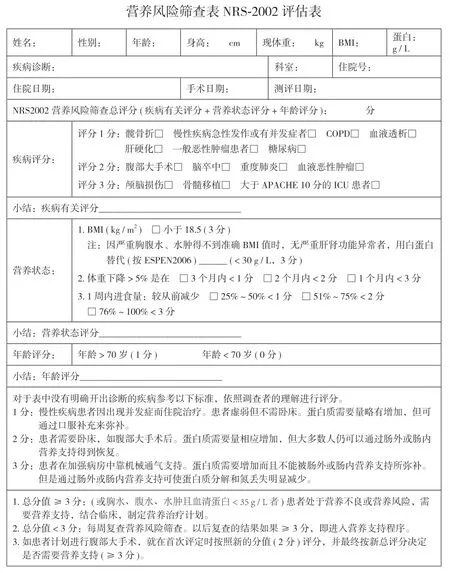
图1 营养风险筛查 NRS-2002 评估量表Tab.1 Nutritional risk screening 2002,NRS-2002
2.微型营养评定精法 (mini nutritional assessmentshort form,MNA-SF):微型营养评定法 (mini nutritional assessment,MNA) 是 ESPEN 推荐适用于老年人的筛查工具之一,该量表由 4 个部分、18 个条目组成,有营养筛查和评估两方面功能 (图2)[4]。MNA-SF 在 MNA 的基础上简化而来,操作更加简便、快捷且易于操作,是 MNA 的营养筛查部分。该量表主要由6 个问题组成,评分 ≥12 分,表示营养状况良好,不需要后续评估;评分 <11 分,需执行完整版 MNA。MNA-SF 对营养不良的诊断具有良好的特异性和敏感性,是专门适用于老年人群的评估工具[25-26]。Inoue 等[27]将 MNA-SF 用于老年髋部骨折患者的营养筛查,指出该量表是预测急性期老年髋部骨折患者术后结局最理想的营养筛查工具。更有研究指出,MNA-SF 涵盖了功能、心理和认知方面的综合评估,可以较全面地反映老年髋部骨折患者的特征,是髋部骨折患者临床结局最合适的营养筛查工具[28]。MNA-SF 只需几分钟即可完成,因此对于骨科护理单元来说,更易于使用和推广。
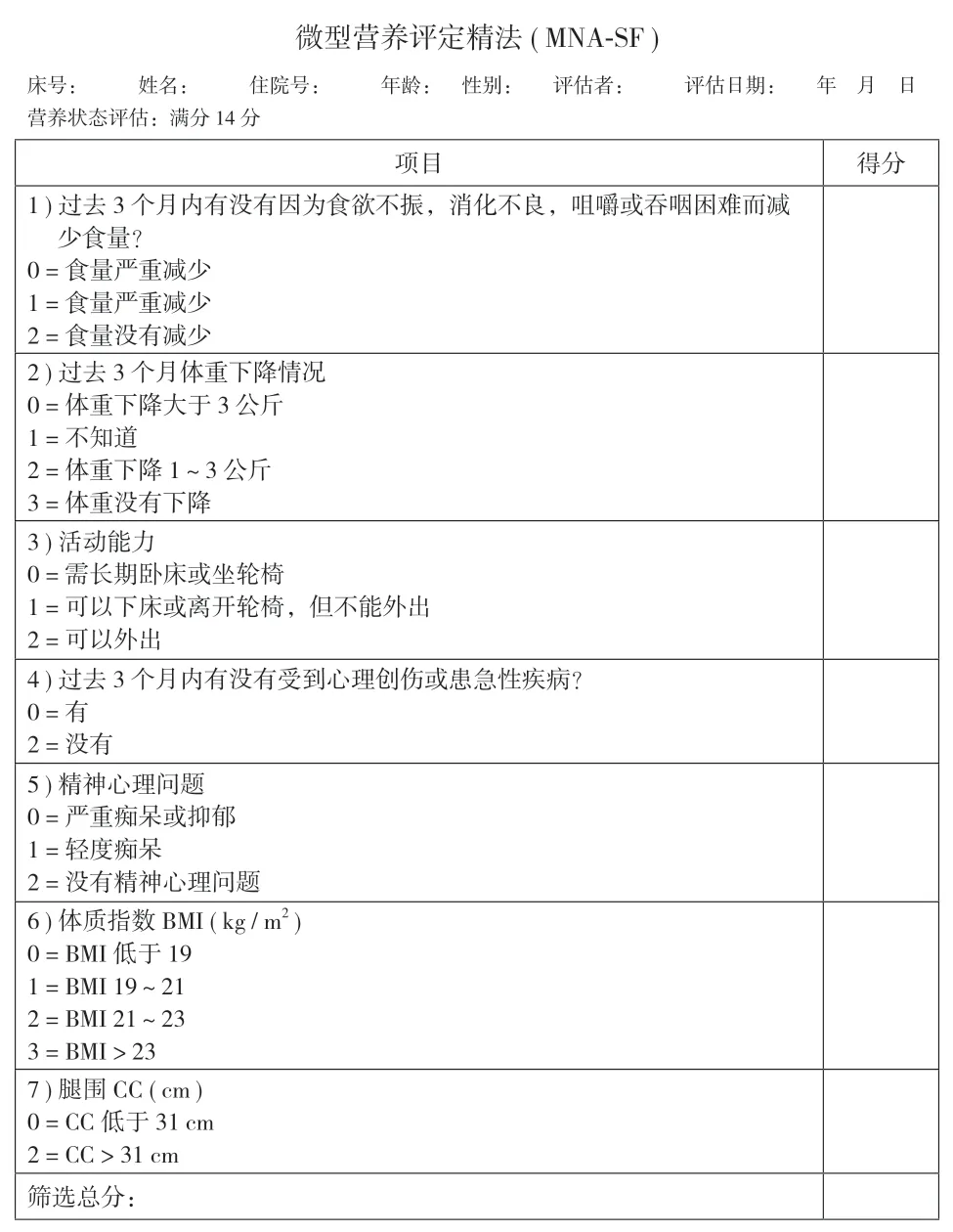
图2 微型营养评定精法 (MNA-SF) 量表Tab.2 Mini nutritional assessment -short form,MNA-SF
3.老年营养风险指数 (the geriatric nutritional risk index,GNRI):GNRI 于 2005 年开发,它是一种简化且准确的筛查工具,使用血清白蛋白水平和患者体重与理想体重的比率进行计算,GNRI <82 指示营养不良的风险[29]。相关研究表明,GNRI 得分与营养不良、衰弱和肌少症等老年综合征呈强负相关[30]。老年髋部骨折常合并衰弱、肌少症等情况,因此,GNRI 可作为一种简单的筛查工具来评估老年髋部骨折的营养情况和预测预后。
三、基于营养不良风险评估的髋部骨折围术期营养综合管理
老年髋部骨折患者容易出现营养不良,多数患者在住院期间存在饮食不足的情况,从而引发能量、蛋白质等营养物质的缺乏。老年髋部骨折患者围术期的代谢需求具有较大的波动性,健康管理者必须基于营养不良风险因素的识别和评估筛查,结合患者个体化需求,通过合适的途径和时机为患者围术期提供足量、全面、合理的营养供应,避免并发症的发生,改善患者预后。老年髋部骨折手术患者营养管理流程见图3。
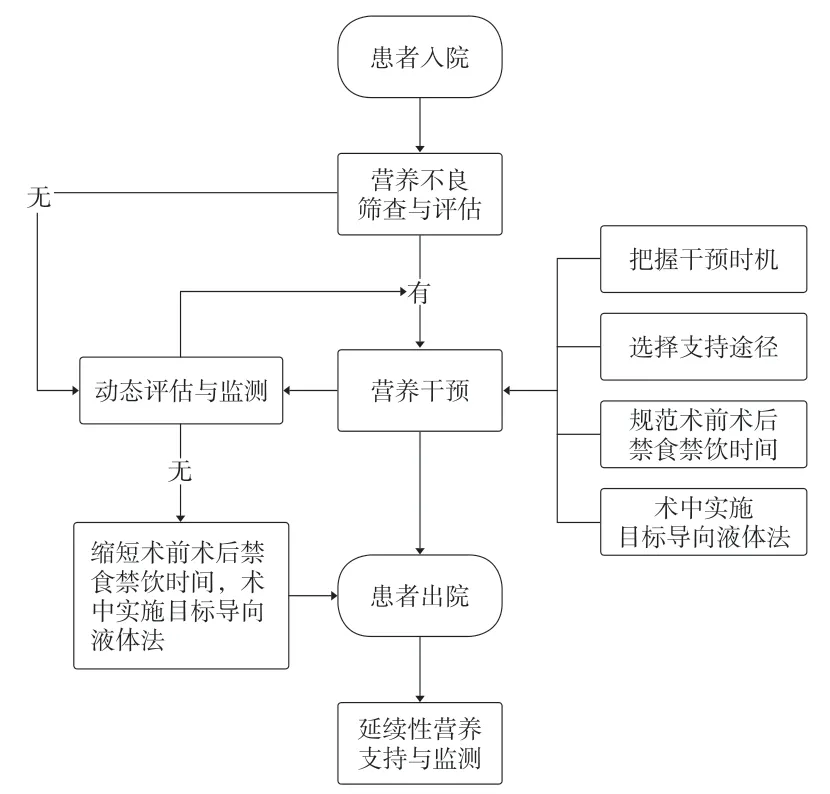
图3 老年髋部骨折手术患者营养管理流程图Fig.3 Flow chart of nutritional management in elderly patients with hip fracture surgery
1.围术期的营养需求:机体摄入的能量水平影响营养干预的效果,能量摄入不足可引起蛋白质消耗,造成器官功能障碍。对于老年患者,应该准确评估计算能量、蛋白质的需要量。相关指南推荐老年住院患者围术期能量需要量为 25~30 kcal/(kg·d),蛋白质的需要量为 1.0~1.5 g/(kg·d)[9]。静息状态下能量的代谢量可通过 Harris-Benediction、Schofied 等公式计算预测。但是在实际的临床情境中,不同患者不同状态下的能量需要是一个复杂的问题。临床上在考虑老年髋部骨折患者基础需要量的同时,需兼顾疾病状态下能量代谢率的增加部分,一般情况下择期手术增加 10%,合并严重创伤、多发骨折、感染时增加约 20%[8,31-32]。老年髋部骨折患者多合并骨质疏松症,因此营养供给中特别强调补充钙和维生素 D。相关指南推荐骨质疏松老年人日常每日需摄入钙约 1000 mg,且建议首先从食物中获取,对于缺口部分再通过钙制品补充;推荐的维生素 D 摄入量约为每天 800~1200 IU[33-34]。在补充钙剂和维生素 D 时,应定期监测血钙、血清 25 (OH) D浓度,评价药效和安全性。髋部骨折患者每天保证足够的饮水量可以增强代谢,对深静脉血栓、感染等并发症都有积极的预防作用。推荐老年髋部骨折患者的每日饮水量为1500~1700 ml,但对于合并心脏、肾脏等疾病的患者,需严格计算出入量[31]。老年人的膳食提倡食物多样化,每天保障足量的蔬菜和水果摄入。
2.围术期营养支持策略
(1) 支持时机:经过营养风险筛查评估患者存在营养不良应立即给予营养干预。另外,预计患者围术期超过7 天不能经口进食,或者连续 10 天进食量低于目标需要量的 60%~75% 时,即使评估患者目前不存在营养不良,也应该采取积极的营养支持策略[31]。由于老年髋部骨折患者入院时可能已存在营养不良,且住院后发生营养不良的风险高,有研究建议患者入院后,应及时开始营养支持治疗[35]。
(2) 支持途径:围术期的营养支持可通过饮食补充、口服营养液、肠内营养和肠外营养几种途径,临床上早期采纳营养师专业意见,并结合患者的具体情况,采取一种或多种途径联合给予营养支持。相关指南指出,围术期患者胃肠道功能正常或者部分存在时,优先推荐口服或者肠内营养,对于无胃肠功能或者病情治疗需要禁食患者,应及时给予肠外营养支持[8-9]。老年髋部骨折患者多属于急性创伤,一般无胃肠道疾病史,入院后一般可以给予口服营养干预。近年来,相关研究结果显示,为老年髋部骨折患者提供口服营养液支持,可以减少相关并发症,加速患者康复,同时该方法能缓解患者口渴、饥饿引起的不适感,患者依从性较高[35-37]。
(3) 各阶段支持方案:近年来,加速康复外科理念下,强调围术期维持患者营养与容量的平衡来减少相关并发症的发生。围术期的营养干预和容量管理应贯穿术前、术中、术后三个阶段。术前阶段,需结合营养评估结果选择适宜的营养支持方案,术前存在营养不良或者营养不良风险时,给予口服营养液或者肠内营养为主的营养支持,对于胃肠功能较弱的患者,辅以肠外营养支持[31]。近年来,随着加速康复理念在老年髋部骨折中深入应用,对于无胃肠动力障碍的患者,术前 6 h 禁固体饮食,2 h 禁清流质饮食的临床实践在减少糖代谢障碍、胰岛素抵抗、肠道功能紊乱方面产生了良好效果[38-39]。有研究表明,对于无糖尿病的老年髋部骨折患者,术前 2 h 饮用 400 ml 含12.5% 葡萄糖饮料,不但不加重手术误吸风险,而且可以使患者在术中处于合成代谢状态,减少术后胃肠道不适,利于患者恢复[31,38]。在术中阶段,不推荐通过静脉补充过量的糖,推荐基于患者生命体征和组织灌注情况给予目标导向液体疗法来维持患者术中液体平衡,减少术后并发症[40-41]。术后提倡早期经口进食,术后 4 h 可饮水,术后6 h 即可进食非产气食物[31,38,42]。老年髋部骨折术后早期进食作用不在于提供营养,而是尽早地给予胃肠道刺激,促进肠黏膜血液再灌注,从而进一步促进胃肠功能的恢复。
3.围术期营养干预效果:对老年髋部骨折患者实施围术期营养干预,可减少患者的摄入障碍,增加每日能量和蛋白质的摄入量,降低手术后相关并发症发生率,缩短住院时间,有利于快速康复[42-44]。但是,目前针对老年髋部骨折患者实施营养干预的原始研究样本较少,在纳入对象、干预方案、评价指标等方面存在差异。一项多中心研究对纳入的 73 例老年髋部骨折患者实施强化营养干预措施后,在术后 1 周时,发现对所有营养素的摄取有显著的正干预作用,术后 3 个月时,总脂肪和钙出现阳性干预作用,体重也较对照组增加[45]。较大样本的二次研究显示,营养干预对围术期并发症预防、实现加速康复等方面有积极意义[43-44]。大量研究探究了老年髋部骨折患者营养不良对病死率的影响,但对于营养干预对病死率的远期影响报道较少,尚有待进一步的深入研究。
四、小结
笔者从老年人发生营养不良的危险因素,常见的营养风险评估工具,髋部骨折围术期营养综合管理策略等方面进行了综述。老年髋部骨折营养不良风险管理是近年来研究的热点,后续研究可从营养管理的延续性和精准化等方面进行,以求为老年髋部骨折患者提供个体化、连续性的营养健康管理服务,改善老年髋部骨折患者的临床结局。

