心脏移植术后早期他克莫司浓度及代谢率与预后的关系
郭琳 王真珍 张向立 刘云霏 张绵 郑华 王长安
郑州市第七人民医院 1重症医学科,2心外科,3肾移植肾内科 (郑州 450003)
钙调磷酸酶抑制剂是心脏移植术后免疫抑制治疗的核心药物,与环孢素相比,他克莫司排斥反应及不良反应发生率更低[1-2]。中国心脏移植注册系统数据显示,我国心脏移植受者出院后他克莫司应用比例超过90%[3]。他克莫司的治疗目标狭窄,移植手术后早期血药浓度监测尤为重要。参照国际指南及专家共识,心脏移植术后3 个月内推荐他克莫司谷浓度(trough concentration,C0)维持10 ~ 15 ng/mL[4-6]。心脏移植术后早期很多受者受基因调控、感染、药物等因素影响,他克莫司血药浓度难以达标。已有研究表明移植术后早期他克莫司浓度、变异度或代谢率与肝移植、肾移植受者预后具有相关性[7-9]。但目前关于心脏移植术后他克莫司早期暴露与患者预后关系的研究较少,笔者曾报道了高他克莫司个体内变异性与心脏移植术后感染的相关性[10],作为该报道的系列研究,本研究回顾性地收集了172 例心脏移植患者术后30 d 内的他克莫司C0,并随访受者预后,评估早期他克莫司C0、代谢率、变异度与移植术后发生感染、排斥反应及死亡的相关性。
1 资料与方法
1.1 研究对象
1.1.1 纳入和排除标准 回顾2018年4月至2022年12 月于本院进行心脏移植的受者信息,纳入标准:(1)首次接受同种异体心脏移植;(2)术后应用以他克莫司为基础的免疫抑制方案;(3)移植后定期监测他克莫司C0。排除标准:(1)移植后存活时间< 10 d;(2)未应用他克莫司或短期内停用免疫抑制剂。189 例受者中,9 例术后因急性并发症存活< 10 d,2 例因感染过重短期内停用免疫抑制剂,6 例未应用他克莫司,最终纳入172 例术后服用他克莫司的受者作为研究对象。他克莫司结合患者实际情况,在移植术后第1 - 4 天口服给药,根据血药浓度调整药物剂量。本研究已通过本院医学伦理委员会审批(批准文号:医科伦审2021第020 号)。
1.1.2 供者基本情况 供心均来源于中国器官获取组织主导的公民器官捐献,并及时有效保存转运,保证供心质量[11]。172 例供者中,男148 例(86.0%),女24例(14.0%),年龄(38.5 ± 10.3)岁,体质量72(51,74)kg;47.6%(82 例)的供者原发病为脑外伤,41.3%(71 例)为脑出血;供心冷缺血时间56 ~ 535 min。
1.2 研究参数与信息收集
1.2.1 研究参数 计算心脏移植受者术后30 d 内他克莫司C0的平均值和峰值,根据目前心脏移植术后相关指南共识建议的他克莫司血药浓度靶目标,将研究对象分为浓度< 10 ng/mL,10 ~ 15 ng/mL和> 15 ng/mL 三组,比较三组受者预后差异。
并计算受者的他克莫司代谢率,他克莫司代谢率=他克莫司谷浓度/他克莫司日剂量[9],用C0/D 表示,C0/D值越大,表明机体对他克莫司的代谢越慢,反之C0/D值越小,表明机体对他克莫司的代谢越快。受者他克莫司浓度及代谢率的变异度使用标准差(standard deviation,SD)表示,,其中xi表示移植术后30 d 内测得的他克莫司血药浓度C0,代表30 d 内的平均血药浓度值,n代表此时间段内血药浓度值的总个数[12]。SD 值越大,表明变异度越大。
1.2.2 信息收集 通过电子病历系统回顾性收集心脏移植受者的相关数据,包括年龄、性别、体质量、原发病、心脏移植手术时间、术后住院天数等,记录术后30 d 内每次他克莫司C0值、对应的每日他克莫司服药剂量及出院时他克莫司C0等信息。他克莫司血药浓度检测均采用高效液相色谱法。
1.3 随访和预后 心脏移植受者术后随访中位时间为505(321,684)d。记录受者术后感染、排斥反应及死亡三种预后结局,为评估他克莫司的影响,上述预后事件均发生在服用他克莫司之后。其中“住院感染”指的是发生在移植手术住院期间的感染,“感染再住院”指出院后随访期间因急性感染需要再次住院治疗,“总体感染”则无论感染发生在移植住院期间或者出院后随访期间因感染再住院。是否发生感染和排斥反应均由心脏移植团队根据移植受者临床表现、实验室检查、影像学和微生物学检测及心肌活检等情况共同判定。
1.4 统计学方法 所有数据使用SPSS 26.0处理分析。正态分布定量数据用均数±标准差表示,使用参数检验比较差异性;偏态分布定量数据用M(P25,P75)表示,差异性比较使用非参数检验;分类数据的比较使用χ2检验。P< 0.05 表示差异有统计学意义。
2 结果
2.1 一般资料 172例心脏移植受者年龄47.0(34.0,56.0)岁,83.1%(143 例)为男性,体质量(66.0 ±16.1)kg;受者原发病以扩张型心肌病为主(118 例,68.6%),其次是冠心病(35 例,20.3%);移植术后发生住院感染者34 例(19.8%),30.8%(52 例)的受者在随访期间因感染再次住院治疗,总体感染例数75 例(43.6%),发生排斥反应和死亡的受者分别占8.7%和14.5%。
2.2 他克莫司浓度分布 术后30 d 内每天他克莫司血药浓度C0分布见图1。172 例研究对象在移植术后30 d 内共检测他克莫司血药浓度1 548 次,平均9.0 次/例。其中有146 次C0值 > 15 ng/mL。每例受者C0平均值分布为8.29(6.82,9.89)ng/mL,峰值分布14.30(11.80,17.53)ng/mL,出院浓度(10.77 ±3.68)ng/mL。
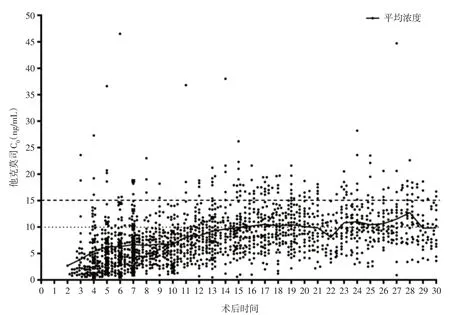
图1 心脏移植受者术后30 d 内他克莫司血药浓度分布Fig.1 Blood concentration distribution of tacrolimus in 30 days after heart transplantation
2.3 他克莫司浓度及代谢率与预后的相关性分析 见表1,他克莫司C0平均值、峰值和服药剂量与预后无统计学相关性(P> 0.05),总体未发生感染、无感染再住院和未发生排斥的受者具有更高的出院时他克莫司C0(t= 2.996、2.043、2.115,P= 0.003、0.043、0.036)。他克莫司代谢率方面,总体感染、住院感染及因感染再住院的受者C0/D 值均明显高于未发生感染的受者,差异有统计学意义(Z = 2.720、2.013、2.377,P=0.007、0.044、0.017)。而排斥反应和死亡方面,C0/D值差异无统计学意义(P> 0.05)。将研究对象分为浓度< 10 ng/mL 组(132 例),10 ~ 15 ng/mL 组(34 例)和 > 15 ng/mL 组(6 例),见表2,三组受者年龄、性别、体质量、住院时间及原发病等组间均差异无统计学意义(P> 0.05)。比较三组受者预后的差异性,见表3,结果表明三组受者在术后感染、排斥反应及死亡方面均差异无统计学意义(P> 0.05)。
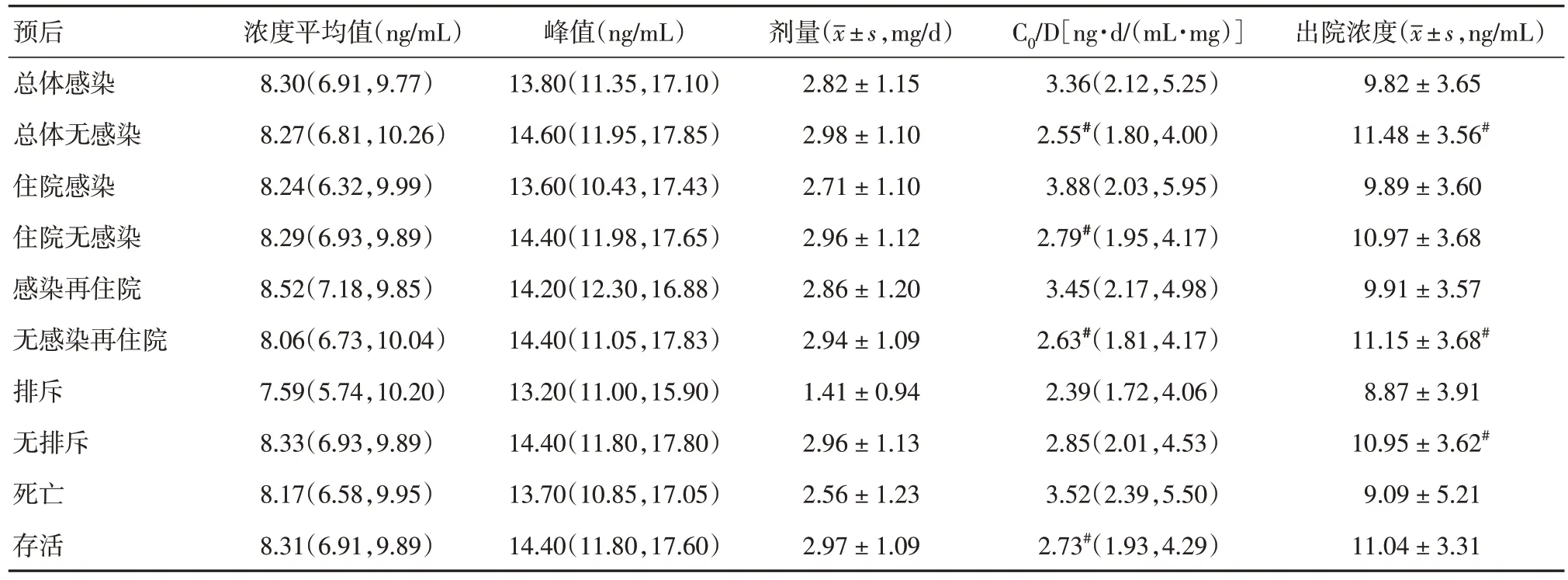
表1 他克莫司C0平均值、峰值,剂量,代谢率及出院浓度与预后的相关性Tab.1 Correlation between mean value,peak value,dose,metabolic rate and discharge concentration of tacrolimus C0 and prognosisM(P25,P75)
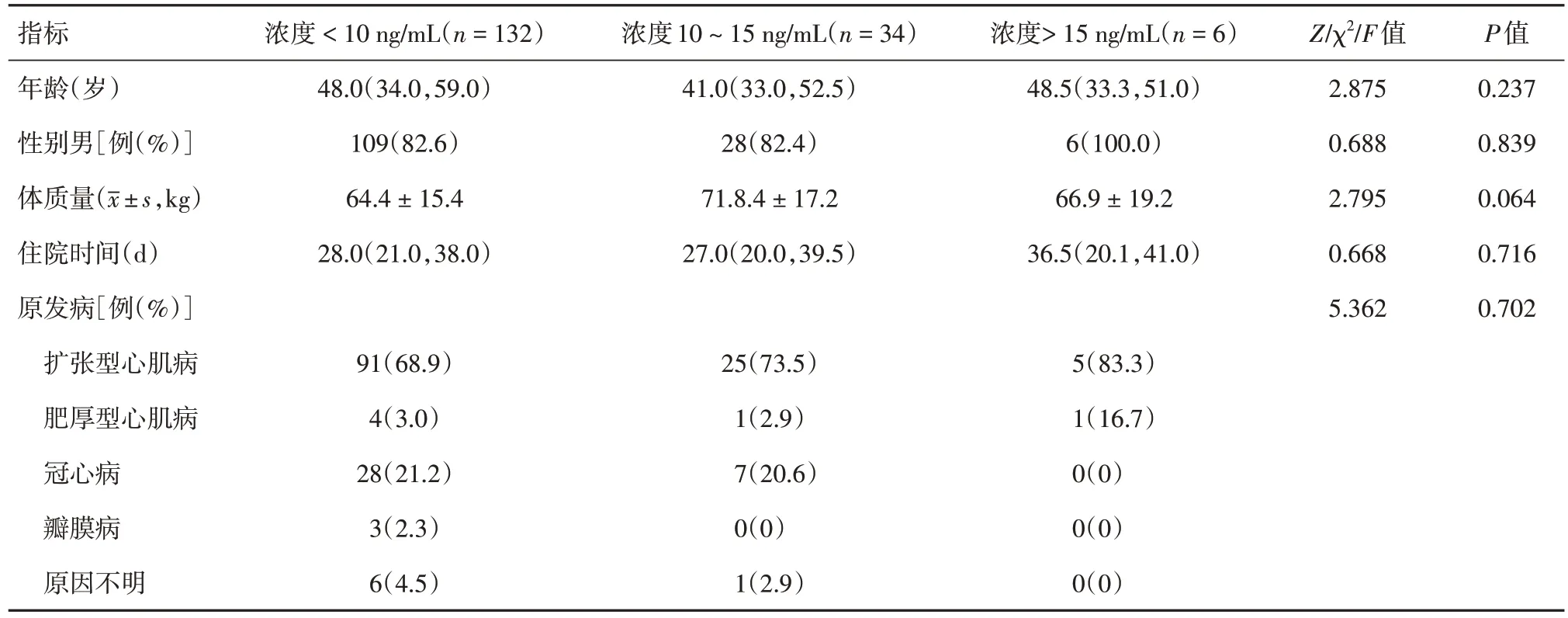
表2 他克莫司不同血药浓度的心脏移植受者基本信息Tab.2 Basic information of heart transplant recipients with different blood concentrations of tacrolimus M(P25,P75)
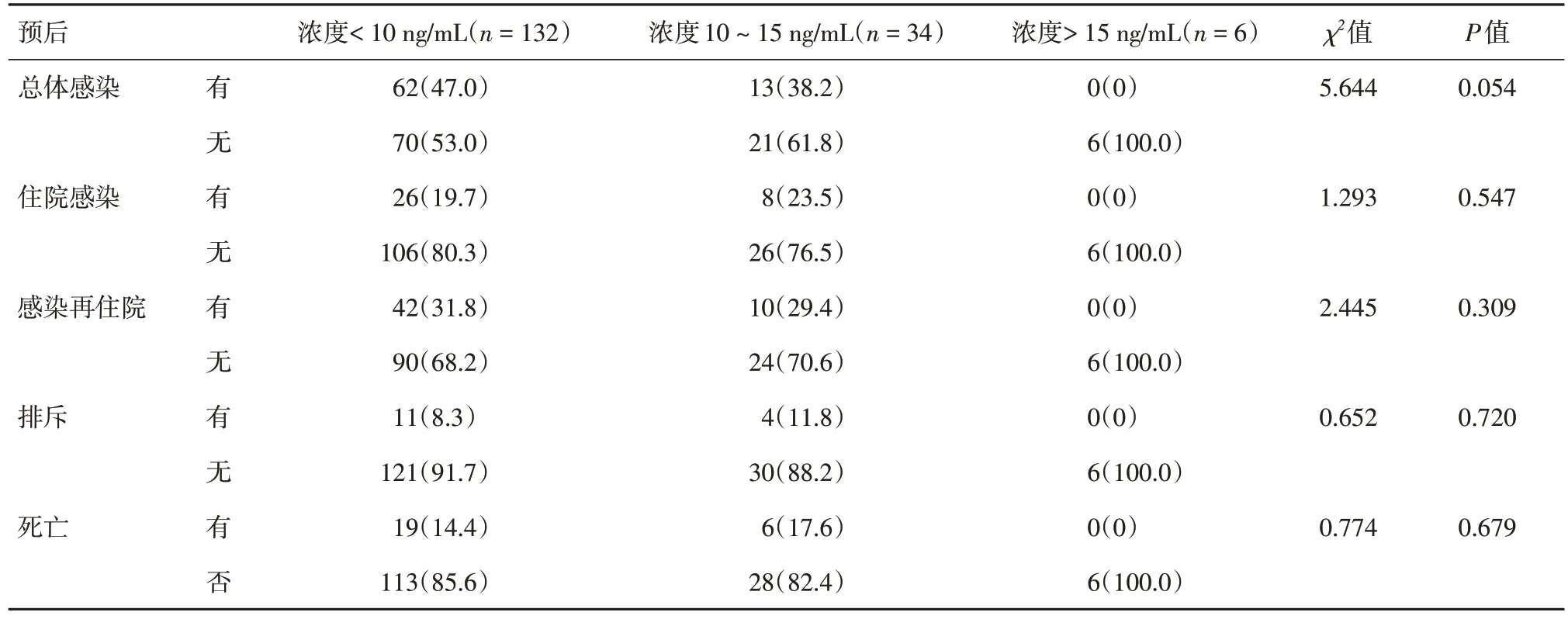
表3 他克莫司不同血药浓度的心脏移植受者与预后的相关性Tab.3 Correlation between prognosis and tacrolimus with different blood concentrations in heart transplant recipients 例(%)
2.4 他克莫司浓度和代谢率的变异度与预后的关系 见表4,发生住院感染、感染再住院或总体感染的受者C0/D 的SD 值明显高于未发生感染者,并且差异有统计学意义(Z= 2.044、2.432、2.816,P= 0.041、0.015、0.005)。此外,死亡受者C0/D 的SD值也高于存活受者(Z= 2.255,P= 0.024)。排斥反应方面,C0/D 的SD 值的差异无统计学意义。
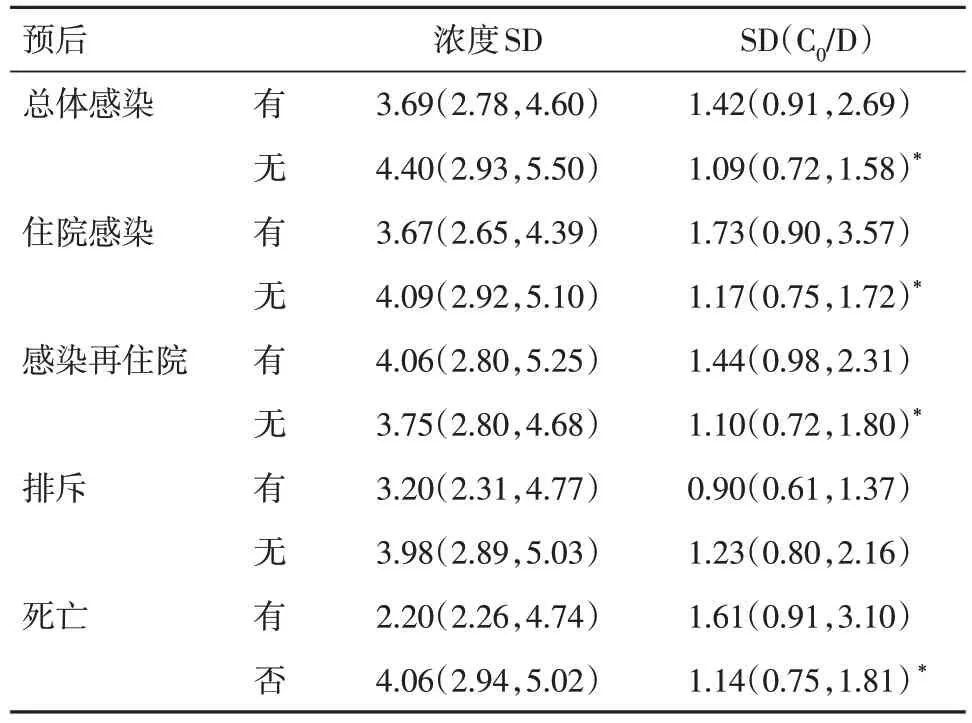
表4 心脏移植术后30 d 内他克莫司浓度及代谢率的变异度和预后的相关性Tab.4 Correlation between variation and metabolic rate of tacrolimus concentration and prognosis within 30 days after heart transplantationM(P25,P75)
3 讨论
因缺乏高质量循证医学证据,目前相关指南和专家共识推荐的心脏移植受者术后早期他克莫司血药浓度C0目标(10~15 ng/mL)已经将近20 年没有改变。2019 年《他克莫司个体化治疗药物监测:第二份共识报告》[13]中也指出,心脏移植受者术后他克莫司C0维持目标可能需要重新修订。
基于此,本研究收集了心脏移植受者术后30 d 内的他克莫司血药浓度C0值,随访追踪受者预后,并对二者相关性进行了评估。结果如表1显示,他克莫司C0平均值、峰值与术后感染、排斥反应及死亡均无统计学相关性。这与周峻臣等[14]针对肾移植受者他克莫司浓度与感染相关性的研究结果类似。本研究进一步将受者根据平均C0浓度是否达到推荐目标分为三组进行分析,结果表明,C0未达治疗目标(> 10 ng/mL)组和达标组(10 ~ 15 ng/mL)受者在术后因感染再住院、总体感染、排斥反应及死亡方面均差异无统计学意义。此研究结果提示了心脏移植术后受者的他克莫司血药C0可能并不需要维持到较高的治疗目标,下调其治疗目标可以减少他克莫司药物本身所带来的不良反应,并降低患者的经济负担。但是此结果的可靠性可能受样本量的限制,尚需要高质量临床试验验证。由于指南和临床实践的约束,移植管理医师会下调药物剂量来避免他克莫司谷浓度> 15 ng/mL,因此该组病例数较少,研究结果未能发现其与预后的相关性。
对心脏移植受者术后30 d 内的他克莫司代谢率进行分析,发现总体感染、住院感染及因感染再住院的受者C0/D 值均明显高于未发生感染者,差异有统计学意义。这表明他克莫司慢代谢者较快代谢者更容易出现感染,这可能与慢代谢受者体内蓄积的药物量更多、免疫抑制状态更强有关。心脏移植术后早期,受者的他克莫司代谢率会受到血细胞比容、基因多态性、合用药物和食物及疾病等多种因素影响[15]。近年来多项研究证实了CYP3A 亚家族基因和ABCB1 基因多态性与实体器官移植受者他克莫司代谢率的相关性[16-19]。虽有研究表明他克莫司快代谢心脏移植受者长期生存率有劣于慢代谢者的趋势[18],但本研究结果发现两者死亡率差异并无统计学意义,这可能与不同研究的样本量及随访时间差异等因素有关,未来需要更多更长随访时间的大样本研究进一步探索。
高的他克莫司代谢变异会缩短移植物生存期,潜在机制可能是急慢性排斥反应、供者特异性HLA抗体和移植物进行性纤维化损伤[20]。SHUKER等[21]在4 年随访后发现,在心脏异体移植物血管病变、急性排斥反应方面,与对照组相比,高他克莫司代谢变异的比例差异无统计学意义(P= 0.57和0.82)。但GUETA 等[22]的 研究结果则表明他克莫司个体内变异高的受者晚期排斥率明显增加(P= 0.04)。本研究发现他克莫司代谢率的变异度与术后感染和死亡的发生具有相关性,代谢率变异度大的受者更易发生不良预后。提示高他克莫司代谢变异可能是心脏移植后一个重要的预后危险因素,可以通过提高患者依从性、避免或调整药物相互作用、药物剂量辅助等措施来降低受者他克莫司代谢变异,从而改善预后。
本研究有一定的局限性,研究对象术后均采用他克莫司+吗替麦考酚酯+糖皮质激素三联免疫抑制方案,而感染或排斥的发生可能无法排除霉酚酸的影响。本研究是回顾性单中心研究,可能存在信息偏倚,结论可能需要未来扩大样本量或前瞻性多中心研究来进一步证实。而且关于他克莫司早期暴露与长期预后的关系需要更长随访时间的研究来验证。
综上所述,本研究发现他克莫司C0与排斥、总体感染和死亡结局之间没有统计学相关性,但他克莫司目标浓度是否能够下调未来需要大样本研究进一步探索;他克莫司慢代谢者较快代谢者更容易出现术后感染;他克莫司代谢率的变异度与术后感染的发生具有相关性,高他克莫司代谢率变异是心脏移植术后感染的危险因素。
【Author contributions】GUO Lin wrote the article.WANG Zhenzhen,ZHANG Xiangli and LIU Yunfei collected the data.ZHANG Mian,ZHENG Hua revised the article.WANG Chang'an designed the study and conducted the literature review.All authors read and approved the final manuscript as submitted.

