Fe2+对厌氧氨氧化EGSB反应器运行性能的影响
史天茜,石永辉,武新颖,张益豪,秦哲,赵春霞,路达
(河北大学生态环境学院,河北 保定 071002)
传统硝化反硝化脱氮工艺存在污泥产量高、有机碳需求量大、二次污染等问题。一种极具发展前景的生物脱氮技术厌氧氨氧化(Anammox)工艺因具有高效、经济、环保等优点,被越来越多的污水处理厂引进使用[1-3]。由于厌氧氨氧化细菌(AnAOB)倍增时间长(11~20d)[4]、对环境因素敏感(金属[5]、温度[6]、底物浓度[7]),限制了其在污水处理厂的进一步应用。
铁是环境中常见的金属元素之一,是大多数生物生长必不可少的营养元素[8]。铁对AnAOB 的生长、繁殖尤为重要。AnAOB 中含有大量铁结合蛋白(如血红素c),是其进行生理代谢不可缺少的成分,能保证Anammox 过程的正常进行。此外,铁还能影响胞外聚合物(EPS)分泌,改变AnAOB活性。可见,Fe2+会影响Anammox反应器的脱氮性能。Ding 等[9]比较了不同Fe2+浓度对细菌繁殖的影响,发现Fe2+为0.12mmol/L 时对AnAOB 生长促进效果最好。Mak 等[10]研究了Fe2+对Anammox 的短期影响,发现0.08mmol/L Fe2+最有利于AnAOB 活性增强。Zhou等[11]发现进水基质浓度不变时,低浓度Fe2+能够增强Anammox反应器稳定性。但这些文章主要研究一定的基质浓度下Fe2+对Anammox系统的影响,少有人探究Fe2+对反应器提高氮负荷的作用以及Fe2+对AnAOB的生理影响。
文章主要研究不断提升氮负荷时,不同浓度的Fe2+对Anammox 膨胀颗粒污泥床(EGSB)反应器脱氮性能、细菌生理变化及表面形态的影响,寻找Fe2+最适投加量,确定Fe2+与EPS、血红素c 的关系,深入了解细菌的生理变化,这将有助于培养高性能Anammox 污泥,优化Anammox 工艺,推进实际应用。
1 材料与方法
1.1 接种污泥和合成废水
接种污泥取自实验室已稳定运行300d的EGSB反应器。接种后每个反应器中初始混合液悬浮固体(MLSS)质量浓度为(370±16)mg/L、混合液挥发性悬浮固体(MLVSS)质量浓度为(297±13)mg/L。
每日处理4L 合成废水,以NH4Cl 和NaNO2充当氮源(NH+4-N∶NO-2-N=1∶1.32),添加CaCl20.150g/L、 KH2PO40.010g/L、 MgSO40.300g/L、NaHCO30.050g/L。另外,每升中分别加入1mL微量元素Ⅰ和Ⅱ。微量元素Ⅰ组成:乙二胺四乙酸二钠(EDTA 2Na)5.00g/L。微量元素Ⅱ组成:ZnSO4·7H2O 0.430g/L, H3BO40.014g/L, CuSO4·5H2O 0.250g/L, CoCl2·6H2O 0.240g/L, MnCl2·4H2O 0.990g/L, NaMoO4·2H2O 0.220g/L, NiCl2·6H2O 0.190g/L,EDTA 2Na 19.100g/L。进水中通N2使溶解氧(DO) 浓度控制在0.100mg/L 以下,使用H2SO4或NaOH将进水pH调整为8.00±0.05。水力停留时间(HRT)为24h。
1.2 Anammox反应器和实验操作
采用4 个工作容积为4L 的EGSB 反应器(R1、R2、R3、R4),结构见图1。反应器由有机玻璃制成,外部用锡纸包裹避免光照,并配备恒温水套保持温度为(35±1)℃,使用蠕动泵将反应器内基质混合均匀。

图1 EGSB反应器结构图
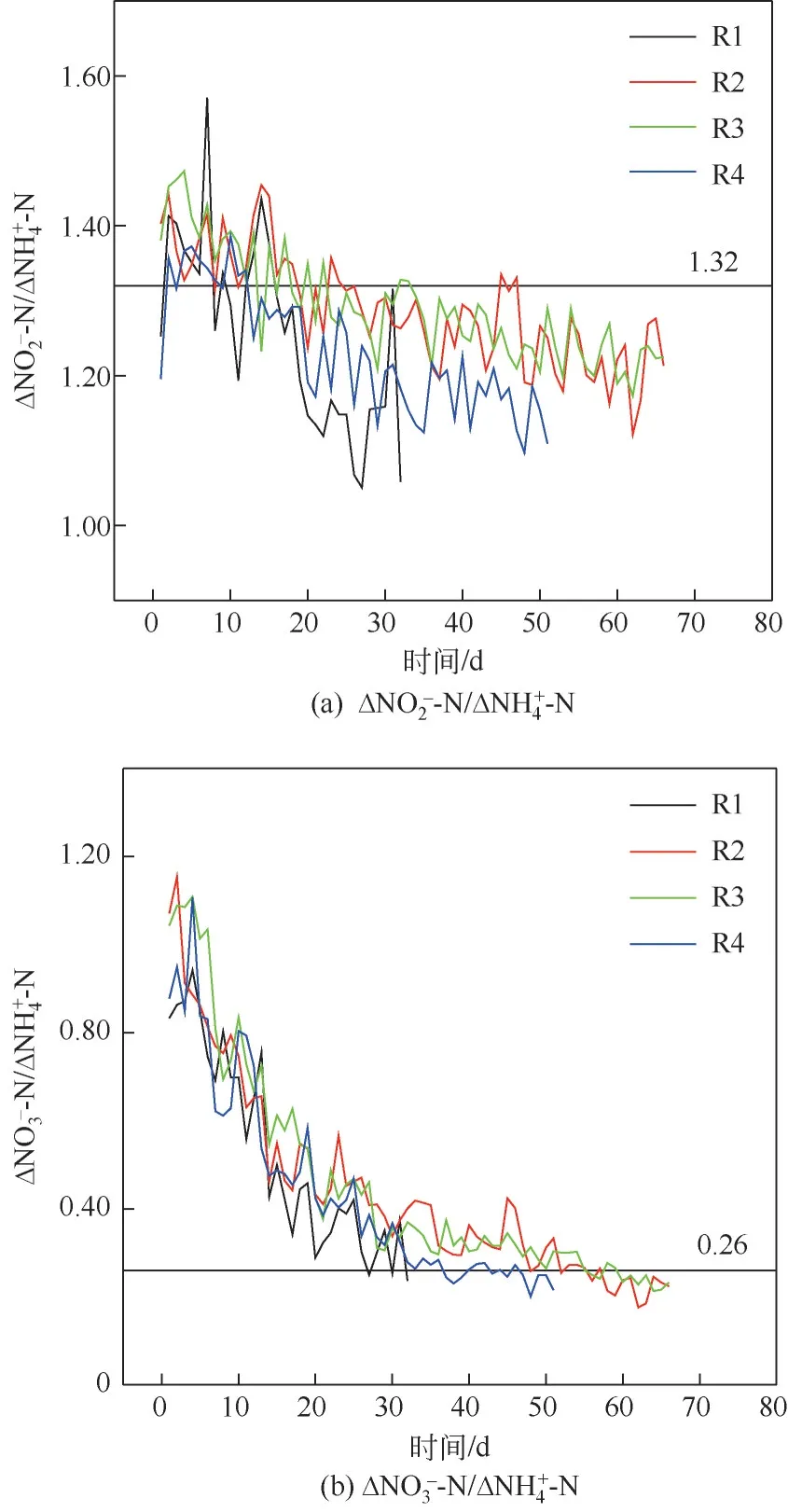
图4 反应器Anammox反应化学计量比变化
实验过程中,通过投加FeSO4·7H2O,使R1、R2、R3、R4 反应器内Fe2+浓度分别为1.00mg/L、5.00mg/L、7.50mg/L、10.00mg/L。逐渐提升氮负荷,当出水NO-2-N 浓度连续5d 大于50.00mg/L 时,认为反应器性能受到严重抑制,停止运行。
1.3 常规分析方法
每日采集水样进行检测,其中NH+4-N 采用纳氏试剂分光光度法测定,NO-2-N 使用N-(1-萘基)-乙二胺分光光度法,NO-3-N使用酚二磺酸分光光度法,Fe2+检测采用邻菲啰啉分光光度法[12]。pH 和DO 使用哈希-HQ40d 型便携式pH 溶氧仪测定,MLSS与MLVSS在第36d采用重量法测定。
1.4 EPS的提取与分析
运行的第36d,采集4 个EGSB 反应器充分混合后的污泥,使用热提取法提取EPS[13]。EPS 含量(mg/g VSS)为多糖(PS)与蛋白质(PN)之和。其中PS 采用蒽酮比色法[14]测量,PN 采用改进的Lowry法[15]测量。
1.5 血红素c的测定
收集EGSB 反应器在第36d 的混合污泥样品,采用吡啶分光光度法[16]对两个反应器的污泥进行血红素c含量的检测。具体步骤为:样品经磷酸缓冲盐溶液(PBS)清洗、超声和离心后加入连二亚硫酸钠和铁氰化钾,采用紫外可见分光光度计,测得550nm和535nm之间的吸光度差异,计算出血红素c浓度(µmol/mg pro)。
1.6 扫描电子显微镜(SEM)
反应器在第36d的混合污泥样品用去离子水洗涤3次,离心后去掉上清液,然后用2.50%戊二醛溶液在4℃下固定24h,保证细胞形态不发生改变。再用无菌水洗涤3次并离心,之后用梯度乙醇水溶液 (30%、 50%、 70%、 80%、 90%、 100%、100%)对细菌进行逐级脱水处理,弃掉上清液。在室温下自然脱水干燥后, 使用SEM(PHENOMPROX,荷兰)观察。
2 结果与讨论
2.1 Fe2+对反应器脱氮性能的影响




此外,4 个反应器的MLSS 变化见图5。R0 为接种污泥的MLSS,运行36d 后R1 中MLSS 出现负增长,降低到284mg/L,反应器内污泥上浮严重。这说明逐渐提高进水氮负荷时,1.00mg/L 的Fe2+不利于AnAOB 生存和繁殖。而R2、R3、R4 反应器MLSS均呈现增长趋势,其增长量R3(367mg/L)>R2(192mg/L)>R4(175mg/L)。可见反应器内投加7.50mg/L 的Fe2+最有利于AnAOB 适应基质变化,细菌增殖最快,有助于抵抗高氮负荷冲击。
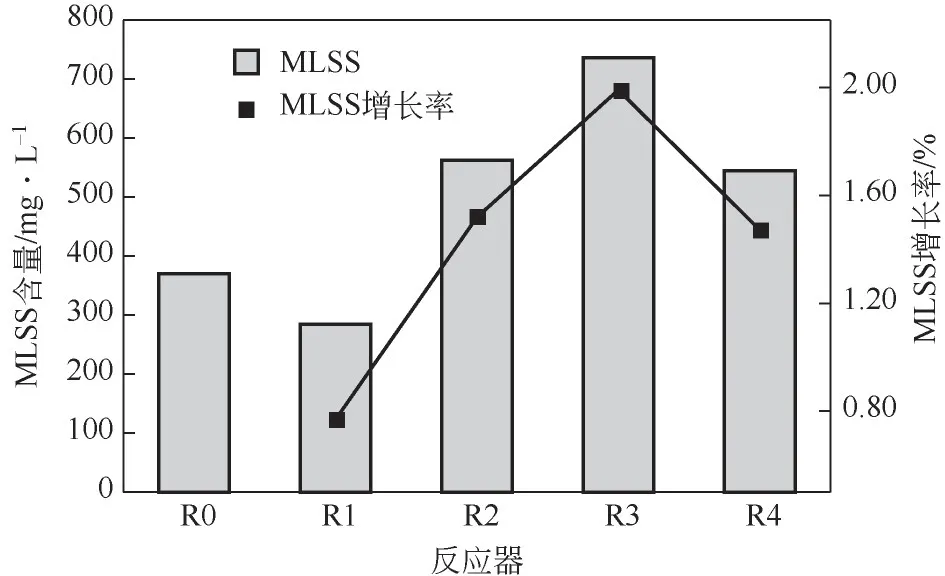
图5 反应器MLSS变化
如图6,在进水NH+4-N、NO-2-N 浓度分别为130mg/L 和172mg/L 时,对比不同Fe2+浓度对反应器脱氮性能的影响,检测4 个反应器在24h 内NH+4-N、NO-2-N浓度变化情况。由于初期反应器内TN 浓度较高,细菌易获得基质,因此4 个反应器前4h NH+4-N 和NO-2-N 的降解速度接近。随着反应器内TN浓度逐渐降低,5h后降解速度出现明显差别。R2、R3、R4 的NH+4-N 降解速度均大于R1。NO-2-N 降解速度由快到慢为R3>R2>R4>R1。随着Fe2+浓度从1.00mg/L 增加到7.50mg/L,反应器内基质降解速度逐渐增加,脱氮能力提高;当Fe2+浓度进一步提高到10.00mg/L,基质降解速度减慢,反应器性能降低。
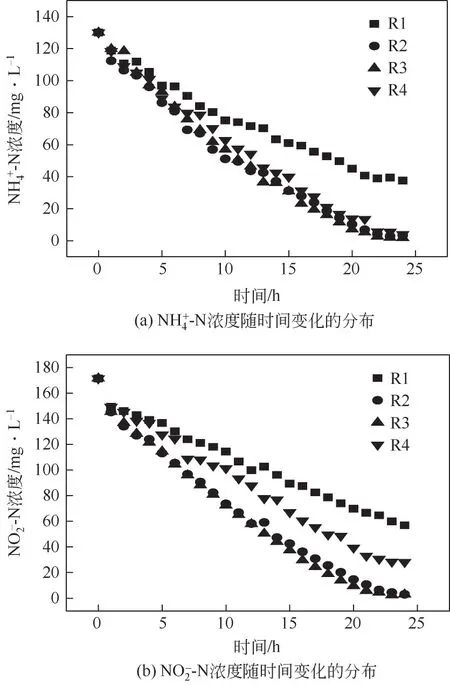
图6 4个反应器NH4+-N和NO2--N浓度随时间变化的分布
2.2 Fe2+对EPS的影响
EPS是细菌分泌的一种黏性物质[18],是AnAOB的重要组成部分,在促进颗粒形成、抵抗外界环境变化、提高污泥沉降性能、维持系统稳定性等方面发挥着重要作用[19]。同时,EPS 中的羟基、羧基等阴离子官能团吸附环境中的Fe2+[11],有利于细菌利用Fe2+,加快细菌生理活动,产生更多含铁蛋白质,提升对基质代谢和不利环境的抵抗能力。并且EPS 吸附的Fe2+还能发挥压缩双电层作用,从而降低细菌间的静电斥力[8],促进造粒。
不同Fe2+浓度下EPS 的变化情况如图7 所示,当Fe2+浓度为1.00mg/L 时,系统内Fe2+浓度无法满足AnAOB 实际需求量,营养物质不足使代谢作用受到影响,细菌活性较低,减少了EPS分泌,导致R1 的EPS 含量最低,为179mg/g VSS。此时R1 对基质的代谢能力最差。Fe2+浓度为5.00mg/L 时,AnAOB从外部环境中获得了较多的Fe2+参与生理活动,EPS 含量明显增加到240mg/g VSS,细菌活性增强,相较于R1,R2 脱氮性能明显提高。当Fe2+含量增加到7.50mg/L,EPS 到最高值242mg/g VSS。Gao 等[20]也发现Fe2+能促进EPS 生成并提高脱氮性能。此外,Fe2+属于还原性物质,有利于维持反应器中厌氧环境[21]。因此,Fe2+浓度最佳时,营造了最适宜的生存环境,促进Anammox 过程和细胞代谢,加快生物量增长,刺激EPS大量分泌,为微生物提供更多的胞外养分和酶[22],增强细胞活性[20,23],提高系统稳定性,使得R3 脱氮性能高于其他反应器。Fe2+浓度增加到10.0mg/L 时,EPS 降低到202mg/g VSS。由于Fe2+具有不可降解特性[11],铁的过量积累抑制了AnAOB 活性,减少了EPS 合成,降低了R4反应器性能。

图7 4个反应器中EPS含量变化情况
PN/PS是反映污泥沉降性能的重要指标,比值越高污泥沉降性能越差[24]、强度越低,污泥越容易流失,导致反应器性能不稳定。图7 中随着Fe2+浓度从1.00mg/L 增加到7.50mg/L,PN/PS 值呈下降趋势,从最大值2.88降低到最小值1.10。且7.50mg/L时PS含量最高,而PS对污泥的聚集作用及沉降性能等方面的影响比PN 更大[25-26]。因此Fe2+浓度为7.50mg/L时,能够改变EPS的组成,使得污泥沉降性能最好、强度最高,有助于保留生物量,反应器脱氮性能得到提升。当Fe2+浓度增加到10.00mg/L后,过量的Fe2+使PN/PS 的比值明显上升到2.59,污泥沉降性能及聚集能力降低,影响AnAOB 对基质的去除能力。
2.3 Fe2+对血红素c的影响
血红素c 能够通过Anammox 合成,是AnAOB进行代谢作用必须的一种物质,有助于AnAOB 维持正常形态。此外,细胞内供能、调节、生长等活动都离不开蛋白质,而与血红素c相关的蛋白质占AnAOB 总蛋白量的38%[27],因此血红素c 对维持AnAOB活性具有重要作用。
各反应器中血红素c 浓度变化情况如图8 所示。在1.00~7.50mg/L 范围内随着Fe2+浓度增加血红素c 含量逐渐提高,从1.18µmol/mg pro 达到3.76µmol/mg pro。AnAOB 的代谢依赖于联氨合成酶(HZS)、联氨脱氢酶(HDH)等酶,这些酶的形成与血红素c 密切相关,而血红素c 的合成需要嵌入Fe2+,从而形成活性区[28],提高AnAOB 活性。此外,血红素c通过与蛋白质主链共价结合,在电子转移和催化中发挥着非常重要的作用[29],能促进Anammox反应进行。可见,适宜的Fe2+(7.50mg/L)能促进血红素c形成,增强细胞活性,提升AnAOB对环境中Fe2+的利用效率[30],加快Anammox 过程,增强基质代谢能力。但Fe2+浓度增加到10.00mg/L后,过量的Fe2+在反应器中积累,产生毒性作用减弱了AnAOB进行代谢等生理活动,减少了细菌对营养物质的吸收,使AnAOB对抑制因子(如NO-2-N)更加敏感[21],降低对高氮负荷的抵抗能力。因此,血红素c含量下降到1.42µmol/mg pro,反应器性能随之降低。Zhang 等[31]和Ma 等[29]的研究也证明了血红素c 与反应器脱氮性能有关,血红素c 含量越高脱氮性能越强。
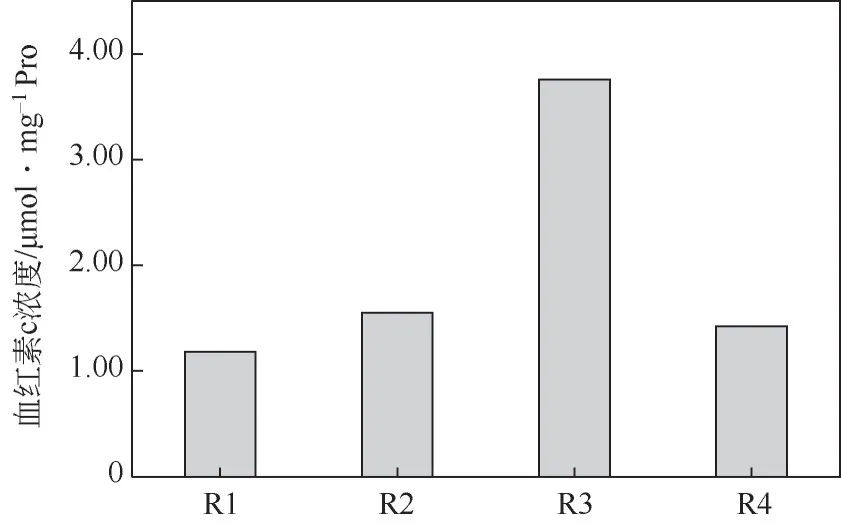
图8 4个反应器中血红素c浓度变化
2.4 Fe2+对AnAOB形态的影响
为了探究不同Fe2+浓度对污泥表面形态的影响,各反应器的SEM图见图9。SEM图像能明显观察到颗粒表面的状态,4个反应器中颗粒表面都存在丝状细菌与球菌。丝状细菌具有支撑颗粒骨架的作用,可为微生物聚集构建框架[32]。如图9(a)和图9(d)微生物表面空洞较多,部分细胞间有较大间隙,颗粒松散,不利于细菌沉降和聚集,阻碍Anammox 过程[28],图9(a)中此现象更为明显。这一现象与Fe2+浓度为1.00mg/L和10.00mg/L时PN/PS值较高一致,说明了Fe2+浓度过低或过高都会对污泥结构产生影响,不利于反应器在高氮负荷下运行。Fe2+浓度为5.00mg/L 和7.50mg/L 时,PN/PS 值降低,有利于污泥沉降和聚集。图9(b)和图9(c)证实了这一点,图中颗粒表面存在紧实和致密的复杂结构,颗粒紧凑,这有利于扩大与营养物质的接触面积,使更多的物质被细菌吸收,加快基质的去除速度。结合4个反应器的脱氮性能,可见菌体表面结构越致密,颗粒稳定性越强,有助于污泥团聚和沉降,增强对基质的去除能力。

图9 污泥SEM图
3 结论
(1)Fe2+浓度为7.50mg/L 时,EGSB 反应器脱氮性能最强;进水TN 为302mg/L 时,TN 去除率达到84.2%。
(2)AnAOB的EPS组成和血红素c变化趋势与反应器脱氮性能一致。Fe2+浓度在7.50mg/L 时,EPS 与血红素c 达到最大值242mg/g VSS 和3.76µmol/mg pro,PN/PS 达到最小值1.10,且颗粒表面更加密实,结构更加牢固,同时MLSS也达到最大值(737mg/L)。因此7.50mg/L 的Fe2+能增强细菌活性,促进基质代谢,有助于抵抗高氮冲击,反应器性能达到最高。
(3)适宜的Fe2+进入Anammox体与细胞内特定结构结合,促进形成血红素c并参与细菌代谢,保证生理活动正常进行,提高细菌活性,分泌大量EPS,吸收更多胞外养分,使颗粒变得更加致密,结构更加牢固。有助于污泥团聚和沉降,保留生物量,应对高氮负荷冲击,最终增强反应器脱氮能力。然而,由于Fe2+对微生物具有双面作用,其促进/抑制Anammox 过程更加深入的作用机理仍有待研究和完善。

