羊膜填塞疗法治疗外伤性角膜穿孔2例
赵文一 薛劲松 徐英男
南京医科大学附属眼科医院,南京210029
例1,患者,男,51岁,2021年9月30日因左眼溅入铁屑后眼红、眼痛伴视力下降于当地医院就诊,予以左眼角膜异物取出术及左氧氟沙星滴眼液点眼治疗后症状好转。2021年10月20日患者再次出现左眼红痛、流泪、视物模糊,至南京医科大学附属眼科医院就诊。眼科检查:裸眼视力左眼0.12,右眼1.0。裂隙灯显微镜下可见左眼角膜中央偏鼻下方约1.5 mm×2.0 mm灰白色溃疡灶,深达基质层,溪流征(+),周边前房近消失,瞳孔直径约3 mm,对光反射迟钝,晶状体轻度混浊,眼底窥不清(图1A)。光学相干断层扫描(optical coherence tomography,OCT)检查显示角膜坏死组织覆盖在角膜穿孔处,呈楔形(图1B)。右眼未见明显异常。诊断:左眼角膜异物取出术后;左眼角膜溃疡穿孔。患者入院后应用头孢他啶注射液2 g静脉滴注1次/d,加替沙星滴眼液、妥布霉素滴眼液1次/h及加替沙星眼膏、妥布霉素眼膏每晚1次点左眼,并加压包扎。治疗后3 d左眼角膜穿孔未愈合,前房仍未形成,于2021年10月26日行左眼羊膜填塞术。术中于显微镜下彻底清除溃疡区坏死组织,于穿孔处向前房内注入黏弹剂,取2 mm×4 mm眼科用湿性生物羊膜(瑞秀复®,广州瑞泰生物科技有限公司)卷成羊膜塞填塞于穿孔处,用10-0尼龙线呈十字形将羊膜卷缝合于角膜穿孔处,另取单层湿性生物羊膜上皮面朝下覆盖于角膜溃疡表面,其尺寸(直径约5 mm)大于溃疡面1.5~2.0 mm,用10-0尼龙线间断缝合于角膜,角膜缘注入复方氯化钠注射液置换前房黏弹剂,检查角膜水密性,确保前房形成,术后佩戴软性角膜接触镜。术后1 d,左眼视力数指/眼前,表层羊膜和羊膜卷贴附平整,前房形成良好,羊膜植片在位,穿孔区密闭良好;术后3 d,左眼视力0.06,单层羊膜开始溶解,角膜上皮及穿孔区基质组织逐渐生长;术后20 d,左眼视力0.1,羊膜卷与周边组织愈合良好,穿孔区角膜上皮愈合,基质层在羊膜卷支架作用下进一步修复,角膜厚度增加;术后3个月,左眼视力0.3,羊膜卷与周边组织愈合良好(图2~5)。
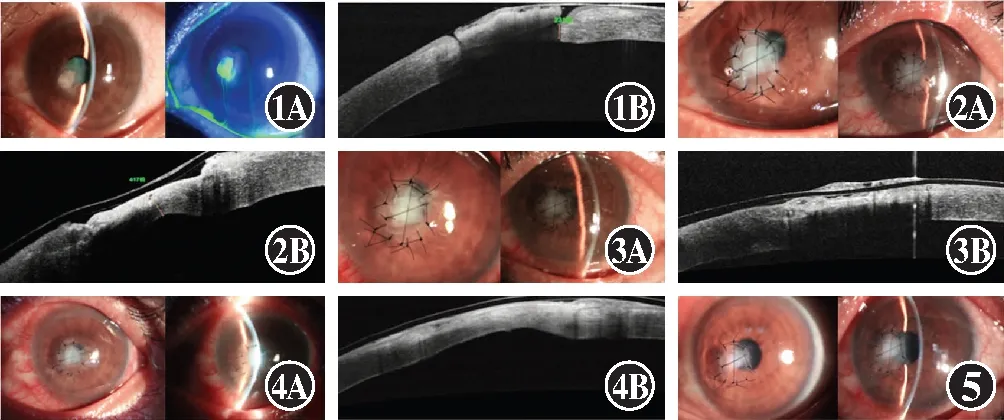
图1 例1患者初诊眼部表现 A:眼前节照相可见角膜类圆形白色溃疡灶 B:OCT检查示角膜坏死组织覆盖在角膜穿孔处 图2 术后1 d眼部表现 A:眼前节照相可见表层羊膜和羊膜卷贴附平整,前房形成良好 B:OCT检查示羊膜片在位,穿孔区密闭良好 图3 术后3 d眼部表现 A:眼前节照相可见角膜表面羊膜开始溶解 B:OCT检查示角膜上皮平滑,穿孔愈合 图4 术后20 d眼部表现 A:眼前节照相可见羊膜卷与周边组织愈合良好 B:OCT检查示穿孔区角膜上皮愈合,角膜厚度增加 图5 术后3个月眼部表现 眼前节照相可见羊膜卷吸收,与周边组织愈合良好
例2,患者,男,25岁,2021年11月18日因左眼被铁屑溅入后视力下降伴异物感于当地医院就诊,行角膜异物取出术,局部抗感染治疗,并于术后7 d及20 d复诊时再次行角膜异物取出术。2021年12月4日因左眼视力明显下降至南京医科大学附属眼科医院就诊。眼科检查:裸眼视力左眼数指/眼前,左眼角膜中央偏下方可见一约1.5 mm圆形角膜穿孔,周边角膜基质铁锈色沉着,前房消失,瞳孔圆,直径约3 mm,对光反射迟钝,虹膜前粘连于角膜穿孔处,晶状体透明,眼底窥不清,眼前节OCT提示角膜穿孔区呈楔形缺损(图6A,B)。诊断:左眼角膜异物取出术后;左眼角膜穿孔。加压包扎4 d后,OCT显示左眼角膜穿孔仍未愈合(图6C),于2021年12月8日行左眼羊膜填塞术,手术方法同例1。术后1 d,左眼羊膜片在位,前房形成良好;术后4 d,左眼视力0.05,羊膜植片平复,前房稳定;术后2个月,左眼视力0.2,表层羊膜完全溶解,羊膜卷吸收,角膜上皮愈合,角膜基质厚度增加;术后3个月,左眼视力0.2,羊膜塞与周边组织愈合良好,角膜瘢痕化,拆除羊膜缝线;术后5个月,左眼视力0.4,验光:-0.25 DS/-1.00 DC×25°=0.8,角膜穿孔区形成角膜白斑,基质层瘢痕愈合(图7~10)。

图6 例2患者初诊眼部表现 A:眼前节照相可见角膜中央偏下方微小圆形孔 B:OCT检查示角膜穿孔区呈楔形缺损 C:保守治疗4 d OCT检查示角膜穿孔未愈合 图7 术后4 d眼部表现 眼前节照相可见羊膜植片平复 图8 术后2个月眼部表现 A:眼前节照相可见表层羊膜完全溶解,穿孔处羊膜卷仍呈白色,但范围缩小 B:OCT检查示角膜上皮愈合,角膜基质厚度增加 图9 术后3个月眼部表现 A:眼前节照相可见羊膜与周边组织愈合良好,角膜瘢痕化 B:OCT检查示角膜厚度基本正常 图10 术后5个月眼部表现 A:眼前节照相可见穿孔区形成角膜白斑 B:OCT检查示基质层瘢痕愈合,角膜厚度稳定
讨论:角膜穿孔可由感染、炎症、外伤等多种原因引起,如不及时诊治,可导致眼球结构破坏及视力丧失。微小型角膜穿孔常见的治疗方法有保守疗法和手术疗法,保守疗法包括局部加压包扎、佩戴软性角膜接触镜、应用组织粘合剂;手术疗法包括角膜清创缝合术、球结膜瓣遮盖术、激光透镜瓣移植术、角膜移植术等[1];但上述疗法可由于组织愈合不良、供体材料缺乏、粘合剂的微弱毒性、透镜基质不可避免的损伤、术后排斥反应、严重散光、影响外观及视力不良等而影响效果[2]。研究发现,羊膜中含有层粘连蛋白、生长因子、酶类等主要生物活性成分,具有促进上皮修复、替代角膜基质、抑制炎症、预防感染、抑制新生血管、抗瘢痕形成等生物学活性[3]。
本研究报道2例角膜异物取出术后角膜穿孔患者,角膜缺损范围均不超过3.0 mm,且位于瞳孔边缘,保守治疗后效果均不佳,故采用羊膜填塞和覆盖法进行手术治疗,术中采用商品化湿性生物羊膜,相比于人新鲜羊膜更易获取并可直接应用,安全性高,透明度好,更贴合创面。此外,采用低温湿态保存技术对人羊膜进行长期保存,最大程度地保留了人羊膜中的生物成分和微观结构,可有效促进角膜完整性的快速重建[4]。与冻干羊膜相比,湿态生物羊膜柔韧性更好,张力性更大,可增加缝合强度,减轻术后散光[5-6],且术后羊膜在病灶处保留时间更长,有利于组织的修复。术中外层羊膜大于溃疡区1 mm左右,一方面可发挥其作为基底膜的支架作用以促进上皮愈合;另一方面使羊膜卷更牢固,与组织贴附更好。此外,患眼术后佩戴软性角膜接触镜,既能减轻眼睑对羊膜的摩擦,缓解缝线对眼表的刺激,又有助于羊膜与角膜的贴附,更有利于促进角膜上皮化。患者术后表层羊膜贴附平整,羊膜卷与周边组织愈合良好,随访过程中羊膜逐渐溶解,前房深度长期稳定,角膜穿孔处瘢痕化愈合,视力不同程度改善。
综上所述,由于外伤性角膜穿孔临床表现多样,一般需根据角膜穿孔大小及时采取对应治疗手段,避免发生感染及视力进一步下降。针对非中央区的微小型角膜穿孔,应用湿性生物羊膜填塞是一种安全有效、简单易行、经济实用的方法。
利益冲突所有作者均声明不存在利益冲突

