响应面法优化提取羊肚菌多酚及其HPLC鉴定分析
芦慧敏,李咏富,2*,邱菊
(1.贵阳学院食品与制药工程学院,贵州贵阳 550005)(2.贵州省农业科学院现代农业发展研究所,贵州贵阳 550006)
羊肚菌(Morchella),又名羊雀菌、羊肚菜或草笠竹,属于子囊菌门、盘菌纲、盘菌目、羊肚菌科大型真菌,因形似羊肚而得名[1,2]。羊肚菌含多糖、优质蛋白、多酚、矿物质和纤维素等营养要素[3-5],具有抗疲劳、抗氧化、抗肿瘤等作用[6,7],是一类低热量、高营养的食用真菌。另外,羊肚菌中含有的脯氨酸类化合物,使其具有独特的香气,这种香气在调味品中得到了广泛的应用[8]。近几年羊肚菌产业大幅度增长,根据行业调查,羊肚菌产量从2018年的3×104t左右增长到2020年的1.5×105t左右,增长了500%左右[9,10]。
多酚类物质是一种天然的抗氧化剂,它含有大量的酚羟基,可以有效地清除自由基[11],因而国内外研究者对其进行了大量的研究。目前多酚的提取方法主要采用溶剂萃取的方式,此外超声辅助提取技术也越来越多地应用于多酚的提取上,并取得了不错的提取效果。Ivana等[12]利用溶剂提取龙葵果多酚,并在乙醇体积分数74.7%、60 ℃下提取40.3 min,提取的多酚含量较高;杨文娟等[13]利用超声辅助溶剂提取花生根多酚,并在体积分数70%乙醇、料液比1:30(g/mL)、45 ℃下提取50 min,提取的多酚中含有较多的儿茶素,且咖啡酸、p-香豆酸、白藜芦醇等也有较不错的吸收;翟飞红等[14]对羊肚菌、香菇、真姬菇进行多酚提取,70%乙醇相同提取条件下,羊肚菌多酚的含量最高,且羊肚菌的抗氧化能力最佳,由此可见羊肚菌中多酚具有较香菇、真姬菇更佳的抗氧化能力;廖霞等[15]对黑脉羊肚菌进行了3种溶剂的提取,对不同溶剂提取的6种多酚组分进行分析,发现甲醇相提取了6种多酚,水相提取了5种,而乙酸乙酯相提取了4种,由此可见溶剂对不同酚类物质的溶出起着关键的作用;卢可可等[16]对三个产地的羊肚菌多酚提取后进行组分测定,没食子酸、原儿茶酸等含量均在500~1 000 μg/g之间,由此可见羊肚菌中含有较为丰富的酚类物质。
近年来,国内外学者对常见食用菌多酚的提取方法进行了研究,但关于羊肚菌多酚提取工艺优化的文献报道很少,而且不同萃取条件下的酚类物质也不清楚,制约了其开发与应用。本研究通过响应面法优化羊肚菌超声辅助溶剂提取多酚类化合物,并对不同提取条件下的羊肚菌多酚进行高效液相色谱(High Performance Liquid Chromatography,HPLC)鉴定,分析不同提取条件下酚类物质提取的差异,以期为羊肚菌后续的开发利用提供参考。
1 材料与方法
1.1 材料与仪器
实验材料:六妹羊肚菌,贵州森之源农业科技有限公司;没食子酸,北京索莱宝科技有限公司;福林酚试剂,北京索莱宝科技有限公司;丙酮,天津市科密欧化学试剂有限公司;无水碳酸钠,天津市致远化学试剂有限公司;乙腈,美国Sigma公司;无水乙醇、甲醇、2-(3,4-二羟基苯基)乙胺、4-羟基苯乙胺、没食子酸、焦性没食子酸、原儿茶酸、对羟基苯甲酸、儿茶素、咖啡酸、绿原酸、荭草苷、芦丁、金丝桃苷、白藜芦醇、木犀草素、槲皮素、阿魏酸,均购于上海麦克林生化科技有限公司。
实验仪器:粉碎机IKA A11 basic,广州艾卡;超声波清洗机,昆山市超声仪器;离心机,湖南湘仪;酶标仪,赛默飞;Agilent HPLC 1260,安捷伦。
1.2 实验方法
1.2.1 羊肚菌多酚的提取工艺流程
将购买的新鲜羊肚菌进行冻干处理后放入密封袋内,干燥器保存。将羊肚菌干品进行粉碎处理,过50目筛备用。称取一定量的羊肚菌粉末,加入不同溶剂,在不同料液比、温度、时间、功率条件下进行提取,超声提取完成后以5 000 r/min离心20 min,从离心管中取出上清液,并用0.45 μm滤头过滤,得到羊肚菌多酚提取液备用。
1.2.2 单因素实验
称取(0.100±0.005)g羊肚菌粉末,以料液比1:60(g/mL)、超声温度45 ℃、超声时间30 min、超声功率300 W为固定因素,分别考察溶剂类型(体积分数为60%的乙醇溶液、体积分数为60%的甲醇溶液、体积分数为60%的丙酮溶液、水)、乙醇体积分数0%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%)、料液比(1:40、1:50、1:60、1:70、1:80)(g/mL)、超声温度25、35、45、55、65 ℃、超声时间30、60、90、120、150、180 min、超声功率240、300、360、420、480 W对羊肚菌多酚含量的影响。以上实验每组三个平行。
1.2.3 响应面实验
基于单因素实验结果,利用Box-Behnken设计实验,以多酚含量为响应值,对实验结果进行回归优化,设计因素水平编码见表1。

表1 Box-Behnken实验因素水平设计Table 1 Box-Behnken experiment factor-level design
1.2.4 多酚测定
多酚的测定以没食子酸作为标准曲线,将没食子酸溶液稀释成0.5、0.25、0.125、0.06、0.03 mg/mL。分别吸取200 μL不同浓度的没食子酸溶液至离心管中,向离心管中加入200 μL福林酚试剂,摇匀,静置10 min,再加入1 mL 75 g/L的Na2CO3,再加入1.6 mL水,避光反应2 h,于765 nm处测定吸光值,平行三次取平均值。以没食子酸浓度为横坐标,吸光值为纵坐标,绘制标准曲线,得回归方程:y=3.90x+0.1,R2=0.994。以同样的方法测定羊肚菌样品的多酚含量。
式中:
A——羊肚菌多酚含量,mg/g;
C——羊肚菌多酚的质量浓度,mg/mL;
V——提取液体积,mL;
N——稀释倍数;
M——羊肚菌粉末质量,g。
1.2.5 HPLC测定羊肚菌单酚
以2-(3,4-二羟基苯基)乙胺、4-羟基苯乙胺、焦性没食子酸、木犀草素、芦丁、对羟基苯甲酸、金丝桃苷、没食子酸、儿茶素、咖啡酸、槲皮素、绿原酸、原儿茶酸、荭草苷、白藜芦醇、阿魏酸为标准品,用甲醇溶解配置成5、25、50、125、250 μg/mL的标准溶液,根据峰面积绘制标准曲线,10种酚类物质的线性关系良好(R2>0.99)。利用HPLC对单因素以及响应面实验的羊肚菌多酚进行稀释、测定,计算样品中单类酚的含量。
HPLC分析条件:色谱柱为YMC-Pack ODS-AQ(250 mm×4.6 mm,3 μm)。流动相A为0.1%甲酸,B为乙腈;梯度洗脱:0~25 min,2% B;25~45 min,12% B;45~55 min,25% B;55~60 min,35% B;60~65 min,40% B;65~70 min,2%B。流速1 mL/min;进样量10 μL;柱温20 ℃;检测波长220、280、320、360 nm。
1.2.6 统计分析
每组实验平行三次,采用Origin 2021对单因素实验结果进行绘图;采用Design-Expert.8软件对各因素进行回归拟合,构建模型,绘制响应曲面图,评估分析统计显著性。
2 结果与讨论
2.1 单因素实验结果分析
2.1.1 不同溶剂对羊肚菌多酚含量的影响
当使用水作为提取溶剂时,羊肚菌多酚的得率最高,其次是体积分数为60%的乙醇溶液、体积分数为60%的甲醇溶液、体积分数为60%丙酮溶液,这可能是由于羊肚菌多酚极性较大,与水的极性更为接近。水可以提取更多的食用菌多酚,这与一些研究者[17-19]提出的鹿茸菇及秀珍菇等其他食用菌中水相提取高于其他相的结论一致。但纯水不一定与羊肚菌多酚的极性完全接近,因此可以向水中加入不同体积的有机溶剂中和极性,从而找到更接近羊肚菌多酚极性的提取液,设计不同有机溶剂体积分数对羊肚菌多酚得率的实验。又因为60%乙醇的得率在体积分数为60%的甲醇溶液、体积分数为60%的乙醇溶液、体积分数为60%丙酮溶液中最高,且乙醇作为溶剂比甲醇、丙酮更加安全可靠,因而在后续实验中将设计不同乙醇浓度的溶剂提取羊肚菌多酚(图1a所示)。
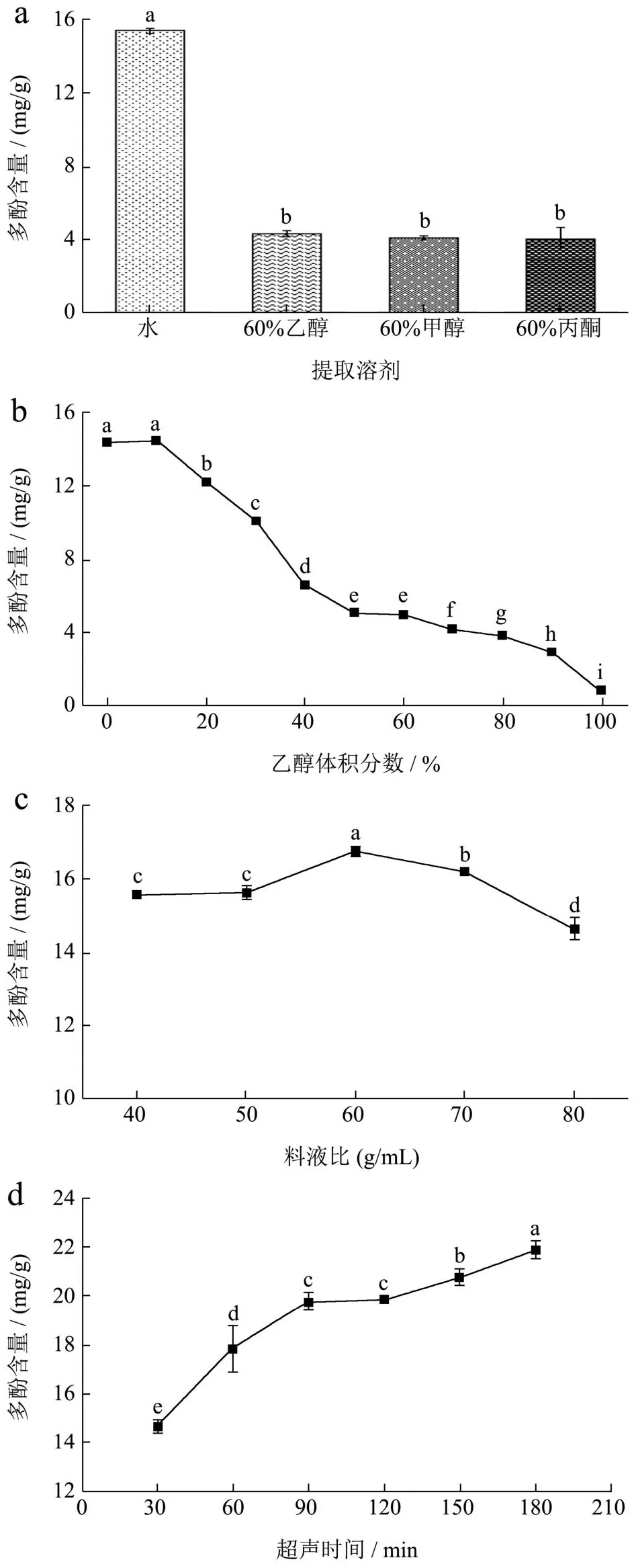

图1 各因素对多酚含量的影响Fig.1 Effect of various factors on the content of polyphenols
2.1.2 不同乙醇体积分数对羊肚菌多酚含量的影响
乙醇体积分数对羊肚菌多酚的得率影响较大,乙醇体积分数在10%~100%范围内,羊肚菌的多酚含量随着乙醇浓度的增大而降低,这可能是由于乙醇浓度的升高,溶剂的极性与羊肚菌多酚的极性差异变大,抑制了某些酚类物质的充分溶解[20],故而羊肚菌多酚的得率下降。当乙醇体积分数为10%时,羊肚菌的得率最高。因此,最终选定乙醇体积分数10%的溶液为最优提取溶剂(图1b所示)。
2.1.3 不同料液比对羊肚菌多酚含量的影响
液料比为1:40~1:60(g/mL)时,羊肚菌多酚会随料液比的增加而增加,其原因在于随料液比的增加,试样与溶剂的接触面积增大,从而避免了介质饱和[21],故而提高了提取效率;到1:60(g/mL)时,多酚的溶出达到平衡;继续增加料液比,多酚含量逐渐下降,这可能是由于杂质的增多抑制了多酚浓度[22]。因此,选定最优料液比为1:60(g/mL)(图1c所示)。
2.1.4 不同超声时间对羊肚菌多酚含量的影响
在180 min内,随着时间的延长,羊肚菌多酚的含量逐渐增多,这可能是由于超声时间的增加,胞内多酚溶出的浓度逐渐增加,在90 min后,溶出的效率相较于前90 min更低,因此,为减少提取成本和提高提取效率,选定最优超声时间为90 min(图1d所示)。
2.1.5 不同超声温度对羊肚菌多酚含量的影响
在25~35 ℃时,羊肚菌多酚的含量随温度的升高而增加,其原因可能是35 ℃时容易软化羊肚菌的细胞壁,进而影响其细胞膜的透过率,从而加速多酚物质的溶出[17];在35~65 ℃范围内,羊肚菌多酚含量随着温度的升高逐渐降低,这可能是由于多酚不耐高温,在更高的温度下极易分解、氧化,导致其多酚结构被破坏,从而降低了多酚的提取[20]。因此,选定最优提取温度为35 ℃(图1e所示)。
2.1.6 不同超声功率对羊肚菌多酚含量的影响
在240~300 W范围内,羊肚菌多酚含量随着功率的增加而增加,这可能是由于超声波产生的空化和振动效应有效地改善了羊肚菌的传质,促进了结构的改变,比如微通道的形成加速了多酚物质的溶出,这大大缩短了羊肚菌多酚的提取时间,并保持了样品的质量[23-25]。在300~480 W范围内,羊肚菌多酚含量随着功率的增加而逐渐降低,这可能是由于过高的功率对羊肚菌的破坏能力更强,导致羊肚菌多酚的结构被破坏[20]。因此,选定最优提取功率为300 W(图1f所示)。
2.2 响应面实验结果分析
2.2.1 响应面模型设计与分析
根据单因素实验,对影响得率较显著的三个因素进行响应面法优化多酚提取工艺,选取料液比、超声温度、超声功率三个因素,共17个试验点进行响应面分析,结果见表2。

表2 Box-Behnken实验设计及实验结果Table 2 Box-Behnken experiment design and result

表3 超声提取回归方程方差分析结果Table 3 Analysis of variance of the constructed regreesion model by ultrasonic-assisted extraction
通过对实验数据进行多元非线性回归分析,建立了预测羊肚菌多酚得率的二阶多项式模型:
Y=22.23-0.46A-0.46B+0.078C-0.81AB+0.011AC-0.35BC-2.31A2-3.35B2-1.00C2
高F值(45.96)和低于0.05的P值(P<0.000 1)表明建议模型具有统计学显著性,而R2值(0.983 4)和R2adj(0.962 0)进一步验证了该模型,模型可解释96.20%响应值变化。相关系数R2接近1,表明模型与实验数据拟合良好。且二次项系数均为负数,有极大值,这也证明了模型的可靠性。根据方差分析结果,料液比和超声温度是影响羊肚菌多酚含量较为重要的因素,独立因素的积极影响意味着他们的积极变化,从而导致响应值的增加;料液比-超声温度对羊肚菌多酚的产率具有较为显著的影响(P<0.01),其他两个的交互作用并不十分明显。由F值大小可知,各因素对羊肚菌多酚含量的影响大致为:超声温度(B)>料液比(A)>超声功率(C)。除了超声功率及其二次效应外,所有统计学上显著的因素和交互作用对羊肚菌多酚的含量都有积极的影响。
2.2.2 响应面分析
各因素间对羊肚菌多酚含量的交互作用影响的响应曲面如图2所示,通过料液比、超声温度、超声功率之间交互关系的直观表现表明,响应曲面均为开口向下的凸型曲面,多酚含量存在最大值。模型响应面3D图清楚地显示了所有分析变化对羊肚菌多酚含量的积极影响。

图2 料液比、超声温度、超声功率之间的交互作用对多酚含量的等高线及响应面图Fig.2 Contour diagram and response surface of the interaction of liquid ratio, ultrasonic temperature and ultrasonic power on polyphenol content
结合P值并结合图2分析可见,图表与上述的方差分析结果一致,液料比-超声温度两者间存在更显著的交互作用。
2.2.3 最佳提取工艺确定及验证实验
通过Design-Expert.8软件求解回归方程,得出最优的羊肚菌提取工艺为:料液比1:66.9(g/mL)、超声温度33.43 ℃、超声功率304.15 W。由于实验室实际操作的局限性,确定试验提取工艺为乙醇浓度10%、料液比1:67(g/mL)、超声时间90 min、超声温度33 ℃、超声功率300 W。在此条件下平行测定三次,验证实验结果的多酚含量为22.39 mg/g,与预测值接近,偏差较小,证实此模型用于羊肚菌多酚提取工艺是可行的。这比前人研究[14-16]提取羊肚菌多酚使用摇床(14.478 mg/g)以及室温放置(4.35 mg GAE/g)的提取方法的得率增加了0.54~4.15倍。
2.3 羊肚菌中单酚物质分析
16种酚类物质混标图谱如图3所示,对照单标图谱,确定混标中16种酚类物质的保留时间,图3中1为2-(3,4-二羟基苯基)乙胺,2为4-羟基苯乙胺,3为没食子酸,4为焦性没食子酸,5为原儿茶酸,6为对羟基苯甲酸,7为儿茶素,8为咖啡酸,9为绿原酸,10为荭草苷,11为芦丁,12为金丝桃苷,13为白藜芦醇,14为木犀草素,15为槲皮素,16为阿魏酸。

图3 16种酚类物质标准品的基峰色谱图Fig.3 Base peak chromatograms of 16 phenolic standards
2.3.1 不同乙醇浓度中酚类物质分析
对羊肚菌不同乙醇浓度提取的10种多酚类物质进行了检测,由表4中十种酚类物质的总量看出,随着乙醇浓度的升高,酚类物质的含量逐渐减小,这与福林酚比色法测定的结果基本一致,这可能是由于乙醇浓度的增大,与某些酚类物质如荭草苷、金丝桃苷等的极性差异较大有关,纯水提取的这10种酚类物质的种类最多,其次是20%、30%乙醇体积分数提取,提取了8种酚类物质;10%、40%乙醇体积分数提取,提取了7种酚类物质。酪胺、没食子酸、对羟基苯甲酸在10%乙醇浓度时得率最高,多巴胺、焦性没食子酸、原儿茶酸、儿茶素、荭草苷、金丝桃苷在纯水提取时得率最高,而木犀草素在20%乙醇体积分数提取时得率最高。

表4 不同乙醇体积分数中酚类物质分析Table 4 Analysis of phenolic substances in different ethanol concentrations (μg/mL)
2.3.2 不同料液比中酚类物质分析
对羊肚菌不同料液比提取的10种多酚类物质进行了检测,由表5中十种酚类物质的总量看出,随着料液比的增加,酚类物质的含量逐渐减小,以mg/g计算得出的结果是1:50(g/mL)时的酚类物质最高,其次是1:60(g/mL),这可能是由于其他未知的酚类物质并未计算其中,导致结果与福林酚比色法有些许差异。使用更高的料液比提取时,检测到了更多的酚类物质,说明较高的料液比有利于这10种酚类物质的溶出。

表5 不同料液比提取酚类物质分析Table 5 Analysis of phenolic substances extracted with different solid-liquid ratios (μg/mL)
2.3.3 不同超声温度下酚类物质分析
对羊肚菌不同超声温度提取的10种多酚类物质进行了检测,由表6中十种酚类物质的总量看出,在25~45 ℃时,随着超声温度的增加,酚类物质的含量逐渐增加;在45~65 ℃时,随着超声温度的增加,酚类物质的含量逐渐减少;且在45 ℃时,检测到的酚类物质种类更多,这说明适当提高温度,有助于酚类物质的溶出,温度过高,酚类物质的内部结构被破坏的更多,导致多酚总量减少。多巴胺、酪胺在35 ℃时得率最高,而焦性没食子酸、原儿茶酸在25℃时得率最高,对羟基苯乙酸、儿茶素、金丝桃苷等在45 ℃时得率最高。

表6 不同超声温度提取酚类物质分析Table 6 Analysis of phenolic substances extracted by different ultrasonic temperatures (μg/mL)
2.3.4 不同超声功率下酚类物质分析
对羊肚菌不同超声功率提取的10种多酚类物质进行了检测,由表7中10种酚类物质的总量看出,功率对这10种酚类物质提取的影响不大,但总体呈现下降的趋势,这可能是由于功率的增加对这10种酚类物质的结构有影响,导致内部结构发生改变,使其由240 W时提取的7种酚类物质减少到了480 W时的5种,这说明较低的功率有利于这10种酚类物质的溶出且保持它们的结构。

表7 不同超声功率提取酚类物质分析Table 7 Analysis of phenolic substances extracted by different ultrasonic powers (μg/mL)

表8 最佳工艺提取酚类物质分析Table 8 Analysis of phenols extracted by optimal process (μg/mL)
2.3.5 响应面优化最佳工艺酚类物质分析
响应曲面中,羊肚菌在乙醇体积分数10%、料液比1:60(g/mL)、35 ℃、300 W下超声90 min,得率最高,以此条件下的提取液进行酚类物质检测,共检测出8种酚类物质,8种酚类物质的总量达到了76.08 μg/mL,达到了较高的含量。
3 结论
本文采用响应面法对羊肚菌多酚的提取工艺进行了优化,首先对溶剂类型、乙醇浓度、料液比、超声时间、超声温度、超声功率等提取条件进行了单因素优化,并对影响较为显著的几个因素进行三因素三水平Box-Behnken设计,得出了最佳工艺参数:10%乙醇体积分数,料液比1:67(g/mL),超声时间90 min,超声温度33 ℃,超声功率300 W,此工艺条件下提取羊肚菌多酚含量为22.39 mg/g。根据响应面实验数据分析,模型较为显著(P<0.000 1),失拟项不显著(P>0.05),拟合程度高(96.2%),三因素对得率影响顺序为:超声温度>料液比>超声功率。同时对各提取条件下的羊肚菌多酚进行了HPLC检测,共检测出10种酚类物质,且各单因素条件下提取的10种酚类物质的含量曲线也与福林酚比色法测定数据基本一致。另外,HPLC测定出其他峰谱成分仍然未知,具体还需进一步研究。

