肾结石老年患者输尿管软镜治疗后重复手术和结石相关事件的风险因素
詹扬 戴廷山 范振永 王二朋 王海江 梅国徽
(阜阳市第二人民医院泌尿外科,安徽 阜阳 236000)
输尿管软镜(FURS)是治疗中小型肾结石的一种有效且侵入性较小的方式,FURS后无结石率为73.0%~93.2%〔1〕。由于技术进步,FURS越来越多地用于治疗肾结石。由于结石复发是十分常见的,预防未来结石事件是除无结石率之外的重要结果〔2〕。结石复发和未来干预显著损害患者的生活质量,并增加医疗费用。然而,关于未来与结石相关的事件的数据很少。几项研究报告了相对较小的队列中结石事件的FURS后复发率,这些研究强调了FURS后复发的风险〔3〕。此外,针对所有肾结石患者的复发预测工具并不能充分适用于术后队列。因此,开发一个专门针对肾结石患者手术人群的精确预测模型尤为重要〔4〕。本研究是一项大型、单中心、回顾性队列研究,旨在评估FURS后未来事件的风险。对所有患者进行随访以确定结石复发或结石相关事件,并在每次就诊时常规询问是否有任何症状。
1 资料与方法
1.1一般资料 本研究通过医院伦理委员会批准,回顾性分析2018年1月至2022年4月接受FURS治疗肾结石合并或不合并输尿管结石的316例患者数据,年龄61~88岁,平均(68.92±5.24)岁;男194例,女122例;体质量指数(BMI)17.32~29.71 kg/m2,平均(23.84±2.76)kg/m2;右侧肾结石122例,左侧194例;并发输尿管结石212例;平均最大结石尺寸(13.75±3.48)mm;平均结石负荷(23.15±1.52)mm;结石手术史123例;术前尿路感染(UTI)50例;辅助手术冲击波碎石术(SWL)7例、输尿管镜检查7例、经皮肾镜碎石术(PCNL)1例;最大残留结石尺寸:肾-输尿管-膀胱造影上无结石181例、<4 mm 84例、≥4 mm 51例;结石成分:草酸钙/磷酸钙279例、尿酸19例、胱氨酸3例、鸟粪石/碳酸盐磷灰石13例、其他2例。在随访期间,49例患者经历了重复手术,64例经历了结石相关事件。纳入标准〔5〕:①年龄>60岁;②接受单次体外超声波碎石治疗失败或拒绝经PCNL取石;③经影像图像确诊为肾结石;④患者均行FURS。排除标准〔6〕:①存在解剖异常者,如孤立肾、膀胱切除术后、重复系统和马蹄肾等;②东部肿瘤协作组体能状态>2分;③临床资料不完整者;④3个月内失访者。
1.2资料收集 从患者记录中收集年龄、性别、BMI、最大结石直径、结石负荷(每颗结石最大直径的累积总和)、结石手术、UTI、术后残留碎片(RF)、结石成分、术后药物治疗(噻嗪类、柠檬酸钾、别嘌醇或硫普罗宁)>3 个月及未来同侧结石事件。在第1个月随访中通过肾脏-输尿管-膀胱造影(KUB)射线照相评估术后残留碎片。结石事件被定义为同侧肾绞痛、症状性输尿管结石、梗阻性尿路感染和手术干预。肾绞痛被定义为腰痛或腹痛,最可能的原因是尿结石。由于无法确定结石的来源(左侧或右侧输尿管),因此不包括其他事件,如血尿或无症状自发排出。任何预先计划的再干预(分阶段干预)均不被视为手术复发。
1.3治疗方法 输尿管镜检查程序:患者术前2~4 w接受了双J支架管置入,以扩张输尿管,避免输尿管损伤。首先,通过输尿管硬镜检查对输尿管进行仔细评估,以识别结石或狭窄。输尿管结石被破碎并取出后,插入输尿管通路鞘(12/14 Fr 或14/16 Fr)。输尿管软镜检查用于肾结石碎裂,采用200 μm钬激光纤维。在专家的监督下,共有10名外科医生在该队列中进行了手术。根据石头大小和硬度,使用除尘和上篮技术。较大的结石首选除尘,而较小的结石则通过篮式导管破碎和提取。术后常规置入双J管支架。根据结石大小和位置,通常建议残留结石>10 mm 的患者进行第2次FURS、SWL或PCNL。初始治疗后,所有患者都得到指导,如每日液体摄入量和均衡饮食。为高危患者(主要是尿酸或胱氨酸结石患者)提供结石特异性代谢评估和医学预防。所有患者在第1个月接受KUB和超声检查(US)评估,随后每6个月进行1次。在每次就诊时,患者都会被常规询问任何与结石相关的事件。
1.4统计学分析 采用SPSS26.0软件行独立样本t检验、Mann-WhitneyU检验、χ2检验或Fisher精确检验。
2 结 果
2.1重复手术的多因素分析 以年龄、性别、BMI、并发输尿管结石、结石手术史、术前尿路感染、最大结石直径、术前结石负荷、最大残留碎片、结石成分、医疗预防时间为自变量,以重复手术为因变量进行Logistic分析。结果显示,年龄>60岁且<68岁、有结石手术史、术前结石负荷≥20 mm及术后最大残留碎片≥4 mm是老年肾结石患者FURS术后重复手术的独立危险因素(P<0.05)。见表1。
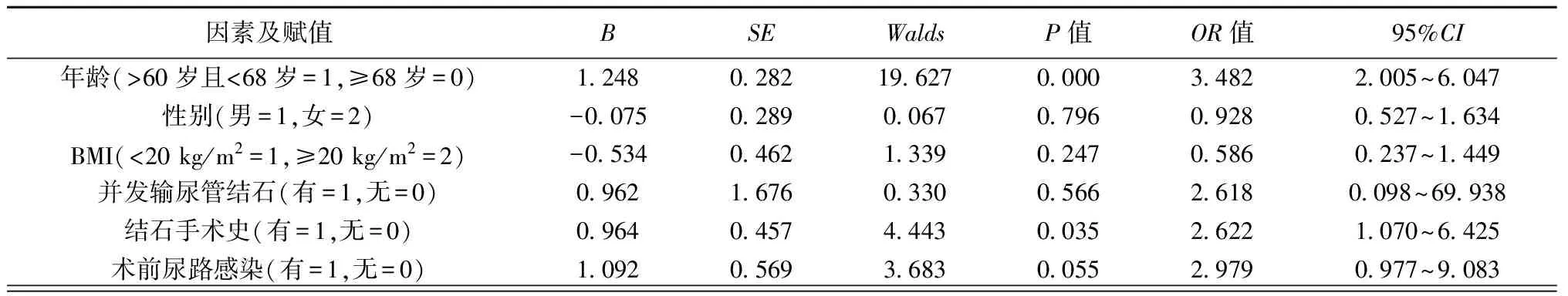
表1 肾结石患者FURS术后重复手术的多因素Logistic回归分析
2.2结石相关事件的多因素分析 以年龄、性别、BMI、并发输尿管结石、结石手术史、术前尿路感染、最大结石直径、术前结石负荷、最大残留碎片、结石成分、医疗预防为自变量,以结石相关事件为因变量进行Logistic分析。结果显示,年龄>60岁且<68岁、有结石手术史、术前结石负荷≥20 mm及术后残留碎片≥4 mm是老年肾结石患者FURS术后结石相关事件的独立危险因素(P<0.05)。见表2。
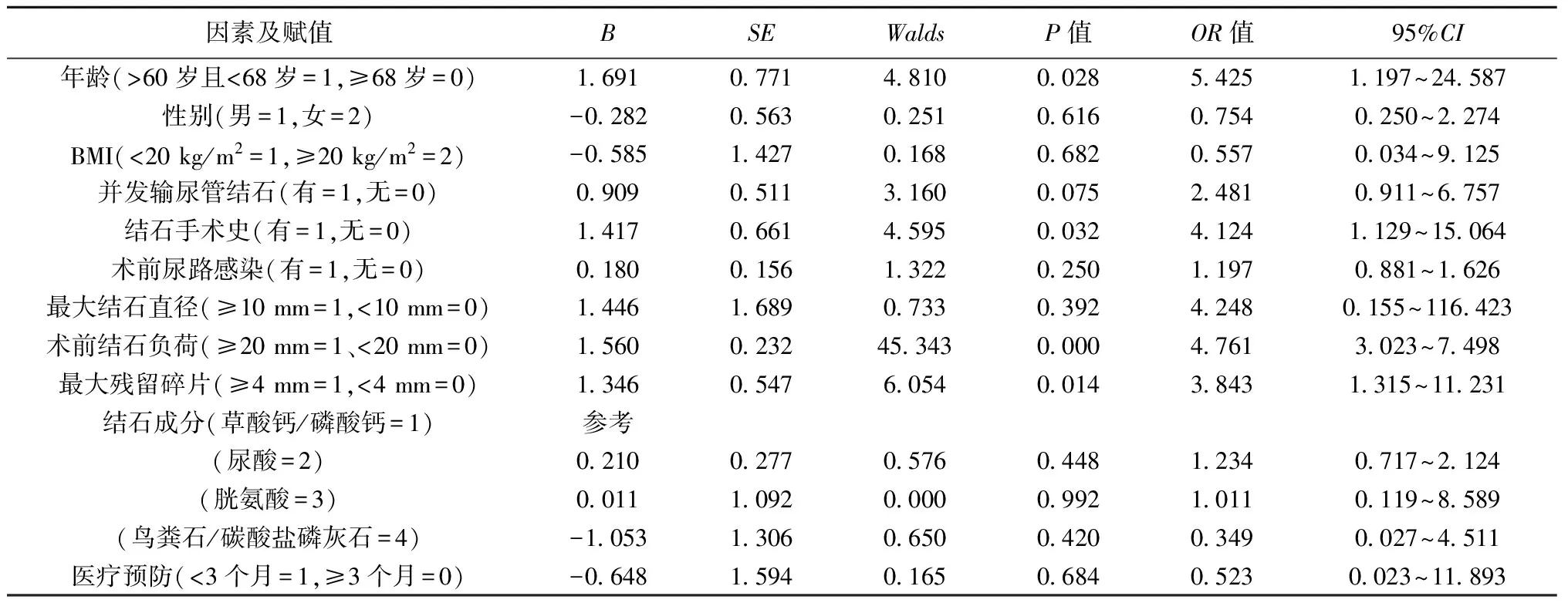
表2 肾结石患者FURS术后结石相关事件的多因素Logistic回归分析
3 讨 论
迄今为止,只有少数研究检查了FURS后的随访结果。在FURS后781例患者的回顾性研究中,在中位随访4.2年期间重复手术率为20%〔7〕。尽管PCNL推荐用于结石负荷≥20 mm的患者,但该队列中的大多数参与者有多颗结石导致结石负荷增加,从而选择FURS〔8〕。在肖路〔9〕的研究中,约1/5的患者在FURS后经历了任何与结石相关的事件。重要的是,即使在没有术后残留碎片的患者中,这些事件也存在一定的风险。这意味着即使是成功的FURS也不一定免于手术干预或结石相关事件〔10〕。且除手术干预外,关于其他与重复手术或结石相关的事件,之前的研究均未报道。
本研究中确定了几个重要的风险因素。年龄较小、有结石手术史、较大的术前结石负荷及较大的术后残留碎片与重复手术及结石相关的事件都相关。还有一些其他研究也已经确定了结石复发的风险因素〔11〕。术后残留碎片通常保持无症状或自发排出,而一些碎片可能是有症状的或作为结石复发的病灶〔12〕。此外,KUB很难区分<4 mm的碎片,尤其是在肥胖患者中。由于对尺寸的高估,选择了不同的超声截断值6 mm〔13〕,因此会对治疗结果造成一定的不良影响。另外,术前结石负荷也是独立于术后残留碎片大小的危险因素。尚未确定术前结石特征(包括结石负荷)与未来干预风险之间的关联〔14〕。然而有研究表明〔15〕,单变量分析揭示了较大的结石负荷(结石长度的总和)与FURS后重复手术具有相关性。由于已经报道了术前结石体积与术后残留碎片之间的关联,结石负荷可能不仅与术后残留碎片的大小相关,还与术后残留碎片的数量相关,但没有经过验证的方法来评估术后残留碎片数量,因为测量KUB射线照片中微弱的不透射线阴影的数量具有挑战性〔16〕。肾结石复发评分及其修订版是公认的有症状肾结石复发的风险预测因子。然而,大多数研究人群没有接受过手术,并且该模型在预测手术队列中重复手术风险的判别能力有限〔17〕。 在Iremashvili等〔18〕研究中,报告了所有外科手术后重复结石手术的预测因素(URS 、SWL和PCNL),值得注意的是,只有少数患者接受了医学预防,而患者都接受了营养师的饮食指导。此外,有指南建议基于24 h尿液分析的综合评估进行预防性治疗,但这些措施在临床实践中并未得到充分利用〔19〕。这是由于24 h尿液分析有几个缺点,包括解释的复杂性、需要重复收集及预测复发的准确性低,还需要确定可能从尿液分析中受益的患者〔20〕,因此临床应用率低。本研究中的一些风险因素均表明存在潜在的代谢异常。在这方面,以代谢评估为指导的选择性治疗可能对预测工具中的高危患者有效。此外,鉴于临床治疗中部分患者的依从性差,因此对其进行宣教,让其了解可能存在的风险将激励他们坚持饮食和医疗预防〔21〕。
本研究也存在一些局限性:首先,研究是在一家三级医院进行的,研究人群是由结石相对复杂的患者组成;手术策略的差异,即除尘或碎裂,也可能导致不同的结果,因此,需要多中心研究来验证研究结果。然而,少量的外科医生和标准化的随访方案可以帮助减少观察偏差。其次,如果患者未接受医疗护理或不回忆事件,则难以捕捉所有与结石相关的事件,因此,选择使用下一个结石干预作为主要终点,因为其相对稳健,对患者和医疗经济具有较高的临床意义。第三,回顾性设计存在固有的局限性。对术后残留碎片进行二次手术或观察的决定没有标准化,家族史或24 h尿液分析数据也不包括在模型中。且坚持饮食或药物预防复发也可能影响结果,需要对这些变量进行前瞻性研究以改进预测模型。第四,FURS后未进行计算机断层扫描。虽然KUB评估术后残留碎片会使患者较少暴露于电离辐射中,避免了部分电离辐射对患者身体造成的危害,但其与计算机断层扫描相比,其评估术后残留碎片的能力有限。因此应进一步研究适当的计算机断层扫描,检测肾结石患者术后残留碎片的优势。
综上,进行肾结石老年患者FURS治疗后重复手术和结石相关事件的风险因素有年龄>60岁且<68岁、有结石手术史、术前结石负荷≥20 mm 和术后残留碎片≥4 mm。临床上可通过对这些因素进行有效治疗。

