几种常见脂肪醇的氢键结构探究
——红外光谱测定结合量化计算的实验
刘禹,郑纪鸣,宗陈纳言,吴红,2,*,胡万群,2,*
1 中国科学技术大学化学与材料科学学院,合肥 230026
2 化学国家级实验教学示范中心(中国科学技术大学),合肥 230026
早在1936年,诺贝尔化学奖获得者鲍林就在《化学键的本质》一书中专门为氢键留下一章,然而,直至现在,氢键特性的研究仍是热点的科学研究之一[1-4],随着研究的深入,人们越发认识到氢键在物理、化学、材料及生命科学中起到的重要作用[5-7]。在氢键特性的研究中,我国科学家也做出了重要贡献。例如,在2013年我国科学家在Science上发表“通过用自主创新技术改装成的非接触原子力显微镜拍下了世界上第一张氢键照片”的研究成果[1],引起了科学界的轰动。研究氢键的方法众多,其中实验测定红外光谱和理论计算振动光谱相结合的研究方法得到广泛采用[8-13]。红外光谱无论是实验技术还是理论计算均已经历了成熟性的发展,广泛应用于物质的成分分析;计算化学以大量的数值运算对化学现象进行系统的理论模拟,用于检验、对照现实实验中的化学现象,还可用于预测、修正以及发展化学理论[14]。因此,将对氢键的研究内容和研究方法引入实验教学中,对于学生理解氢键形成的本质及其在相关领域中的研究意义具有重要作用,对于开拓学生的科学视野和创新思维具有一定的促进作用。
Gaussian软件是目前计算化学领域中使用范围极广的一款计算软件。它由约翰·波普(John. A.Pople)等人于1970年开发。Gaussian软件图形化界面友好、大多参数已被设置好,大大降低了科研工作者从事理论与计算化学研究的门槛,同时也是初学者利用量子力学理解化学体系的首选工具。本实验使用Gaussian 16软件进行计算,其中采用密度泛函理论(Density functional theory),在B3LYP/6-31+G(d,p)水平上结合色散校对结构进行优化和频率计算,从而获得红外光谱的计算数据。对于存在弱相互作用的有机分子体系,结合色散校正的B3LYP泛函通常可以给出较为准确的结果[15,16]。实验中对几种脂肪醇-四氯化碳(CCl4)溶液进行红外光谱测定,对应的所有结构选用IEFPCM溶剂模型来进行计算。
红外光谱法具有灵敏度高、分辨率高、测量准确快速的特点,在众多高校的仪器分析实验课程中均有开设。调研国内外的相关教材和文献并结合现有的红外光谱实验教学,引入量化计算,以几种常见脂肪醇的氢键结构探究为例,量化计算与实验的结合,引导学生对微观结构联系宏观现象的思考,进而引发学生探究实验宏观现象与微观结构的规律,从微观层次上认识分子间作用力、氢键的形成与红外吸收频率的影响。
1 教学设计
1.1 实验器材和试剂及计算软件
实验仪器:傅里叶变换红外光谱仪(德国Bruker公司,TENSOR II型),液体池(液膜厚度0.025 mm),25 mL容量瓶,移液管,分析纯的无水乙醇、正丙醇、异丙醇和正丁醇,四氯化碳(纯度98%),实验试剂均来自国药集团化学试剂有限公司,所用试剂未经进一步处理。
计算软件:Gaussian 16,GaussView 6.0[17];台式电脑:Lenovo微型计算机(启天W435-B444)。
1.2 实验内容和学时安排
首先,学生应在课前对实验内容进行预习,包括氢键的定义[1-4,10-13]、红外光谱的原理[18,19]以及量化计算的背景知识[20,21],在课堂上以翻转课堂的形式进行考核;课中需要完成红外光谱测定和量化计算两部分实验内容。为合理安排时间并提高学生的协作能力,红外测定和量化计算均为分组完成(通常2-4人一组,合作完成);课后学生需要分析实验结果,完成实验报告。实验项目的总学时约5学时。
1.3 红外光谱测试
(1) 溶液配制:用移液管分别移取0.25、0.50、1.25、1.75、2.25 mL的乙醇溶液于5个25 mL容量瓶中,再依次加入四氯化碳溶液稀释、定容、摇匀,得到乙醇-四氯化碳的体积百分比(V/V%)为1%、2%、5%、7%和9%的溶液。同样的方法,配制不同体积百分比的正丙醇、异丙醇、正丁醇的四氯化碳溶液,待测。
(2) 设置测试参数:光谱范围4000-400 cm-1,分辨率4 cm-1,扫描16次。
(3) 分别测试乙醇、正丙醇、异丙醇、正丁醇和四氯化碳及上述(1)配制溶液的红外光谱。
1.4 量化计算
1.4.1 建立结构模型
打开GaussView 6.0软件,依次点击“File”-“New Molecule Group”后,再依次点击“Builder”-“Element Fragment”。在弹出的周期表中选择碳元素,选择四面体构型,在建模窗口绘制乙烷分子骨架。再次点击“Builder”-“Element Fragment”,选择醚键形式,将乙烷分子中的一个氢原子替换为羟基,构建好乙醇的分子模型。依次点击“File”-“Save”,将此模型保存为*.gjf格式的文件。按上述方式,分别建立乙醇、正丙醇、异丙醇、正丁醇的单分子、二聚体、三聚体构型(图1),其中二聚体、三聚体的分子间O-H…O氢键距离调整为合适的长度(约200 pm)。
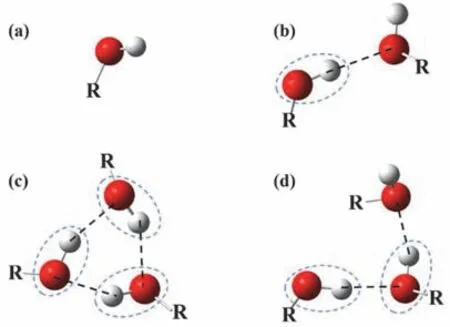
图1 氢键作用下的脂肪醇构型的单体(a)、二聚体(b)、环状三聚体(c)和链状三聚体(d)的构型
三聚体考虑环状和链状两种构型:三个O-H分别两两形成氢键,形成闭合的环状构型;三个O-H依次作用形成两个氢键键合的O-H和一个自由的O-H。构型如图1所示,其中虚线框中O-H的为氢键缔合的O-H (记为Bonded OH),其余为自由的O-H (记为Free OH);红色和白色的球分别表示氧和氢原子,R表示烷基。
1.4.2 建立输入文件
以乙醇单分子模型进行结构优化和频率计算为例,输入文件中的参数设置如表1所示。计算不同结构时设置的chk文件名、笛卡尔坐标不同,其他设置相同。
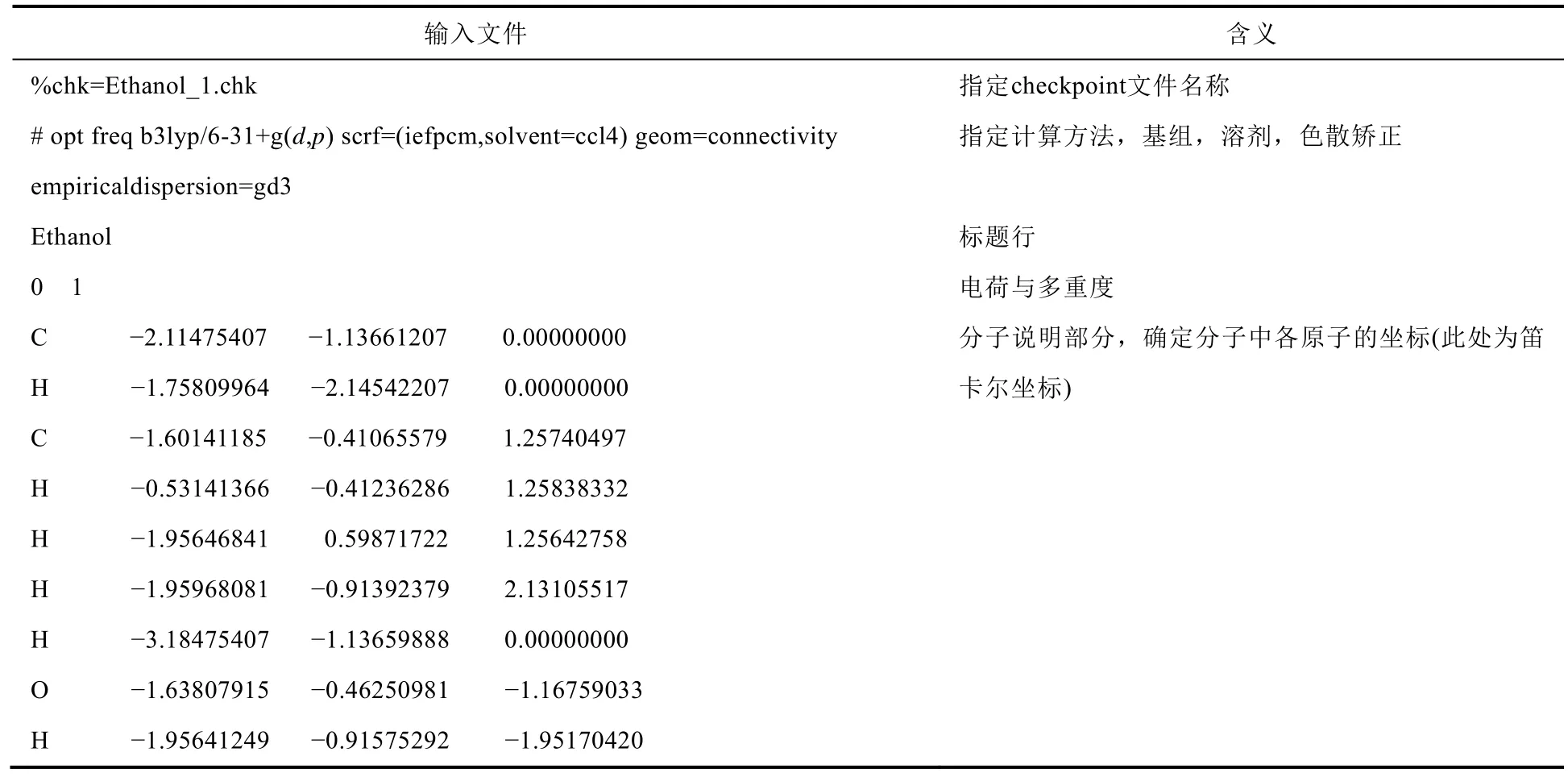
表1 Gaussian计算输入文件的参数设置
1.4.3 查看输出信息
用文本编辑软件打开*.log文件可查看全部计算结果数据。使用GaussView 6.0打开*.log文件,依次点击“Results”-“Summary”,查看计算结果。若几何优化结果收敛,频率分析无虚频出现,则认为其分子构型稳定。
依次点击“Results”-“Vibrations”,查看优化后分子的频率计算结果。点击“Start Animation”,可以查看分子简振模式的振动动画图像。为使B3LYP泛函、6-31+G(d,p)基组进行的频率计算结果更加准确,需要对计算得到的频率进行校正。在“Scale frequencies?”选项栏中选择“Specify...”,输入校正因子0.9648[22]。点击“Spectra...”,可查看红外吸收光谱。在弹出的谱图中依次点击“Plots”-“Properties...”,对x轴和y轴均勾选“Invert Axis”选项,此时谱图与实验所得谱图的排布形式相同。
2 结果与讨论
2.1 红外光谱测试数据处理
(1) 测试的乙醇、正丙醇、异丙醇、正丁醇和四氯化碳的红外光谱图,如图2所示,主要吸收峰的官能团归属如表2所示。

表2 红外吸收峰的官能团归属
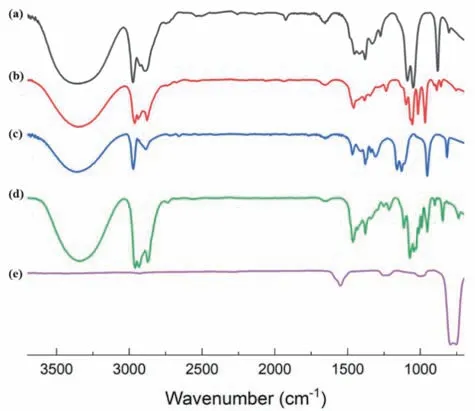
图2 测试的纯溶剂的红外光谱图
通过对图2(a)-(e)中测试的5个样品的红外光谱图和对应的标准谱图比对分析:在测试条件相同的情况下,测试样品的红外谱图与标准谱图中的主要吸收峰的峰位置、峰形、峰的相对强度与标准图谱完全吻合,说明未经处理的试剂纯度符合本实验的红外光谱测试要求。同时,从图2(e)可以看出,四氯化碳在4000-1700 cm-1没有红外吸收,因此,以四氯化碳为溶剂,配制不同体积比的脂肪醇(乙醇、正丙醇、异丙醇和正丁醇)-四氯化碳溶液,观察氢键作用下的脂肪醇中羟基的红外频率变化,不会干扰谱图分析。
(2) 分别测试配制的不同体积百分比的脂肪醇-四氯化碳溶液的红外谱图,如图3所示。
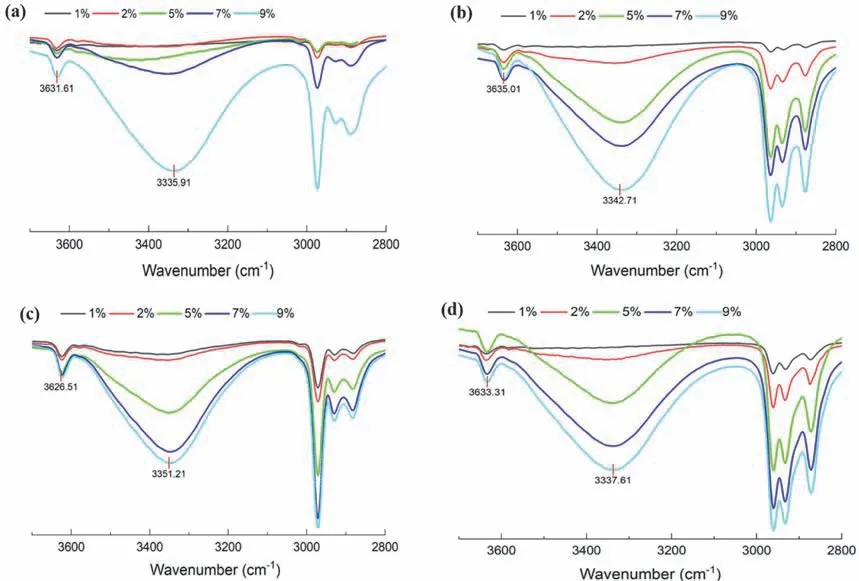
图3 脂肪醇-四氯化碳溶液的红外光谱图
从图3可以看出,在脂肪醇-四氯化碳溶液中,在体积百分比1%时,几种脂肪醇均出现了~3600 cm-1以上的羟基游离峰;当脂肪醇-四氯化碳的体积百分比逐渐增大时,可看出游离羟基峰和缔合羟基峰的强度均随之增大,不同的脂肪醇的缔合羟基吸收频率有所位移,在体积百分比为9%时呈现出较大的~3300 cm-1附近的氢键缔合羟基峰,说明溶液中存在两个或多个分子缔合的分子间氢键[23]。
2.2 量化计算结果
计算得到的四种脂肪醇(乙醇、正丙醇、异丙醇和正丁醇)的单体、二聚体和三聚体的结构和O-H振动频率ν(cm-1),分别如图4和表3所示。
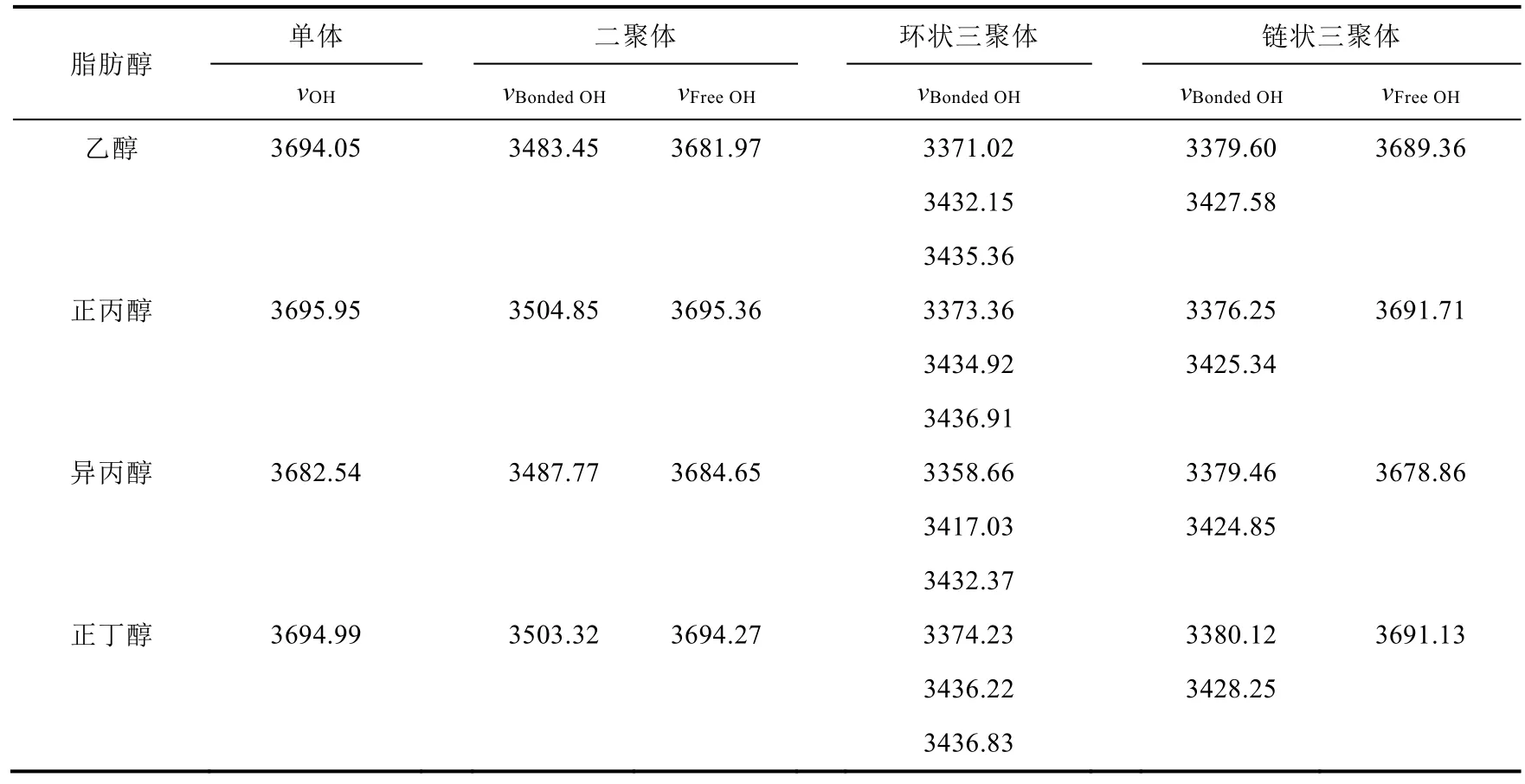
表3 计算的四种脂肪醇(乙醇、正丙醇、异丙醇和正丁醇)的O-H振动频率ν (cm-1)
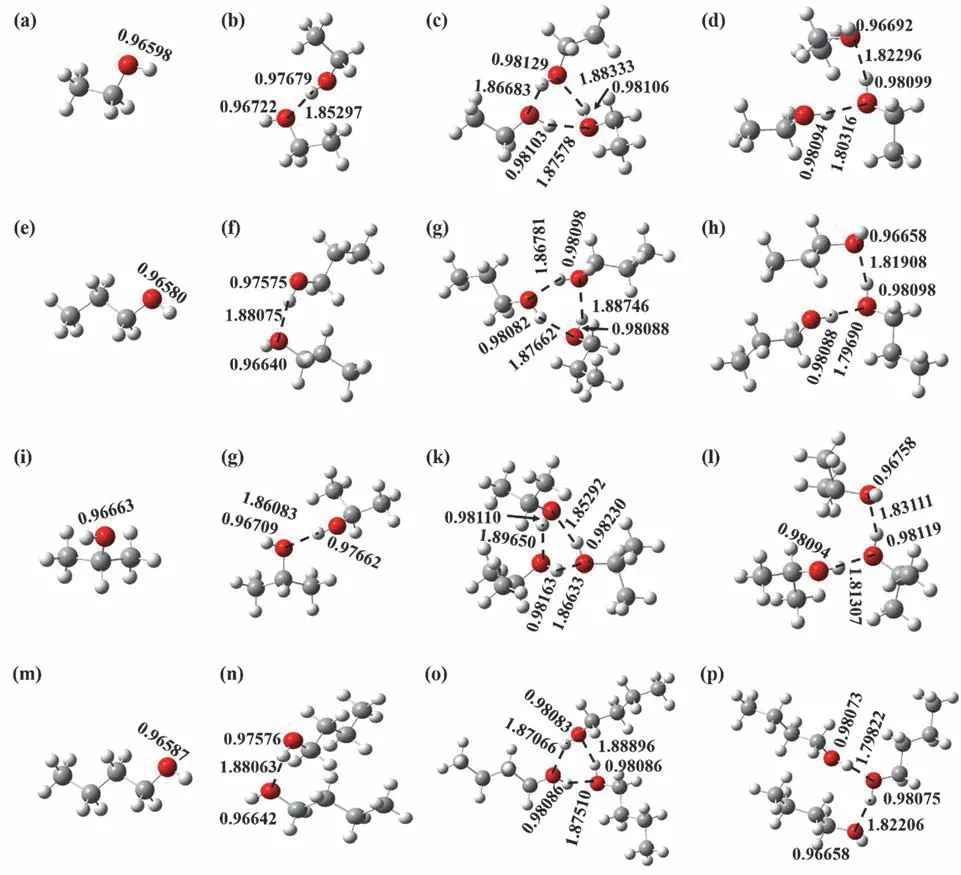
图4 计算优化后的脂肪醇的单体、二聚体、环状三聚体和链状三聚体的结构
从图4中可以看到,这几种脂肪醇的二聚体和三聚体的结构中,形成的O-H…O氢键键长约为1.8-1.9 Å (1 Å = 0.1 nm)。比较优化后的单体、二聚体和三聚体中的O-H键长,如乙醇单体中O-H键长为0.96598 Å,二聚体中氢键缔合的O-H键长为0.97679 Å,环状三聚体中氢键缔合的O-H键长为0.98129、0.98106和0.98103 Å和链状三聚体中为0.98098和0.98088 Å,可以发现氢键作用改变了O-H键长,在乙醇二聚体和三聚体中氢键缔合的O-H的平均键长相对于乙醇单体中O-H来说逐渐增大,而二聚体和三聚体中自由的O-H的平均键长(0.96722和0.96692 Å)与乙醇单体中(0.96598 Å)的非常相近。对于正丙醇、异丙醇和正丁醇也呈现出同样的规律。
比较单体、二聚体和三聚体中O-H的计算伸缩振动频率,可以发现在氢键作用下,随着分子数目的增加,氢键缔合作用下的O-H伸缩振动频率逐渐减小。而二聚体和链状三聚体中自由O-H伸缩振动频率与单体的O-H伸缩振动频率几乎一致。而从上述的结构分析可知,从单体、二聚体到三聚体,氢键作用使得O-H的键长逐渐增大,自由O-H的键长几乎不变,这也说明了氢键作用影响O-H伸缩振动频率与氢键作用改变O-H键长变化有关,O-H键拉伸,O-H伸缩振动频率减小[10]。
2.3 结果对比分析
如图5所示,选择2800-4000 cm-1的振动峰区域,比较实验测得的不同体积百分比(V/V%)下的脂肪醇-四氯化碳溶液的红外光谱图与相应脂肪醇的单体、二聚体、三聚体的计算红外谱图,从而分析分子间氢键对O-H振动频率的影响。从图5中看出,计算所得的红外谱图中自由O-H的振动峰与实验测得红外光谱中3600 cm-1以上的峰对应;脂肪醇单体和链状的多聚体中存在自由的O-H;脂肪醇二聚体、三聚体中氢键缔合的O-H振动峰出现在3300 cm-1附近的宽峰中。
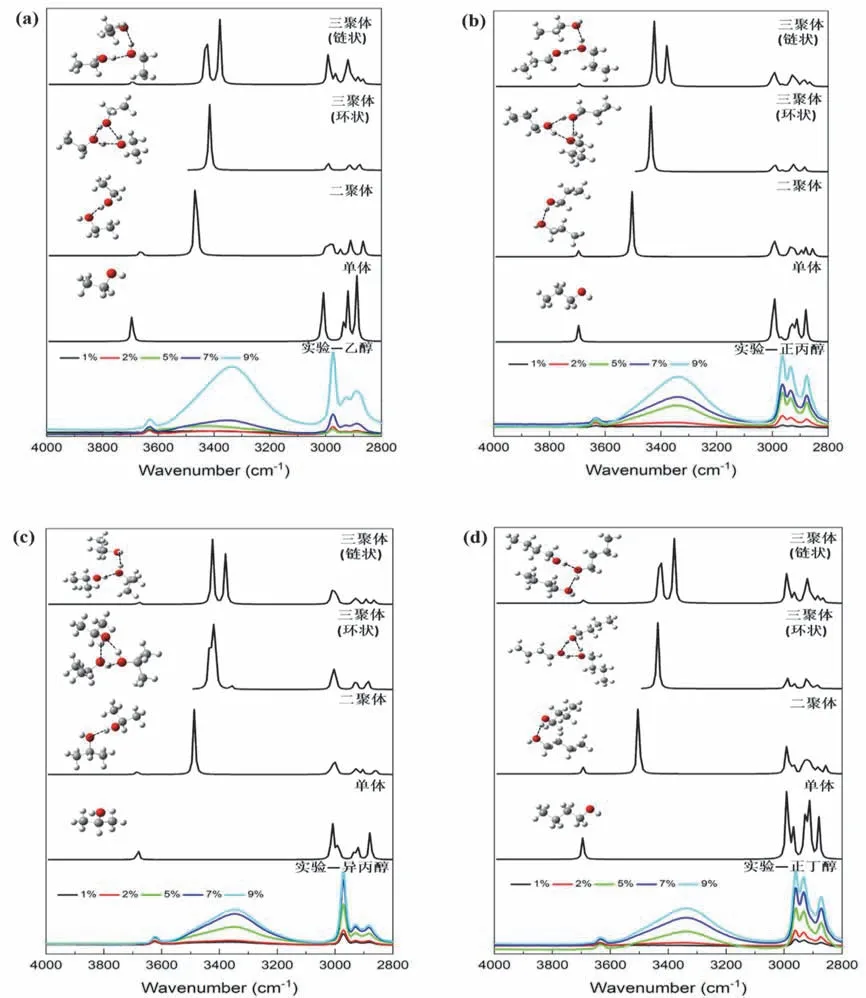
图5 实验和计算的红外光谱图
在脂肪醇-四氯化碳溶液的体积百分比为1%时,O-H伸缩振动区域主要有3600 cm-1以上的吸收峰,可以判断3600 cm-1以上的峰为脂肪醇单体的O-H振动峰,此时溶液中主要存在的是脂肪醇游离的分子。当脂肪醇-四氯化碳溶液的体积百分比为2%时,3300 cm-1附近出现微弱的吸收峰,溶液中的脂肪醇在氢键作用下开始形成多聚体。随着脂肪醇-四氯化碳的体积百分比从5%、7%增大到9%时,3300 cm-1附近的峰强度明显增加,反映了溶液中的脂肪醇多聚体数目也明显增加。除了本实验中考察的脂肪醇二聚体和三聚体,溶液中可能还存在环状和链状的脂肪醇四聚体、五聚体和六聚体等多种形式[24,25],可作为课后探究模块的内容。当脂肪醇-四氯化碳的体积比增大时,3600 cm-1以上的吸收峰可能是脂肪醇的单体和链状的多聚体两者中协同的自由O-H伸缩振动峰,而吸收峰强度只有稍许增加的原因可能是形成的每个链状多聚体只包含一个自由O-H,而氢键缔合的O-H的数目和构型相对丰富[26]。
3 结语
该实验以几种常见脂肪醇的氢键结构探究为例,设计了一项红外光谱测定结合量化计算的综合实验。弥补了传统红外光谱测定实验教学中存在的一些不足:如教学内容相对单一,主要侧重于以红外光谱实验测试为主的化合物的定性和定量分析;谱图解析中,对谱图信息对应的微观结构缺乏深刻认识;对分子间作用力知识点涉及较少,缺乏对氢键影响基团频率位移的深入探究。
通过该教学的实施,不仅可以使得学生掌握红外光谱的基础知识:如红外振动光谱的原理、样品制备、仪器操作、谱图解析,还能培养学生分析数据、处理数据的能力;量化计算与实验的结合,深入探究氢键的结构与形成,引导学生对微观结构联系宏观现象的思考,培养学生思辨和创新能力,开拓科学思维,为以后的学习和科研工作奠定基础。
4 实验改进的特点及创新性
(1) 教学内容创新:在传统的红外光谱测定实验中,增加探究氢键作用的内容,结合量化计算,引导学生对微观结构联系宏观现象的思考。
(2) 教学体系简单:以几种脂肪醇-四氯化碳为红外光谱测定实验对象,体系简单,易于推广,也在一定程度上保证了教学时间内完成相应量化计算的可行性。
(3) 教学方法普适:实验结合量化计算探究氢键对基团振动频率影响的方法可拓展用于其他适宜的教学体系中。

