HPLC 法同时测定曲安奈德苯海拉明水杨酸酊中三种有效成分的含量
陈霞飞,简淑娟,林凤屏,刘丽婷,欧阳珠,黎晓敏
惠州市食品药品检验所,广东 惠州 516001
曲安奈德苯海拉明水杨酸酊是惠州市皮肤病防治研究所生产的医院制剂,与药厂制剂比较,具有密切结合临床、适应性强、治疗作用明确、专科特色强、副作用少等优点,其主要成分是醋酸曲安奈德、盐酸苯海拉明、水杨酸,具有抗菌消炎和抗过敏等作用。临床主要用于治疗神经性皮炎、慢性湿疹、结节性痒疹、皮肤淀粉样变及疥疮结节等。由于原制剂的质量标准中只有高效液相色谱法测定醋酸曲安奈德的含量,而盐酸苯海拉明、水杨酸采用的是滴定法,其中盐酸苯海拉明的测定中使用了大量的易制毒化学品三氯甲烷。三氯甲烷有毒,为可疑致癌物。为了实现对该制剂质量的更好把控,通过查阅相关文献资料[1-9],本研究建立了高效液相色谱法同时检测醋酸曲安奈德、盐酸苯海拉明和水杨酸含量的方法,有利于更好地控制该制剂的质量和减少有毒有害溶剂的使用。
1 仪器与试药
1.1 仪器
高效液相色谱仪(安捷伦科技公司,型号:1260);高效液相色谱仪(日本岛津公司,型号:LC-20A);电子天平(梅特勒-托利多集团,型号:XS105DU);电热干燥箱(德国宾德集团,型号:ED-53)。
1.2 试药
盐酸苯海拉明对照品(中国食品药品检定研究院,批号:100066-200807,含量:99.9%);醋酸曲安奈德对照品(中国食品药品检定研究院,批号:100125-202007,含量:98.4%);水杨酸对照品(中国食品药品检定研究院,批号:100106-202106,含量:99.8%);色谱甲醇(默克股份有限公司);水(超纯水);盐酸苯海拉明水杨酸酊(惠州市皮肤病防治研究所,批号:202210201、202210211、202210251、202210271、202210281 和202211011,规格:60 mL/瓶;含醋酸曲安奈德0.000 5 g/mL、盐酸苯海拉明0.01 g/mL、水杨酸0.01 g/mL)。
2 实验方法与结果
2.1 色谱条件
色谱柱为资生堂CAPCELL PAK C18 MG Ⅱ(250 mm×4.60 mm,5 μm);以甲醇-水(每1 000 mL水中加三乙胺7 mL,磷酸调节pH 值为7.2)(70∶30)为流动相;检测波长为240 nm;流速为1.0 mL/min;柱温为35 ℃;紫外检测器;进样量为20 μL。
2.2 对照品溶液的制备
精密称取盐酸苯海拉明对照品39.96 mg,置10 mL 量瓶中,加水振摇使溶解并稀释至刻度,摇匀,作为对照品贮备液①。精密称取醋酸曲安奈德对照品10.47 mg,置50 mL 量瓶中,加甲醇振摇使溶解并稀释至刻度,摇匀,作为对照品贮备液②。精密称取水杨酸对照品40.56 mg,置10 mL 量瓶中,加甲醇振摇使溶解并稀释至刻度,摇匀,作为对照品贮备液③。精密吸取上述三种对照品贮备液各5 mL置同一200 mL 量瓶中,加甲醇-水(70∶30)稀释至刻度,摇匀,即得对照品溶液。
2.3 供试品溶液的制备
精密吸取供试品1 mL,置100 mL 量瓶中,加甲醇-水(70∶30)稀释至刻度,摇匀,即得供试品溶液。
2.4 阴性对照溶液的制备
按制剂处方工艺制备不含醋酸曲安奈德、盐酸苯海拉明和水杨酸的空白制剂。按供试品溶液制备方法稀释,即得阴性对照溶液。
2.5 系统适用性试验
取对照品溶液、供试品溶液和阴性对照溶液按“2.1”项下色谱条件分别进行测定,在相同保留时间位置上,阴性对照溶液未检测出水杨酸、盐酸苯海拉明和醋酸曲安奈德峰。各色谱峰分离度均符合规定,结果表明,辅料对样品含量测定无干扰,专属性良好。结果见图1。
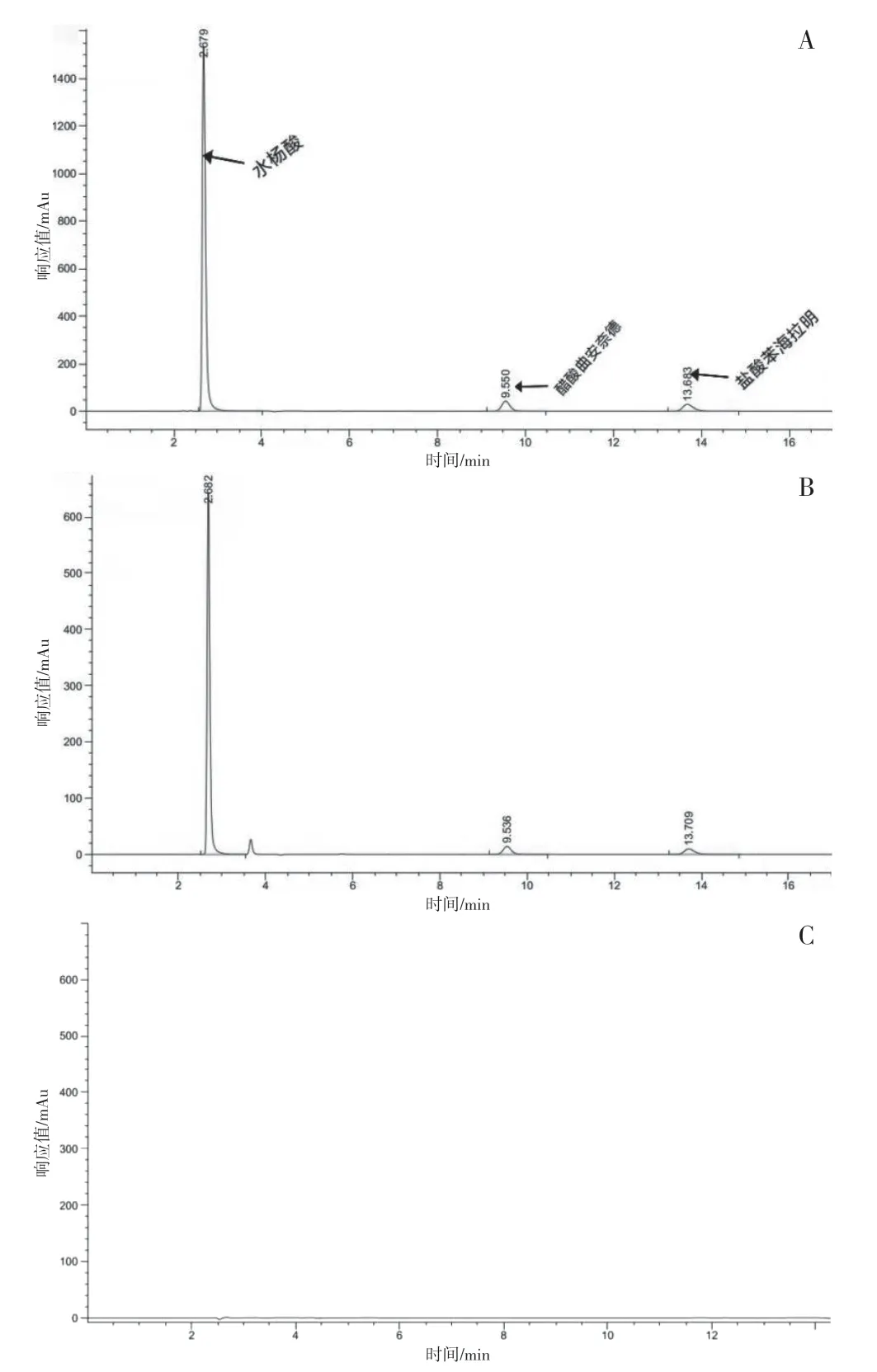
图1 HPLC色谱图:A.混合对照品溶液;B.供试品溶液;C.阴性对照溶液
2.6 线性关系考察
取“2.2”项下的对照品溶液,分别进样5 μL、10 μL、20 μL、40 μL 和60 μL,记录色谱图,以进样量(μg)为横坐标,以峰面积为纵坐标绘制标准曲线,醋酸曲安奈德回归方程为:y=1 930.770 3x+1.705 6(r=1.000 0);盐酸苯海拉明回归方程为:y=82.867 3x+2.423 6(r=0.999 9);水杨酸回归方程为:y=131 0.109 6x+227.513 8(r=0.996 4)。结果表明,醋酸曲安奈德在0.026~0.309 μg、盐酸苯海拉明在0.499~5.988 μg、水杨酸在0.506~6.072 μg 范围均呈现良好的线性关系。
2.7 重复性试验
取样品6 份(批号为202210211),按“2.3”项下的方法制备供试品溶液,并按“2.1”项下的色谱条件进样,记录色谱图。醋酸曲安奈德含量为99.92%,RSD 为0.55%;盐酸苯海拉明含量为100.50%,RSD 为0.53%;水杨酸含量为100.70%,RSD 为0.38%。结果表明本方法重复性良好。
2.8 稳定性试验
取同一份供试品溶液,分别在0、2、4、6、8、10、12、24、48 h 测定峰面积。醋酸曲安奈德、水杨酸、盐酸苯海拉明峰面积的RSD 分别为0.66%、0.55%、0.73%。结果表明三种组分在48 h 内稳定性良好。
2.9 耐用性试验
按“2.3”项下的方法制备供试品溶液,分别用不同厂家的色谱柱(厂家:资生堂,填料:CAPCELL PAK C18 MG II,规格:250 mm×4.6 mm,5 μm,柱号:A4AD 09543;厂家:安捷伦,填料:ZORBAX Eclipse XDB-C18,规 格:250 mm×4.6 mm,5 μm,柱 号:USNH023988,厂家:月旭,填料:Xtimate C18,规格:250 mm×4.6 mm,5 μm,柱号:411502491)和不同的液相色谱仪进行测定,记录色谱图,三种组分的含量均在90.0%~110.0% 范围,醋酸曲安奈德、盐酸苯海拉明、水杨酸RSD 分别为0.31%,0.24%,0.32%。结果表明,此方法耐用性良好。
2.10 回收率试验
取样品9 份(批号为202210211),每份精密吸取供试品0.5 mL,分别按标示含量的80%、100%、120%加入混合对照品溶液,每个浓度平行制备3 份,按“2.3”项下的方法制备回收率供试品溶液,并按“2.1”项下的色谱条件进行测定,计算回收率,结果如表1 所示。
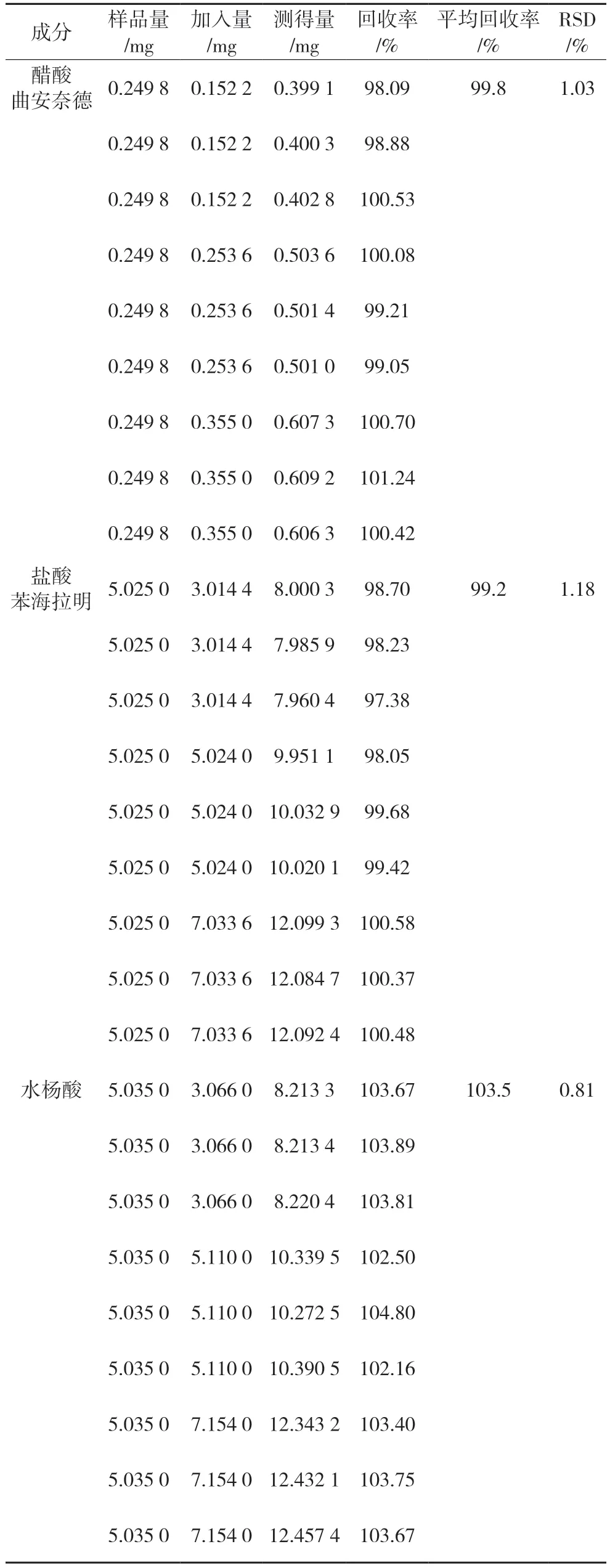
表1 回收率试验测定结果(n=9)
结果,醋酸曲安奈德平均回收率为99.8%,RSD 为1.03%;盐酸苯海拉明平均回收率为99.2%,RSD 为1.18%;水杨酸平均回收率为103.5%,RSD为0.81%。
2.11 含量测定
取6 批样品,按“2.3”项下的方法制备供试品溶液,按“2.1”项下的色谱条件进样,记录色谱图,结果如表2 所示。
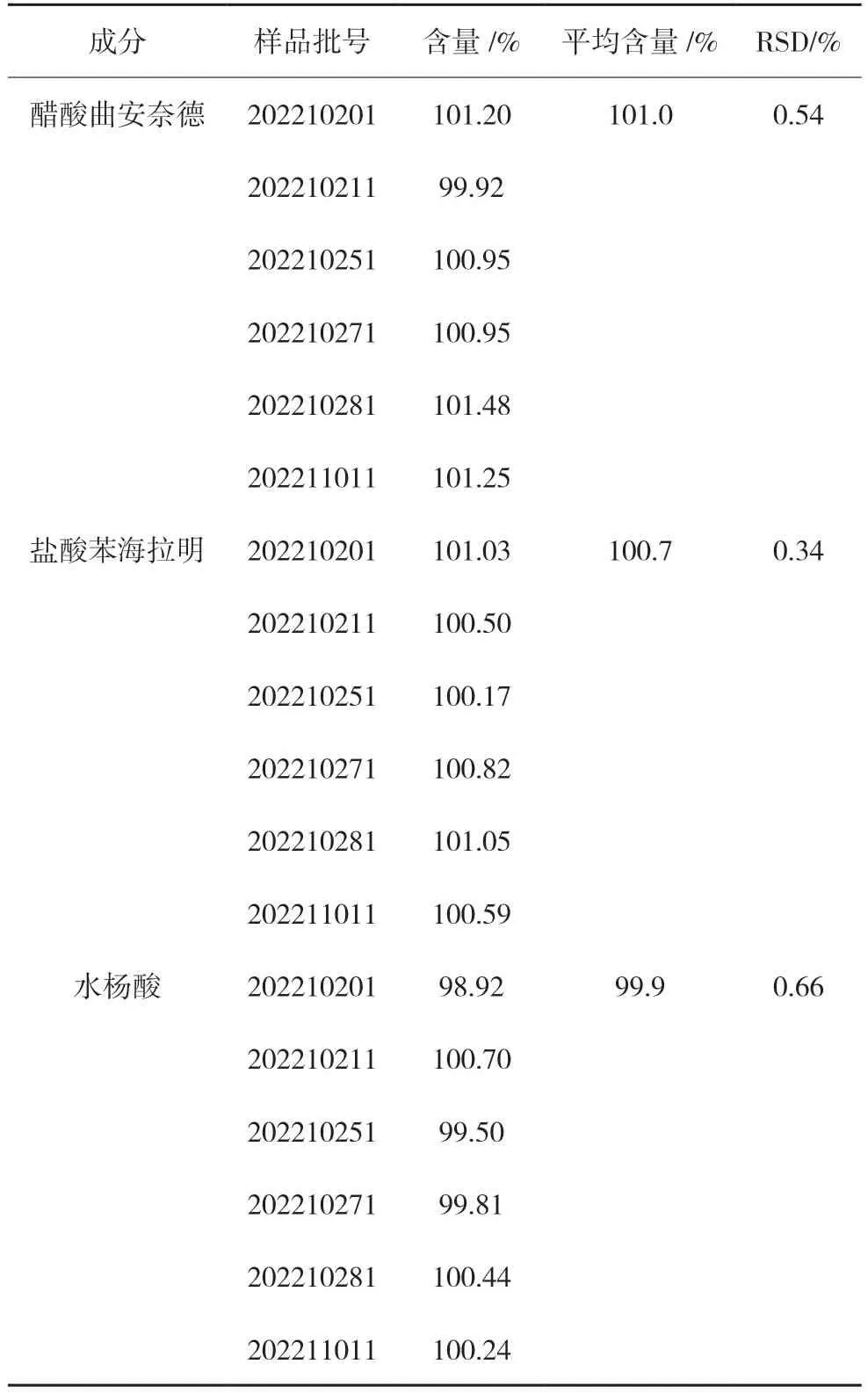
表2 含量测定结果
3 讨论
曲安奈德苯海拉明水杨酸酊的医疗机构制剂标准为采用滴定法分别测定其中水杨酸和盐酸苯海拉明的含量,方法较为烦琐。本研究参考相关文献,采用HPLC 的方法同时测定醋酸曲安奈德、盐酸苯海拉明和水杨酸的含量,该方法快捷、灵敏,专属性好,方法准确度高,可为药品质量的全面评价提供试验依据。
本实验过程中比较了不同品牌的色谱柱,还比较了不同的液相色谱仪,同时参考《中国药典》2020 年版二部盐酸苯海拉明原料含量测定的色谱条件,确定了盐酸苯海拉明和水杨酸均可采用240 nm 的吸收波长进行测定。原标准中醋酸曲安奈德的稀释溶剂采用的是流动相,实验过程中发现运用流动相稀释样品容易降解,后来考察了用甲醇-水(70∶30)作为稀释剂,发现样品稳定性良好。
本实验共测定6 个不同批号的曲安奈德苯海拉明水杨酸酊的含量,结果均在标准规定的限度范围内。说明应用HPLC 法测定曲安奈德苯海拉明水杨酸酊的含量是适用可行的,其分析准确,高效,专属性强,耐用性好,操作简便快速,灵敏度高,可有效地控制该产品的质量。

