核仁素对伯基特淋巴瘤细胞长春新碱敏感性的影响及其机制
徐伟格,郝秀君,李英新,贾鑫新,杨艳敏,原现华
邢台市第一医院血液科,河北邢台054001
伯基特淋巴瘤是一种高侵袭性B细胞非霍奇金淋巴瘤,在临床上分为非洲地区性、散发性和免疫缺陷相关性三种流行病学亚型[1]。目前,化疗仍然是伯基特淋巴瘤最主要的治疗手段,而化疗耐药是导致治疗失败和预后较差的主要原因[2]。核仁素是一种多功能蛋白,广泛分布于真核细胞的核仁、核质、细胞质和细胞膜等部位,能够参与多种生物学过程。有研究报道,核仁素在多种肿瘤细胞中表达上调,并能调控凋亡过程中各种蛋白质分子的稳定性,从而促进肿瘤的发生、发展[3]。另外,与亲本CA46细胞相比,核仁素在阿霉素耐药的CA46细胞中表达显著升高[4]。核仁素在肿瘤细胞中高表达,尤其是耐药肿瘤细胞,据此推测核仁素可能与肿瘤耐药性密切相关[5]。但核仁素参与肿瘤耐药的机制尚不清楚。Bcl-2基因是一种抑制细胞凋亡的癌基因,其编码蛋白属于细胞凋亡蛋白家族。研究表明,Bcl-2蛋白过表达能够抑制细胞凋亡,并导致血液肿瘤化疗耐药[6-7]。肿瘤细胞中核仁素和Bcl-2高表达均能参与细胞凋亡过程,它们与肿瘤细胞耐药可能具有一定关系。2021年6月—2022年10月,本研究探讨了核仁素对伯基特淋巴瘤细胞长春新碱敏感性的影响及其机制。现报告如下。
1.料与方法
1.1.料 伯基特淋巴瘤CA46细胞,购自上海博尔森生物科技有限公司。长春新碱,购自上海源叶生物科技有限公司。对照质粒(5'-CGAACGTCTACTGTCAC-3')、核仁素shRNA质粒(5'-AGTCGTAGCTGTGAGCTG-3')、核仁素mRNA质粒(5'-TGCACTAATGCTAGCTGTGAC-3'),由上海美迪西生物医药股份有限公司构建。Lipofectamine®2000转染试剂,购自赛默飞世尔科技(中国)有限公司;RIPA裂解液,购自美国MCE公司。TaKaRa实时荧光定量PCR试剂盒,购自翌圣生物科技(上海)股份有限公司;凋亡检测试剂盒,购自江苏碧云天生物技术有限公司。Bcl-2、β-actin单克隆抗体及相应的二抗,购自美国CST公司。
1.2.胞培养 将CA46细胞接种于含10% FBS的RPMI 1640培养基,置于37 ℃、5% CO2、饱和湿度的细胞培养箱中孵育。每2~3天换液一次。待细胞生长至85%左右融合时,0.25%胰蛋白酶消化、计数,按1∶3传代。取传3代、对数生长期、生长状态良好的CA46细胞进行后续实验。
1.3.粒转染 取传3代、对数生长期、生长状态良好的CA46细胞,以2 × 105/孔接种于6孔板,随机分为Control组、核仁素-NC组、核仁素-KD组和核仁素-OE组,每组设5个复孔。将6孔板置于37 ℃、5% CO2、饱和湿度的细胞培养箱中孵育24 h,按Lipofectamine®2000转染试剂说明,将对照质粒、核仁素shRNA质粒、核仁素mRNA质粒分别转染至核仁素-NC组、核仁素-KD组和核仁素-OE组CA46细胞中,Control组不予转染。转染6 h,更换新鲜的培养基继续培养24 h,收集细胞。
1.4.仁素、Bcl-2 mRNA表达检测 收集上述各组CA46细胞,按总RNA提取试剂盒说明提取细胞总RNA。经紫外可见分光光度计鉴定,提取的总RNA浓度和纯度合格。然后将提取的总RNA逆转录为cDNA。以cDNA为模板,按TaKaRa实时荧光定量PCR试剂盒说明进行PCR扩增。引物序列:核仁素上游引物5'-GAGGATCCCCGGGTACCGGTCGC-3'、下游引物5'-TACCTTCAAACTTCGTCTTCTTTCC-3';Bcl-2上游引物5'-CGACGACTTCTCCCGCCCGCTACCG-3'、下游引物5'-CCGCATGCTGGGGGCCGTACAGT-3';GAPDH上游引物5'-CCTCAAGATCAGCAAT-3'、下游引物5'-GATGTTCTGGAGAGCCCCCG-3'。反应条件:95 ℃ 5 min,95 ℃ 30 s、60 ℃ 30 s、72 ℃ 30 s共40个循环。采用2-ΔΔCT法计算核仁素、Bcl-2 mRNA相对表达量。实验重复3次,取平均值。
1.5.胞存活率检测及长春新碱的半数抑制浓度(IC50)计算 收集上述各组CA46细胞,以5 × 103/孔接种于96孔板,置于37 ℃、5% CO2、饱和湿度的细胞培养箱中孵育24 h。然后分别加入0、25、50、100、200、400 μg/L长春新碱,继续孵育48 h。每孔加入5 mg/L MTT溶液20 μL,继续孵育2 h。每孔加入DMSO溶液200 μL,轻轻振荡,使结晶物充分溶解。酶标仪于450 nm波长处检测各孔的光密度(OD)值,按公式计算细胞存活率。细胞存活率=1-[(观察组OD450值-空白对照组OD450值)/(对照组OD450值-空白对照组OD450值)]×100%。利用SPSS21.0统计软件计算各组CA46细胞长春新碱的IC50。
1.6.胞凋亡率检测 收集上述各组CA46细胞,以3 × 106/孔接种于6孔板,每孔加入100 μg/L长春新碱,置于37 ℃、5% CO2、饱和湿度的细胞培养箱中孵育48 h,0.25%胰蛋白酶消化,4 ℃下300 × g离心5 min,收集细胞。预冷的PBS洗涤2次,1 × Binding Buffer 100 μL重悬,然后分别加入Annexin V-FITC 5 μL、PI 10 μL,轻轻混匀,室温避光孵育15 min。最后加入1 × Binding Buffer 400 μL,混匀后置于冰盒中,1 h内上流式细胞仪检测细胞凋亡率。
1.7.cl-2蛋白表达检测 取上述各组CA46细胞,加入适量细胞裂解液,提取细胞总蛋白。经BCA法蛋白定量合格,加入蛋白上样缓冲液混匀,100 ℃水浴充分变性。取部分变性蛋白,SDS-PAGE分离,电泳结束后转印至PVDF膜上。5%脱脂奶粉室温封闭1 h,TBST洗膜。然后分别加入Bcl-2、β-actin单克隆抗体,4 ℃孵育过夜。次日,TBST洗膜后,加入IgG二抗,室温孵育1 h。ECL发光,暗室内曝光、显影。采用Image J软件分析各蛋白电泳条带灰度值。以目的蛋白电泳条带灰度值与内参蛋白电泳条带灰度值的比值作为目的蛋白相对表达量。
1.8.仁素蛋白与Bcl-2相互作用观察 CA46细胞经RIPA裂解液充分裂解,与抗核仁素抗体和蛋白A/G磁珠交联,以小鼠IgG作为对照抗体。将抗核仁素抗体与蛋白A/G磁珠交联产物置于RNA免疫沉淀缓冲液,4 ℃孵育过夜。用蛋白酶K缓冲液消化磁珠中的蛋白,用苯酚、氯仿、异戊醇混合物提取和纯化RNA,并将其逆转录为cDNA,然后进行PCR扩增。反应条件:95 ℃ 10 min,95 ℃ 15 s、60 ℃ 60 s共40个循环。PCR产物经1.5%琼脂糖凝胶分离,GoldView染色,观察核仁素免疫沉淀复合物中Bcl-2 mRNA条带强度。
1.9.计学方法 采用SPSS22.0统计软件。符合正态分布的计量资料以±s表示,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2.果
2.1.组CA46细胞核仁素mRNA表达比较 Control组、核仁素-NC组、核仁素-KD组、核仁素-OE组CA46细胞核仁素mRNA相对表达量分别为1.00 ±0.08、0.90 ± 0.05、0.30 ± 0.06、1.86 ± 0.09。Control组与核仁素-NC组CA46细胞核仁素mRNA相对表达量比较差异无统计学意义(P>0.05),核仁素-KD组CA46细胞核仁素mRNA相对表达量低于核仁素-NC组和Control组(P均<0.05),核仁素-OE组CA46细胞核仁素mRNA相对表达量高于核仁素-NC组和Control组(P均<0.05)。
2.2.组CA46细胞长春新碱的IC50比较 不同浓度长春新碱干预下各组CA46细胞存活率变化见图1。Control组、核仁素-NC组、核仁素-KD组、核仁素-OE组CA46细胞对长春新碱的IC50分别为(143.2 ± 5.8)、(148.0 ± 4.2)、(68.3 ± 4.0)、(304.2 ± 15.7)μg/L。Control组与核仁素-NC组CA46细胞对长春新碱的IC50比较差异无统计学意义(P>0.05),核仁素-KD组CA46细胞对长春新碱的IC50低于Control组和核仁素-NC组(P均<0.05),核仁素-OE组CA46细胞对长春新碱的IC50高于Control组和核仁素-NC组(P均<0.05)。
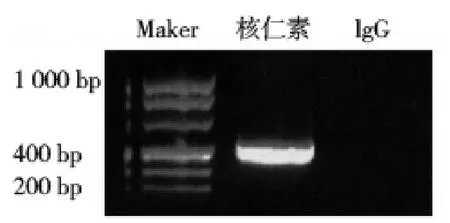
图1.仁素蛋白与Bcl-2 mRNA的免疫共沉淀结果观察
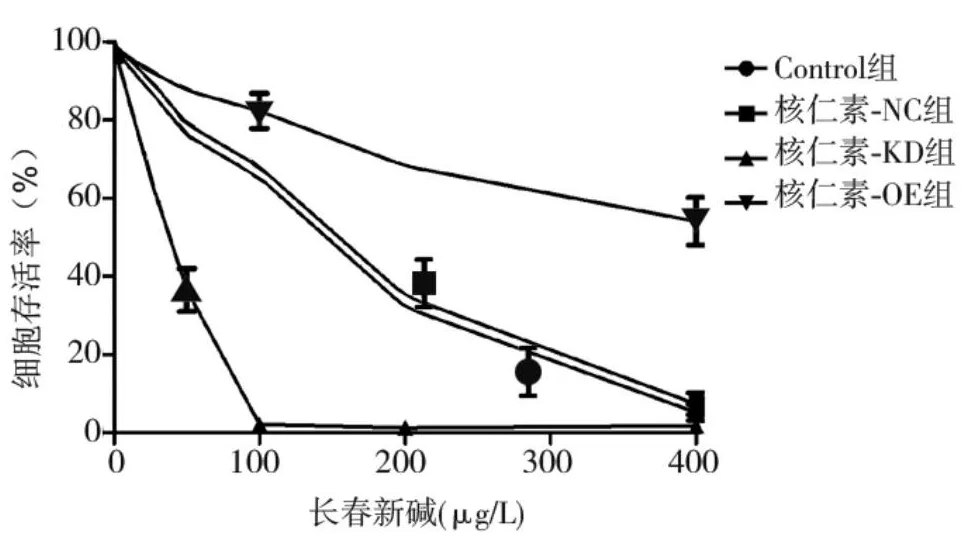
图1.同浓度长春新碱干预下各组CA46细胞存活率变化
2.3.组CA46细胞长春新碱诱导后凋亡率比较Control组、核仁素-NC组、核仁素-KD组、核仁素-OE组CA46细胞长春新碱诱导后凋亡率分别为(26.3 ±2.1)%、(28.4 ± 2.6)%、(20.5 ± 3.7)%、(75.3 ±6.8)%。Control组与核仁素-NC组CA46细胞长春新碱诱导后凋亡率比较差异无统计学意义(P>0.05),核仁素-KD组CA46细胞长春新碱诱导后凋亡率均低于Control组和核仁素-NC组(P均<0.05),而核仁素-OE组CA46细胞长春新碱诱导后凋亡率均高于Control组和核仁素-NC组(P均<0.05)。
2.4.组CA46细胞Bcl-2 mRNA和蛋白表达比较 见表1。
表1.组CA46细胞Bcl-2 mRNA和蛋白相对表达量比较(±s)

表1.组CA46细胞Bcl-2 mRNA和蛋白相对表达量比较(±s)
注:与Control组比较,*P<0.05;与核仁素-NC组比较,#P<0.05。
组别Control组核仁素-NC组核仁素-KD组核仁素-OE组Bcl-2 mRNA 1.00 ± 0.05 0.98 ± 0.02 0.41 ± 0.03*#1.59 ± 0.05*#蛋白0.78 ± 0.06 1.05 ± 0.07 0.31 ± 0.03*#1.24 ± 0.10*#
2.5.仁素蛋白与Bcl-2 mRNA的免疫共沉淀观察 与抗IgG相比,核仁素免疫沉淀复合物中Bcl-2 mRNA显著富集,见图1。
3.论
伯基特淋巴瘤是一种来源于滤泡生发中心细胞的高度侵袭性B细胞非霍奇金淋巴瘤。目前,化疗仍然是伯基特淋巴瘤最主要的治疗手段,而化疗耐药是导致治疗失败和预后较差的主要原因[2]。因此,改善伯基特淋巴瘤细胞对化疗药物的耐药性并提高其敏感性是临床亟需解决的问题。普遍认为,伯基特淋巴瘤细胞化疗耐药与基因突变、细胞凋亡异常、骨髓微环境改变等因素有关。
核仁素是一种多功能蛋白,广泛分布于真核细胞的核仁、核质、细胞质和细胞膜等部位,能够参与多种生物学过程。研究表明,核仁素在多种肿瘤细胞中表达上调,并且其表达与肿瘤细胞的增殖和存活密切相关[8]。临床研究发现,核仁素在复发或难治性急性白血病预后较差患者中过表达[9]。另有研究报道,核仁素在急性白血病细胞中具有促进增殖和耐药性进化的作用[10]。此外,有学者认为下调核仁素表达有望成为肿瘤化疗增敏的有效措施之一[11-12]。有研究报道,化疗药物诱导的髓细胞白血病细胞凋亡发生之前,Bcl-2 mRNA表达下调且不稳定[13]。核仁素是否通过上调Bcl-2表达进而降低CA46细胞对长春新碱的敏感性,目前尚不明确。
本研究通过瞬时转染技术构建了CA46细胞核仁素低表达和过表达细胞株,进一步观察了核仁素对CA46细胞增殖、凋亡以及Bcl-2表达的影响。结果发现,长春新碱作用于核仁素过表达CA46细胞株的IC50显著增加,说明核仁素过表达可降低CA46细胞对长春新碱的敏感性。有研究认为,核仁素表达下调可能通过降低Bcl-2表达而增强人脐静脉内皮细胞顺铂耐药株对顺铂的敏感性[14]。此外,核仁素抑制剂AS1411通过破坏Bcl-2 mRNA稳定性而抑制人胶质瘤和乳腺癌细胞增殖[15-16]。本研究还发现,核仁素低表达CA46细胞株Bcl-2 mRNA和蛋白表达显著降低,核仁素过表达CA46细胞株Bcl-2 mRNA和蛋白表达显著升高。Bcl-2基因是一种抑制细胞凋亡的癌基因,其编码蛋白属于细胞凋亡蛋白家族。核仁素过表达CA46细胞株对长春新碱的敏感性降低,可能与上调Bcl-2 mRNA和蛋白表达有关。本研究采用免疫共沉淀技术进一步验证核仁素与Bcl-2在体内的相互作用,结果发现免疫沉淀复合物中Bcl-2 mRNA显著富集,证实核仁素可与Bcl-2直接结合。
综上所述,核仁素可能通过上调Bcl-2表达,并直接与Bcl-2 mRNA结合而促进其稳定性,从而降低伯基特淋巴瘤细胞对长春新碱的敏感性。

