超高效液相色谱质谱联用技术测定动物源食品中的11种磺胺类兽药残留
李雯雯 杜蒙 王晓军 孙允超

摘 要:本研究建立了基于超高效液相色谱串联质谱技术(Ultra Performance Liquid Chromatography Tandem Mass Spectrometry,UPLC-MS/MS)的磺胺类兽药残留分析方法。方法学考察表明,11种磺胺类兽药残留在10~200 μg·L-1呈现良好的线性关系;方法检出限为0.84~1.62 μg·kg-1,方法定量限为2.8~5.4 μg·kg-1;在3个浓度水平下,目标化合物的加标回收率为74.5%~109.9%,相对标准偏差为0.09%~8.12%。该方法可用于动物源食品中多种磺胺类兽药残留的定性、定量分析及筛查。
关键词:磺胺类兽药残留;液相色谱串联质谱技术;分析筛查
Abstract: In this study, a method for the analysis of sulfa veterinary drug residues based on ultra-high performance liquid chromatography tandem mass spectrometry (UPLC-MS/MS) was established. Methodological investigation showed that the residues of 11 sulfonamides showed a good linear relationship in the range of 10~200 μg·L-1. The limits of detection were 0.84~1.62 μg·kg-1, and the limits of quantification were 2.8~5.4 μg·kg-1. The recoveries were 74.5%~109.9% and the relative standard deviations were 0.09%~8.12% at the three concentration levels. The method is suitable for qualitative and quantitative analysis and screening of various sulfonamides veterinary drug residues in animal derived food.
Keywords: sulfonamides veterinary drug residues; ultra performance liquid chromatography tandem mass spectrometry; analysis and screening
磺胺類药物是一类以对氨基苯磺酰胺为基本母核结构的化学合成抗菌药物,具有广谱、高效、价低等特点,在畜禽养殖过程中,为预防和控制疾病,常被添加到饲料中使用[1]。但磺胺类药物在人体中代谢时间较长,易在人体内蓄积。随着近年来兽药的大量使用,甚至滥用和误用,出现了耐药性、药物残留过高、部分人群过敏中毒等问题。动物源食品中的磺胺类药物残留逐渐引起人们的重视,从2005年起,农业农村部对动物产品中的磺胺类药物残留进行重点管控。2022年9月,农业农村部发布了第594号公告,发布了《食品安全国家标准 食品中41种兽药最大残留限量》(GB 31650.1—2022)[2],对磺胺类药物(总量)和磺胺二甲嘧啶的最大残留量分别进行了补充。与此同时,磺胺类药物残留的检测技术逐步更新。传统的磺胺类兽药残留检测方法包括液相色谱质谱法、液相色谱法、酶联免疫分析法和荧光分析法,其中液相色谱质谱联用技术因灵敏度高、准确度好、高通量等优点,被广泛应用于动物源食品中的兽药多残留检测分析[3-4]。
本研究拟建立11种磺胺类兽药残留的液相色谱质谱检测技术,通过对质谱的检测参数进行优化和方法学评估,形成一种高效、精确的磺胺类兽药残留分析方法。
1 材料与方法
1.1 材料与试剂
磺胺类标准品:磺胺嘧啶、磺胺噻唑、磺胺甲恶唑、磺胺甲嘧啶、磺胺二甲异恶唑、磺胺甲噻二唑、磺胺二甲嘧啶、磺胺间甲氧嘧啶、磺胺甲氧哒嗪、磺胺邻二甲氧嘧啶和磺胺间二甲氧嘧啶,均购于坛墨质检科技股份有限公司;Knorth HLB固相萃取柱,北京科德诺思技术有限公司;猪肉,购自聊城华盛超市;HPLC甲醇、HPLC乙腈,美国Fisher Scientific公司;超纯水,广州屈臣氏食品饮料有限公司。
1.2 仪器与设备
Triple Quad 5500+超高效液相串联质谱,AB SCIEX公司;氮吹浓缩仪,广州得泰仪器科技有限公司;冷冻离心机,湖南平凡科技有限公司;涡旋混合器,海门市其林贝尔仪器制造有限公司。
1.3 试验方法
1.3.1 标准储备溶液和工作液
将11种兽药标准品(100 mg·L-1)分别移取100 μL于10 mL容量瓶中,用甲醇定容,得到1 mg·L-1的磺胺混合标准溶液;称取(1.00±0.02)g不含11种兽药残留的空白猪肉样品,提取和净化,得到空白基质溶液;混合标准溶液用空白基质溶液逐级稀释,分别得到10 μg·L-1、20 μg·L-1、50 μg·L-1、100 μg·L-1、150 μg·L-1和200 μg·L-1的基质混合标准工作液,用于绘制基质匹配校准曲线。
1.3.2 上机溶液制备
取猪肉样品,绞碎并均质,称取试样(1.00±0.02)g,加入Na2EDTA-Mcllvaine缓冲溶液,涡旋振荡、超声、离心,取上清液,残渣用磷酸盐缓冲液重复提取,合并两次上清液备用;采用Knorth HLB固相萃取柱对上清液进行净化和洗脱,洗脱液涡旋混匀、氮吹至干,用10%甲醇-10%乙腈水溶液(含0.1%甲酸)复溶过膜,得到待上机样品溶液。
1.3.3 仪器检测条件
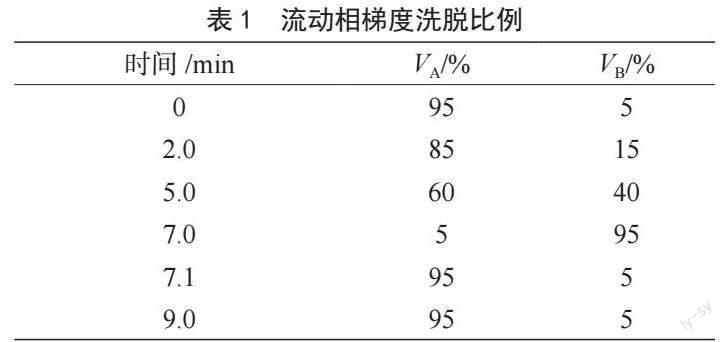
(1)色谱条件。Waters Acquity UPLC BEH C18色谱柱,柱温35 ℃,流速0.3 mL·min-1,进样量1 μL,流动相A为含0.1%甲酸的水溶液,流动相B为含0.1%甲酸的甲醇∶乙腈(2∶8,体积比)溶液,洗脱方式为梯度洗脱,见表1。
(2)质谱条件。电喷雾离子源(ESI),喷雾电压为正离子模式(ESI+)5 500 V;离子源温度350 ℃,气帘气(Curtain gas)35 psi,离子源气体1(Gas Ⅰ)和气体2(Gas Ⅱ)分别设置为50和60,检测方式MRM。
2 结果与分析
2.1 净化方法选择
动物源食品的基质比较复杂,易对液质联用的电喷雾离子化过程中形成的目标化合物分子信号造成干扰,影响检测灵敏度和准确性。有效的基质净化前处理方法能减弱和消除基质效应。其中,固相萃取技术在动物源性食品基质净化领域中应用广泛,能够快速、简便、高效地去除各类食品中的干扰基质,达到分离和富集待测组分的目的[5]。故本试验选择固相萃取柱净化样品,通过方法学评估,能满足磺胺类兽药残留的检测需求。
2.2 质谱条件优化及谱图
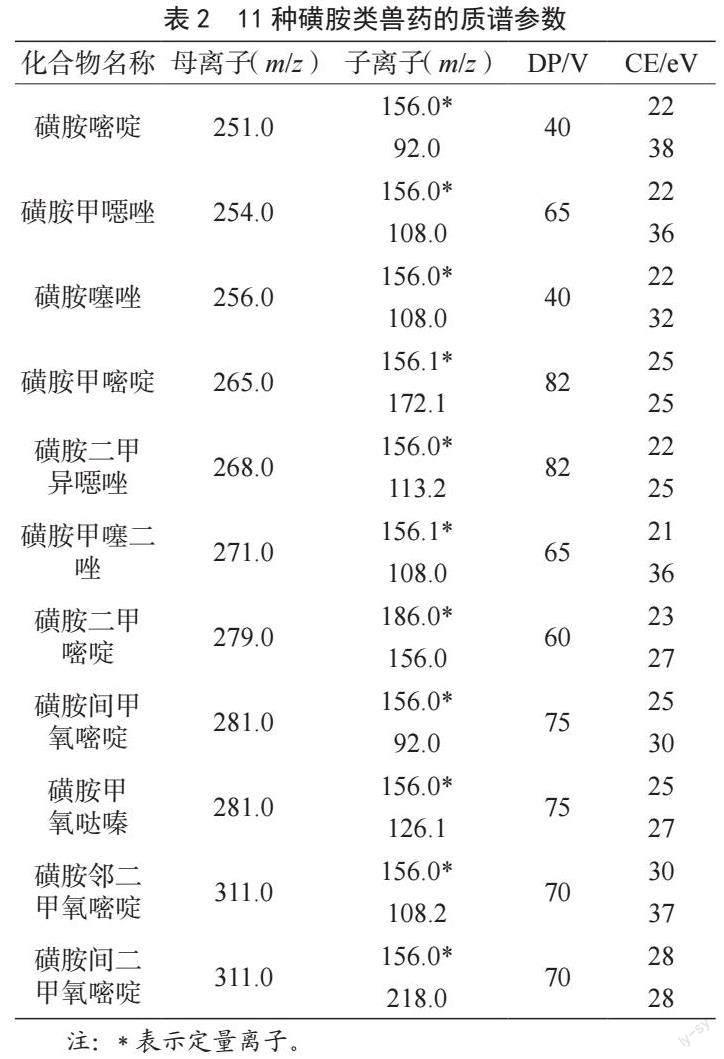
将200 μg·L-1的11种磺胺混合标准溶液以针泵的方式连续进样,在正离子模式下,采用一级质谱扫描(Q1 Scan)确定母离子质荷比;采用碎片离子扫描(Product Ion Scan)确定干扰少、信噪比高的1~2个子离子,分别作为定性离子和定量离子;采用多反应监测扫描(Multiple Reaction Monitoring,MRM)优化定性离子和定量离子的去簇电压(Declustering Potential,DP)和碰撞能量(Collision Energy,CE),最终建立质谱采集参数,结果见表2。以优化的质谱参数为方法,获得11种磺胺类化合物的总离子流图(见图1)和磺胺甲噁唑质谱图(见图2、图3)。
2.3 方法学评估
2.3.1 线性关系和检出限、定量限
使用基质空白溶液配制10~200 μg·L-1的标准工作液,以磺胺类化合物的浓度为横坐标,定量离子峰面积为纵坐标绘制标准曲线,本试验在猪肉空白基质中加入10 μg·kg-1混合标准物质,参考章萍萍等[6]的计算方法,按试验方法进行6次平行試验,计算检测结果的标准偏差(Standard Deviation,SD)、3SD(检出限)、10SD(定量限),结果见表3。11种磺胺类化合物在10~200 μg·L-1呈现良好的线性关系,相关系数大于0.994 8,检出限为0.84~1.62 μg·kg-1,定量限为2.8~5.4 μg·kg-1,均满足《食品安全国家标准 动物性食品中四环素类、磺胺类和喹诺酮类药物残留量的测定 液相色谱-串联质谱法》(GB 31658.17—2021)[7]的要求,且低于标准。
2.3.2 精密度和回收率
准确称取空白基质样品,在低、中、高3个浓度水平下,采用优化后的检测方法,进行6次平行试验,根据结果计算回收率和精密度,用于评价方法。由表4可知,3个水平下,回收率为74.5%~109.9%,相对标准偏差(Relative Standard Deviation,RSD)为0.09%~8.12%,本方法的回收率和精密度均符合兽药多残留分析要求。
3 结论
本研究建立了一种同时测定11种磺胺类化合物的UPLC-MS/MS兽药多残留分析方法,采用固相萃取法净化,通过优化质谱参数,用电喷雾正离子(ESI+)多反应监测模式对目标化合物进行定性定量分析。通过方法学考察评估,证明该方法灵敏、快速、高效,可以满足实际工作需要。
参考文献
[1]王晓茵,宋翠平,孙晓亮,等.改良柱前荧光胺衍生化-高效液相色谱法测定猪肉中11种磺胺类药物残留[J].肉类研究,2022,36(2):33-38.
[2]中华人民共和国农业农村部,国家卫生健康委员会,国家市场监督管理总局.食品安全国家标准 食品中41种兽药最大残留限量:GB 31650.1—2022[S].北京:中国标准出版社,2022.
[3]KANDA M,NAKAJIMAT,HAYASHIH,et al.Multi-residue determination of polar veterinary drugs in livestock and fishery products by liquid chromatography/tandem mass spectrometry[J].Journal of AOAC International,2015,98(1):230-247.
[4]DESMARCHELIER A,FAN K,MINH TIEN M,et al.Determination of 105 antibiotic, anti-inflammatory, antiparasitic agents and tranquilizers by LC-MS/MS based on an acidic QuEChERS-like extraction[J].Food Additives & Contaminants: Part A,2018,35(4):647-661.
[5]季宝成,杨澜瑞,韩雨,等.动物源性食品兽药多残留检测中基质净化与液相色谱-质谱联用技术研究进展[J/OL].轻工学报:1-9[2023-07-20].http://kns.cnki.net/kcms/detail/41.1437.ts.20230625.0928.006.html.
[6]章萍萍,方如意,任可.动物源性食品中十三种磺胺类药物检测方法优化[J].中国食品工业,2023(5):62-66.
[7]中华人民共和国农业农村部,国家卫生健康委员会,国家市场监督管理总局.食品安全国家标准 动物性食品中四环素类、磺胺类和喹诺酮类药物残留量的测定 液相色谱-串联质谱法:GB 31658.17—2021[S].北京:中国标准出版社,2021.

