rhGH 联合亮丙瑞林对特发性中枢性性早熟女童性激素水平的影响
杨海浛
(河南省南阳市中心医院内镜诊疗部 南阳 473000)
特发性中枢性性早熟(Idiopathic Central Precocious Puberty,ICPP)是常见的儿科内分泌疾病,因下丘脑-垂体-性腺轴(HPG 轴)过早启动导致患儿体内促性腺激素和性激素水平升高而引起[1]。ICPP受遗传基因,外界环境等多种因素影响,且女孩的发病率高于男孩,可导致患儿生长潜能受损,影响心理健康[2]。ICPP 女童的临床症状主要表现为第二性征过早显现、骨骼迅速发育等,如出现阴毛、腋毛、乳房发育、体质量及身高迅速增长等现象,若未及时采取治疗措施会导致骨龄(Bone Age,BA)提前,骨骺提前闭合、生长期缩短、生长早期停止,导致成年后身材矮小[3]。 促性腺激素释放激素类似物(Gonadotropin Releasing Hormone Analogue,GnRHa)治疗ICPP 是当前主要的治疗选择,通过亮丙瑞林等药物来控制与缓解第二性征的发育速度,抑制过早或过快的性发育,但GnRHa 在治疗过程中也会抑制患儿正常生长,部分患儿生长减速明显,引起身体肥胖,且对成年身高无改善作用[4~5]。2015 年《中枢性性早熟诊断与治疗共识》[6]建议对预测成人身高严重受损者可考虑应用重组人生长激素(Recombinant Human Gowth Hormone,rhGH),以达到理想的终身高。rhGH 可以改善患儿的生长速率和成年后身高。基于此,本研究探究rhGH 联合亮丙瑞林在ICPP 女童中的应用效果。现报道如下:
1 资料与方法
1.1 一般资料 按随机数字表法将南阳市中心医院2020 年1 月至2022 年6 月收治的76 例ICPP女童分为对照组与观察组,各38 例。对照组年龄7~10 岁,平均年龄(8.39±0.52)岁;BA 8~13 岁,平均BA(10.43±0.93)岁;遗传靶身高152~170 cm,平均(160.9±2.96)cm;实际身高123~145 cm,平均身高(135.52±4.96)cm;体质量19~32 kg,平均体质量(25.46±2.31)kg;病程6~18 个月,平均病程(12.46±2.42)个月。观察组年龄6~9 岁,平均年龄(7.63±0.43)岁;BA 8~12 岁,平均BA(10.11±0.66)岁;遗传靶身高152~169 cm,平均(160.20±2.52)cm;实际身高125~145 cm,平均身高(135.78±4.52)cm;体质量18~34 kg,平均体质量(25.24±2.16)kg;病程7~20 个月,平均病程(13.56±2.52)个月。两组一般资料对比,差异无统计学意义(P>0.05)。本研究经医院医学伦理委员会批准(伦理审批号:2020KYTL-4680)。
1.2 入组标准 纳入标准:年龄6~10 岁女童;经检查确诊,符合《性早熟诊疗指南(试行)》[7]中ICPP 相关诊断标准;第二性征显现;生长激素缺失;检测出性激素水平异常;患儿及家属对本研究知情,并签署知情同意书。排除标准:合并骨发育功能障碍者;合并重要脏器异常者;合并其他内科疾病者;过敏体质者;合并免疫缺陷者。
1.3 治疗方法 两组患儿均采取适量运动、控制饮食、充足睡眠等措施干预。对照组给予注射用醋酸亮丙瑞林缓释微球(国药准字H20093809)皮下注射,首次用量为100 μg/kg,次月再次注射用量为75 μg/kg,1 次/月;观察组在此基础上给予注射用重组人生长激素(国药准字S20063085)皮下注射治疗,0.15 U/(kg·d),1 次/d,于睡前0.5 h 注射。两组均持续治疗6 个月。
1.4 观察指标 (1)临床疗效评价。患儿第二性征发育未继续且有逆向改变的情况为治愈;第二性征发育情况停止为显效;第二性征发育减缓为有效;第二性征发育情况无明显变化为无效。治疗总有效率=治愈率+显效率+有效率。(2)性激素水平。取患儿清晨空腹静脉血3 ml,采用化学发光免疫分析法检测两组患儿治疗前后性激素水平,包括促黄体生成激素(LH)、促卵泡生成激素(FSH)、雌二醇(E2)。(3)生长发育指标。比较两组患儿治疗前后的身高(Ht)、体质量指数(BMI)、BA、预测成年身高(PAH)。 采 用 Greulich-Pyle 法 测 定 BA,Bayley-Pinneau 法PAH。(4)骨代谢指标。取患儿清晨空腹静脉血3 ml,离心取上清液采用酶联免疫法检测骨代谢指标,包括Ⅰ型胶原羧基端肽β 特殊序列(β-CTx)、Ⅰ型原胶原氨基端肽(PⅠNP)、N 端骨钙素(N-MID)。(5)不良反应。包括肥胖、局部疼痛、内分泌紊乱等。
1.5 统计学方法 采用SPSS22.0 软件处理数据。计量资料以()表示,采用t检验;计数资料用%表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组性激素水平比较 治疗前,两组性激素水平比较,差异无统计学意义(P>0.05);治疗后,两组LH、FSH、E2水平均降低,且观察组低于对照组(P<0.05)。见表1。
表1 两组性激素水平比较()
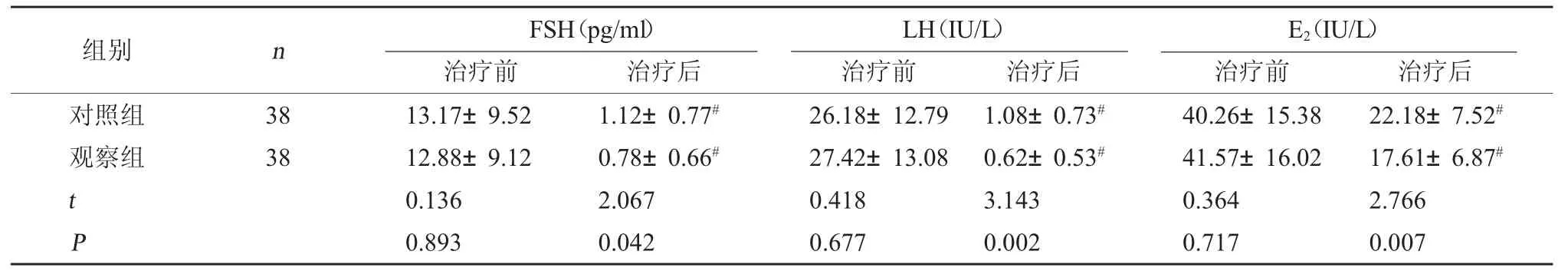
表1 两组性激素水平比较()
注:与同组治疗前比较,#P<0.05。
?
2.2 两组生长发育指标比较 治疗前,两组生长发育指标比较,差异无统计学意义(P>0.05);治疗后,两组生长发育指标均改善,且观察组优于对照组(P<0.05)。见表2。
表2 两组生长发育指标比较()
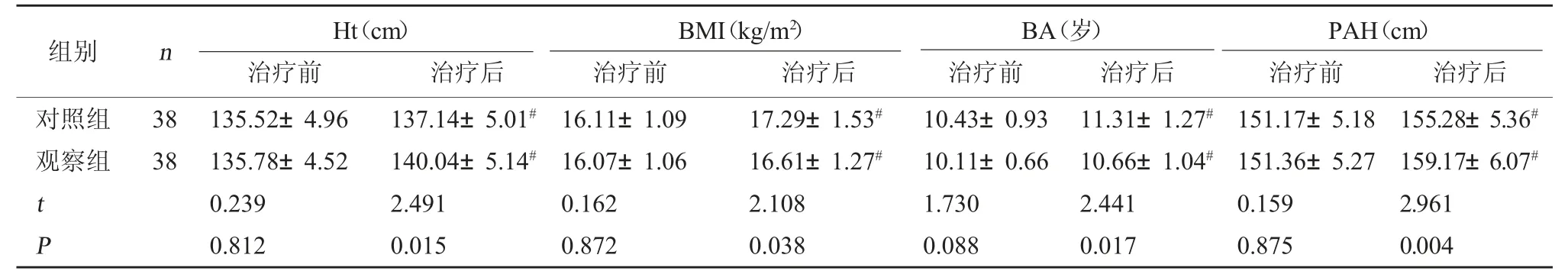
表2 两组生长发育指标比较()
注:与同组治疗前比较,#P<0.05。
?
2.3 两组骨代谢指标比较 治疗前,两组骨代谢指标比较,差异无统计学意义(P>0.05);治疗后,两组β-CTx、PⅠNP、N-MID 均改善,且观察组优于对照组(P<0.05)。见表3。
表3 两组骨代谢指标比较(μg/L,)
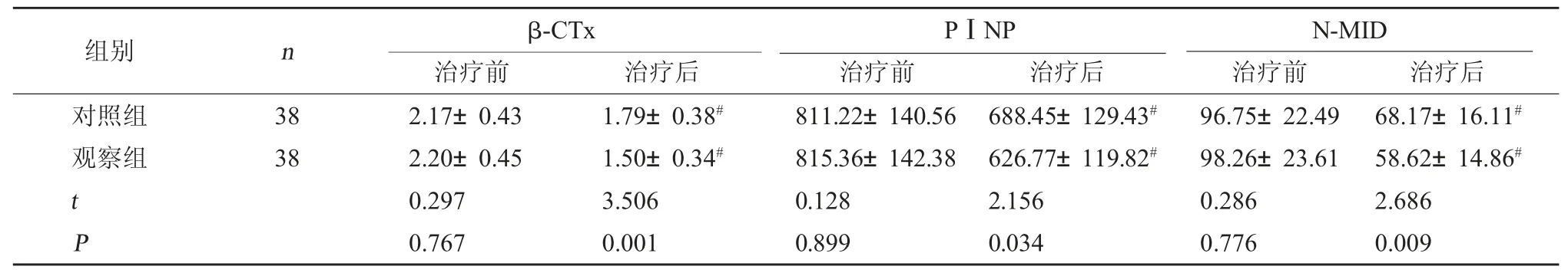
表3 两组骨代谢指标比较(μg/L,)
注:与同组治疗前比较,#P<0.05。
?
2.4 两组临床疗效比较 观察组治疗总有效率高于对照组(P<0.05)。见表4。
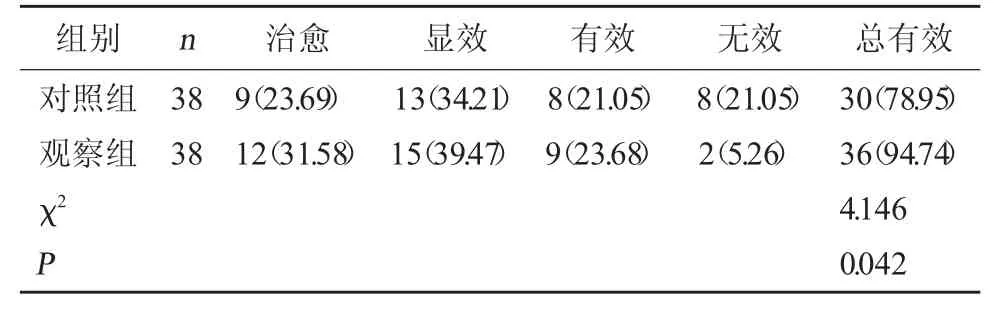
表4 两组临床疗效比较[例(%)]
2.5 两组不良反应比较 两组不良反应比较,差异无统计学意义(P>0.05)。见表5。
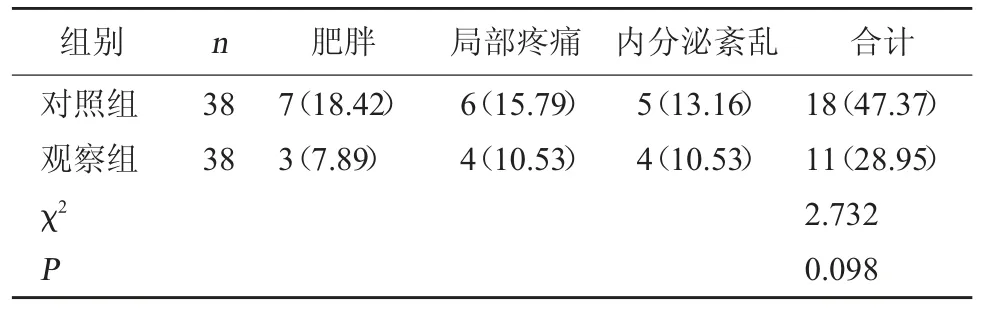
表5 两组不良反应比较[例(%)]
3 讨论
随着生活水平质量的提高,由于饮食不节制、过度服用滋补品、外界环境刺激及食品安全等问题,导致ICPP 发病率逐年升高,已成为儿童常见内分泌疾病[8]。ICPP 患儿由于性腺发育过早,导致第二性征提前显现,生长发育周期缩短,骨龄增大及骨骺提前闭合等状况,降低成年后身高,影响患儿心理健康。ICPP 发病机制复杂,中枢神经系统病变、肿瘤及肾上腺皮质增生等均会诱发该病。目前,治疗ICPP 主要目标是减缓与控制第二性征发育速度与程度,延缓骨龄生长速度,改善最终成年身高。GnRHa 皮下注射是治疗ICPP 患儿的主要方法,但GnRHa 会双向抑制,在抑制第二性征发育的同时也会抑制儿童正常生长,影响未来身高[9]。
注射用醋酸亮丙瑞林微球是治疗ICPP 患儿的常用GnRHa 药物,具有生物活性强、半衰期长、特异性高等特点,能特异性的与GnRH 受体结合,调控垂体分泌功能,抑制LH、FSH、E2等性激素分泌,阻断分泌性甾体信号通路,调节HPG 轴,改善体内性激素水平和活性,从而控制与延缓第二性征发育,降低骨骺闭合速度,促进患儿生长发育;亮丙瑞林可抑制性腺发育,延缓性发育进程,延缓BA 进展,但也会抑制骨骼生长,延缓发育速度,引起患儿肥胖,降低成年后身高;此外,亮丙瑞林药物成分复杂,长时间注射会刺激消化系统、内分泌系统、中枢神经系统等,引起恶心呕吐、皮肤瘙痒、潮热多汗、头晕头痛等多种不良反应[10~11]。本研究结果显示,观察组治疗总有效率高于对照组,观察组治疗后性激素水平、生长发育指标和骨代谢指标均优于对照组(P<0.05),两组不良反应比较无显著差异(P>0.05)。提示rhGH联合亮丙瑞林治疗效果显著,能有效改善患儿性激素水平,抑制性腺发育,有效控制与延缓第二性征发育,延缓BA,降低骨骺闭合速度,改善成年后身高,使生长与成熟平衡发展,且具有较高的安全性。王喜平等[12]研究表明,rhGH 联合亮丙瑞林能明显改善ICPP 患儿性激素水平,改善成年身高及生长速度,与本研究结果基本一致。rhGH 是由重组DNA 技术生产得到,其氨基酸含量、序列和蛋白质结构上与人垂体生长激素完全相同,能刺激骨骺端软骨细胞增殖分化、软骨基质细胞增长、成骨细胞增殖分化,引起线性生长速度及骨骼变宽,促进纤维细胞与心肌蛋白合成,调节脂肪代谢,补充身体生长激素不足或缺乏,调节骨代谢功能[13~14]。在儿科领域,采用rhGH进行替代治疗,可明显促进儿童的身高增长,并改善其全身各器官组织的生长发育[15]。rhGH 能促进骨骼增长,提高增长速度,缓解GnRHa 治疗产生的肥胖,增强GnRHa 的治疗效果,两者联合既能弥补GnRHa对骨生长限制的不足,缓解其对生长激素的抑制分泌,又可推迟骨骺闭合,延长生长发育周期,保障患儿健康成长[16]。
综上所述,rhGH 联合亮丙瑞林治疗ICPP 患儿效果显著,可调节体内性激素水平,控制或缓解第二性征发育,延缓骨龄,降低骨骺闭合速度,利于促进骨骼线性增长,改善成年后身高,且无明显不良反应,临床应用安全性较高,值得推广应用。

