石墨烯季铵基水凝胶对阴离子染料的高效吸附机理研究*
刘士清 王志刚 邱军科 尹梦楠# 石 林 安 珂 张 迪,
(1.山东省滨州市生态环境服务中心,山东 滨州 256600;2.云南省土壤固碳与污染控制重点实验室,昆明理工大学环境科学与工程学院,云南 昆明 650500;3.山东省水土保持与环境保育重点实验室,临沂大学资源环境学院,山东 临沂 276005)
阴离子染料广泛应用于纺织、造纸、皮革、制药和食品等行业[1],印染废水不仅降低水环境中的光合作用,还会造成水毒性[2]。因此,从废水中去除阴离子染料至关重要。吸附法由于简单、高效和成本低廉等优点已被广泛应用于染料废水处理[3]。目前,三维石墨烯基纳米材料已作为高效吸附剂用于去除废水中的染料。有研究者制备的氧化石墨烯(GO)/魔芋葡甘聚糖水凝胶对甲基橙(MO)及亚甲基蓝的最大吸附量分别为93.5、133.67 mg/g[4]。
然而,石墨烯基水凝胶(GH)材料在环境pH下对阴离子染料吸附能力较低。研究发现,石墨烯基三维材料对阴离子染料MO和苋菜红的吸附性能随pH增加逐渐降低,当pH为11时出现零吸附[5]8。类似现象在其他研究中也多有报道[6]。因此,改善静电作用环境,提高高pH条件下阴离子染料与GH间相互作用至关重要。已有研究表明,季铵基对环境pH变化不敏感,可借助静电吸引作用,在高pH条件下仍实现阴离子染料的较高吸附。AN等[7]将季铵基嫁接于中空玻璃微球上,使其在pH为2~10均保持对阴离子染料较高的吸附率。KANG等[8]将季铵盐嫁接于硅胶表面,在pH为4~10时该硅胶均可保持对硝酸盐的有效去除。
尽管利用季铵基改性GO的吸附研究已取得一些进展,但关于GH的季铵化改性研究仍较少,且对于改性后GH对阴离子染料吸附机理研究仍缺失。本研究利用季铵基对GH进行改性,系统研究了不同pH下GH对MO吸附效果的影响,进一步讨论了MO在GH上的吸附机理。
1 实验部分
1.1 实验材料
MO、GO粉末和聚二甲基二烯丙基氯化铵(PDADMAC)均外购。MO分子量为327.33,密度为0.987 g/cm3,辛醇-水分配系数为4.15。
1.2 实验方法
1.2.1 材料的制备及改性
采用水热合成法制备GH。将GO悬浮液(2 mg/mL)置于高压反应釜中,180 ℃下反应12 h。反应结束取出材料,并用去离子水冲洗以去除未反应物质,得到GH。
控制PDADMAC加入量(质量分数)分别为2%、3%,将GO悬浮液与PDADMAC溶液混合后也按上述操作水热合成,将得到的石墨烯季铵基水凝胶(GHP)分别命名为GHP-2%和GHP-3%。
1.2.2 材料的表征
利用扫描电子显微镜(SEM,Fei quanta-450,美国)观察材料形貌;元素分析仪(vario Microcube,德国)分析材料元素组成;傅立叶红外光谱仪(Varian 640-IR,美国)表征材料表面官能团;Zeta电位测试仪(Brookhaven,美国)测试不同pH下材料的Zeta电位。
1.2.3 批量吸附实验
吸附等温线:在固液比为40 000∶7(质量比)下,将不同初始浓度MO溶液(pH为3.0、7.0)与各材料混合振荡3 d。待吸附平衡后,用紫外分光光度计(Shimadzu UV-2600,日本)定量上清液中剩余MO浓度。
吸附动力学:在固液比为40 000∶7下,将50 mg/L的MO溶液(pH为3.0、7.0)与各材料混合,按固定时间间隔取出上清液,用紫外分光光度计定量MO浓度。
1.3 数据拟合分析
利用Langmuir模型(见式(1))和Freundlich模型(见式(2))拟合各材料对MO的吸附等温线。利用拟一级动力学模型(PFM,见式(3))、拟二级动力学模型(PSM,见式(4))和颗粒内扩散模型(IDM,见式(5))拟合各材料对MO的吸附动力学。
Qe=Qm×Ce/(1/KL+Ce)
(1)
(2)
Qt=Qe×(1-e-k1t)
(3)
(4)
Qt=kp×t0.5+C
(5)
式中:Qe为平衡吸附量,mg/g;Qm为固相最大吸附量,mg/g;Ce为液相平衡质量浓度,mg/L;KL为Langmuir吸附亲和力系数,L/mg;KF为Freundlich吸附系数,mg1-n·Ln/g;n为非线性因子;Qt为t时固相吸附量,mg/g;k1为PFM的速率常数,h-1;t为时间,h;k2为PSM的速率常数,g/(mg·h);kp为IDM的速率常数,mg/(g·h0.5);C为与边界层厚度有关的常数,mg/g。
2 结果与讨论
2.1 材料的性质
材料的SEM图如图1所示。GO片层间堆积严重,有明显的褶皱,这是由于石墨烯片层间存在较强的π-π及氢键等相互作用[9],这种堆积使得GO暴露在水相中的表面积大量减少,进而造成吸附性能显著降低[10]。经水热合成法形成GH后,片层转变为相互交联,内部产生丰富的多孔结构。值得注意的是,相比于其他材料,GHP-2%表现出最丰富的多孔结构,这归因于PDADMAC有利于水凝胶多孔结构的产生。然而,当PDADMAC加入量增加到3%时,孔隙减少,这是由于大量的PDADMAC分子缠绕在石墨烯片层上,在π-π作用下与其他片层间发生再聚合,同时也占据石墨烯片层上的活性吸附位点。类似结果[5]3也被其他研究者观察到。

图1 材料的SEM图Fig.1 SEM images of materials
材料中元素的质量分数见表1。相比于其他材料,GO含有最高的O(52.54%),这是由于GO表面或边缘通常有丰富的含氧官能团[11]8570;GH的O明显下降,由于在水热过程中发生了还原反应,大量的含氧官能团被还原[12];GHP-2%和GHP-3%同样发生了水热还原,O分别下降为24.45%和31.04%。值得注意的是,GO本身N很低(0.02%),GH也没有明显增加(0.04%),但加入PDADMAC后,N明显增加,且随着PDADMAC加入量的增加而增加,表明季铵基的成功嫁接,且随PDADMAC增加,N含量也增多。
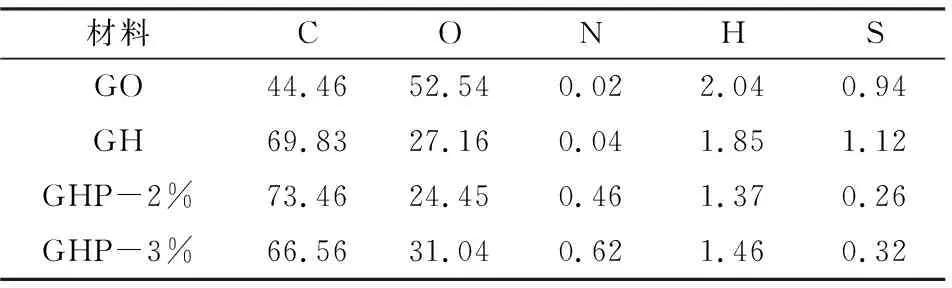
表1 材料中元素的质量分数Table 1 Mass fraction of elements in materials %
材料的红外吸收图谱见图2。与GO相比,GH中3 479 cm-1处的-OH、1 396 cm-1处的C-O-C特征峰明显减弱,1 096 cm-1处的C-O特征吸收峰振动,这是由于水热过程中GO表面的含氧官能团被还原[13]。GHP-2%和GHP-3%在1 000、1 640 cm-1处出现C-N和N-H振动峰[14],再次表明季铵基的成功嫁接。
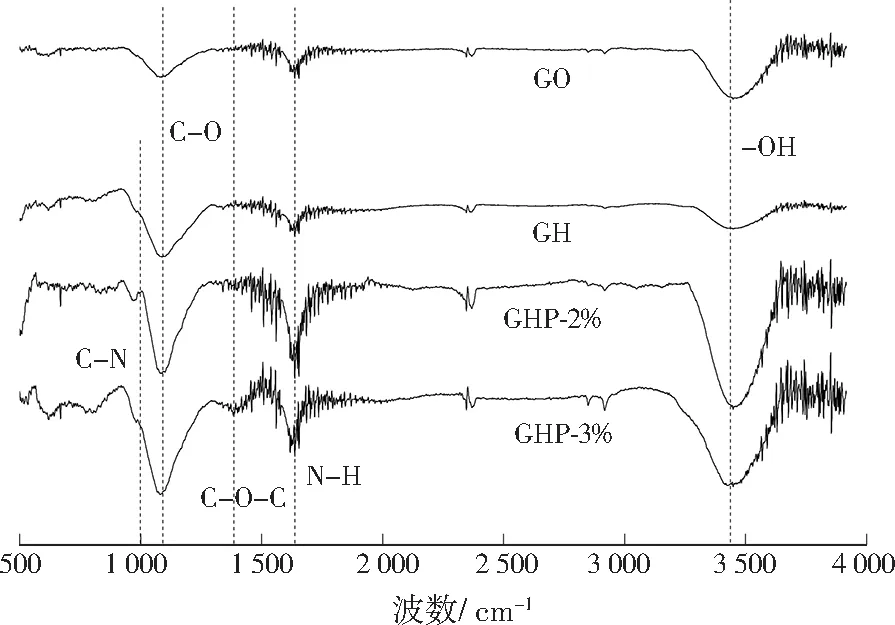
图2 材料的红外吸收图谱Fig.2 FT-IR spectrum of materials
当pH为1~7时,材料的Zeta电位如图3所示。GO的Zeta电位均小于0,这归因于GO表面丰富的羟基、羧基、环氧基等含氧官能团[11]8570。GH的Zeta电位随pH增加而降低,这是由于石墨烯基材料表面含氧官能团在低pH下会发生质子化作用,使其所带正电荷量增加,而在高pH下,含氧官能团会发生去质子化作用,从而使其所带负电荷量增加。GH的等电点约为2,GHP-2%和GHP-3%则为2.3~2.4。在嫁接PDADMAC后,GHP所带正电荷有所增加,这是由于嫁接的季铵基带正电荷,能中和一部分材料表面的负电荷。然而,当PDADMAC加入量超过3%时,材料表面的电位并没有明显增加,这是由于大分子PDADMAC在GO片层中缠绕现象严重,导致季铵基大量与GO表面含氧官能团相结合,材料表面正电荷没有明显增加。
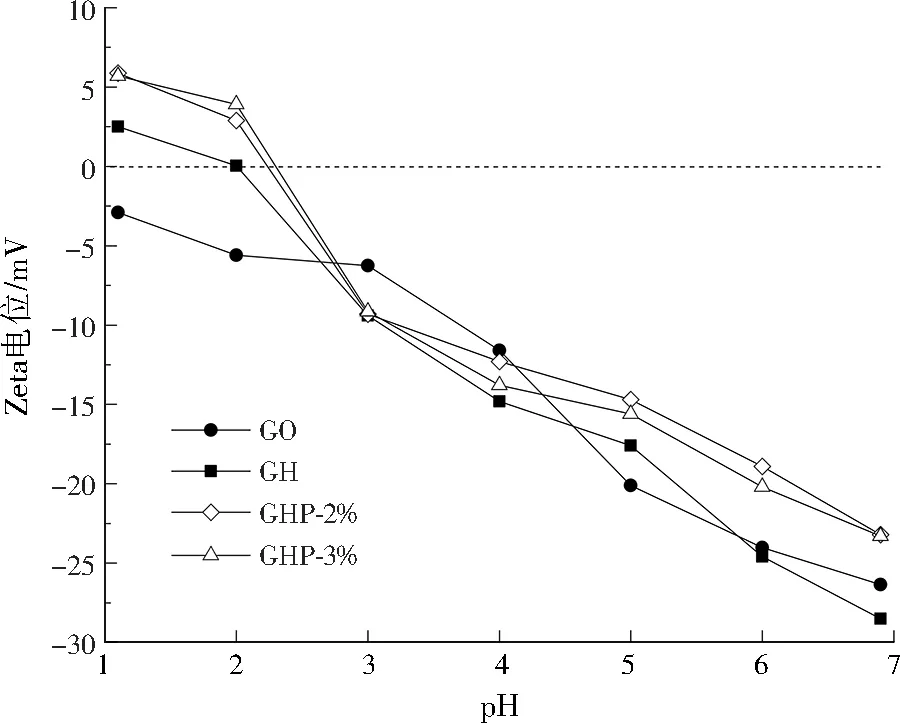
图3 材料的Zeta电位Fig.3 Zeta potential of materials
另外,由于本研究的水凝胶由GO片层在水中经水热还原[15]自组装形成,材料整体浸于水中,传统基于N2吸附的BET比表面积测量仪无法测量水中材料的比表面积。并且,水凝胶经冷干处理后将破坏原有的多孔结构,从而减少多孔材料的表面积[16]。因此,材料改性前后的比表面积在本研究中暂不分析。
2.2 MO的吸附等温线
为探究水热合成及季铵基嫁接对材料吸附MO的影响,在pH分别为7.0和3.0(pH为整个吸附过程中体系内所保持的pH,且在吸附过程中pH无明显变化)下进行了批量吸附实验,结果见图4,Langmuir和Freundlich模型的拟合结果见表2。比较r2发现,Langmuir模型的拟合更适用于描述各材料对MO的吸附,表明各材料对MO的吸附是单层吸附[17]。当pH为3.0、7.0时,GH对MO的最大吸附量均高于GO。这是由于GH能形成多孔的稳定结构,继承了原始纳米材料分散后比表面积巨大的优点,并且可将这种分散状态长久固定[5]8,同时也会因为这种多孔结构而产生额外的吸附位点[18]。另外,GO表面的含氧官能团明显多于其他材料,官能团发生电离后所带的负电荷也最多,其与MO间静电斥力增强,从而导致吸附量减少。
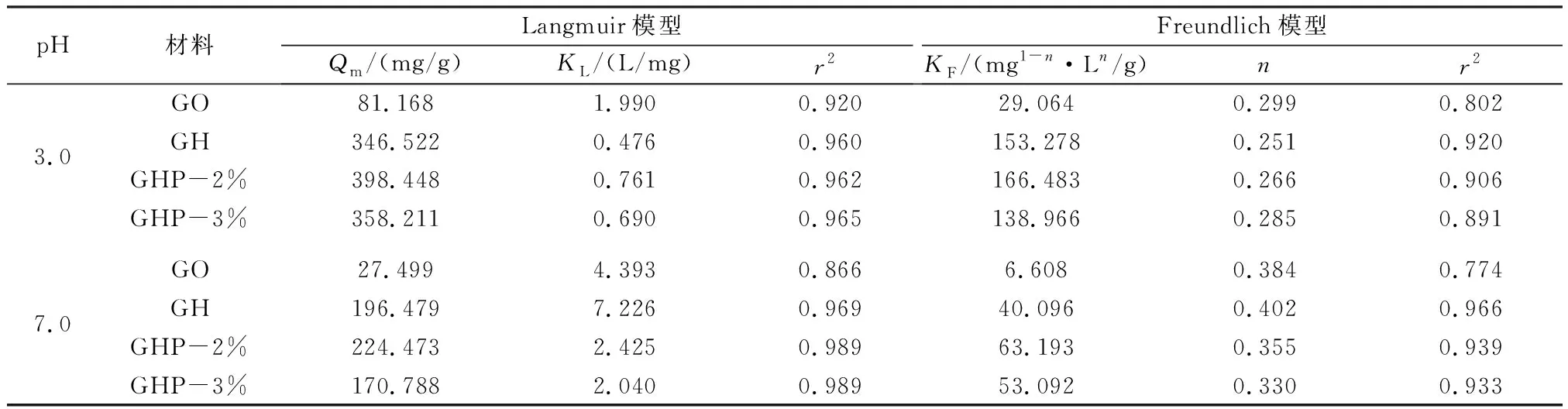
表2 Langmuir和Freundlich模型拟合结果Table 2 The fitting results by Langmuir and Freundlich models
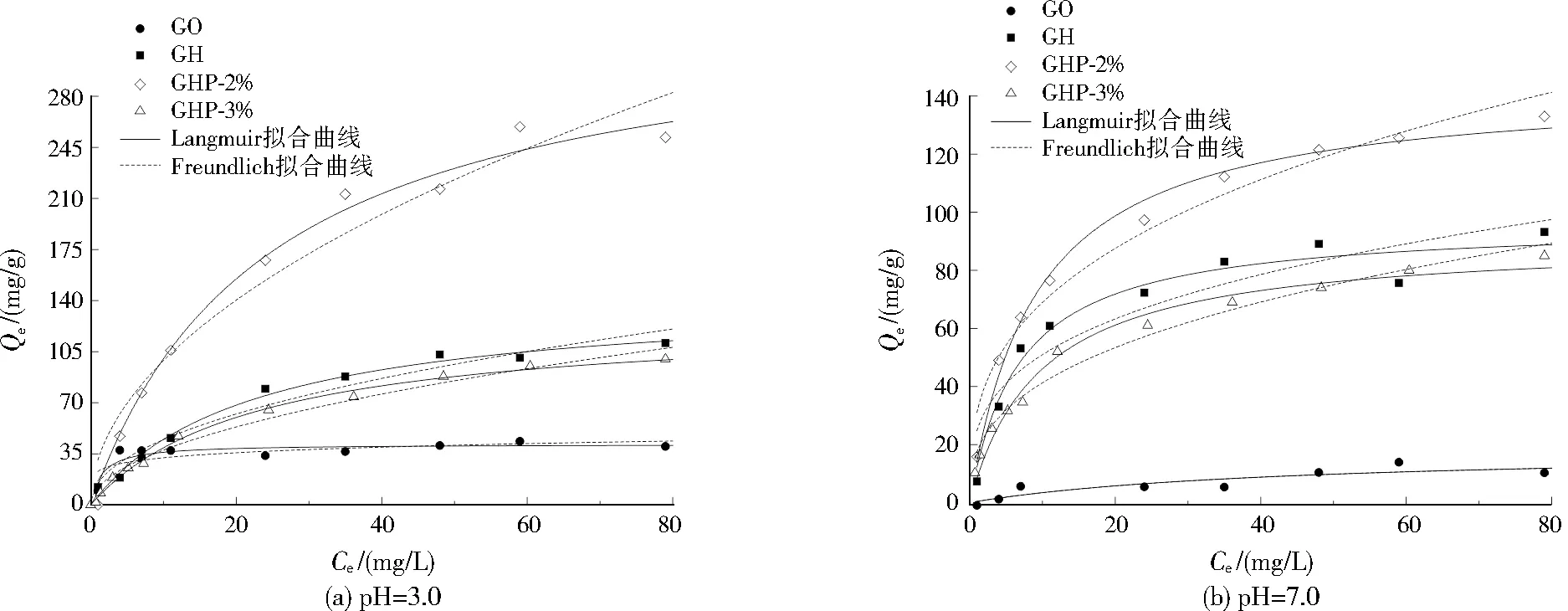
图4 不同pH下材料对MO的吸附等温线Fig.4 The adsorption isotherm of materials for MO at different pH
当pH=3.0时各材料的吸附量均明显高于当pH=7.0时。这归因于当pH=3.0时材料表面官能团质子化,所带负电荷减少,且此时MO以中性分子形态存在,污染物与材料间静电斥力较小,吸附量增加;当pH=7.0时,材料表面官能团去质子化,负电荷明显增加,与MO间的静电斥力增加,导致吸附量降低[19]。当pH=3.0和7.0时,GHP-2%对MO的吸附量均高于其余材料,且高于MA等[20]制备的活化多壁碳纳米管对MO的吸附量(199 mg/g)。这一方面归因于GHP-2%拥有高孔隙度的三维多孔稳定结构(见图1(c)),拥有更多的活性吸附位点;另一方面,季铵基增加了正电荷数量(见图3),降低了材料与MO间的静电斥力,吸附量增加。GHP-3%的吸附能力与GH相当,且低于GHP-2%,PDADMAC的过量添加会抑制对MO的吸附,这是由于过量的大分子高聚物与GO片层之间相互缠绕,覆盖了材料表面有效的吸附位点,且这种缠绕会使得GO片层间距缩小,导致材料表面的有效吸附位点进一步减少。
2.3 MO的吸附动力学
当pH分别为3.0和7.0时,材料对MO的吸附动力学结果见图5,PFM和PSM的拟合结果见表3。比较r2发现,PSM的拟合更适用于描述各材料对MO的吸附,表明各材料对MO的吸附是化学吸附[21]。GO的k2高于其余材料,表明GO吸附MO的平衡时间最短。这是由于GO对MO的吸附没有孔内扩散过程,仅在GO表面发生吸附,因此吸附的平衡时间短但吸附量较低。而对于其他材料,吸附的平衡时间较长是由MO在孔内扩散过程导致,这与其他多孔碳材料吸附较慢的原因相同。在水凝胶中,MO首先通过氢键、π-π等作用吸附于水凝胶表面,然后通过粒子内扩散作用转移到多孔结构中。值得注意的是,GHP-2%的k2最小,表明其吸附的平衡时间最长,这是由于GHP-2%高度发达的孔隙导致MO的内扩散时间最长。大量PDADMAC的添加导致GHP-3%孔隙明显减少(见图1(d)),内扩散作用减弱,因此GHP-3%吸附MO的平衡时间缩短,吸附量下降。
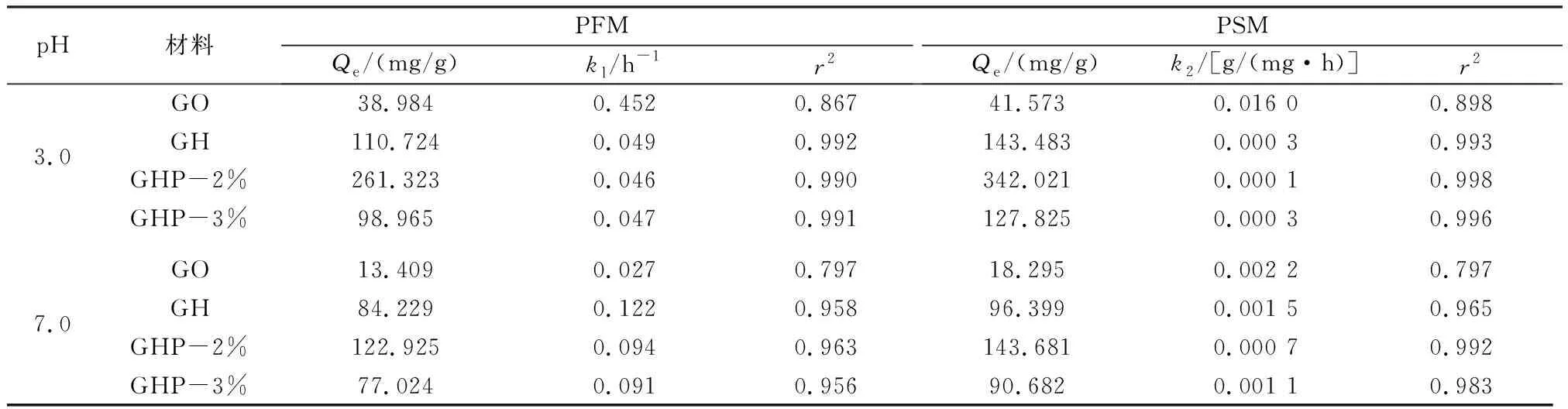
表3 PFM和PSM的拟合结果Table 3 The fitting results by PFM and PSM
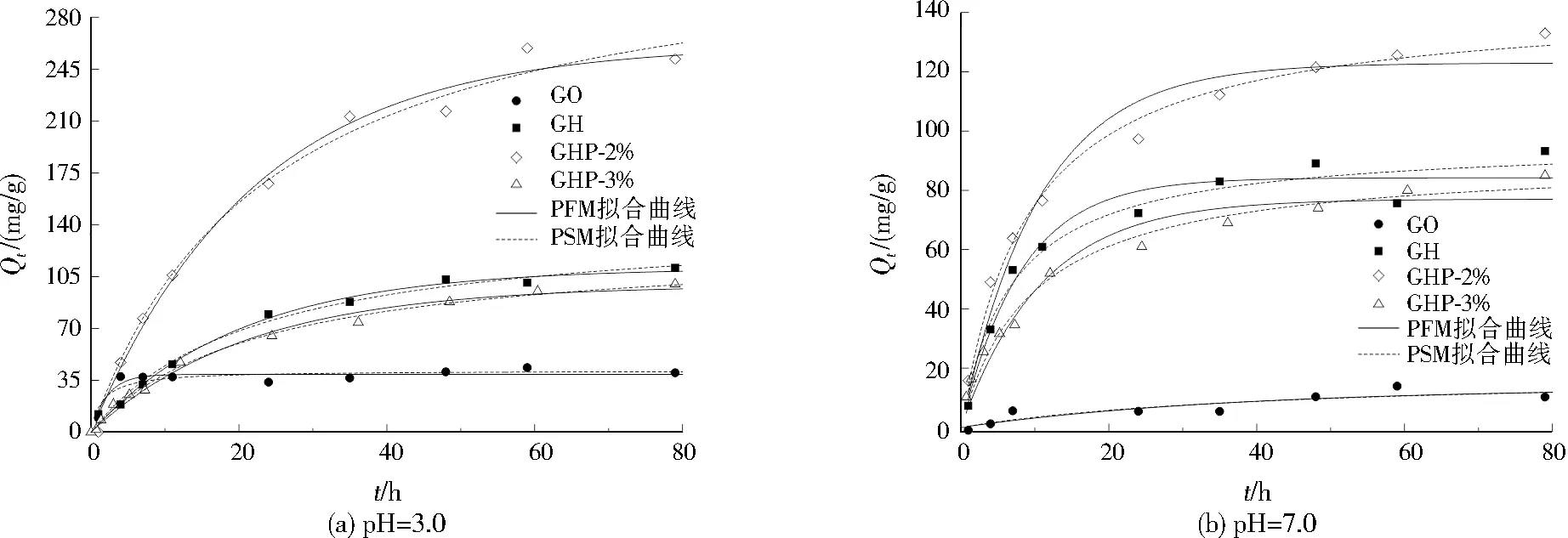
图5 不同pH下材料对MO的吸附动力学Fig.5 The adsorption kinetics of materials for MO at different pH
为验证颗粒内扩散对吸附动力学的作用,采用IDM对吸附动力学过程进行拟合,结果见图6和表4。材料对MO的吸附动力学拟合曲线基本呈3个阶段,说明MO的吸附动力学受控于3个步骤:(1)MO分子在材料表面扩散过程;(2)MO分子在孔隙内扩散过程;(3)动态吸附平衡过程。对于GO,MO的动力学过程仅包括步骤(1)和步骤(3),这是由于GO内部孔隙较少(见图1(a)),MO的吸附动力学不受颗粒内扩散过程的控制。当pH=3.0时,第2阶段MO在材料孔隙内的扩散速度快于当pH=7.0时。这是由于溶液中H3O+在低pH下明显增加,而材料的官能团发生质子化,使材料所带的正电荷增加,从而导致MO与材料间的静电吸引力增加,吸附速率明显加快;在高pH条件下,材料的官能团由于去质子化作用而带负电荷,与MO间的静电斥力增加,导致MO的吸附速率明显减慢。
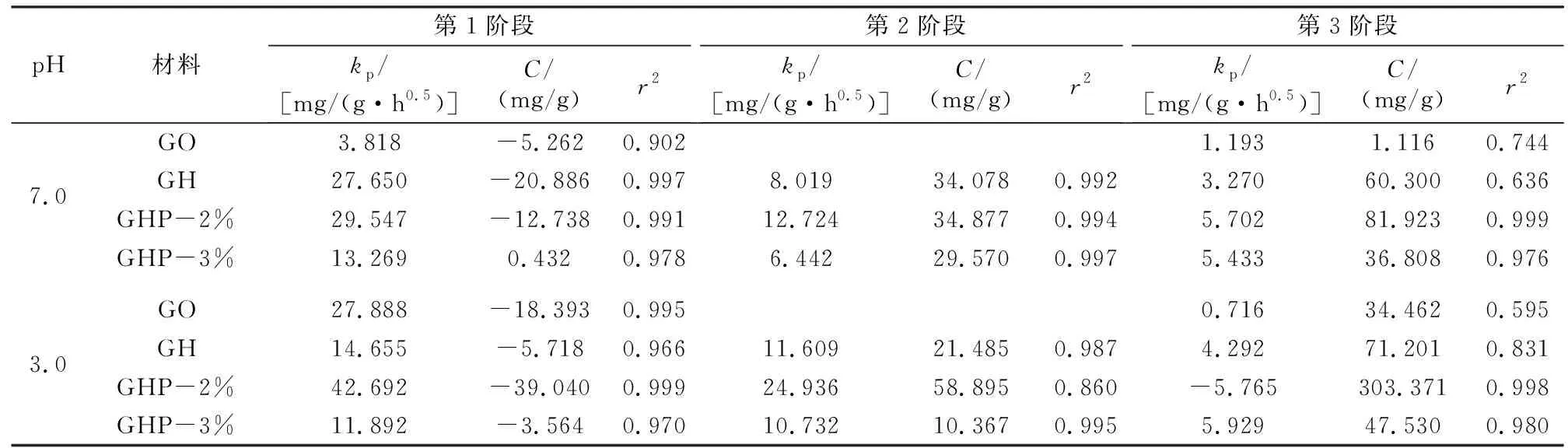
表4 IDM的拟合结果Table 4 The fitting results by IDM
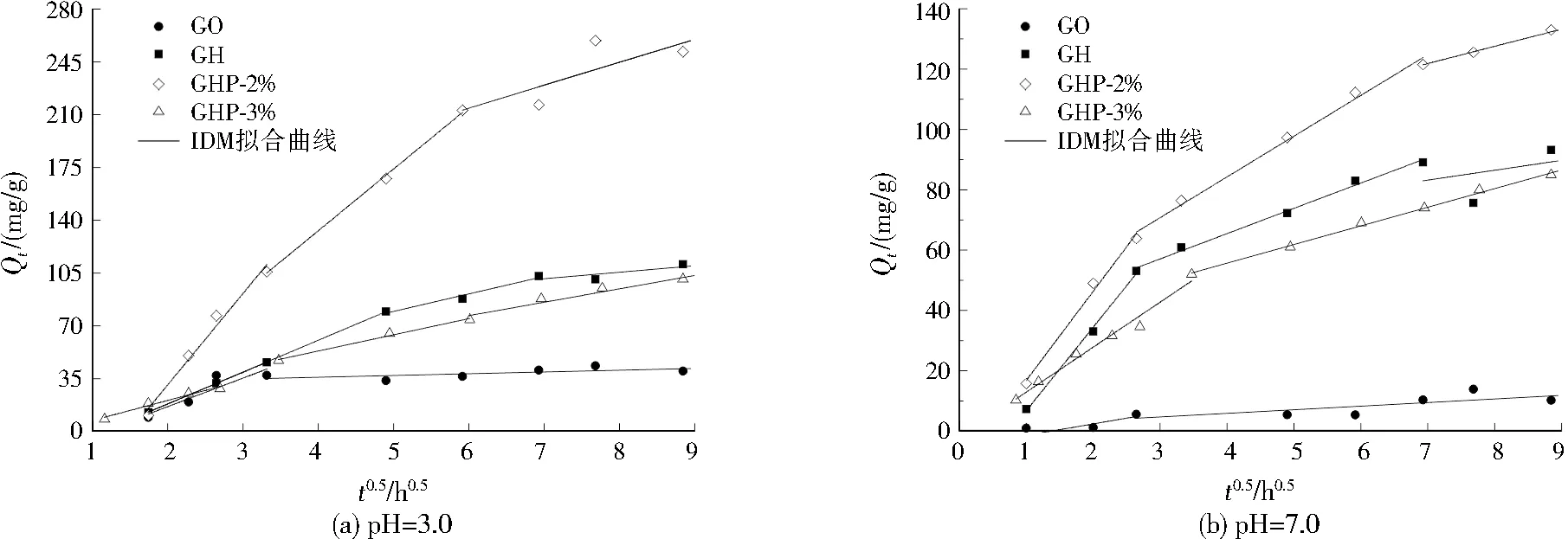
图6 不同pH下IDM拟合的吸附动力学Fig.6 The adsorption kinetics by IDM at different pH
3 结 语
(1) 当pH=3.0和7.0时,GHP-2%对MO均表现出较强的吸附能力。Langmuir模型和PSM能较好拟合材料对MO的吸附过程,表明该吸附过程为单层的化学吸附。
(2) 当pH=3.0和7.0时,GHP-2%对MO的最大吸附量分别为398.448、224.473 mg/g。随溶液pH增加,材料表面官能团产生去质子化,所带负电荷增加,对MO的吸附能力下降,而在嫁接季铵基后,季铵基能在较宽pH范围内保持正电,使其与MO间静电斥力减弱,吸附量增加。
(3) GHP-2%吸附MO的平衡时间明显长于其他材料,这归因于GHP-2%高度发达的孔隙,导致MO的内扩散时间较长。但过量季铵基的添加会导致三维材料孔隙坍塌,GHP-3%对MO的吸附动力学平衡时间缩短,同时吸附量降低。
(4) GHP-2%在pH为3~7内均保持对水体中阴离子染料的高效去除,是一种很有应用前景的阴离子染料吸附剂。

