慢性肾脏病维持性血液透析患者高磷血症与心血管参数的相关性
邹欢,张游
(1重庆医科大学附属第一医院肾脏内科,重庆 400016;重庆市南川区人民医院: 2全科医学科,3肾内科,重庆 408400)
慢性肾脏病(chronic kidney disease,CKD)已成为近年来我国愈发显著的公共卫生问题。2009至2010年期间进行的一项全国范围的横断面调查显示,我国CKD患病率为10.8%[1]。随着我国新一轮医疗卫生体制改革的推进,一项针对全国住院患者的数据库显示[2],2010至2017年CKD住院患者的比例从3.58%上升至4.95%,每年仅CKD患者的透析费用就可达153亿,给医疗保健系统带来巨大负担。有研究发现,心血管疾病是CKD患者死亡的主要病因,>50%的透析患者死于心血管疾病[3]。除了高血压、糖尿病、血脂异常及吸烟等传统因素外,炎症、蛋白尿及矿物质代谢异常等,也会增加CKD患者心血管疾病的风险,尤其是钙、磷含量的增加[3]。一项关于CKD患者心血管事件的meta分析显示,血清磷浓度升高与心血管事件风险增加显著相关[4],血清磷水平较高患者,发生左心室肥厚(left ventricular hypertrophy,LVH)及主动脉钙化(aortic calcification, AC)的可能性更大。本研究探讨CKD维持性血液透析患者高磷血症与心血管参数LVH及AC的相关性,以期为临床心血管疾病的治疗提供依据。
1 对象与方法
1.1 研究对象
回顾性分析2018年1月至2019年3月于重庆医科大学附属第一医院肾脏内科进行维持性血液透析治疗的465例CKD患者的临床资料。纳入标准:(1)年龄18~65岁;(2)维持性透析时间>6个月。排除标准:(1)有严重的共存疾病,包括慢性心力衰竭(纽约心脏病协会心功能分级3级或4级心力衰竭)、肝硬化、艾滋病及器官移植;(2)需要在6个月内使用免疫抑制剂治疗的肾病或免疫性疾病;(3)2年内有化疗史的恶性肿瘤;(4)孕妇及哺乳期妇女;(5)有介入治疗手术史;(6)急性肾损伤。
1.2 方法
1.2.1 基线资料 收集患者透析龄、人口统计学资料、生活行为方式、用药史、静息血压、身高和体质量等一般资料。记录钙、磷、血红蛋白、白蛋白、甲状旁腺激素等生化指标。
1.2.2 LVH的诊断 对患者进行二维超声心动图检查,由1名具有心脏超声学诊断经验的主治及以上职称医师进行评判分析。患者采取适宜体位(仰卧位、左侧卧位等)露出皮肤,涂耦合剂、探头紧贴皮肤后即可进行检查。测量指标包括:室间隔舒张末厚度(inter-ventricular septum end-diastolic thickness,LVST)、左心室后壁舒张末厚度(left ventricular posterior wall end-diastolic thickness,PWTH)、左心室舒张末径(left ventricular end-diastolic diameter,LVEDd)及左心室质量(left ventricular mass,LVM)。计算LVM及左心室质量指数(left ventricle mass index,LVMI)。LVM=0.8[1.04(IVST+PWT+LVEDd)3-LVEDd3]+0.6[5]。LVMI=LVM/体表面积。体表面积=0.0061×身高(cm)+0.0128×质量(kg)-0.1529。男性LVMI>125g/m2、女性LVMI>120g/m2为LVH[6]。
1.2.3 AC的诊断 对患者行胸部CT平扫或胸部X线检查,由1名具有主治及以上职称的影像学医师进行诊断分析。
1.3 统计学处理
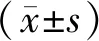
2 结 果
2.1 患者的一般资料
本研究共465例患者均为CKD5期,年龄(52.56±11.39)岁,其中男性263例(56.56 %)。所纳入患者病因较多,其中肾小球肾炎147例(31.61%)、糖尿病肾病102例(21.94%)、高血压肾病108例(23.23%)、多囊肾26例(5.59 %)、梗阻性肾病14例(3.01%)、痛风13例(2.80%)、抗中性粒细胞胞浆抗体相关性血管炎13例(2.80%)、乙肝相关性肾炎5例(1.08%)、缺血性肾病2例(0.43%)、免疫球蛋白A肾病3例(0.65%)、移植肾失功能2例(0.43%)以及紫癜性肾炎3例(0.65%)。
2.2 LVH组与非LVH组患者一般资料比较
将328例行二维超声心动图检查的CKD维持性血液透析患者按是否存在LVH,分为LVH组234例及非LVH组94例。与非LVH组比较,LVH组患者收缩压、舒张压、血清磷及糖尿病患病率均显著升高,年龄、血红蛋白、血清钙及白蛋白水平均显著降低,差异均有统计学意义(均P<0.05;表1)。
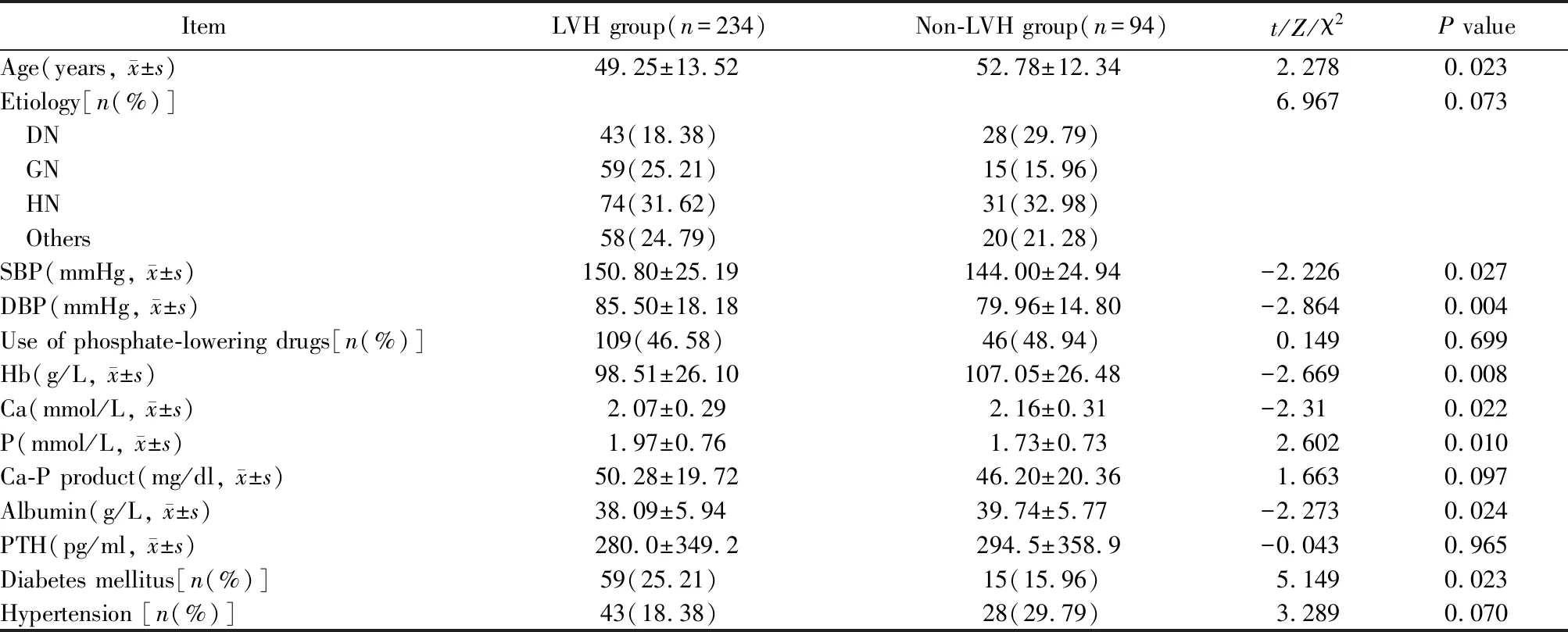
表1 LVH组与非LVH组患者一般资料比较
2.3 CKD维持性血液透析患者LVH的多因素logistic回归分析
多因素logistic回归分析进一步证实,舒张压升高、血清磷升高、合并糖尿病以及白蛋白下降是CKD维持性血液透析患者合并LVH的独立危险因素。详见表2。
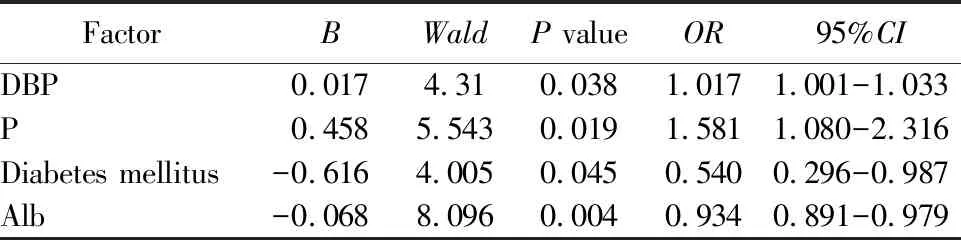
表2 CKD维持性血液透析患者LVH的多因素logistic回归分析
2.4 AC组与非AC组患者一般资料比较
将330例行胸部CT平扫或胸部X线检查的CKD维持性血液透析患者按是否存在AC,分为AC组199例及非AC组131例。与非AC组相比,AC组的患者年龄、血红蛋白、血清钙、血清磷、钙磷乘积、糖尿病及高血压患病率均显著升高,舒张压及降磷药物的使用率均显著降低,差异均有统计学意义(均P<0.05;表3)。
表3 AC组与非AC组患者一般资料比较
2.5 CKD维持性血液透析患者AC的多因素logistic回归分析
多因素logistic回归分析证实,年龄、血清磷升高、钙磷乘积以及合并糖尿病是CKD维持性血液透析患者合并AC的独立危险因素。详见表4。
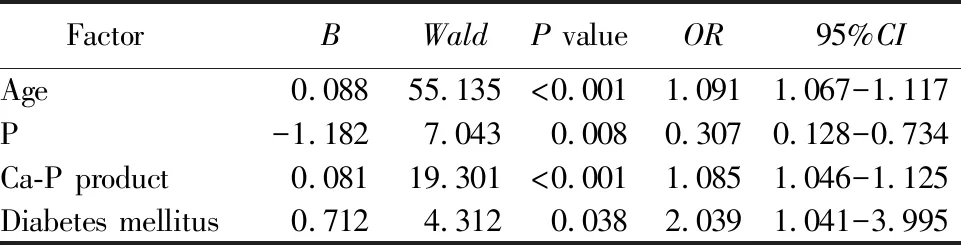
表4 CKD维持性血液透析患者AC的多因素logistic回归分析
2.6 血清磷水平与心血管参数的相关性
根据改善全球肾脏病预后组织指南建议,将269例既有二维超声心动图,也有影像学检查结果的患者分为低血清磷组36例(血清磷<0.81mmol/L)、高血清磷组127例(血清磷>1.45mmol/L)及正常血清磷组106例(0.81≤血清磷≤1.45mmol/L),3组间AC患病率比较,差异无统计学差异(P>0.05)。3组间LVH患病率比较,差异有统计学意义(P<0.05;表5)。高血清磷组LVH患病率显著高于正常血清磷组,差异有统计学意义(P<0.05;表5)。
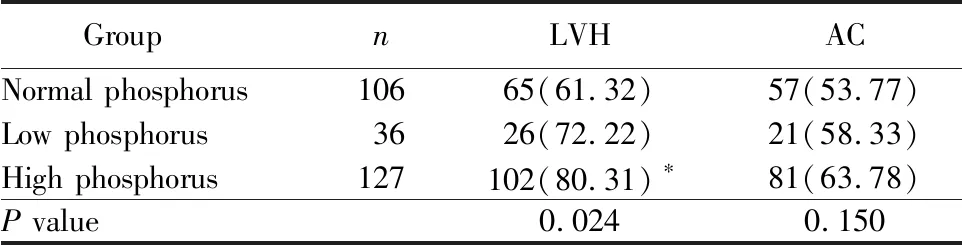
表5 血清磷水平与LVH及AC的相关性分析
3 讨 论
CKD患者常常出现高磷血症,肾脏对磷滤过下降导致磷在体内潴留是CKD患者发生高磷血症最根本的原因,而高磷血症又是诱发心血管疾病的常见因素。一项对3300例无心力衰竭和CKD人群进行的前瞻性研究显示[7],血清磷每增加10mg/L,心力衰竭的风险增加1.74倍。此外,一项关于动脉粥样硬化的多种族研究中,纳入4494例未发生过任何心血管疾病的参与者,发现膳食磷酸盐摄入量每增加预计值的1/5,LVM增加1.06g[8]。目前,关于CKD人群中磷与心血管参数LVH及AC之间关系的研究较少。Chue等[9]采用心血管磁共振成像技术对208例CKD 2~4期非糖尿病患者血清磷(平均血清磷1.1mmol/L)与LVMI之间的相关性进行研究,发现即使大多数患者血清磷在改善全球肾脏病预后组织指南的推荐范围内,磷对透析前CKD各阶段患者的心血管结构仍有影响。本研究针对CKD维持性血液透析患者进行回顾性分析,探讨高磷血症与LVH和AC的相关性。
本研究中,与非LVH组比较,LVH组患者血清磷显著升高,同时高血清磷组患者LVH发生率显著高于正常血清磷组(P<0.05)。血清磷水平是CKD维持性血液透析患者合并LVH的独立危险因素。CKD患者血清磷和LVH之间的关联可能与以下原因有关:第一,高磷血症引起的血管钙化和动脉僵硬降低了大血管顺应性[10],从而使心脏后负荷增加,引起LVH;第二,磷对心肌细胞的毒性作用可能是心肌细胞肥大和间质细胞增殖的原因[11]。
高磷血症作为肾病矿物质和骨代谢异常的代表,与血管钙化的关系最为密切。随着血清磷升高,血管平滑肌钙化的易感性增加,会对多个信号通路产生影响。研究显示,高磷血症、高密度脂蛋白胆固醇低水平是AC的危险因素[12]。本研究显示CKD维持性血液透析患者AC的患病率为60.30%(199/330)。与非AC组比较,AC组患者血清磷显著升高,血清磷水平是CKD维持性血液透析患者合并LVH的独立危险因素。高磷血症、高钙磷乘积常伴随心血管钙化、左室肥大、心血管事件(如心肌梗死、充血性心力衰竭)出现。有研究称,血清磷升高可增加AC的发生率,磷酸钙晶体在血管中沉积引起的AC是CKD相关死亡和心血管并发症的主要原因[13]。钙化血管弹性降低,更易发生AC,引起心脏功能障碍[14]。动物实验表明,高水平的细胞外磷酸盐可刺激血管平滑肌细胞(vascular smooth muscle cells, VSMCs)转分化为成骨样细胞,增加VSMCs中钙的积累,从而诱导钙化[15]。高血清磷也可诱导VSMCs中特定平滑肌蛋白表达的缺失,并使VSMCs获得软骨表型[16]。有研究指出,血液透析患者随着年龄的增加,血管在不断血流冲击和舒缩活动的刺激下,发生脂类物质堆积、平滑肌及弹力蛋白减少等结构性改变,也会造成血管壁内膜发生钙化,且随着血液透析时间的增加,患者血管内钙磷被动沉积、钙化促进因子活性增加以及钙化抑制因子活性降低,会促进血管钙化[12]。此外,本研究AC组患者降磷药物使用率显著低于非AC组。2016年的一项研究[17]也发现了磷结合剂在中国的使用情况并不令人满意,提醒临床医师需要重视CKD患者矿物质代谢紊乱的治疗。
综上,CKD维持性血液透析患者高磷血症与心血管参数LVH和AC独立相关。对CKD患者血清磷水平进行控制,有利于减少心血管事件的发生率及改善预后。本研究有以下局限性:首先,本研究为基于横断面数据的回顾性研究,无法做出因果推断;其次,本研究虽对血清磷浓度分层分析,但例数较少,仅初步探讨不同血清磷浓度与LVH及AC的关系;第三,研究中心血管参数的测量并没有包含整个队列。

