低管电流低管电压扫描联合人工智能重建技术在胸部肋骨骨折中的应用
李锦田,左 卫
(1广东省第二人民医院放射科 广东 广州 510000)
(2广东省第二人民医院影像科 广东 广州 510000)
胸部外伤的检查中常规使用X线进行,X线在胸部骨折诊断中具有准确率高、费用低廉等优势,但对细小骨折敏感度低,需要进一步CT诊断[1]。目前胸部外伤的细小肋骨骨折诊断主要以CT为主,然而CT扫描存在辐射,相关研究发现CT检查所带来的辐射会使患者增加患癌风险,因此降低患者检查所受辐射剂量具有重要临床意义[2]。降低辐射剂量的胸部扫描会导致图像噪声增大、信噪比降低,影响肋骨骨折的观察,因此,寻找一种能够增加低管电流低管电压扫描信噪比的方法尤为重要。人工智能(artificial intelligence,AI)重建技术是一种基于随机森林等机器学习得出的优化重建算法,AI重建能有效减少图像噪声,达到提升图像信噪比的效果[3]。本次研究在于探讨AI重建技术在低管电流低管电压胸部扫描CT中改善图像质量的可行性。
1 资料与方法
1.1 一般资料
选取2021年1月—2022年6月在广东省第二人民医院因胸部外伤申请胸部CT检查的72例(男45例、女27例)患者,平均年龄为(58.68±8.59)岁。纳入标准:因外伤胸部,主诉胸部疼痛。排除标准:①因剧烈疼痛导致呼吸伪影过大的图像。②无法进行图像识别、无法重建的患者图像,本研究通过医院伦理委员会审核(2023-KY-KZ-059-02)。
1.2 方法
1.2.1 分组方法 本研究为前瞻性研究,对胸部CT检查的患者进行随机分组。A组采用230 mAs管电流,100 kV管电压进行扫描,B组、C组采用100 mAs管电流,80 kV管电压进行扫描,A组、B组使用滤波反投影法重建图像,C组采用AI重建算法重建图像。
1.2.2 设备 使用联影320排螺旋CT(UNITED IMAGING uCT320),螺距0.6,扫描层厚0.5 mm,探测器覆盖宽度64×0.625 mm,A、B组采用滤波反投影法,C组采用AI重建技术,扫描层面包括所有肋骨。
1.3 图像后处理与质量评价
1.3.1 图像质量主观评价 利用后处理系统,将A、B组图像使用滤波反投影法处理后进行胸部CT骨窗重建,将C组图像使用AI重建技术进行胸部CT骨窗重建,三组重建后数据进行MIP重建、VR重建等处理,图像评分采用4级评分法进行,图像全局清晰,肋骨边缘清晰,能有效观察骨小梁评为4分;图像全局清晰,肋骨边缘模糊,但仍可以观察到骨小梁是否连续评为3分;图像全局模糊,肋骨边缘不清,无法区分骨小梁连续性评为2分;图像出现高噪声,肋骨边缘无法观察,无法诊断肋骨情况评为1分[4]。
1.3.2 图像质量客观评价 对三组噪声进行测量并计算CNR及SNR,测量肋骨CT值并以CT值标准差SD为肋骨噪声,测量胸背部肌肉CT值SD为背景噪声,计算胸部CT图像CNR及SNR,计算公式:SNR Chest =CTChest/SDChest;CNRChest=(CTChest-CTFAT)/SDFAT(Chest:胸部;FAT:背景噪声)[5]。
1.4 统计学方法
所有数据利用SPSS22.0软件处理:符合正态分布数据用()表示,不符合正态分布用[M(Q1,Q3)]表示,三组患者性别的比较采用卡方检验进行,三组患者CT值、噪声、CNP、SNP、DLP、CTDIvol、年龄比较采用单因素方差分析,P<0.05为具有统计学意义。
2 结果
2.1 三组患者一般资料与图像质量比较
三组患者年龄、性别不具有统计学意义(P>0.05),见表1,A、B两组图像CNR、SNR、图像评分具有统计学意义(P<0.05),A、C两组图像CNR、SNR、图像评分差异不具有统计学意义(P>0.05),B、C两组图像CNR、SNR、图像评分差异具有统计学意义(P<0.05),见表2、图1。
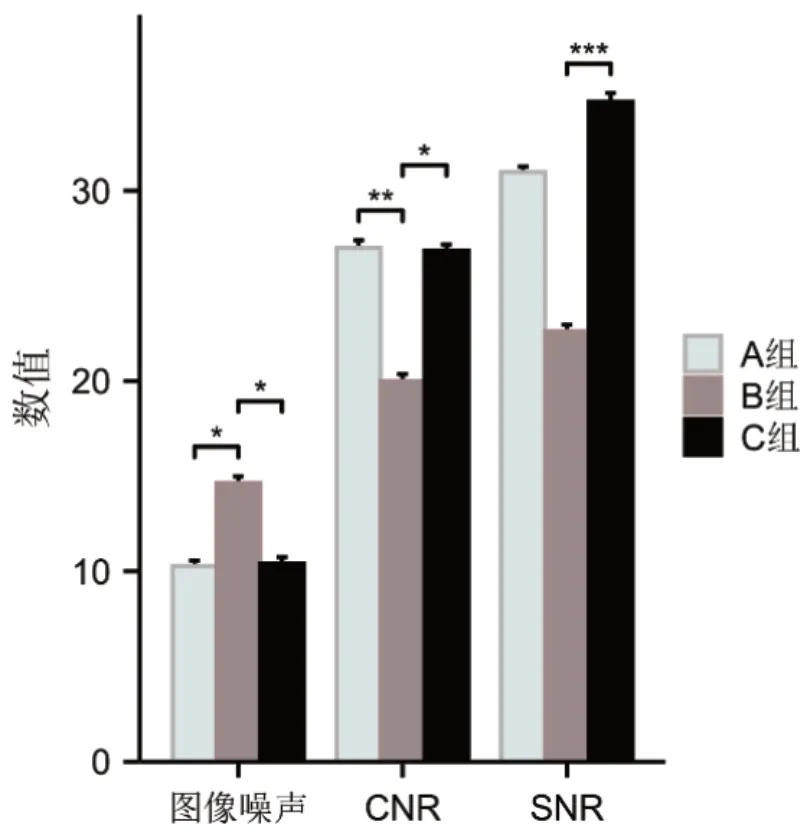
图1 三组胸部CT图像质量数据柱形图
表1 三组患者一般资料对照表()

表1 三组患者一般资料对照表()
组别平均年龄(images/BZ_15_1875_1021_1974_1069.png,岁)男/女(例)A组(n=24)56.84±7.2814/10 B组(n=21)60.32±8.4715/6 C组(n=27)58.42±9.8716/11 F[χ2]2.189[1.013]P 0.3870.603

表2 三组患者图像噪声、CNR、SNR比较
2.2 三组患者辐射剂量比较
A、B两组胸部CT患者DLP、CTDIvol、ED差异均具有统计学意义(P<0.05),A、C两组胸部CT患者DLP、CTDIvol、ED差异均具有统计学意义(P<0.05),B、C两组胸部CT患者DLP、CTDIvol、ED差异均不具有统计学意义(P>0.05)。见表3。
表3 三组患者辐射剂量比较()

表3 三组患者辐射剂量比较()
注:①表示与B组比较,差异具有统计学意义,②表示与C组比较,差异具有统计学意义。
组别CTDIvol/mGy)DLP/mGy·cmED/mSv A组(n=24)10.51±1.76①②334.5±28.51①②6.46±0.34①②B组(n=21)5.62±1.65184.2±22.153.52±0.83 C组(n=27)5.01±1.26175.1±21.543.41±0.62 F 23.84321.15834.593 P 0.0340.0280.021
3 讨论
目前X线双斜位摄影诊断肋骨骨折是最经济、快捷的方式,然而,较细小的肋骨骨折容易漏诊,导致延误治疗,进一步发生二次伤害甚至导致气胸的形成。因此常增加胸部CT检查发现细微肋骨骨折。然而,CT检查辐射剂量明显大于X线检查,如何对检查的辐射损害减少,是目前研究的重要方向[6]。本研究在对三组不同扫描方案与重建技术的研究中发现,B组、C组在低管电流低管电压的扫描下辐射剂量明显低于A组的常规剂量。但B组较A组出现了明显的图像评分下降,而C组在低管电流低管电压的同时引入AI重建技术对图像噪声进行优化,使得C组图像的CNR、SNR明显优于B组。
电离辐射是CT检查中的主要辐射形式,对人体染色体具有一定损害。本研究B、C组低管电流低管电压方案DLP、CTDIvol、ED明显低于A组,降低了辐射剂量,合理控制患者潜在的辐射伤害。胸部CT肋骨骨折检查的原则是要保证肋骨能清晰观察、明确诊断,但尽量减少患者所受辐射,本研究在低管电流低管电压扫描出现噪声上升,主要因为管电压下降后,CT射线穿透能力下降,增加的散射线导致了信号采集出现颗粒[7]。然而,C组使用胸部AI重建技术进行肋骨重建,图像噪声低于同条件B组,而CNR、SNR高于B组,且与A组的正常管电流管电压对比无明显差异,因此本次研究中B组因扫描条件的降低使得图像噪声上升、CNR、SNR下降,但相同扫描条件下由于C组引入AI重建技术进行肋骨重建,使图像优化过程中最大限度保留图像的真实细节,从而达到优化低剂量图像的效果。
AI重建技术是基于一种基于随机森林模型机器学习得出的新一代重建模型,该模型多用于CT血管造影的检查优化中,AI通过训练图像噪声进行优化,利用神经网络分离噪声-图像后重建出新图像,进一步优化高噪声的图像[8]。目前AI重建算法多用于CT血管造影低辐射剂量研究中,利用深度学习AI算法对抗反馈训练生产与常规剂量一致的低剂量CT图像[9]。本研究将低剂量CT图像质量优化最新算法利用于胸部平扫图像肋骨重建中得到了很好的结果,利用AI重建技术获得的低管电流管电压图像与常规管电流管电压图像一致,实现AI重建技术不同应用,开拓新AI低剂量研究场景。本次研究100 mAs管电流,80 kV管电压胸部CT肋骨重建可满足临床需求。说明低管电流管电压联合AI重建技术在胸部肋骨骨折诊断中具有可行性。
本次研究不足在于样本量偏小,由于外伤患者多数疼痛感觉明显、配合度差,容易造成呼吸伪影[10],对于呼吸伪影的肋骨重建,能否通过AI重建技术改善评估需要进一步研究。
综上所述,人工智能重建技术能优化低管电流低管电压图像中的噪声,提升图像信噪比,成像可达到常规条件的肋骨骨折观察图像质量。

