中医疗法靶向干预SCF/c-kit信号通路治疗功能性消化不良机制研究进展
陶永彪 ,汪龙德 ,牛媛媛 ,李正菊 ,靳三省 ,吴毓谦 ,张瑞婷
1.甘肃中医药大学,甘肃 兰州 730000; 2.甘肃中医药大学附属医院,甘肃 兰州 730020
功能性消化不良(functional dyspepsia,FD)是一种临床常见的功能性胃肠疾病,病变部位涉及胃肠道的胃十二指肠区。FD包括2种不同病理生理的亚型:餐后窘迫综合征(postprandial distress syndrome,PDS)、胃脘痛综合征(epigastric pain syndrome,EPS)[1]。其症状包括餐后饱腹感、上腹部疼痛和胃脘部灼烧感。大约80%的消化不良患者的症状没有结构性解释[2]。据报道,FD的全球发病率为7%~45%。目前FD发病的病理生理学机制仍未完全阐明,一般认为脑肠互动紊乱、内脏过敏变化、胃肠动力异常、十二指肠屏障受损等是其主要发生机制[3]。因此,其治疗常存在局限性,缺乏有效的治疗选择,多针对病因及症状给予抑酸剂、促胃肠动力药和中枢神经调节剂等,作用较为单一。中医在FD 的诊疗中举足轻重,具有明显优势,中医疗法多成分、多靶点、多通路的特点是其发挥整体调节作用的基础。多项研究证实抑制干细胞因子(SCF)/c-kit信号通路活化是治疗FD的有效途径,且表明中医疗法具有靶向调控该通路治疗FD的作用。
1 SCF/c-kit信号通路在功能性消化不良中的作用
c-kit是由原癌基因c-kit编码的跨膜蛋白,在胞外配体结合区与神经元表达的配体SCF结合,产生均聚反应,磷酸化细胞膜上氨基残基,启动SCF/c-kit信号通路,介导下游信号转导。目前基于SCF/c-kit通路研究FD的靶向细胞主要集中于卡哈尔间质细胞(ICC),然而,c-kit并不只在胃肠ICC上表达,其他非ICC细胞类型,如神经细胞(NC)和肥大细胞(MC),也存在表达高水平的c-kit,表明ICC、NC和MC均是SCF/c-kit系统调控的细胞系[4],见图1。
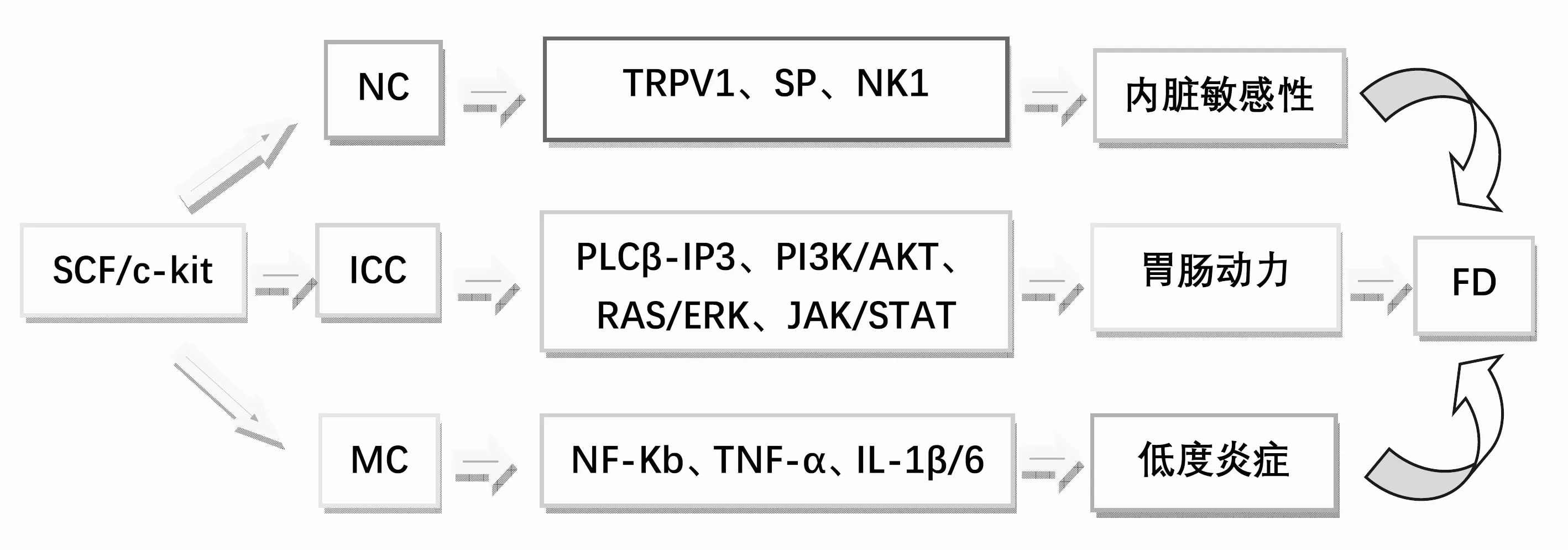
图1 SCF/c-kit信号通路调控机制
ICC广泛分布于整个胃肠道的肌层中,是消化道运动的起搏细胞、胃肠道节律运动的发起者和胃肠道节律电位的传递者[5]。SCF/c-kit通路参与ICC的发育和表型分化,扮演ICC起搏功能产生的维持者角色。c-kit由ICC表达,是ICC的特异性受体。SCF/c-kit系统在ICC的开发中至关重要[6]。SCF蛋白可调控ICC的增殖分化,增加ICC数量,修复ICC超微结构,进而促进胃肠动力[7-8]。Jensen等[9]研究发现,SCF/c-kit信号系统具有诱导调控MC的潜力,并通过抑制剂干预c-kit受体,证实该通路对MC的增殖分化具有重要作用。SCF是主要的MC生长因子,具有诱导MC发育、存活、趋化、细胞黏附、活化等作用[10-11],在十二指肠区,SCF促进肠道MC 增生,加速MC 衍生的促炎介质的释放[12-14],包括组胺、血清素和白三烯、白细胞介素等,降低局部微循环的完整性,引起胃、十二指肠的炎症反应[15-17]。SCF/c-kit通路与NC的调节机制尚未被阐述,相关研究发现SCF/c-kit系统与神经末梢释放的各种神经递质联系密切,并参与保护和重塑神经元,促进神经结构网络的重组,这一过程可能介导了FD疼痛反应的发生。
2 病因病机
依据FD症状可将其归属于中医学“胃痞”“胃脘痛”“嘈杂”等范畴。病位涉及胃、肝、脾,《临证指南医案》有“肝为起病之源,胃为受病之所”,肝木不疏横逆犯伤脾土,阳明斡旋升降失常,清阳不升,浊阴不降,进而影响中焦运化,䐜胀之疾由此而生。《素问·阴阳应象大论篇》载“清气在下,则生飧泄,浊气在上,则生䐜胀”;《素问病机气宜保命集》云:“脾不能行气于肺胃,结而不散,则为痞。”脾失健运,胃纳不振,升降失司,则出现痞满不适之症。其病多因饮食劳倦、七情内伤所致,初期以邪气盛为主要矛盾,邪气久羁,则易出现虚实夹杂证候,如《景岳全书·杂证谟·非风》所言“肝邪之见,本由脾肾之虚,使脾胃不虚,则肝木虽强,必无乘脾之患”,因此,当首辨虚实,以恢复肝脾胃三脏功能为要。《血证论·脏腑病机》有“木之性主于疏泄,食气入胃,全赖于肝木之气以疏泄之,而水谷乃化”,肝疏泄条达,脾胃升降有度,方能健运不息,正如《素问·宝命全形论篇》言“土需木疏,土得木而达”。若肝疏泄太过,肝强凌弱,横逆脾土;若疏泄不及,木不疏土,则脾失健运。
当代医家认为FD的基本病机为脾虚气滞,胃失和降[18-20],病位在胃,涉及肝脾两脏。目前,FD的证候大致分为脾虚气滞证、脾胃湿热证、脾胃虚弱证、寒热错杂证、脾胃虚寒证五型[21]。单兆伟教授认为,内因和外因合而致病是导致FD发生主要病因,中虚内伤,肝胃气滞,加之饮食七情失宜久而成痞[22],治疗上主张顾护中焦、疏理肝气,强调情志疏导、移情易性的重要性。张声生教授重视中焦为斡旋之枢,强调脾胃气机升降平衡有赖于脏腑协同,因此,在临床治疗时以运脾升清,和胃降浊为法,亦不忽视他脏他腑的作用,兼顾痰浊、湿热及瘀血等病理产物的生成,形成特有的“升清降浊”辨治体系[23]。吕林等[24]从“脾主运化水液”角度着手,认为FD脾虚的源头为湿邪困脾,如《素问经注节解》所云:“脾本湿土而性则喜燥,盖湿极则气滞不能运化矣。”其症状如胃脘部胀满、疼痛,大便稀溏、黏腻难下等均为湿邪作祟。治疗上重视虚实,病程久者补益脾胃,初期兼以化痰、理气、泻热。
脾虚气滞,胃失通降是FD病情缠绵,迁延难愈的宿根,湿、热、痰、瘀等病理产物贯穿FD发病的中末期,从而进一步引起气机阻滞,影响脾胃升降,导致胃肠功能障碍。其治疗多着眼于疏肝健脾、升清降浊,兼顾去除病理产物的堆积。一方面,通过疏肝健脾和胃、调畅气机,能够有效促进胃肠动力,缓解患者疼痛症状;另一方面,去除痰、湿、热、瘀等邪气,有助于改善胃肠黏膜低度炎症状态。
3 中医调控SCF/c-kit 信号通路干预功能性消化不良机制研究
目前中医治疗FD取得一定进展,临床疗效确切。研究表明,中药复方、单味药及提取物及针灸等传统方式能够调控SCF/c-kit信号通路,干预ICC增殖分化,维持ICC表型和生长发育,从而恢复ICC起搏功能,促进胃肠动力。
3.1 中药复方
中药复方的多成分特性赋予其治疗作用多样性的特点,目前,中医药治疗的靶向作用研究繁多,其中,以分子信号通路为切入点阐明中医药的作用机制是目前的主要研究方式。多项研究认为SCF/c-kit信号通路调控ICC结构和数目的变化是FD发病的重要病理生理学基础,中医药在干预SCF/c-kit信号通路治疗FD方面取得了一定的进展。王立等[25]利用胃肠舒泰颗粒治疗肝郁脾虚气滞型FD模型大鼠,发现中药组大鼠胃窦组织SCF、c-kit表达升高,表明胃肠舒泰颗粒能够调控SCF/c-kit信号通路,介导ICC分化增殖过程,从而促进胃肠动力。和胃理气方是王垂杰教授临床治疗FD的经验方剂,基础研究发现该方能够促进胃肠动力,姜巍等[26]给予治疗组和胃理气方,通过免疫组织化学实验发现,c-kit、SCF阳性细胞光密度值升高,胃排空和小肠推进率显著增加,表明和胃理气方能够调节SCF/c-kit系统相关因子影响胃肠运动。高颖等[27]纳入142例脾虚气滞证FD患者,经安胃一号治疗后,临床总有效率达81.4%,乏力、恶心呕吐、排便无力等症状显著减轻,且患者血清中胃动素、SCF水平显著升高,显著优于对照组。王敏等[28]基于对疏肝和胃方的实验研究发现,该方可明显改善肝郁脾虚型FD大鼠的精神行为不适症状,并通过免疫组化法检测大鼠胃窦区c-kit及SCF表达,结果显示中药组表现出与促胃肠动力相同的效应,均能升高c-kit和SCF表达及下调ICC凋亡率,从而改善胃肠动力。柴胡疏肝散是临床治疗FD的经典名方,邓静等[29]运用此方,通过比较各组大鼠胃窦组织ICC超微结构及SCF、c-kit表达水平,发现中药低、中、高剂量组ICC内细胞器及结构较模型组完整,并推测其机制与柴胡疏肝散调控SCF/c-kit通路有关。连俊兰等[30]通过调中汤干预脾虚肝旺型FD 幼鼠后,发现调中汤能显著升高血清SCF含量,从而恢复胃肠道内ICC数目及结构,改善胃肠功能紊乱。周恒等[31]基于舒胃汤的研究发现,该方能够提高SCF 表达,促进ICC再生和网络样结构修复,从而恢复胆碱能神经-ICC-平滑肌细胞(SMC)网络结构。朱贞敏等[32]发现,加味肾气丸可纠正大鼠SCF/c-kit信号通路的负向作用引起的ICC 数量减少,进而促进胃肠道活动。孔梦梦等[33]研究发现黄芪建中汤可上调SCF/c-kit途径相关蛋白表达量,以恢复ICC变性及网络结构受损。系列研究可见,中药复方治疗FD临床疗效显著,用药局限性较小,并具有靶向调节SCF/c-kit 通路,修复ICC结构的作用,对于恢复FD发展过程中造成的肠神经系统(ENS)-ICC-SMC网络受损,具有积极意义。
3.2 单味药及成分
目前,单味药及其成分干预SCF/c-kit通路的研究较少,研究方向多涉及理气药厚朴、枳实、白术、姜黄及相关成分(厚朴酚、白术内酯-1、姜黄素),其机制与促进胃肠动力有关,与中医“气机失调致病”理论相吻合。单味药及其成分药的组成较中药复方单一,在体内的作用途径相对明确,是研究中药作用机制和靶向调控作用的重要路径之一。
厚朴酚是从厚朴中提取出的疏水性烯丙基联苯酚类化合物,具有抗炎、抗氧化应激等作用[34]。王振奋等[35]发现厚朴酚能够显著改善FD小鼠食欲及活动状态,通过ELISA检测血清中胃肠激素,结果表明厚朴酚组胃肠激素含量显著升高,具有明显促胃肠动力效应,并提出该效应与SCF/c-kit通路相关。Miao等[36]指出厚朴酚的干预机制与调节该通路上下游相关因子的表达状态,从而改善ICC结构和数目有关。王红阳[37]通过对岭南特色炮制饮片制枳壳的研究发现,制枳壳能显著提高FD大鼠血浆中胃动素和脑肠肽含量,协同调节胃肠动力,并从分子层面揭示制枳壳改善胃肠动力的机制与增加c-kit、SCF表达水平,修复ICC的超微形态和网络结构密切相关。枳实是临床治疗FD的常用药物,其功效为破气消积、化痰散痞。研究发现,枳实改善胃肠功能紊乱的机制与厚朴相似,通过改善SCF/c-kit通路活化引起的ICC形态结构异常发挥生物学效应[38]。同时,枳实水煎液可降低血清IL-6水平,改善炎症刺激胃肠道神经元引起的上腹部疼痛等症状[39]。Li等[6]发现白术内酯-1能够改善胃轻瘫大鼠胃肠动力,可能与其激活SCF/c-kit信号通路调节氧化应激反应,并抑制ICC 凋亡有关。白术破壁饮片可升高SCF、c-kit蛋白含量,诱导ICC发育,改善胃肠电慢波节律,并调节神经递质释放,促进胃肠排空[40]。Jin等[41]研究表明,姜黄素可通过调控SCF/c-kit信号通路恢复ICC表型和可塑性,并阻断氧化应激、抑制NF-κB活化水平,发挥保护ICC的效应。黄芪甲苷可增加胃固有肌层中c-kit蛋白表达水平,促进恢复ICC梭状形态及数量[42]。上述单味药及提取物为临床治疗FD常用药,以理气药为主,具有激活SCF/c-kit 通路、促进ICC结构修复效应,部分研究发现单味药对炎症及神经症状亦有改善。
3.3 针灸疗法
针灸作为传统的中医特色治疗手段,临床应用广泛,具有“简便验廉”的特点。目前,针灸作用于人体的效应机制逐渐被深入挖掘,针灸的靶向治疗作用同样是研究的重点。针灸治疗FD常用腧穴有足三里、太冲及背俞穴等。王计雨等[43]采用夹尾刺激+不规则喂养+冰生理盐水灌胃的复合多因素方法制备FD大鼠模型,电针刺激模型大鼠“足三里”后,ICC超微结构趋于正常化,且电针组中SCF和c-kit mRNA表达升高,表明电针刺激“足三里”可调控SCF/c-kit信号通路,从而修复ICC网络功能,调节胃肠动力。陈峭等[44]结合“以俞调枢”理论,通过针刺足太阳膀胱经背俞穴发现,针刺不仅能够靶向调控SCF/c-kit通路,升高该通路相关因子蛋白和mRNA表达,还能显著增加模型胃排空和小肠推进率,降低胃内残留物。缝隙连接蛋白43(Cx43)是ICC与SMC相互沟通的桥梁,ICC中的电偶联将兴奋性或抑制性信号通过缝隙连接蛋白传入SMC,刺激SMC舒缩,产生持续性动力。张晓明等[45]研究发现,电针刺激“后三里”“太冲”能明显促进大鼠胃肠动力,其机制可能与有效地增加胃窦组织中SCF、c-kit 和Cx43 蛋白表达有关,SCF/c-kit 通路的异常激活是ICC结构和数目减少,引起胃肠动力障碍的直接诱因。韩永丽等[46]研究发现,艾灸“足三里”能调节细胞间质内通讯,并刺激经络信息传导效应,发挥增殖活化ICC作用,其机制可能与艾灸调控SCF/c-kit通路,增加ICC/Cx43、SCF蛋白表达密切相关。胡舒宁等[47]将针刺与艾灸“足三里”进行对照,得到相似结论,且2种疗法的作用效果相似。潘小丽等[48]发现miR-221-3p具有负向调节c-kit的作用,通过电针刺激“足三里”和“太冲”能够抑制miR-221-3p的靶向调节作用,激活SCF/c-kit和加速纤维肉瘤蛋白(Raf)/细胞外信号调节激酶(ERK)信号通路,促进ICC增殖和Cx43表达,从而增强ICC内部及与SMC之间的信息交流。
4 不足与展望
综上所述,中医在改善患者临床症状和恢复组织病理改变方面的优势显著。随着中医药现代化的发展,中医对FD的认知更为深刻,并借助现代科学技术平台,结合现代医学理论,挖掘中医方剂、单味药成分及针灸的治疗机制,使中医体系更加科学化。中医疗法不仅可有效改善患者临床症状,而且可促进胃肠动力、改善十二指肠炎症及恢复内脏敏感性等,其机制可能与干预SCF/c-kit信号通路密切相关。
胃肠动力障碍是FD发生的病理学基础,但并非唯一机制,胃肠动力受神经、免疫和微炎症等多种因素影响,因此,相关细胞(ICC、NC、MC)的功能正常是维持胃肠动力的关键,研究发现,SCF/c-kit通路可通过调控ICC、NC、MC内相关因子及信号通路传导(TRPV1、SP、NK1;PLCβ-IP3、PI3K/AKT、RAS/ERK、JAK/STAT;NF-κB、TNF-α、IL-1β/6等)和形态结构变化,促进胃肠动力,恢复内脏敏感性,减少炎症损伤。
目前,中医疗法干预SCF/c-kit通路作用的靶向细胞研究尚有局限性,多项研究聚焦于调控ICC,以胃肠动力的起搏细胞为切入点,忽略了FD发生中ICC、NC和MC的协同作用。通过SCF/c-kit通路调控NC、MC治疗FD 的研究尚无报道,我们推测NC、MC 也是SCF/c-kit通路的靶向细胞,在FD的发生发展中具有重要的病理生理学意义,亟待今后的研究论证,其中涉及的靶向细胞及分子信号通路可为后续研究提供新的思路。

