卡瑞利珠单抗联合化疗对D-TACE后病情进展肝癌患者的效果
徐秋平
【摘要】 目的:研究卡瑞利珠單抗与化疗联用对经载药微球-肝动脉化疗栓塞(D-TACE)后病情恶化肝癌患者的效果,以期为该类患者提供安全有效的治疗方案。方法:选取2020年1月-2022年1月丰城市人民医院接收的94例经D-TACE后病情恶化肝癌患者。以单双数字法将其分作单抗组47例及化疗组47例。化疗组开展单纯化疗,单抗组则在化疗的基础上增用卡瑞利珠单抗治疗。分析两组临床疗效、肝功能、血清肿瘤标志物水平及不良反应。结果:在疾病控制率(DCR)方面对比,单抗组高于化疗组(78.72% vs. 57.45%)(P<0.05)。治疗后在丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、总胆红素(TBIL)水平方面对比,单抗组均低于化疗组(P<0.05)。治疗后在甲胎蛋白(AFP)、α-L-岩藻糖苷酶(AFU)、癌胚抗原(CEA)水平方面对比,单抗组均低于化疗组(P<0.05)。两组不良反应发生率比较,差异均无统计学意义(P>0.05)。结论:卡瑞利珠单抗联合化疗可提高D-TACE后进展的肝癌患者临床疗效,具有一定安全性,应用价值良好。
【关键词】 肝癌 载药微球-肝动脉化疗栓塞 卡瑞利珠单抗
Effect of Carrilizumab Combined with Chemotherapy on Patients with Advanced Liver Cancer after D-TACE/XU Qiuping. //Medical Innovation of China, 2023, 20(12): 0-046
[Abstract] Objective: To study the effect of Carrelizumab combined with chemotherapy on liver cancer patients with worsening disease after drug-loaded microspheres-transcatheter arterial chemoembolization (D-TACE), so as to provide a safe and effective treatment plan for these patients. Method: A total of 94 patients with liver cancer whose condition worsened after D-TACE in Fengcheng People's Hospital from January 2020 to January 2022 were selected, they were divided into monoclonal antibody group (47 cases) and chemotherapy group (47 cases) by single and even number method. The chemotherapy group was treated with chemotherapy alone, and the monoclonal antibody group was treated with Carrelizumab on the basis of chemotherapy. The clinical efficacy, liver function and serum tumor markers and adverse reactions between the two groups were compared. Result: The disease control rate (DCR) in the monoclonal antibody group was higher than that in the chemotherapy group (78.72% vs. 57.45%) (P<0.05). Alanine aminotransferase (ALT), aspartate aminotransferase (AST) and total bilirubin (TBIL) levels after treatment were compared, those in the monoclonal antibody group were lower than those in the chemotherapy group (P<0.05). Alpha fetal protein (AFP), α-L-fucosidase (AFU), and carcino-embryonic antigen (CEA) levels after treatment were compared, those in the monoclonal antibody group were lower than those in the chemotherapy group (P<0.05). There was no significant difference in the incidence of adverse reactions between the two groups (P>0.05). Conclusion: Carrelizumab combined with chemotherapy can improve the clinical efficacy of patients with advanced liver cancer after D-TACE, with certain safety and good application value.
[Key words] Liver cancer Drug-loaded microspheres-transcatheter arterial chemoembolization Carrelizumab
First-author's address: Fengcheng People's Hospital, Jiangxi Province, Fengcheng 331100, China
doi:10.3969/j.issn.1674-4985.2023.12.011
肝癌呈全球高发特点,亦是癌因性死亡的重要原因,因其发病隐匿性极强,患者往往首次确诊便已处于进展期,无法通过手术根治,5年生存率较低[1]。载药微球-肝动脉化疗栓塞(drug-loaded microspheres-transcatheter arterial chemoembolization,D-TACE)是当前临床用以治疗肝癌的可靠手段之一,其治疗效果及安全性得到有关研究报道证实[2]。然而,实际工作中发现有部分肝癌患者经D-TACE治疗后病情仍无法获得有效控制,为了控制肿瘤持续恶化,分子靶向药物及免疫检查点抑制剂开始受到广泛关注[3]。其中卡瑞利珠单抗作为国产抗癌制剂,其主要作用机制可能与调控程序性死亡受体表达有关,目前已有研究发现其应用于肝癌中的效果显著[4-5],但对D-TACE后进展肝癌患者的作用研究鲜有报道。鉴于此,本文通过研究卡瑞利珠单抗联合化疗在D-TACE后进展的肝癌患者中的应用效果并予以分析,以期为D-TACE后进展的肝癌患者提供一种行之有效的治疗方案,现报道如下。
1 资料与方法
1.1 一般资料 选取2020年1月-2022年1月丰城市人民医院接收的94例经D-TACE后病情恶化的肝癌患者。纳入标准:(1)受试者均有明确的肝癌病理诊断结果;(2)接受≥2次D-TACE治疗后疾病进展;(3)可耐受靶向及免疫治疗;(4)均为成年人。排除标准:(1)其他脏器功能出现异常;(2)合并重大感染;(3)伴有其他恶性肿瘤;(4)既往有靶向或/和免疫治疗史;(5)药物过敏。以单双数字法将患者分作单抗组47例及化疗组47例。入组人员均已签同意书,医院医学伦理委员会批准本研究。
1.2 方法 (1)治疗方案:化疗组开展单纯化疗,药物选用阿帕替尼(生产厂家:江苏恒瑞医药股份有限公司,批准文号:国药准字H20140104,规格:0.375 g),口服给药,1片/次,1次/d,并以患者不良反应发生情况为根据适当调整剂量和用药间隔时长。单抗组则在化疗的基础上增用卡瑞利珠单抗(生产厂家:苏州盛迪亚生物医药有限公司,批准文号:国药准字S20190027,规格:200 mg/瓶)治疗,剂量3 mg/kg,静脉给药,2周1次。两组均连续治疗直至疾病进展或不良反应无法耐受。
1.3 观察指标及判定标准 分析两组临床疗效、肝功能指标、血清肿瘤标志物水平及不良反应等方面的差异。(1)临床疗效的判定参照文献[6]完成,完全缓解(complete response,CR):治疗后未发现病灶,且持续时长不低于4周;部分缓解(partial remission,PR):病灶体积缩小30%以上,且在4周内无新发病灶;稳定(stable disease,SD):病灶体积缩小不超过30%,或增大不超过20%,且在4周内无新发病灶;进展(progress disease,PD):未达上述标准。疾病控制率(disease control rate,DCR)=(总例数-PD例数)/总例数×100%。(2)治疗前后抽取患者空腹静脉血5 mL,离心处理获取血清置于-70 ℃冰箱备用。离心参数:半径10 cm,速度3 000 r/min,时间10 min。肝功能指标包括丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、总胆红素(total bilirubin,TBIL)。检测方式选用蛋白芯片-化学发光法,操作以试剂盒说明书为准,有关试剂盒选用三诺生物传感股份有限公司产品。肿瘤标志物包括甲胎蛋白(alpha fetal protein,AFP)、α-L-岩藻糖苷酶(α-L-fucosidase,AFU)、癌胚抗原(carcino-embryonic antigen,CEA)。其中AFP与CEA均选用雅培i2000化学发光分析仪实施检测,AFU则以速率法完成检测。(3)不良反应包括发热、手足综合征、白细胞减少、胃肠道不适。
1.4 统计学处理 以SPSS 24.0软件分析数据,疗效及不良反应均采用率(%)表示,比较采用字2检验;肝功能指标与肿瘤标志物水平均采用(x±s)表示,比较采用t检验。P<0.05表示差异有统计学意义。
2 结果
2.1 两组一般资料比较 单抗组男27例,女20例;年龄41~68岁,平均(55.12±4.71)岁;TNM分期:Ⅲ期31例,Ⅳ期16例;病灶部位:左叶14例,右葉21例,双叶12例。化疗组男28例,女19例;年龄39~69岁,平均(55.24±4.76)岁;TNM分期:Ⅲ期33例,Ⅳ期14例;病灶部位:左叶15例,右叶22例,双叶10例。两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
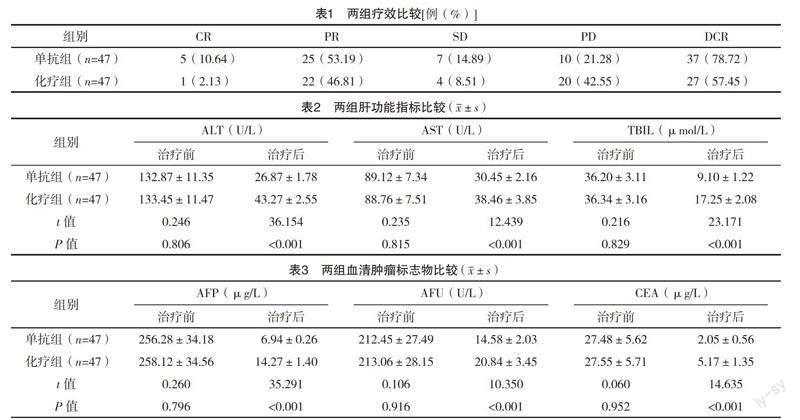
2.2 两组疗效比较 单抗组DCR高于化疗组(字2=4.896,P=0.027),见表1。
2.3 两组肝功能指标比较 治疗前,两组ALT、AST、TBIL比较,差异均无统计学意义(P>0.05);治疗后,单抗组ALT、AST、TBIL均低于化疗组(P<0.05)。见表2。
2.4 两组血清肿瘤标志物比较 治疗前,两组AFP、AFU、CEA比较,差异均无统计学意义(P>0.05);治疗后,单抗组AFP、AFU、CEA均低于化疗组(P<0.05)。见表3。
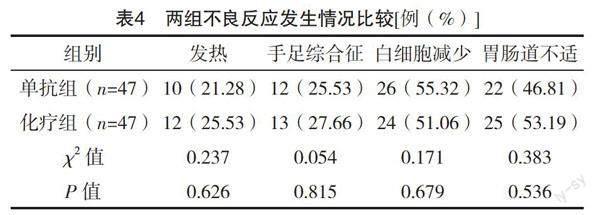
2.5 两组不良反应发生情况比较 两组发热、手足综合征、白细胞减少、胃肠道不适发生率比较,差异均无统计学意义(P>0.05),见表4。
3 讨论
肝动脉化疗栓塞(TACE)是目前国内用以治疗无法手术切除肝癌患者的首选方案,其中载药微球可实现对肿瘤血管的彻底、长期栓塞,并通过长期缓慢释放药物,提升病灶内药物浓度,从而实现对肿瘤细胞的长期灭杀[7-8]。因此,D-TACE在临床上的应用价值相较于传统TACE有一定优越性,可作为TACE治疗不佳的有效弥补手段[9-10]。然而,仍有肝癌患者尽管接受D-TACE治疗,病情控制效果并不理想,甚至复发或远处转移,对患者预后造成不利影响[11-12]。故此,寻找一种积极可靠的治疗手段,对改善经D-TACE治疗后进展肝癌患者的预后具有积极意义,更是当前国内外广大医务工作者共同关注的热点。卡瑞利珠单抗是中国自主研发的一种程序性死亡受体-1(programmed death receptor-1,PD-1)抑制剂,已有研究报道证实,该药应用于原发性肝癌患者中的效果显著,且有效延长患者生存期[13-14]。若研究证实经D-TACE治疗后进展肝癌患者可从该药中获益,可为广大患者带来福音。
本研究结果显示,在DCR方面对比,单抗组高于化疗组。其中国内一项临床研究发现,卡瑞丽珠单抗与阿帕替尼联用治疗中晚期肝癌患者的DCR为93.8%,显著高于单药组[15]。这为本研究结果提供了强有力的佐证。与此同时,在治疗后ALT、AST及TBIL水平方面对比,单抗组均低于化疗组。这充分证实了卡瑞利珠单抗联合化疗可提高D-TACE后进展的肝癌患者的临床疗效,促进肝功能的改善。究其原因,卡瑞利珠单抗通过和相关受体结合,从而实现对机体免疫功能的增强[16]。而阿帕替尼具有促进肿瘤血管恢复正常的作用,从而调控肿瘤微环境的免疫抑制情况,加强卡瑞利珠单抗的作用效果,进一步提高病灶对D-TACE的应答[17]。此外,在治疗后血清AFP、AFU及CEA水平方面对比,单抗组均低于化疗组。其中AFP与AFU均是临床上用以评估肝癌的重要标志物,对肝癌治疗效果的监测具有一定作用;CEA作为肿瘤标志物,在多种恶性肿瘤中均存在异常表达,而在肝癌患者中存在异常高表达,可提示病情严重程度及预后状况。上述结果更加证明了单抗组治疗方案的效果显著。分析原因,卡瑞利珠单抗入体后可直接阻断PD-1和相关配体的结合,调节有关信号通路的活性,促进机体抗肿瘤免疫能力,从而对疾病的控制起到积极促进作用[18-20]。值得注意的是在实施单抗组治疗方案时,需注意加强对患者的保肝治疗及不良反应的干预,针对不良反应控制效果欠佳的患者可考虑减少药物剂量及调整用药间隔时间,以保证安全性。
综上所述,D-TACE后进展的肝癌患者可从卡瑞利珠单抗联合化疗方案中获益,有助于疗效的提高及肝功能恢复,且不会增加不良反应,可能具有良好的应用前景。
参考文献
[1] LI Q J,HE M K,CHEN H W,et al.Hepatic arterial infusion of Oxaliplatin, Fluorouracil, and Leucovorin versus transarterial chemoembolization for large hepatocellular carcinoma: a randomized Phase Ⅲ Trial[J].J Clin Oncol,2022,40(2):150-160.
[2] YUAN P,ZHANG Z,KUAI J.Analysis on efficacy and safety of TACE in combination with RFA and MWA in the treatment of middle and large primary hepatic carcinoma[J].J BUON,2019,24(1):163-170.
[3]王玉峰,何东风.载药微球经导管肝动脉化疗栓塞治疗肝脏恶性肿瘤研究进展[J].解放军医学杂志,2022,47(5):524-532.
[4]方剑,姜仁鸦,汪正飞.CalliSpheres载药微球联合索拉非尼治疗TACE后进展的不可切除肝癌患者中的疗效分析[J].浙江医学,2021,43(14):1555-1558,1588.
[5]邓泽锋,潘丽娟.卡瑞利珠单抗联合仑伐替尼治疗晚期肝癌的临床效果评价[J].中国医学创新,2022,19(9):153-157.
[6] LENCIONI R,LLOVET J M.Modified RECIST (mRECIST) assessment for hepatocellular carcinoma[J].Semin Liver Dis,2010,30(1):52-60.
[7]龚元川,邵国良.载药微球的理化特性及其在肝癌介入治疗中的应用进展[J].介入放射学杂志,2022,31(6):616-622.
[8]顾朋,叶尔麦克·阿哈提,樊喜文.原发性肝癌TACE治疗栓塞剂对疗效和预后影响[J].中华肿瘤防治杂志,2018,25(23):1658-1663.
[9]李红,尹芳,罗贯虹,等.CalliSpheres载药脂微球联合TACE与传统TACE治疗肝癌疗效对比分析[J].胃肠病学和肝病学杂志,2019,28(2):171-174.
[10]张辉,张庆桥,徐浩,等.国产CalliSpheres载药微球治疗原发性肝癌的疗效评价[J].临床放射学杂志,2019,38(3):530-533.
[11]周素军,吴宝林,周军,等.药物缓释微球肝动脉化疗栓塞术治疗中晚期原发性肝癌的近期疗效及安全性分析[J].武汉大学学报(医学版),2019,40(5):742-746.
[12]陈猛,许荣德,胡宝山,等.HepaSphere载药微球栓塞治疗原发性肝癌的近期疗效及安全性[J].肿瘤防治研究,2019,46(7):627-631.
[13]杨秋雨,魏宁,徐浩,等.TACE联合卡瑞利珠单抗治疗中晚期肝癌短期疗效及疗效相关性分析[J].医学影像学杂志,2021,31(7):1212-1219.
[14]滕颖,丁晓燕,李文东,等.程序性细胞死亡受体1抑制剂联合仑伐替尼治疗晚期原发性肝癌的效果及不良反应[J].临床肝胆病杂志,2021,37(3):606-610.
[15] XU J,ZHYANG Y,JIA R,et al.Anti-PD-1 antibody SHR-1210 combined with Apatinib for advanced hepatocellular carcinom, gastric, or esohagogastric junction cancer: an open-label,dose escalation and expansion study[J].Clin Cancer Res,2019,25(2):515-523.
[16]朱風婷,曾江正,姜靖雯,等.卡瑞利珠单抗联合射频消融术及FOLFOX方案治疗原发性肝癌疗效研究[J].中国药业,2021,30(15):38-41.
[17]杨荷,陈晓琦,王新亭,等.扶正消瘤颗粒联合卡瑞利珠单抗与阿帕替尼治疗晚期原发性肝癌临床观察[J].中西医结合肝病杂志,2021,31(8):679-682.
[18]徐金发,宋文灿,郑中显,等.国产细胞程序性死亡受体1抑制剂卡瑞利珠单抗联合阿帕替尼一线治疗中晚期原发性肝癌的疗效研究[J].中国全科医学,2022,25(26):3258-3262.
[19]王瑛,袁鹤立,赵利,等.清热利胆自拟方对仑伐替尼联合卡瑞丽珠单抗治疗晚期原发性肝癌患者炎症因子、免疫细胞水平和生活质量的影响[J].现代中西医结合杂志,2021,30(24):2664-2669.
[20]吴婧婧,黄琦.原发性肝细胞癌免疫治疗药物的临床药理研究进展[J].安徽医科大学学报,2021,56(11):1842-1846.
(收稿日期:2022-11-15) (本文编辑:张明澜)

