恩格列净调节AMP依赖蛋白激酶/蛋白激酶B/环磷腺苷效应元件结合蛋白信号通路对肺动脉高压大鼠肺血管重构的影响
童凯 罗红兰
肺动脉高压(PH)也可称为肺高血压,主要特征为肺动脉压异常增高[1]。肺血管重构是PH典型的病理学变化,是PH进行性发展和疗效不理想的重要因素之一[2],因此减轻或改善肺血管重构对治疗PH意义重大。AMP依赖蛋白激酶(AMPK)在调控细胞能量代谢过程中具有重要作用[3]。蛋白激酶B(AKT)参与细胞生长、增殖、代谢、转录等多种功能的调控[4]。研究发现在肺组织平滑肌细胞中环磷腺苷效应元件结合蛋白(CREB)的缺失会引起PH发生发展,而AMPK和AKT是CREB的上游蛋白,磷酸化AMPK(p-AMPK)和p-AKT能够促进磷酸化CREB(p-CREB)蛋白表达水平升高,减少CREB缺失,发挥维持血管稳态的转录功能[5]。恩格列净目前临床主要用于糖尿病治疗,但有研究发现其对改善PH、败血症引起的急性肾损伤、心力衰竭等疾病也有一定效果[6]。本研究旨在探究恩格列净对PH大鼠肺血管重构的影响及可能机制。
材料与方法
1.材料:SPF级雄性SD大鼠60只,体质量(200±20)g,6周龄,购于常州卡文斯实验动物有限公司,许可证号:SCXK(苏)2016-0010。恩格列净购于康德乐大药房(国药准字J20171073);AMPK抑制剂Compound C购于美国Med Chem Express公司;HE染色试剂盒购于上海吉至生化科技有限公司;大鼠低氧诱导因子(HIF)-1α ELISA试剂盒购于无锡云萃生物科技有限公司;大鼠内皮素(ET)-1 ELISA试剂盒购于上海酶研生物科技有限公司;一抗及二抗均购于Cell Signaling Technology。ZF-258凝胶成像分析系统购于上海嘉鹏科技有限公司;Power Lab系统购于澳大利亚AD仪器有限公司。
2.方法
(1)分组及PH模型构建:将60只大鼠随机分为对照组、PH组、恩格列净低、中、高剂量组及恩格列净+Compound C组,每组各10只。除对照组外,其余5组均低氧处理:在大鼠饲养仓注入氮气以维持低氧状态(氧气浓度维持在10%±0.5%、每天8 h),持续3周、每周6 d,以构建PH模型[7]。大鼠在低氧处理前1周,先进行药物处理。恩格列净低、中、高剂量组分别以7.5 mg/kg、15.0 mg/kg、30.0 mg/kg恩格列净灌胃[8],恩格列净+Compound C组以30 mg/kg恩格列净灌胃同时腹腔注射10 mg/kg Compound C,对照组和PH组予同体积生理盐水灌胃,6组大鼠均每天1次,连续4周。
(2)大鼠平均肺动脉压(mPAP)和右心室肥厚指数(RVHI)检测:通过右心导管插入肺动脉测量大鼠mPAP。实验结束后,采用戊巴比妥钠腹腔注射麻醉大鼠,分离颈部血管,将连接压力传感器的聚乙烯导管经右颈外静脉,穿过右心房、右心室,插入至肺动脉,当Power lab系统的监视器上显示压力波形时,记录右心室收缩压和肺动脉压(包括收缩压和舒张压),计算mPAP。mPAP(mmHg)=1/3×肺动脉收缩压(mmHg)+2/3×肺动脉舒张压(mmHg)。上述操作完成后摘取大鼠眼球取血,离心后取血清,置于-20 ℃冰箱保存。随后处死大鼠,分别剪去右心室(RV)、左心室(LV)和室间隔(S),称量并记录,计算RVHI。RVHI(μg/mg)=RV重量(μg)/[LV重量(mg)+S重量(mg)]。
(3)大鼠肺小动脉组织病理学变化观察:将大鼠肺组织取出放置冰上,取部分肺动脉组织置于多聚甲醛固定24 h,剩余肺动脉组织置于-80 ℃冰箱保存备用。24 h后取出固定的肺动脉组织,经脱水、石蜡包埋后切片、HE染色,在光学显微镜下观察,选取6条外径﹤50 μm的肺小动脉,分别测量血管总面积(TA)、管腔面积(IA)、血管外径(ED)及管壁厚度(WT),并计算肺血管重构指标:肺小动脉管壁面积在血管总面积中的占比(WA%)=[TA(μm2)-IA(μm2)]/TA(μm2)×100%,肺小动脉管壁厚度在血管外径中的占比(WT%)=[WT(μm)/ED(μm)]×100%。
(4)大鼠血清HIF-1α、ET-1水平及肺动脉组织AMPK/AKT/CREB信号通路相关蛋白表达水平检测:取冻存血清解冻后,采用ELISA试剂盒检测HIF-1α、ET-1水平。取冻存肺动脉组织,于液氮中研磨并制备匀浆,分别使用放射免疫沉淀分析(RIPA)试剂盒和二辛可宁酸(BCA)试剂盒提取总蛋白并检测蛋白水平。通过十二烷基硫酸钠(SDS)-聚丙烯酰胺(PAGE)凝胶电泳后,半干转印至聚偏氟乙烯(PVDF)膜上;使用5%脱脂奶粉封闭1 h;分别加入一抗(1∶1 000),4 ℃孵育过夜;加入二抗(1∶5 000),室温孵育1 h;采用化学发光法显色、Tanon软件处理图像并进行半定量分析。
结 果
1.6组大鼠mPAP及RVHI比较:6组大鼠mPAP及RVHI比较差异均有统计学意义(P<0.001)。PH组大鼠mPAP及RVHI均明显高于对照组;恩格列净低、中、高剂量组及PH组mPAP和RVHI均依次降低;恩格列净+Compound C大鼠组mPAP及RVHI均明显高于恩格列净高剂量组(P<0.05)。见表1。
2.6组大鼠肺小动脉组织病理学变化比较:对照组大鼠肺小动脉管腔面积大,管壁较薄;与对照组比较,PH组大鼠肺小动脉管腔明显变小,管壁明显增厚;与PH组比较,恩格列净低、中、高剂量组及恩格列净+Compound C组大鼠管腔面积和管壁厚度均有改善,且恩格列净高剂量组改善效果较为明显。见图1。
表1 6组大鼠mPAP及RVHI比较
3.6组大鼠肺小动脉WT%及WA%比较:6组大鼠肺小动脉WT%及WA%比较差异均有统计学意义(P<0.001)。PH组大鼠肺小动脉WT%及WA%均明显高于对照组;恩格列净低、中、高剂量组及PH组大鼠肺小动脉WA%和WA%均依次降低;恩格列净+Compound C组大鼠肺小动脉WT%及WA%均明显高于恩格列净高剂量组(P<0.05)。见表2。
表2 6组大鼠肺小动脉WT%及WA%比较
4.6组大鼠血清HIF-1α及ET-1水平比较:6组大鼠血清HIF-1α及ET-1水平比较差异均有统计学意义(P<0.001)。PH组大鼠血清HIF-1α及ET-1水平均明显高于对照组;恩格列净低、中、高剂量组及PH组大鼠HIF-1α、ET-1水平均依次降低;恩格列净+Compound C组大鼠血清HIF-1α及ET-1水平均明显高于恩格列净高剂量组(P<0.05)。见表3。
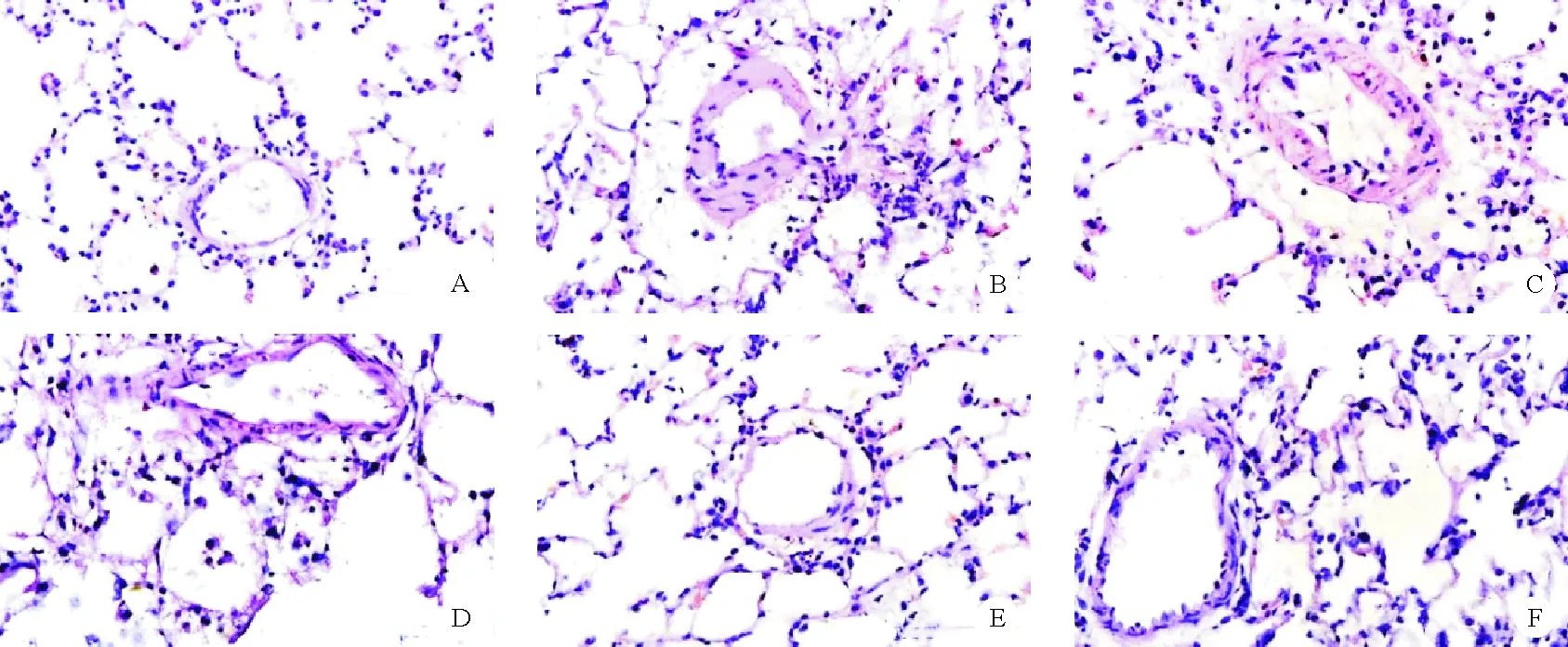
图1 6组大鼠肺小动脉组织病理学变化(A:对照组;B:PH组;C:恩格列净低剂量组;D:恩格列净中剂量组;E:恩格列净高剂量组;F:恩格列净+Compound C组,HE染色,×200)
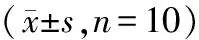
表3 6组大鼠血清HIF-1α及ET-1水平比较
5.6组大鼠肺动脉组织AMPK/AKT/CREB信号通路相关蛋白表达水平比较:6组大鼠肺动脉组织AMPK/AKT/CREB信号通路相关蛋白表达水平比较均有统计学意义(P<0.001)。PH组大鼠肺动脉组织p-AMPK/AMPK、p-AKT/AKT、p-CREB/CREB表达水平均明显低于对照组;恩格列净低、中、高剂量组及PH组大鼠肺动脉组织p-AMPK/AMPK、p-AKT/AKT、p-CREB/CREB表达水平均依次升高;恩格列净+Compound C组大鼠肺动脉组织p-AMPK/AMPK、p-AKT/AKT、p-CREB/CREB表达水平均明显低于恩格列净高剂量组(P<0.05)。见表4。
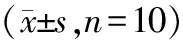
表4 6组大鼠肺动脉组织AMPK/AKT/CREB信号通路相关蛋白表达水平比较
讨 论
缓解肺血管重构是治疗PH的重要方法之一,可通过调节肺血管阻力,改善肺动脉顺应性实现[9]。WT%和WA%是肺血管重构的两个衡量标准[10]。本研究结果显示,PH组大鼠mPAP、PVHI及肺小动脉WA%、WT%均明显升高,表明大鼠出现PH病理学改变,且血管平滑肌细胞增殖引起了血管重构。与PH组比较,恩格列净低、中、高剂量组大鼠mPAP、PVHI及肺小动脉WA%、WT%均依次降低,提示恩格列净具有缓解肺血管重构、减轻右心室肥厚的效果,可能通过抑制平滑肌细胞增殖、减轻肺动脉压发挥作用。HE染色结果显示,恩格列净能够改善大鼠肺小动脉管壁增厚、管腔面积减小等,与上述研究结果一致,再次提示恩格列净可改善肺血管重构。
HIF-1α是包括α、β两个亚单位的一种异源二聚体,能够促进肺血管重构,引起肺动脉压持续提高,推动PH发生发展[11]。ET-1具有较强的血管收缩功效,是引起PH的重要原因之一[12]。本研究中PH组大鼠血清HIF-1α及ET-1水平均明显升高,而与PH组比较,恩格列净低、中、高剂量组大鼠血清HIF-1α及ET-1水平均依次降低,提示恩格列净可能通过降低血清HIF-1α及ET-1水平缓解肺血管重构,进而减轻PH。
PH的主要特征之一是肺血管重构,肺血管重构主要由外周阻力引起,由整个肺循环阻力发展到一定程度造成[13]。在肺血管重构过程中,血管壁细胞结构和功能发生改变,如内侧平滑肌细胞增殖和肥大、细胞外基质增生,进而导致血管壁增厚,血管扩张性降低,此外外侧成纤维细胞增殖也会引起管腔变窄等现象[14]。研究发现CREB能够调控平滑肌细胞增殖并影响巨噬细胞募集,在维持血管正常内稳态方面发挥关键作用,CREB减少或表达降低是造成肺组织血管重塑的一个重要因素[5]。AMPK和AKT是CREB的上游蛋白,能够促进CREB活化[15]。有研究报道,恩格列净能够激活AMPK,引起CREB上游AKT蛋白磷酸化,从而促进CREB磷酸化,上调尿酸转运体ABCG2蛋白表达,减轻高尿酸血症[16]。本研究显示,PH组大鼠肺动脉组织p-AMPK/AMPK、p-AKT/AKT、p-CREB/CREB表达水平均明显降低,而与PH组比较,恩格列净低、中、高剂量组大鼠肺动脉组织p-AMPK/AMPK、p-AKT/AKT、p-CREB/CREB表达水平均依次升高,提示恩格列净可能通过提高AMPK、AKT及CREB磷酸化蛋白表达水平发挥维持血管内稳态的作用,缓解肺血管重构。此外,AMPK抑制剂Compound C可逆转恩格列净对PH大鼠肺血管重构的缓解作用,亦验证了上述推测。
综上,恩格列净可减轻PH大鼠肺血管重构,其机制可能通过提高AMPK、AKT及CREB磷酸化蛋白表达水平,减轻血管壁增厚。此外,恩格列净也可降低PH大鼠血清HIF-1α及ET-1水平,缓解PH,从而发挥对肺血管重构的保护作用。但本研究未进行体外实验,未能从细胞层面验证恩格列净的作用,后期我们将通过分离培养原代肺动脉平滑肌细胞,观察恩格列净对缺氧处理的肺动脉平滑肌细胞增殖和AMPK/AKT/CREB信号通路的影响,进一步证实本研究结论。

