氨磷汀与17种静脉用药物在模拟Y型输液通路中物理相容性
王梦琳,鞠营辉,吴 睿,朱高超,徐先进,朱 岳,刘 圣,2*
0 引言
氨磷汀(Amifostine)是一种有机硫化磷化合物,在体内经碱性磷酸酶水解脱磷酸,转化成具有活性的代谢产物WR-1065,通过清除自由基产生细胞保护作用[1]。由于碱性磷酸酶在正常组织中的表达远高于肿瘤组织,因此,氨磷汀在有效减轻放疗或细胞毒药物对正常组织毒性作用的同时并不减弱抗肿瘤作用,是目前抗肿瘤治疗常用的辅助药物之一[2]。
肿瘤患者放、化疗前静脉使用氨磷汀能降低细胞毒性药物引起的肾毒性、神经毒性等不良反应,减轻放疗引起的组织损伤,增加患者放疗耐受性[3-5]。肿瘤患者治疗过程常伴有胃肠道反应、肝肾损伤、骨髓抑制等[4,6],本品用药前可能同时联合静脉给予地塞米松、5-HT3受体拮抗剂等药物,联合用药常为序贯给药或另行开通输液通道,增加用药时间或穿刺次数,增加患者用药痛苦,降低患者用药依从性。考察氨磷汀与临床常用静脉用药物通过Y型输液器混合用药物理相容性,有着重要的临床意义。目前对氨磷汀配伍研究仍停留在1995年该药批准上市前Trissel等[7]对以5%葡萄糖注射液为溶媒调配的氨磷汀与100种静脉药物的配伍研究,而国内尚缺乏氨磷汀与其他药物配伍的相关研究报道。为了避免氨磷汀与临床常用静脉用药物联合使用过程中发生物理不相容,本研究以0.9%氯化钠为溶媒,模拟Y型静脉输液通路,考察氨磷汀与临床常用静脉用药物在Y型输液通路中的物理相容性,为临床用药提供参考。
1 材料
1.1 试验药品与试剂 注射用氨磷汀(南京绿叶制药有限公司,批号:21060210,规格:0.5 g);注射用奥美拉唑钠(山东罗欣药业有限公司,规格:20 mg,批号:522053102);注射用泮托拉唑钠(扬子江药业集团有限公司,规格:40 mg,批号:22070242);注射用艾司奥美拉唑钠(福安药业集团湖北人民制药有限公司,规格:40 mg,批号:20210729);西咪替丁注射液(山东鲁抗医药股份有限责任公司,规格:0.2 g∶2 ml,批号:21121601):盐酸昂丹司琼注射液(哈尔滨三联药业股份有限公司,规格:8 mg∶4 ml,批号:2202171L);注射用盐酸托烷司琼(哈尔滨三联药业股份有限公司,规格:2 mg,批号:2111032E1);盐酸甲氧氯普胺注射液(河南润弘制药股份有限公司,规格:10 mg∶1 ml,批号:2111242);注射用谷胱甘肽(重庆药友制药有限公司,规格:0.6 g,批号:22230780);地塞米松磷酸钠注射液(辰欣药业股份有限公司,规格:5 mg∶1 ml,批号:2202062211);注射用甲泼尼龙琥珀酸钠(辉瑞制药比利时公司,规格:40 mg,批号:FA4614);利巴韦林注射液(辰欣药业股份有限公司,规格:0.1 g∶1 ml,批号:2202122261);注射用阿昔洛韦(辅仁药业集团有限公司,规格:0.25 g,批号:202203053);硫酸庆大霉素注射液(广州白云山天心制药股份有限公司,规格:80 mg∶2 ml,批号:220263);注射用头孢呋辛钠(广州白云山天心制药股份有限公司,规格:1.5 g,批号:211274);注射用头孢哌酮钠舒巴坦钠(辉瑞制药有限公司,规格:1 g,批号:8138780);注射用哌拉西林钠他唑巴坦钠(山东鲁抗医药股份有限责任公司,规格:2.25 g,批号:41220303);左氧氟沙星氯化钠注射液(浙江医药股份有限公司新昌制药厂,规格:0.5 g∶100 ml,批号:118211032);氯化钠注射液(安徽丰原药业股份有限公司,规格100 ml∶0.9%,批号:3222032301)。
1.2 仪器与设备 E201-C精密酸度计(杭州齐威仪器有限公司),WGZ-20B便携式浊度计(测量范围:0.000~20.000 NTU,上海仪电物理光学仪器有限公司),DL552004B激光笔(波长:650 nm,功率:80~100 mW,宁波得力工具有限公司),BSC-1304ⅡB2生物安全柜(苏州安泰空气技术有限公司),HR-RO/120反渗透纯水机(杭州汇邦净水设备有限公司)。
2 方法与结果
2.1 供试品溶液调配 室温(25 ℃)自然光条件下于洁净环境,在生物安全柜中取注射用氨磷汀,用适量0.9%氯化钠注射液溶解并稀释至浓度为10 mg/ml配伍前药液;注射用奥美拉唑钠、注射用泮托拉唑钠等17种配伍药物根据药品说明书,参照《静脉用药物临床应用指导》[8]配置为配伍前药液。模拟Y型输液通路中的药物配伍,将10 mg/ml的氨磷汀溶液与17种配伍药物溶液按体积比1∶1的比例混合均匀,得到17种配伍液。同时向用0.9%氯化钠注射液调配的10 mg/ml氨磷汀溶液中加入等体积的0.9%氯化钠注射液,混合均匀后设为阴性对照溶液。供试品溶液调配技术参数见表1。
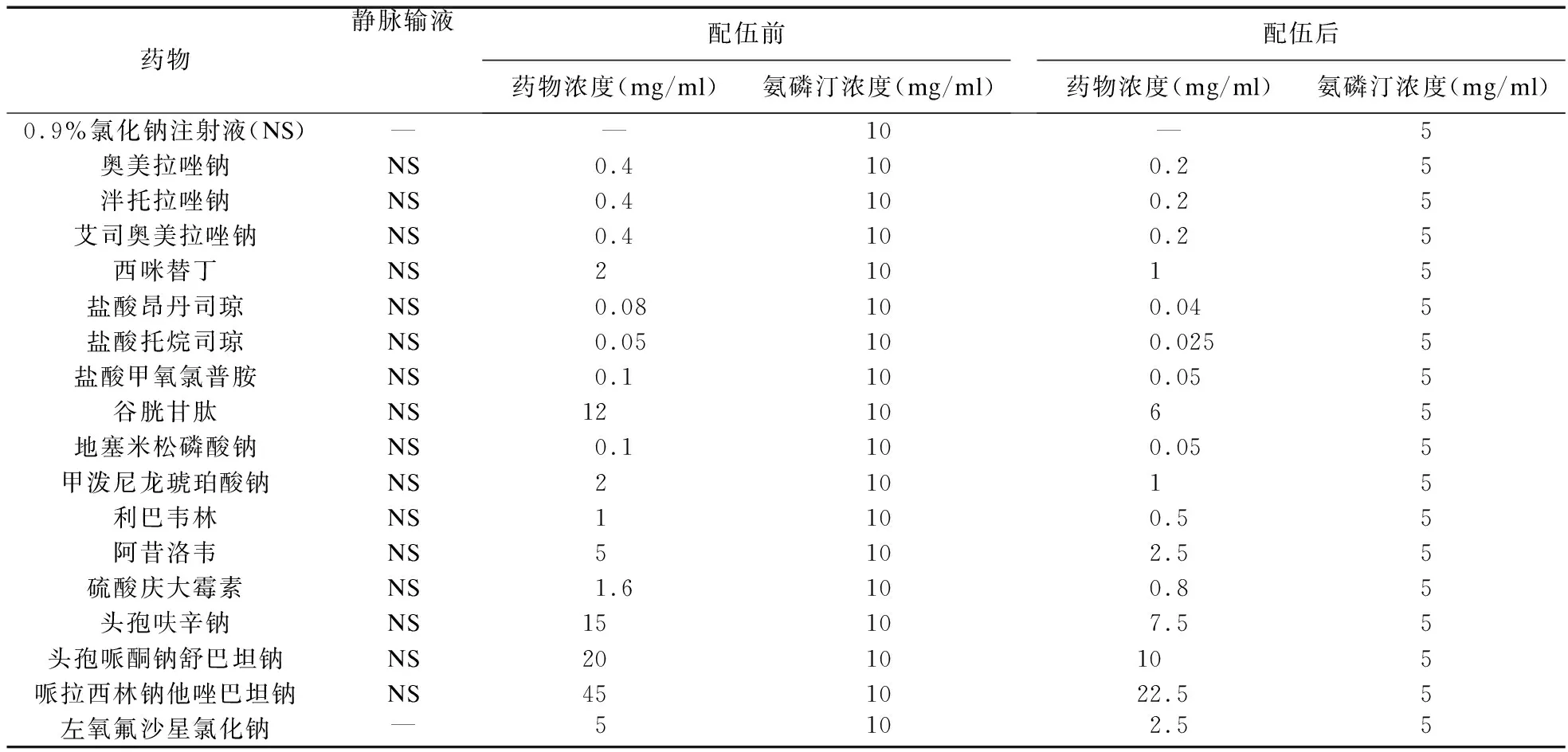
表1 氨磷汀与17种静脉用药物调配技术参数
2.2 性状、丁达尔效应、浊度与pH检测 取“2.1”项下各配伍液置于洁净无色透明玻璃试管中,于配伍液配置后立即(0)、0.5、1、2、4 h,目测其性状,在暗处用红色激光光束照射配伍液检测其丁达尔效应,若在红色激光光束的照射下观察到配伍液中有光路则存在丁达尔效应[9];取配伍液约20 ml置于洁净浊度计样品瓶中,按时间点将样品瓶置于浊度计中检测其浊度,各时间点重复测量3次,取平均值;另取配伍液适量于洁净烧杯中,按时间点将pH计电极插入配伍液中,搅拌使电极与配伍液充分接触,检测配伍液pH值。物理相容性规定:溶液无颜色变化,不产生浑浊、结晶、沉淀或气体,不产生丁达尔效应,浊度与0 h比较增加<0.5 NTU,pH值与0 h比较变化<1,以上任一项不符合规定定义为溶液物理不相容[10-11]。氨磷汀与阿昔洛韦配伍液约15 min浊度增加>0.5 NTU,且产生白色针状结晶,结晶随时间推移增多,见图1;阴性对照溶液及与其他16种静脉用药物配伍液4 h内无颜色改变,未产生浑浊、结晶、沉淀或气体,未产生丁达尔效应,浊度与0 h比较变化均<0.5 NTU,pH与0 h比较变化均<1。氨磷汀与静脉用药物相容性见表2。

图1 氨磷汀与阿昔洛韦配伍液性状图(2×)注:a.阴性对照溶液;b.氨磷汀与阿昔洛韦配伍液。A:0 h;B:15 min;C:0.5 h;D:1 h;E:2 h;F:4 h

表2 Y型输液通路中氨磷汀与静脉用药物的物理相容性
2.3 低浓度氨磷汀与阿昔洛韦物理相容性 参照“2.1”,将注射用氨磷汀调配至浓度为2.5、5.0 mg/ml的配伍前药液,注射用阿昔洛韦调配至浓度为5 mg/ml的配伍前药液。模拟“Y”型输液通路,将上述浓度氨磷汀溶液分别与阿昔洛韦溶液按照体积比1∶1的比例混合均匀,得到不同浓度氨磷汀与阿昔洛韦配伍液,另设0.9%氯化钠注射液与阿昔洛韦溶液按照体积比1∶1的比例混合均匀为阴性对照溶液。参照“2.2”,于配伍液配置后,立即(0 h)、0.5、1、2、4 h,目测性状,检测配伍液丁达尔效应、浊度及pH。5.0 mg/ml氨磷汀与阿昔洛韦配伍液产生白色絮状沉淀(见图2),配伍液4 h内浊度增加>0.5 NTU;2.5 mg/ml氨磷汀与阿昔洛韦配伍液4 h内外观没有明显改变,未观察到丁达尔效应,pH与0 h比较变化<1,浊度与0 h比较增加<0.5 NTU。低浓度氨磷汀与阿昔洛韦物理性状见表3。

图2 低浓度氨磷汀与阿昔洛韦配伍液配伍4 h性状图(2×)注:a.阴性对照溶液;b.2.5 mg/ml氨磷汀与阿昔洛韦配伍液;c.5.0 mg/ml氨磷汀与阿昔洛韦配伍液
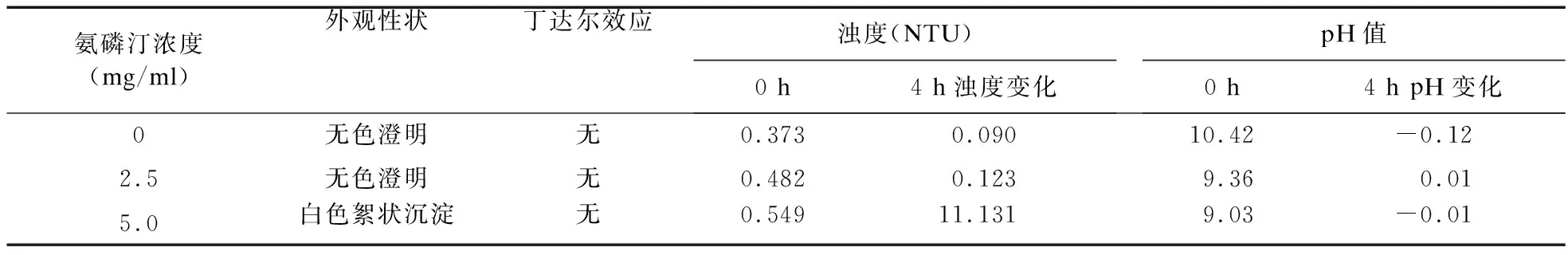
表3 低浓度氨磷汀与阿昔洛韦配伍液物理性状
3 讨论
静脉用药物的物理性质不相容是指药物配伍时产生性状或者物理性质改变,如配伍液颜色改变、浑浊、分层,产生沉淀、气体、丁达尔效应等[10,12]。目前,相关研究常通过观察配伍液外观、丁达尔效应,检测配伍液浊度、pH值变化等考察药物的物理相容性[9,13-14]。
静脉用药物通过Y型输液通路配伍时,由于接触时间较短,国内外学者多通过观察配伍液物理相容性,考察Y型输液通路中的药物相容性[10,14]。药物的溶解度与溶液pH值有关,pH值的变化可能导致药物溶解度降低,因此,检测配伍液pH值是考察药物物理相容性的重要指标[11]。目前,国内外学者多以与配伍液混合后0 h相比pH变化<1[10-11,15]或10%[9,14]作为物理相容的标准。氨磷汀溶液近中性[8],本研究中氨磷汀与17种药物配伍液pH范围在5.55~8.92,多为中性或碱性,故规定配伍液pH与0 h比较变化<1为物理相容。
氨磷汀是第一个上市使用的正常细胞保护剂,应用于临床肿瘤患者放、化疗的辅助治疗[3-5]。本研究参照De Basagoiti、Jiménez-Lozano等[10-11]的实验方法,以0.9%氯化钠为溶媒调配供试药品,将氨磷汀分别与17种静脉用药物按照1∶1的比例混合,模拟临床Y型输液通路中的药物配伍,观察配伍液外观、丁达尔效应、浊度及pH值变化,考察药物物理相容性。结果显示,氨磷汀与阿昔洛韦配伍后产生白色针状结晶,与Trissel等[7]结果相似,提示氨磷汀与阿昔洛韦物理不相容。为了进一步研究氨磷汀与阿昔洛韦的物理相容性,本研究另设低浓度氨磷汀与阿昔洛韦配伍,结果表明,5.0 mg/ml氨磷汀与阿昔洛韦配伍后产生白色絮状沉淀,2.5 mg/ml氨磷汀与阿昔洛韦配伍液未出现明显变化;结合药品说明书及《静脉用药物临床应用指导》[8],氨磷汀临床使用推荐剂量为化疗前500~600 mg/m2或放疗前200~300 mg/m2,单次用量药物溶解稀释于50 ml的0.9%氯化钠注射液中供静脉输注使用,而浓度为2.5 mg/ml的氨磷汀溶液远低于临床使用浓度,因此,在临床实践中,建议两种药物联合使用时,避免通过Y型输液通路同时输注,序贯输注时,应在输注前后用相容性输液冲洗管路。虽然本研究未观察到氨磷汀与其他16种药物的物理不相容,但在临床使用过程中,因药品生产厂家、批号、浓度或溶媒等不同,可能产生不同变化,因此,在通过Y型输液通路联合用药时,仍应密切关注输液管路中有无颜色、沉淀等变化,避免因药物发生物理不相容而产生不良事件,保障患者用药安全。

