戊酸雌二醇片联合克罗米芬对排卵障碍性不孕患者雌激素水平和卵泡发育的影响
李艳美,马 芳,魏红英,李红娟
商丘市第五人民医院微创外科,河南 商丘 476000
排卵障碍性不孕(ODI)是由于受到某些疾病因素的影响,使卵巢的排卵功能受阻,卵子不能正常排出,由此引发不孕[1]。排卵障碍的出现可能会影响女性的月经功能,导致闭经、月经失调等异常现象,严重者甚至可能出现肥胖、多毛,甚至可能引发子宫内膜癌、乳腺癌[2]。临床上一般采用克罗米芬(CC)来治疗ODI患者。但有研究发现[3],单独使用CC 的治疗效果并不理想,通常将其与其他促排卵药物联合给药治疗,以解决ODI患者的排卵以及生育等相关问题。ODI患者体内的雌激素一般处于较低水平。因而需要适量补充雌激素来激活卵泡发育,帮助胚泡着床,从而提高不孕症患者的妊娠率。戊酸雌二醇片(EV)属于的雌激素类药物,能有效治疗卵巢功能障碍、增加子宫内膜厚度,提高妊娠率[4]。因此,本研究观察了接受EV联合CC治疗的ODI患者,以期了解该药物的联合应用对患者雌激素水平和卵泡发育的影响及对该患者排卵率及妊娠率的影响,现将结果报告如下。
1 资料与方法
1.1 一般资料
选取2019年6月—2020年6月商丘市第五人民医院接受治疗的80例ODI患者作为研究对象。纳入标准:(1)符合ODI诊断标准[5]。(2)性生活规律。(3)患者及家属知情同意。(4)双方未采取任何避孕措施。排除标准:(1)子宫肌瘤。(2)子宫畸形。(3)对本研究药物过敏。(4)治疗期间行其他促排卵治疗。(5)配偶生育功能异常。(6)合并肝、肾等功能器官障碍。(7)存在凝血系统障碍。将患者随机分为联合组(n=40)和对照组(n=40)。两组ODI患者的年龄、病程、月经周期等一般资料具有可比性(P>0.05),见表1。本研究经医院医学伦理委员会通过。
表1 两组ODI患者一般资料情况(±s)

表1 两组ODI患者一般资料情况(±s)
组别联合组(n=40)对照组(n=40)t值P值年龄(岁)33.26±4.57 32.15±4.61 1.081 0.283病程(年)2.71±0.58 2.69±0.47 0.169 0.866月经周期(d)37.21±4.25 38.39±5.14 1.119 0.267
1.2 治疗方法
两组ODI患者均采用常规对症治疗及护理。对照组患者给予CC (上海衡山药业有限公司,国药准字H31021107,50 mg/片)口服,100 mg/次,1次/d,连服5 d。联合组患者给予CC 联合EV(浙江仙琚制药股份有限公司,国药准字H20020299,0.5 mg/片)口服,1 片/d,连续服用21 d。CC同对照组。
1.3 观察指标
(1)治疗前及治疗3个月经周期后,两组患者均于月经来潮后的第3~5 d,采集清晨空腹肘静脉血2 mL。采用继圣(上海)医疗器械有限公司生产的全自动生化分析仪SD1SD2 干式生化分析仪以及配套试剂检测两组患者的促卵泡生成激素(FSH)、雌二醇(E2)及促黄体生成激素(LH)水平。(2)治疗后,采用深圳安盛生物医疗技术有限公司生产的彩色多普勒超声诊断系统,检测两组患者的优势卵巢直径及子宫内膜厚度。(3)电话及门诊随访3个月经周期,记录两组患者的排卵和妊娠情况,计算排卵率及妊娠率。排卵率=排卵例数/总例数×100%;妊娠率=妊娠例数/总例数×100%。(4)记录两组患者治疗期间是否出现面部潮红、下腹部胀痛、乳房不适、恶心、视力模糊等不良反应。
1.4 统计学方法
采用SPSS 18.0软件进行统计分析。计量资料以均数±标准差(±s)表示,组间比较采用t检验。计数资料以例数和百分比(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组ODI患者治疗前后的血清性激素水平情况
治疗前,两组ODI患者血清性激素水平比较,差异无统计学意义(P>0.05);治疗3 个月经周期后,联合组患者FSH、LH 及E2水平均高于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组ODI患者治疗前后性激素水平情况(±s)
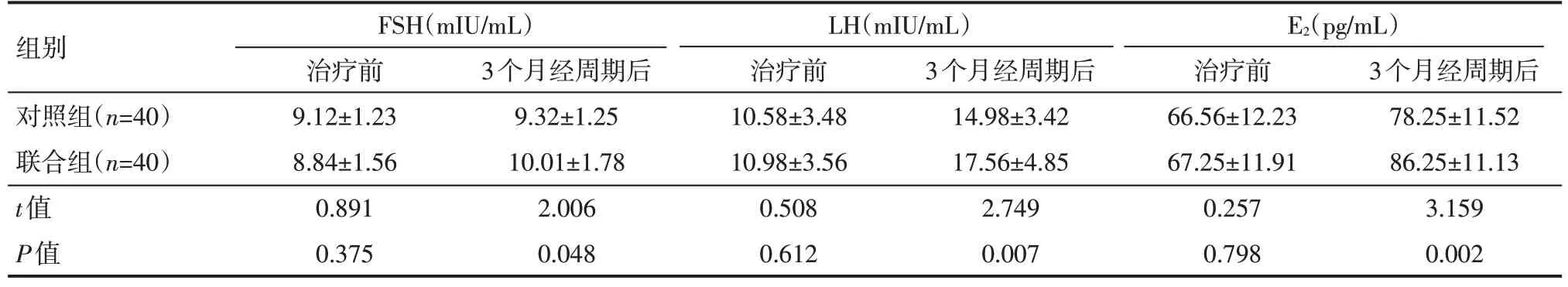
表2 两组ODI患者治疗前后性激素水平情况(±s)
组别对照组(n=40)联合组(n=40)t值P值FSH(mIU/mL)治疗前9.12±1.23 8.84±1.56 0.891 0.375 3个月经周期后9.32±1.25 10.01±1.78 2.006 0.048 LH(mIU/mL)治疗前10.58±3.48 10.98±3.56 0.508 0.612 3个月经周期后14.98±3.42 17.56±4.85 2.749 0.007 E2(pg/mL)治疗前66.56±12.23 67.25±11.91 0.257 0.798 3个月经周期后78.25±11.52 86.25±11.13 3.159 0.002
2.2 两组ODI患者治疗前后子宫内膜厚度、优势卵泡直径情况
治疗前,两组ODI患者的子宫内膜厚度、优势卵泡直径比较,差异无统计学意义(P>0.05);治疗3 个月经周期后,联合组ODI患者的子宫内膜厚于对照组,优势卵泡直径长于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组ODI患者治疗前后子宫内膜厚度、优势卵泡直径情况(±s)mm

表3 两组ODI患者治疗前后子宫内膜厚度、优势卵泡直径情况(±s)mm
组别对照组(n=40)联合组(n=40)t值P值子宫内膜厚度优势卵泡直径治疗前7.25±2.25 7.75±1.71 1.119 0.267 3个月经周期后8.23±1.32 9.23±2.13 2.523 0.014治疗前12.83±3.42 12.85±3.52 0.028 0.979 3个月经周期后17.52±3.57 20.41±4.23 3.302 0.001
2.3 两组ODI患者妊娠率及排卵率情况
治疗后,联合组妊娠率为60.00%高于对照组的25.00%,差异有统计学意义(P<0.05);联合组排卵率为77.50%高于对照组的47.50%,差异有统计学意义(P<0.05),见表4。

表4 两组ODI患者妊娠率及排卵率情况 例(%)
2.4 两组ODI患者治疗期间发生的不良反应情况
联合组治疗期间总不良反应发生率为12.50%,与对照组的20.00%相比,差异无统计学意义(P>0.05),见表5。
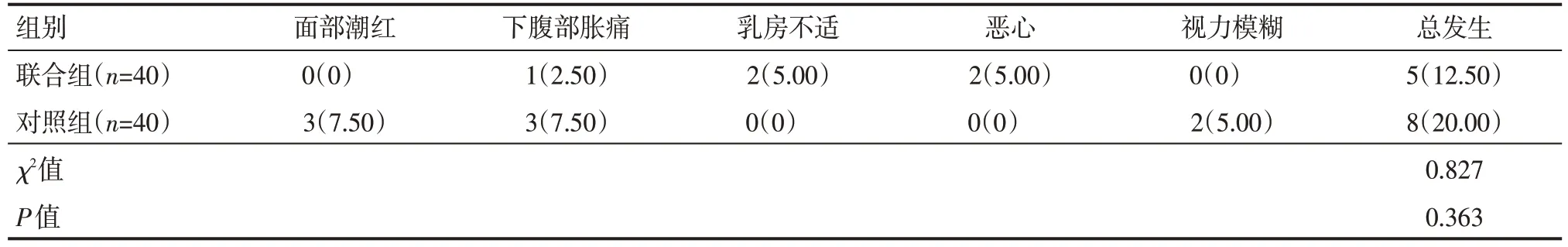
表5 两组ODI患者治疗期间发生的不良反应情况 例(%)
3 讨论
中枢内分泌紊乱、妇科疾病、排卵障碍等因素均可导致女性不孕情况的发生[6]。其中排卵障碍是女性无法怀孕的最常见原因之一[7]。排卵障碍是指自身卵子成熟过程出现障碍,无法产生和排出正常卵子的情况,其致病因素主要有卵子排出调节轴,下丘脑—垂体—卵巢某一环节出现病变或内分泌失调、免疫功能障碍等,另外,由于患者长期处于焦虑、紧张等不良状态也会出现排卵障碍的症状[8]。排卵障碍除了会导致女性不孕之外,还可能引起其他症状,例如肥胖、身体多毛、子宫内膜癌等[9]。因此,需要引起患者的注意,并且积极接受治疗。当前临床对于排卵障碍主要采用药物调节患者的月经周期,促进卵巢排卵等方法进行治疗[10]。
本研究采用EV 与CC 联合用药,EV 是一种由人工合成的雌激素类药物[11],其中的主要成分E2是一种天然的雌激素,主要由卵巢中的成熟滤泡分泌产生,经过雌激素的持续性刺激,使雌激素浓度呈上升趋势,导致子宫肌细胞出现增生,从而使子宫肌层增厚;也可以修复子宫内膜腺体间质,从而使子宫平滑肌对于缩宫素的敏感性增加;另外,对于子宫内膜的生长、输卵管的蠕动也具有重要的作用。CC的临床应用比较广泛,可以用于治疗ODI,首先通过干扰内源性雌激素的负反馈,可以促使LH 与FSH 的分泌增加,同时可以刺激卵泡的生长。卵泡成熟之后雌激素的释放量增加,通过正反馈激发排卵前促性腺激素的释放,达到峰值,从而使患者可以发生排卵[12]。结果显示,联合组患者3个月经周期后的FSH、LH及E2水平显著高于对照组,提示以上药物联合应用可有效提高ODI患者的雌激素水平。雌激素是女性主要的荷尔蒙,其具有促进女性附性器官成熟、导致第二性征出现的作用,可以帮助维持女性的正常性欲,调节生殖功能,排卵障碍患者体内雌激素低于正常水平。由于EV 属于雌激素类药物,因而联合使用此药物可提高该患者的雌激素水平。而雌激素水平的提高,还可刺激患者的卵泡发育,促进排卵。
本研究结果显示,联合组3个月经周期后的子宫内膜厚于对照组,优势卵泡直径长于对照组,提示CC联合EV能够刺激子宫内膜增生变厚,为ODI患者创造了良好的子宫内环境,同时其能促进优势卵泡的发育,为受精卵的植入做好准备,对治疗ODI患者有较好的疗效。
本研究结果显示,联合组治疗后的妊娠率和排卵率高于对照组,提示EV联合CC可以提高该患者的排卵率及妊娠率。原因可能是由于CC 是一种人工合成的非甾体类制剂,没有直接的促排卵作用,但具有较强的抗雌激素效应和较弱的雌激素作用。这种药物作用于宫颈黏液,导致其分泌减少,同时也会使子宫内膜变薄。虽然该药物能提高患者的排卵率,是受孕成功率并不高。EV 能刺激子宫平滑肌,增强子宫内膜接受胚胎的能力,提高妊娠率[11]。
有研究指出,EV 能促进雌激素分泌,有利于受精卵顺利植入子宫内膜,增加ODI患者的妊娠率。本研究结果显示,联合组治疗期间总不良反应发生率与对照组相比无显著差异,提示联合使用EV 未增加不良反应的发生,较为安全。
综上所述,EV联合CC治疗ODI患者可提高性激素水平,促进优势卵泡的发育,提高该患者的妊娠率及排卵率,且未增加不良反应的发生。

