鼻颅底沟通性肿瘤的诊断及外科治疗
李朝曦,韩林,张所军,游学俊,陆翔,刘争,舒凯
(华中科技大学同济医学院附属同济医院 1.神经外科;2.耳鼻咽喉头颈外科,湖北 武汉 430034)
鼻颅底沟通性肿瘤为神经外科少见的肿瘤,毗邻解剖结构关系复杂[1],病理类型繁多,恶性肿瘤多见,涉及神经外科与耳鼻咽喉头颈外科等学科交叉,诊断及外科治疗难度大。我们自2011年1月—2021年12月共收治37例该类患者,总结分析以供参考。
1 资料与方法
1.1 临床资料
回顾性分析2011年1月—2021年12月华中科技大学同济医学院附属同济医院神经外科接诊的37例鼻颅底沟通性肿瘤的临床资料,其中男23例,女14例;年龄6~67岁,平均49岁;肿瘤最大径4.7~8.5 cm,平均6.3 cm。临床表现头痛25例,鼻塞13例,嗅觉失常9例,视力下降5例,复视4例,眼球突出3例。37例鼻颅底沟通性肿瘤,良性肿瘤10例,包括脑膜瘤7例,颅底骨纤维异常增殖症2例,朗格汉斯组织细胞增多症1例;恶性肿瘤27例,包括嗅神经母细胞瘤8例,鳞状细胞癌6例,恶性黑色素瘤5例,软骨肉瘤3例,腺癌3例,黏液表皮癌2例。
1.1.1 影像学检查、三维模型重建 所有患者术前均行头部MRI平扫+增强扫描,CT薄层扫描,头颈动脉CT血管造影(CTA)检查。CT成像使用64排多层螺旋CT扫描仪,层厚0.625 mm;MRI成像使用3.0T磁共振成像仪,层厚1 mm,将获取的DICOM格式影像资料通过软件进行三维重建(武汉联影智融医疗科技有限公司)。
1.1.2 术前评估 根据影像资料及三维重建结果,评估肿瘤与周围结构解剖关系,制定手术方案。
1.2 手术方法
本组患者肿瘤主体大部分位于颅内,脑实质侵犯明显,手术方式主要采用神经外科开颅显微手术,少部分患者序贯耳鼻咽喉头颈外科二期手术。根据肿瘤位置,颅外沟通情况及与中线结构关系,病变累及双侧,颅外侵犯筛窦及鼻腔等患者采用冠状切口双侧额底入路术式,术中可见肿瘤质地较硬,与颅底硬膜及骨质关系密切,颅底血供丰富,部分可见粗大供血血管;病变主体位于一侧,颅外侵犯筛窦、额窦及鼻腔等患者采用半冠状切口单侧额底入路,术中可见肿瘤质地软至稀软,颅底血供一般,与颅底硬膜及骨质边界相对清晰;病变主要累及眶及上颌窦等患者采用翼点入路。根据肿瘤向颅底生长情况,骨窗下缘至同侧或双侧鼻窦(额窦、筛窦、蝶窦),沿肿瘤生长间隙扩大鼻窦肿瘤入口,鼻窦及鼻腔肿瘤处理前后双氧水反复冲洗避免颅内感染。术后颅底骨性重建采用钛板,软组织重建采取帽状腱膜-骨膜瓣修复,颞肌-肌筋膜瓣修复及颞肌-大腿阔筋膜瓣修复。恶性肿瘤患者均于术后1个月内序贯耳鼻咽喉头颈外科手术治疗和/或肿瘤科放化疗。
2 结果
2.1 手术情况
本组37例患者行冠状切口双侧额底入路21例,半冠状切口单侧额底入路11例,翼点入路5例。37例患者均顺利完成手术,完全切除26例,次全切除术4例,大部分切除7例。术后19例采取帽状腱膜-骨膜瓣修复,10例采用颞肌-肌筋膜瓣修复,8例采用颞肌-大腿阔筋膜瓣修复。27例恶性肿瘤患者7例患者术后耳鼻咽喉头颈外科进一步手术治疗。
2.2 并发症
所有患者无术中大出血、术后出血再次手术及颅内感染等严重并发症。2例脑膜瘤患者术后脑脊液鼻漏,1例嗅神经母细胞瘤患者术后皮下积液,给予腰大池置管引流后均治愈。
2.3 术后辅助治疗
27例恶性肿瘤患者,20例患者神经外科手术后直接肿瘤科序贯放化疗,放疗剂量60 Gy,30次给药,化疗方案主要为环磷酰胺+多柔比星+长春新碱或者环磷酰胺+多柔比星+长春新碱+强的松; 7例耳鼻咽喉头颈外科进一步手术治疗后再转肿瘤科行放化疗。
2.4 生存率
所有患者术后均定期随访,27例恶性肿瘤随访5~10年,平均8.3年,5年生存率为63.0%(17/27);10例良性肿瘤患者随访1~11年,平均6.7年,其中1例非典型脑膜瘤(WHO II 级)术后5年复发,给予再次手术,余患者无复发。
3 典型病例
患者钱某,女,49岁,因“鼻塞2个月,恶心呕吐伴全身乏力4 d”入院,既往高血压病史3年余,最高血压180/100 mmHg,口服药物控制可;体格检查嗅觉减退,余未见明显异常;辅助检查:头颅MRI平扫+增强现实左侧前颅窝底及左侧筛窦肿块,累计左侧中鼻甲,考虑肿瘤性病变伴大脑镰下疝(图1),三维重建示左额底肿瘤,经筛窦向鼻腔内生长,向右侧推挤双侧大脑前动脉(图2)。入院诊断考虑左侧鼻颅底沟通性肿瘤,嗅神经母细胞瘤可能(Kadish C期)。患者完善相关术前检查,排除手术禁忌,行半冠状切口单侧经额底入路显微切除术,术中见主体位于额底巨大肿瘤,侵袭突破硬膜推挤额叶,质韧,血供丰富,大小约7 cm×6 cm×6 cm,大部分切除肿瘤,骨膜修补硬膜缺损,帽状腱膜-骨膜瓣修复颅底。患者术后病理示嗅神经母细胞瘤(Hyams分级:Ⅳ级),Ki67(Li约50%),见图3。术后恢复良好,无并发症,术后3个月复查肿瘤大部分切除(图4)。患者术后转肿瘤科进一步行放疗(66 Gy,33次放疗)+化疗(环磷酰胺+阿霉素+长春新碱),随访5年至发稿患者仍定期门诊随诊。
4 讨论
颅底沟通性肿瘤是指源于颅内或颅外,穿通颅底骨质和硬膜,造成颅内外沟通的肿瘤,约占颅底肿瘤的10%[2],累及鼻窦及鼻腔可进一步定义为鼻颅底沟通性肿瘤。随着现代医学进步带动的肿瘤早期诊断及早期治疗,鼻颅底沟通性肿瘤越来越少见,临床表现根据肿瘤大小及与周围结构关系可表现为颅高压症状、嗅觉减退、鼻塞、眼球突出等,患者多为恶性肿瘤,诊断主要依赖影像学(CT、MRI)及病理,良恶性肿瘤单纯影像学鉴别有难度[3],多模态影像学重建不仅有利于诊断,更有利于个体化手术方案的制定[4]。恶性肿瘤主要包括嗅神经母细胞瘤、鳞状细胞癌及黑色素瘤等,其中嗅神经母细胞瘤因其起源及解剖特点最具代表性。嗅神经母细胞瘤在鼻颅底沟通性肿瘤中较多见,该病常发生于鼻穹隆上部分,肿瘤起源于嗅神经上皮或嗅基板神经外皮质。嗅神经母细胞瘤起病隐匿,生物学行为多样,既有惰性肿瘤缓慢生长的特性,也可表现出高侵袭性肿瘤所具有的局部和远隔部位转移的潜能。嗅神经母细胞瘤有多种分期方法,最常用的是Kadish分期(A期肿瘤局限于鼻腔;B期肿瘤累及鼻腔和鼻窦;C期肿瘤扩展到鼻腔和鼻窦之外)[5]。病理分级系统为Hyams分级法,该系统根据细胞有丝分裂活性、核多形性、坏死、结构紊乱、显微基质稀疏,“菊形团”形成等特征,将嗅神经母细胞瘤按照分化程度从高(Ⅰ级)到低(Ⅳ级)分为4级[6]。Kadish A期和B期患者主要采用内镜手术,Kadish C期患者亦可尝试内镜手术,但广泛侵袭的嗅神经母细胞瘤患者,传统开颅显微手术仍是首选[7-8]。
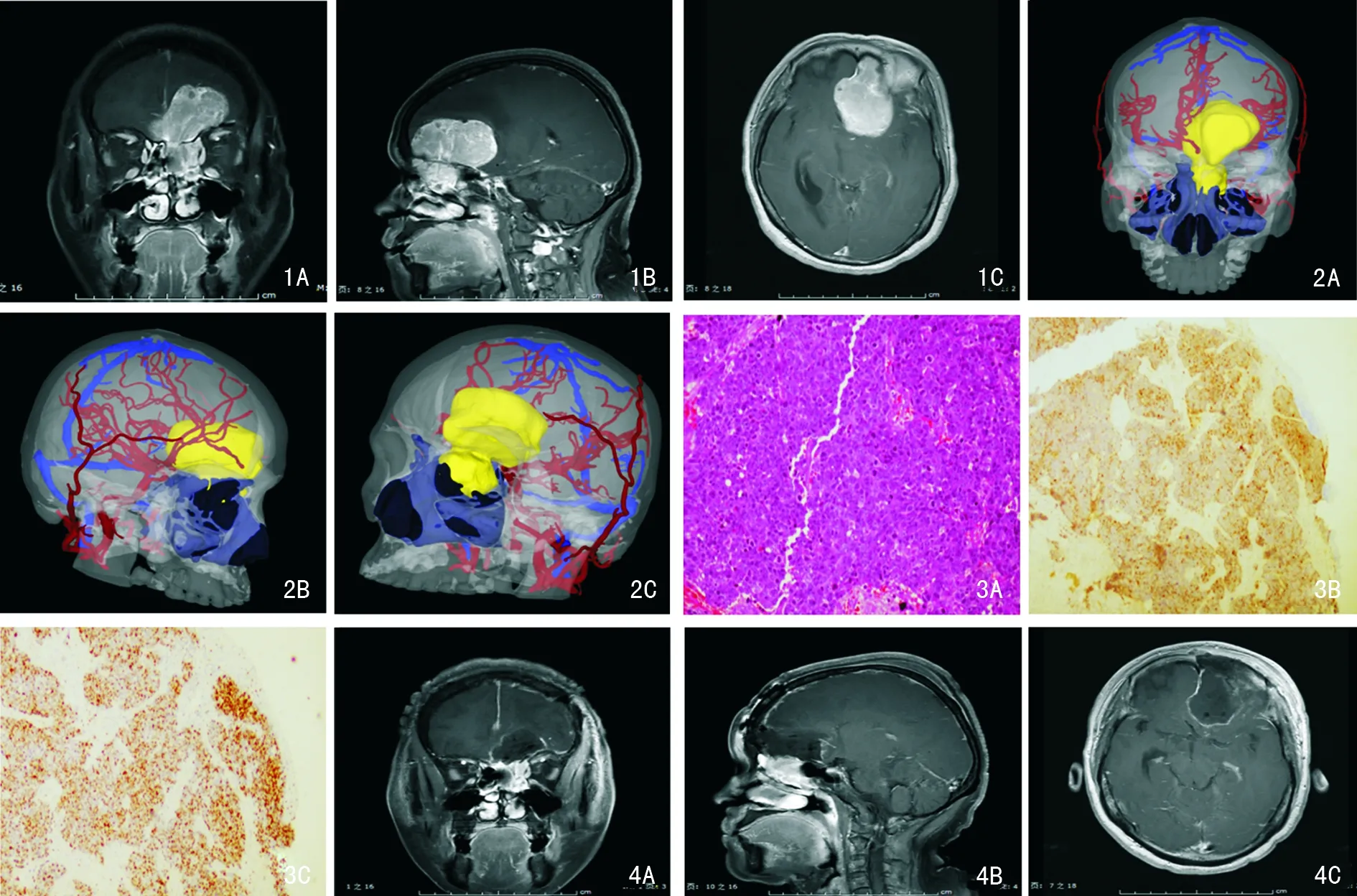
图1 典型病例术前MRI增强扫描 1A:冠状位; 1B:矢状位; 1C:水平位 图2 典型病例三维模型重建 2A:正面观; 2B:右侧面观; 2C左侧面观(红色示动脉,蓝色示静脉,深蓝色示鼻窦,黄色示肿瘤) 图3 典型病例术后病理示嗅神经母细胞瘤 3A:组织病理图 (HE ×20); 3B:CgA阳性染色 (免疫组化 ×20); 3C:Ki67染色阳性约50% (免疫组化 ×20) 图4 典型病例术后MRI增强扫描 4A:冠状位; 4B:矢状位; 4C:水平位
鼻颅底沟通性肿瘤同时侵犯前颅底及鼻腔,甚至眼眶,外科手术涉及神经外科,耳鼻咽喉头颈外科及眼科等多个科室,神经外科患者首诊临床症状多以颅高压及神经功能障碍起病,肿瘤体积巨大,主体多位于颅内,脑实质受损明显,本组患者肿瘤最大径4.7~8.5 cm,平均6.3 cm。鼻颅底沟通性肿瘤往往难以一期全切肿瘤,通常需要分期切除,初次手术直接决定了预后及后续手术效果。因此,争取全切肿瘤或者大部分切除肿瘤并妥善颅底重建是鼻颅底沟通肿瘤的理想手术方式。
目前鼻颅底沟通性肿瘤的主要手术方式包括显微手术和/或内镜手术[9-13]。①内镜经鼻手术显露范围大,带蒂黏膜瓣的应用也减少了术后脑脊液漏及颅内感染风险[12],但内镜手术也可能因肿瘤对鼻中隔的破坏影响带蒂黏膜瓣的成型,同时由于硬脑膜难以修复;单纯软组织修补颅底远期可能引起缺损区域脑膨出及脑脊液漏;另外对血管神经广泛侵袭肿瘤,内镜难以切除;最后因为内镜最先处理鼻腔内肿瘤,而以颅内肿瘤为主体的鼻颅底沟通性肿瘤滋养血管往往起源于颅内或颅底血管,鼻腔内少有大的滋养血管,对血供丰富的肿瘤,内镜手术可能造成致命性大出血[11]。②经颅面联合入路也是鼻颅底肿瘤经典手术方式[14],通过显微镜下切除颅内肿瘤,之后颜面部手术切除颅外肿瘤,但该入路手术创面大,面部手术瘢痕容易造成患者心理负担。③内镜联合显微镜手术目前报道较多,按手术顺序可分为内镜-显微镜及显微镜-内镜手术,与单纯内镜手术相比联合手术优势明显,补齐了内镜手术的短板,通过显微镜手术切除颅内肿瘤,修补缺损硬脑膜,并尽可能切除鼻窦内肿瘤,修补颅底,之后内镜下经鼻切除鼻腔及鼻窦内肿瘤。④开颅显微手术也是鼻颅底肿瘤重要治疗方法,通过扩大经额底入路可以切除颅内侵犯蝶窦筛窦的肿瘤,在无需切开面部皮肤的情况下也可以实现对筛窦、蝶窦、眶及鼻腔等的充分显露,甚至可以全切部分鼻颅底肿瘤[11,15]。本组大部分患者通过开颅手术对额底、鼻窦及鼻腔的充分显露均可以实现肿瘤的大部分切除甚至全切,少部分患者因肿瘤位置过低需要耳鼻咽喉头颈外科进一步手术治疗。
鼻颅底手术术后主要并发症为脑脊液漏及其引起的颅内感染,开颅手术后颅底重建至关重要,主要包括硬膜的修补及前颅窝底的重建[16]。硬脑膜的缝合因为鼻窦的开放,应视为2类切口,要避免使用人工硬膜修补,多采用自体组织(骨膜、颞肌筋膜)水密缝合[17]。前颅底骨质大范围缺损可导致脑组织膨出及波动性突眼,所以颅底骨性重建意义重大,修补多采用钛网修复,不强求螺钉固定,可通过术中钛网塑性与颅底嵌顿固定[18-19],软组织重建也非常重要,大的缺损常用颞肌瓣转位修补[20],小的缺损可用阔筋膜、帽状腱膜及骨膜等修复。妥善的颅底重建可最大程度减少脑脊液漏的发生,若术后仍有脑脊液漏后皮下积液,可通过腰大池置管引流控制。鼻颅底沟通性肿瘤恶性肿瘤多见,外科手术最大程度切除肿瘤,往往需要进一步行放化疗,治疗时机选择须根据肿瘤病理及切口恢复情况而定,过早行放疗可引起伤口愈合不良,增加脑脊液漏风险。
综上所述,神经外科首诊的鼻颅底沟通性肿瘤往往颅内肿瘤为主体,手术难度大,一期手术全切或大部分切除意义重大,开颅术后颅底修复避免脑组织膨出及脑脊液漏是进一步治疗的基础。

