乳及乳制品中环氧乙烷及2-氯乙醇的检测
周 静,徐红斌,周泽琳,周耀斌,符昌雨,刘 洋
(上海市质量监督检验技术研究院,国家市场监管重点实验室(乳及乳制品检测与监控技术),上海 200233)
环氧乙烷是一种广谱杀菌剂,能杀灭各种微生物,例如芽孢、结核杆菌、细菌、病毒和真菌等[1]。环氧乙烷已被明确具有一定致癌性、诱变性和生殖毒性[2],美国国立卫生研究院将其定义为“已知的人类致癌物”[3]。世界多国已纷纷将环氧乙烷移出食品添加剂列表[4-5]。我国的《消毒技术规范》(2002年版)[6]中也明确规定,环氧乙烷不适用于食品灭菌。然而近几年却不断发生因食品中检出环氧乙烷的召回和预警事件,欧盟食品和饲料类快速预警系统已累计发布500 次以上通报,产品涉及20多个国家[7]。
食品中频繁被检出环氧乙烷,主要是由于目前仍有一些国家使用环氧乙烷作为熏蒸剂控制香料和食品等的虫害。但冰淇淋等食品中检出环氧乙烷,一方面可能来自于食品包装的印刷油墨迁移。另外,受新冠肺炎疫情影响,部分国家使用环氧乙烷对食品原料及外包装进行熏蒸消杀,可能导致原料或成品中发生残留[8]。低浓度的环氧乙烷无法通过肉眼和嗅觉分辨,食品企业难以通过常规手段对含有环氧乙烷的原料进行管控。尤其是冷冻饮品、乳制品等不使用高温加工工艺的产品,更容易有环氧乙烷残留。另外,在使用环氧乙烷进行灭菌的过程中,残留的环氧乙烷会与食品中的氯接触后发生代谢反应,生成2-氯乙醇[8-9]。
目前仅有欧盟、美国、加拿大、韩国等对环氧乙烷和2-氯乙醇设有限量值。欧盟规定环氧乙烷与2-氯乙醇之和以环氧乙烷计,在各类食品中的限量为0.02~0.10 mg/kg,并于2020年发布了气相色谱-三重四极杆串联质谱检测方法[10]。美国、加拿大规定不同食品、药品等中的环氧乙烷限量为7~50 mg/kg不等,2-氯乙醇小于940 mg/kg,美国环境保护署采用气相色谱法检测香料中环氧乙烷和2-氯乙醇[11]。在韩国,环氧乙烷属于未登记的农药,执行0.01 mg/kg的统一标准,补充设定了2-氯乙醇临时限量标准,即农畜水产品及其加工品≤30 mg/kg,婴幼儿食品≤10 mg/kg。
国内目前可供参考的环氧乙烷和2-氯乙醇的检测方法适用范围主要集中在医疗器械类[12-15]、医用口罩[16-18]、个人防护用品[19-21]、纺织品类[22-25]、药品与药品包装材料[26-28]及食品接触材料方面[29]。上述方法均采用气相色谱仪或气相色谱-质谱联用仪进行检测,前处理方法基本采用顶空或吹扫捕集技术。对比欧美等食品基质中的方法,美国将环氧乙烷和2-氯乙醇分开测定,检测效率不高;欧盟的方法前处理较复杂,采用程序升温进样口和四极杆串联质谱,对设备的配置要求很高,韩国的方法亦是如此[30],因此目前仍无法在国内推广应用。我国尚未制定可以广泛适用于食品中环氧乙烷及2-氯乙醇的相关检测和限量标准,导致出口食品存在极大的退运风险[31]。虽有文献报道了食品中环氧乙烷及2-氯乙醇的同步测定方法,但只集中于芝麻、香辛料和方便面[32-33]。对于如冰淇淋、低温乳制品等不使用高温加工工艺的食品较少涉及,有研究[34]报道了采用顶空-气相色谱仪测定冰淇淋中环氧乙烷的方法,但该方法未实现2-氯乙醇的同步测定,且气相色谱法的定性准确度也不如质谱法。因此本研究建立一种顶空-气相色谱-质谱联用检测方法,以实现乳及乳制品中环氧乙烷及2-氯乙醇的同时测定,旨在为乳及乳制品中环氧乙烷灭菌残留的判断提供技术评价依据,进一步保障消费者饮食健康。
1 材料与方法
1.1 材料与试剂
实验样品:在当地超市购买35 批次实验样品,包括液态乳(10 批次)、婴幼儿配方乳粉(10批次)、低温发酵乳(10 批次)和冰淇淋(5 批次)。
环氧乙烷(2 000 μg/mL,溶于水)、2-氯乙醇(1 000 μg/mL,溶于水)、BePure®标准物质北京曼哈格生物科技有限公司;实验用水:一级纯水。
1.2 仪器与设备
GCMS QP2020 NX顶空-气相色谱-质谱联用仪(带有HS-20顶空进样器) 日本岛津公司;DENVER分析天平 美国Denver公司;SK8210LHC超声仪上海科导超声仪器有限公司;Vortex Genie 2涡旋混合器美国Scientific Industries公司;Milli-Q超纯水器 美国Millipore公司。
1.3 方法
1.3.1 标准溶液配制
标准混合中间液:吸取环氧乙烷标准溶液(2 000 μg/mL)0.05 mL和2-氯乙醇(1 000 μg/mL)0.50 mL于10 mL容量瓶中,加超纯水定容至刻度,混匀并转移至棕色储液瓶中,于4 ℃冰箱冷藏避光保存。得到的标准混合中间液中环氧乙烷质量浓度为10.0 mg/L,2-氯乙醇质量浓度为50.0 mg/L。
标准混合系列工作液:分别吸取上述混合标准中间液0.05、0.10、0.15、0.25、0.50、1.00 mL于5 mL容量瓶中,加空白样品基质,用超纯水定容至刻度,混匀并转移至顶空瓶中,及时压盖密封,现用现配。得到的标准混合系列工作液中环氧乙烷质量浓度分别为0.1、0.2、0.3、0.5、1.0、2.0 mg/L,2-氯乙醇质量浓度分别为0.5、1.0、1.5、2.5、5.0、10.0 mg/L。
1.3.2 样品前处理
1.3.2.1 液态乳
用移液枪准确吸取5.0 mL液态乳样品于20 mL顶空进样瓶中,为防止目标物挥发,尽快用密封盖压紧密封,涡旋混匀。待上机分析。
1.3.2.2 婴幼儿配方乳粉
称取1.0 g左右婴幼儿配方乳粉样品于15 mL定容管中,先加入2 mL超纯水溶解,超声15 min,再加入超纯水定容至5.0 mL,涡旋混匀,转移至20 mL顶空进样瓶中。同上操作,待分析。
1.3.2.3 冰淇淋、低温发酵乳
取100~200 g样品于均质器中均质,待用。移取上述均质后的冰淇淋或低温发酵乳样品5.0 mL于20 mL顶空进样瓶中,称质量,同上操作,待上机分析。
若是样品性状浓稠,则称取3.0 g左右样品于15 mL定容管中,加入少许超纯水稀释溶解,超声5 min,最终用超纯水定容至5.0 mL,涡旋混匀后转移至20 mL顶空进样瓶中。同上操作,待分析。
1.3.3 色谱条件
色谱柱:DB-624石英毛细管柱(60 m×0.32 mm,1.8 μm);进样方式:分流进样,分流比10∶1;进样口温度220 ℃;载气:高纯氦气,纯度≥99.999%;流速:恒流模式,1.0 mL/min;程序升温:40 ℃保持3 min,然后以25 ℃/min程序升温至240 ℃,保持5 min。
1.3.4 质谱条件
电离方式:电子轰击电离源;电离能量70 eV;离子源温度230 ℃;四极杆温度150 ℃;传输线温度260 ℃;溶剂延迟3.0 min;扫描方式:选择离子监测(selected ion monitor,SIM)模式采集,SIM扫描离子见表1。
1.3.5 结果计算
样品中环氧乙烷和2-氯乙醇含量按下式计算。
式中:X为样品中环氧乙烷或2-氯乙醇含量/(mg/kg);ρ为由线性方程计算得到的试样溶液中环氧乙烷或2-氯乙醇的质量浓度/(mg/L);ρ0为试样空白溶液中环氧乙烷或2-氯乙醇的质量浓度/(mg/L);V为顶空瓶体积/mL;m为取样量/g(mL)。
1.4 数据处理
运用Excel 2016软件进行数据分析并作图。
2 结果与分析
2.1 仪器条件优化
2.1.1 色谱柱的选择
冰淇淋、低温发酵乳和婴幼儿配方乳粉样品基质较复杂,尤其还含有香精等挥发性成分,因此色谱柱的选型和分离条件的优化至关重要。关于环氧乙烷和2-氯乙醇的测定,文献[32]比较了几款常见的中等极性和极性色谱柱,得出结论,DB-624色谱柱(30 m×0.25 mm,1.4 μm)对环氧乙烷和2-氯乙醇均有较好的保留。因此,本研究在全扫描模式下,进一步考察不同规格DB-624色谱柱对环氧乙烷和2-氯乙醇的分离效果。同样升温程序条件下,DB-624色谱柱(30 m×0.25 mm,1.4 μm)对环氧乙烷和2-氯乙醇的保留时间分别为2.01 min和5.95 min,环氧乙烷出峰较早,在这个时间段存在较多小分子的挥发性物质及载气背景干扰,不利于色谱分离与目标物定量;而另一款DB-624色谱柱(60 m×0.32 mm,1.8 μm)对环氧乙烷和2-氯乙醇有更好的保留,其保留时间分别为5.62 min和9.81 min,避免了大部分挥发性物质的干扰(图1)。因此,选择DB-624色谱柱(60 m×0.32 mm,1.8 μm)作为最终的分析柱。
2.1.2 分流比的选择
气相色谱分流比条件的设定不仅是决定方法检出限的重要影响因素,同时也会对目标物出峰峰型及干扰等情况产生影响,从而影响积分和定量准确性。因此本研究比较不同分流比条件下环氧乙烷和2-氯乙醇的出峰情况。比较不分流与分流比10∶1、20∶1、50∶1的目标物出峰情况,由图2可知:在不分流条件下,化合物拖尾严重,且存在检测器过饱和风险;而分流比20∶1和50∶1条件下仪器响应值较低,严重影响方法灵敏度,因此最终确定方法分流比设定为10∶1。

图2 分流比对环氧乙烷和2-氯乙醇色谱峰响应的影响Fig.2 Effect of split ratio on chromatographic peak responses of ethylene oxide and 2-chloroethanol
2.2 顶空条件优化
顶空进样模式下,顶空的平衡时间和平衡温度会直接影响方法的灵敏度,因此重点对这2 个参数条件进行实验优化。
2.2.1 顶空平衡温度的确定
通过基质加标的手段考察不同顶空平衡温度下目标物的仪器出峰响应变化。向液态乳空白样品中添加1.0 mL混合标准中间液(环氧乙烷质量浓度2.0 mg/L、2-氯乙醇10.0 mg/L),保证液体体积为5.0 mL,密封后涡旋混匀,于50、60、70、80、90 ℃条件下平衡30 min(一般情况下,30 min平衡时间基本都能达到气-液平衡)。由图3可知,环氧乙烷和2-氯乙醇的仪器响应峰面积随温度升高而增大。这是由于对于易挥发性物质而言,温度越高越利于其从食品基质中挥发释放。考虑到顶空瓶平衡温度过高会出现水蒸气和密封性等问题,同时还会出现乳制品中蛋白质的变性问题,因此本研究中最高加热至90 ℃。同时由于100 ℃已达到水的沸点,水的沸腾会扰乱顶空瓶中的气-液平衡,影响实验数据的重现性。在90 ℃温度条件下,连续重复7 次实验,结果偏差控制在10%以内,满足实验灵敏度和稳定性的测试要求。
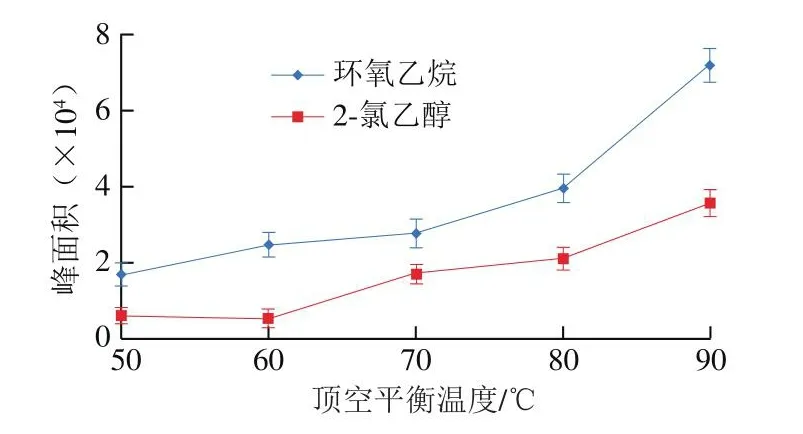
图3 顶空平衡温度对环氧乙烷和2-氯乙醇色谱峰面积的影响(nn==77)Fig.3 Effect of headspace equilibrium temperature onchromatographic peak areas of ethylene oxide and 2-chloroethanol (n = 7)
2.2.2 顶空平衡时间的确定
向液态乳空白样品中添加1.0 mL混合标准中间液(环氧乙烷2.0 mg/L、2-氯乙醇10.0 mg/L),定容体积为5.0 mL,密封后涡旋混匀。顶空加热温度为90 ℃条件下,考察不同平衡时间对环氧乙烷和2-氯乙醇响应峰面积的影响。选取顶空平衡时间10、20、30、40 min 4 种条件下分别进样。由图4可知,环氧乙烷在20 min左右可达到基本的气-液两相平衡,20 min后即使平衡时间再延长,环氧乙烷的峰面积也无大的变化。而2-氯乙醇从10 min一直到40 min,其峰面积基本都处于稳定状态,说明2-氯乙醇的挥发较快,受顶空温度的影响更大。考虑到色谱分离时长及兼顾实验的快速高效性,选择最佳的顶空平衡时间为20 min。

图4 顶空平衡时间对环氧乙烷和2-氯乙醇色谱峰面积的影响(nn==77)Fig.4 Effect of headspace equilibrium time on chromatographic peak areas of ethylene oxide and 2-chloroethanol (n = 7)
3 方法学验证
3.1 方法的线性范围、检出限及定量限
按照前述的仪器条件,对各质量浓度的混合标准溶液进行测定,以目标峰面积响应为纵坐标,以目标物质量浓度为横坐标进行线性拟合。由表2可知,环氧乙烷和2-氯乙醇分别在0.1~2.0 mg/L和0.5~10.0 mg/L质量浓度范围内线性良好,环氧乙烷在液态乳、发酵乳和冰淇淋中的检出限均为0.12 mg/kg,定量限均为0.40 mg/kg,在婴幼儿配方乳粉中的检出限均为0.60 mg/kg,定量限均为2.0 mg/kg,在半固体冰淇淋、半固体发酵乳中的检出限均为0.20 mg/kg,定量限均为0.67 mg/kg。2-氯乙醇在液态乳、发酵乳和冰淇淋中的检出限均为0.60 mg/kg,定量限均为2.0 mg/kg,在婴幼儿配方乳粉中的检出限均为3.0 mg/kg,定量限均为10.0 mg/kg,在半固体冰淇淋、半固体发酵乳中的检出限均为1.0 mg/kg,定量限均为3.3 mg/kg。
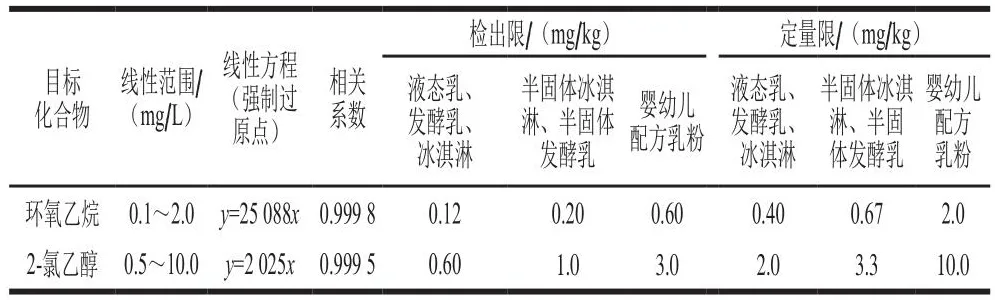
表2 环氧乙烷和2-氯乙醇的线性范围、线性方程、相关系数、检出限和定量限Table 2 Linear ranges, regression equations, correlation coefficients,limits of detection and limits of quantification for ethylene oxide and 2-chloroethanol
3.2 回收率及精密度
在空白液态乳(牛乳)、婴幼儿配方乳粉以及冰淇淋基质中分别添加低、中、高3 个水平的环氧乙烷和2-氯乙醇,按实验步骤进行测定。由表3~5可知,加标回收实验结果显示,不同基质空白加标回收率能达到75.9%~101.6%,变异系数均小于10%,方法精密度和准确度良好,加标检测结果稳定可靠,且方法灵敏度高,满足乳粉复杂基质的检测与限量要求,符合实验室分析基本要求。
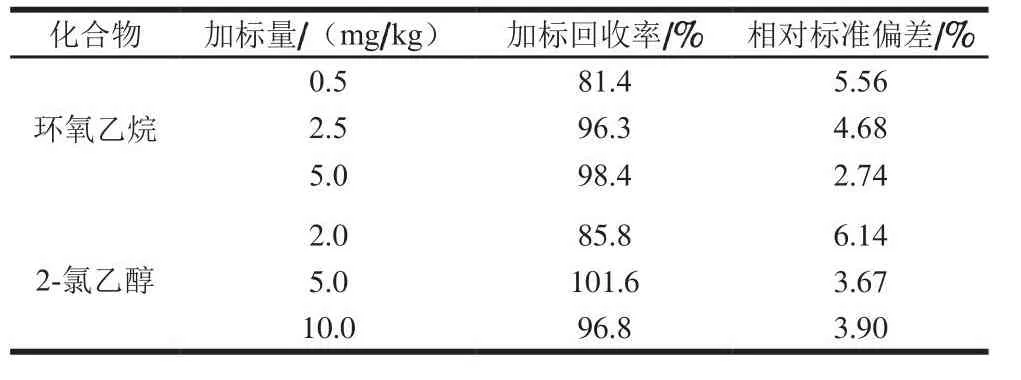
表3 空白液态乳基质加标回收实验结果(nn==77)Table 3 Recoveries of spiked blank milk matrix (n = 7)
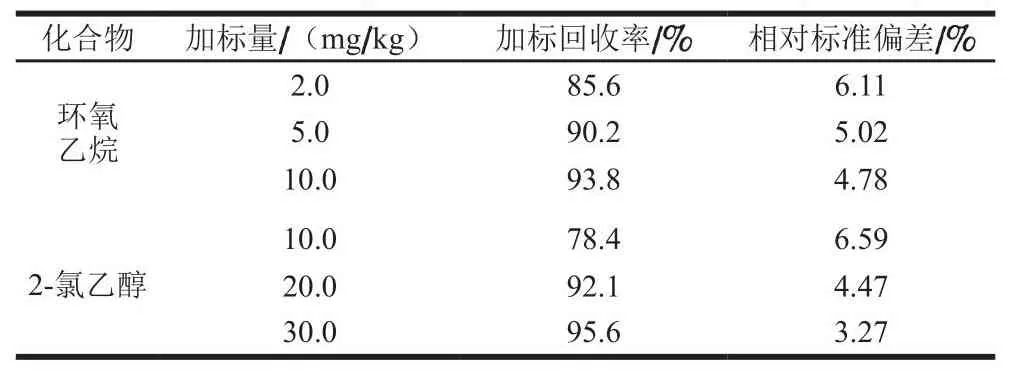
表4 空白婴幼儿配方乳粉基质加标回收实验结果(nn==77)Table 4 Recoveries of spiked blank infant formula milk powder (n = 7)

表5 空白冰淇淋基质加标回收实验结果(nn==77)Table 5 Recoveries of spiked blank ice cream (n = 7)
3.3 市售样品测定
对采购的35 批次产品进行测定后,发现所有样品中均未检出环氧乙烷和2-氯乙醇。在我国,将环氧乙烷用于食品消毒是被严格禁止的,上述检测结果也证实了这一点,说明一般情况下消费者无需担心这些产品中的环氧乙烷残留问题。但是从食品安全监管角度出发,为了控制食品安全风险,对食品中环氧乙烷和2-氯乙醇进行检测及监控仍然很有必要,尤其是对于某些地区的进口食品而言。
4 结 论
由实验结果可知,用本实验建立的方法测定乳及乳制品中环氧乙烷及其代谢物2-氯乙醇残留量,样品前处理过程简单易操作,方法分析时长较短,挥发性目标物不易损失,用DB-624毛细管柱(60 m×0.32 mm,1.8 μm)分离目标峰出峰时间合理且附近无干扰峰出现。采用质谱检测定性、定量准确且线性范围宽,方法检出限较低;低、中、高3 个水平加标样品测试也表现出较高的精密度和准确度,满足乳及乳制品中环氧乙烷和2-氯乙醇检测分析要求。

