甲状腺激素及抗体表达水平与糖尿病周围神经病变的相关性分析
陶琪,毛樱
绍兴市人民医院特检科,浙江绍兴 312000
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)是糖尿病常见的微血管并发症,在2 型糖尿病患者中的患病率高达50%[1-2]。DPN 发病机制复杂、临床表现多样[3-4]。甲状腺激素水平与2 型糖尿病的发生有相关性,甲状腺激素水平会影响胰腺β 细胞的增殖,从而影响胰岛素的分泌,它还会改变肝脏、脂肪组织对胰岛素的敏感性,导致血糖升高[5-6]。有研究显示甲状腺激素水平与糖尿病微血管并发症的发生、发展有关[7-8]。近年来,临床上发现2 型糖尿病患者甲状腺激素水平改变和抗体升高的现象较非糖尿病人群要常见,但国内外针对甲状腺激素及抗体水平与DPN 的相关性研究较少,本研究旨在通过DPN 患者和non-DPN 患者甲状腺激素及抗体水平进行对比分析,探讨甲状腺激素及抗体表达水平与糖尿病周围神经病变的相关性。
1 资料与方法
1.1 一般资料
选取2021 年1 月至2022 年2 月绍兴市人民医院肌电图室就诊的糖尿病患者186 例,按照合并DPN的情况分为DPN 组(n=68)和NDPN 组(n=118)。纳入标准:符合2009 年糖尿病诊断标准[9]。排除标准:①有非糖尿病引起的神经病变,如神经卡压综合征、格林-巴利综合征、酒精性周围神经损害等;②有甲状腺相关疾病史;③有下丘脑或垂体疾病史。本研究通过绍兴市人民医院伦理委员会的审查(伦理审批号:2022050),所有参与者知情同意。
1.2 方法
1.2.1 临床资料 收集所有患者的详细病史,登记患者的性别、出生年月、年龄、病程,测量身高、体质量、腰围,记录实验室检查指标,包括糖化血红蛋白(glycosylated hemoglobin,HbA1c)、游离三碘甲状腺原氨酸(free triiodothyronine,FT3)、游离甲状腺素(free thyroxine,FT4)、促甲状腺激素(thyroid-stimulating hormone,TSH)、甲状腺球蛋白抗体(thyroglobulin antibody,TGAb)、甲状腺过氧化物酶抗体(thyroid peroxidase autoantibody,TPOAb)。
1.2.2 糖尿病慢性并发症的诊断[9]①DPN:确诊糖尿病,有周围神经损伤的证据,包括临床体征和(或)肌电图的证据,排除其他原因引起的周围神经病变;②糖尿病肾病(diabetic nephropathy,DN):有明确的糖尿病史,尿白蛋白排泄率>200μg/min 或尿常规尿蛋白阳性(尿蛋白定量>0.5g/24h);③糖尿病视网膜病变(diabetic retinopathy,DR):Ⅰ期:视网膜微动脉瘤形成和小出血点;Ⅱ期:视网膜硬性渗出或少量出血斑;Ⅲ期:视网膜软性渗出或少量出血斑;Ⅳ期:视网膜新生血管形成或玻璃体出血;Ⅴ期:视网膜新生血管出血形成纤维增殖;Ⅵ期:增殖牵拉继发视网膜脱离。④糖尿病足(diabetic foot,DF):符合糖尿病诊断标准,伴不同程度下肢神经病变和/或血管病变,包括刺痛、感觉减退或缺失、间歇性跛行、色素沉着、皮温下降,静息痛、足背动脉搏动减弱、无痛性肿胀、溃疡、截肢等。
1.3 统计学方法
采用SPSS 21.0 统计学软件对数据进行分析处理。呈正态分布的计量资料以均数±标准差()表示,均数与总体间比较采用单样本t检验,两组间均数比较采用独立样本t检验,非正态分布的用中位数(四分位数间距)[M(Q1,Q3)]表示,采用Mann-WhitneyU检验;计数资料以[n(%)]表示,组间比较采用χ2检验。变量间相关性分析采用Spearman相关分析,糖尿病周围神经病变的影响因素采用二元Logistic 回归分析,P<0.05 为差异有统计学意义。
2 结果
2.1 临床资料比较
与NDPN 组相比,DPN 组年龄更大、DM 病程更长,高血压患病率、糖尿病慢性并发症比例更高,差异有统计学意义(P<0.05),见表1。
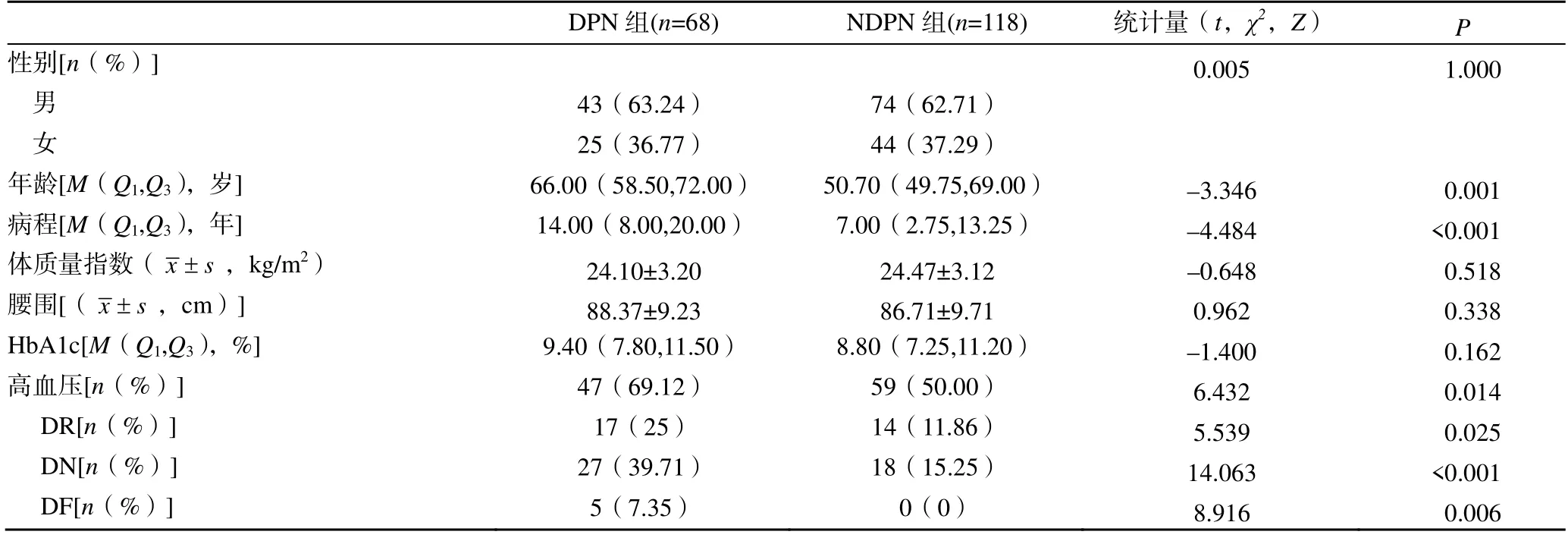
表1 两组患者临床资料比较
2.2 甲状腺功能、抗体水平比较
DPN 组患者FT3显著低于NDPN 组,差异有统计学意义(P>0.05)。两组间FT4、TSH、TGAb、TPOAb比较,差异无统计学意义(P>0.05),见表2。
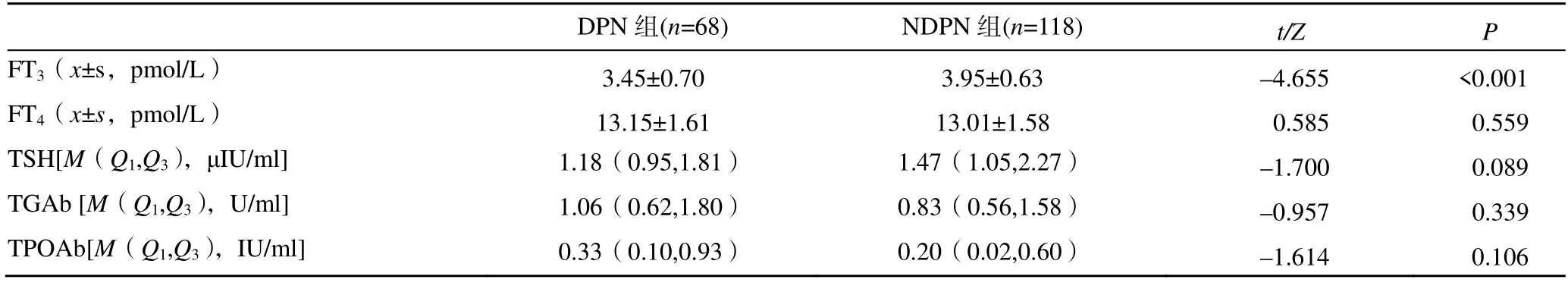
表2 两组患者甲状腺功能、抗体水平比较
2.3 一般临床资料、甲状腺指标与DPN 的相关性分析
Spearman 相关性分析显示,患者年龄、糖尿病病程、高血压及糖尿病慢性并发症(DN、DR、DF),与DPN 呈正相关(P<0.05),FT3与DPN 呈负相关(P<0.05),见表3、4。
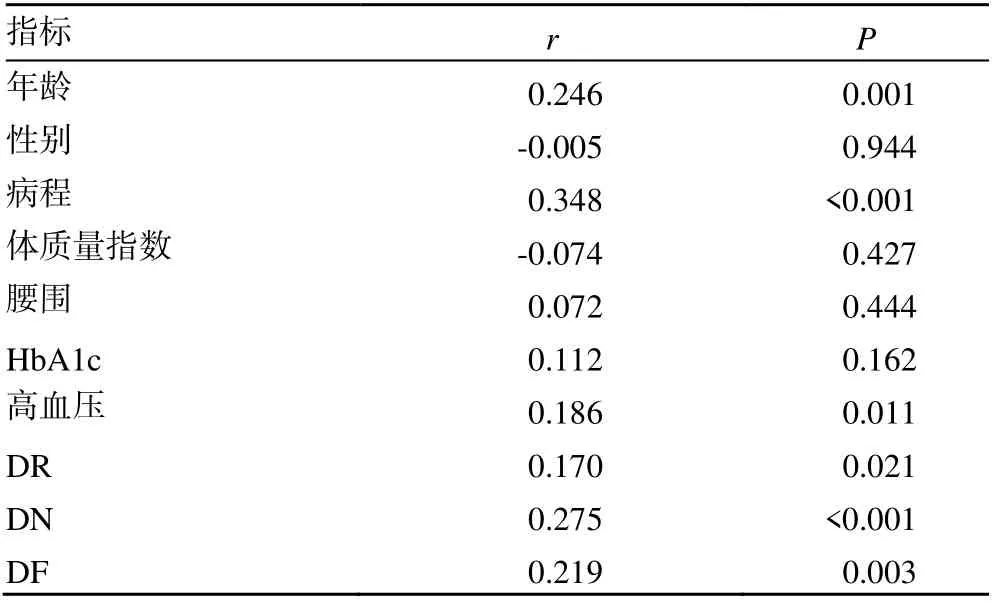
表3 一般临床资料与DPN 相关性分析
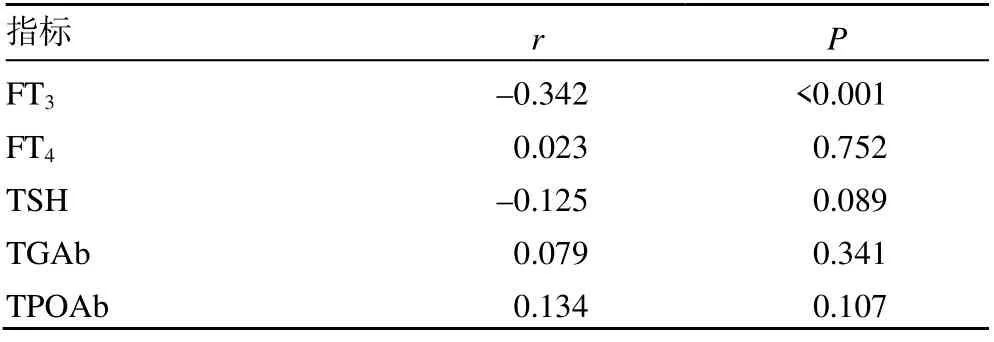
表4 甲状腺指标与DPN 相关性分析
2.4 糖尿病患者发生DPN的多因素Logistic回归分析
以有无合并DPN 为因变量,相关分析中有统计学意义的因素为自变量,进行Logistic 回归分析。结果显示,糖尿病病程、FT3是 DPN 的影响因素(P<0.05),见表5。
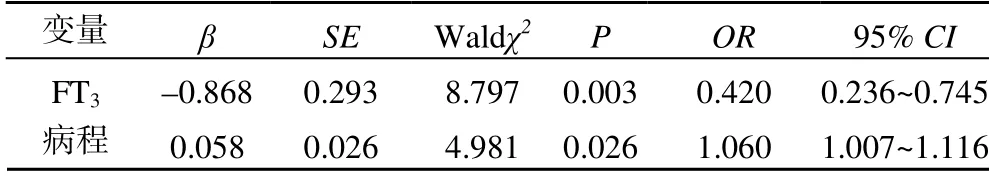
表5 糖尿病患者发生DPN 的多因素Logistic 回归分析
3 讨论
DPN 是糖尿病常见的微血管并发症,长期的高血糖环境会破坏微血管内皮细胞,最终导致微循环发生异常[10]。DPN 的发病机制非常复杂,一般认为与过高的血糖、胰岛素抵抗、活跃的多元醇通道、过多的氧化应激产物、晚期糖基化终产物的积累等存在密切联系[11]。机体氧化应激反应增强、葡萄糖多元醇代谢增加、神经元内酶糖基化终末产物增多,使得神经血供减少、神经细胞损伤,血管基底部增厚、血管内皮功能损伤,从而阻碍神经微循环,促进神经病变的发展,诱发DPN[12-13]。
甲状腺激素与机体多项功能密切相关,包括机体的生长、发育和能量代谢等,而且在神经系统的发育中,甲状腺激素也是不可或缺的[14]。3,5,3'-三碘甲腺原氨酸(3,5,3'-triiodothyronine,T3)可抑制感觉神经元的轴索化,刺激新的轴突产生活性神经元数量增多,神经得到修复、再生。既往动物实验发现,T3能够促进背根神经节、单纯神经元的生长[15]。甲状腺激素与DPN 密切相关,甲状腺功能减退患者体内氧化应激反应增强,自由基生成增加,合并糖尿病的患者因长期处于高血糖的环境,自由基的清除能力变差,游离自由基增多,这些自由基会攻击、损害神经,最终导致周围神经受到侵害;而且神经元DNA、神经元的蛋白质和脂质会因为增强的氧化应激反应遭到直接破坏,轴索运输和信号转导也会受到影响;此外,氧化应激使神经营养因子减少,这使得受损的神经纤维自我修复能力减弱,最终导致神经纤维的损伤[7,16]。
糖尿病患者血糖代谢紊乱,机体长期处于高血糖环境,这使得肝脏中甲状腺激素5’-脱碘酶活性减弱,甲状腺素(thyroxine,T4)脱碘转换为T3的过程受阻,导致血清总T3值下降。Vicinanza 等[17]报道甲状腺激素介导内皮细胞产生一氧化氮(nitric oxide,NO),NO 可以调节血管扩张,甲状腺激素减少会使NO 的生成减少。既往研究证明,NO 的利用率下降与内皮功能障碍有关[18-19],内皮功能障碍可引起神经供血不足,从而促进2 型糖尿病患者DPN发展[20]。在慢性高血糖状态下,T3下降会导致血管内皮功能障碍,引起神经供血不足,从而损伤周围神经。因此,甲状腺激素可以保护微血管内皮细胞,从而保护周围神经免受高血糖的侵害。
甲状腺激素在提高葡萄糖氧化速度、加快葡萄糖消耗中有积极作用[21]。葡萄糖转运进入细胞是由细胞表面的葡萄糖转运体(glucose transporters,GLUTs)负责的,甲状腺激素可以促进GLUTs 的基础表达,因此FT3升高使得细胞表面GLUTs 表达增加,更多的葡萄糖被转运进入细胞,这有利于降低血糖和改善代谢,从而减少了糖尿病并发症的发生[22]。反之,FT3的下降会影响GLUTs 的表达,葡萄糖转运进入细胞受到影响,导致血糖升高、代谢紊乱,从而促进糖尿病并发症的发生、发展。另外,T3可发动Kruppel 样因子9 表达,这个因子与髓鞘的形成相关[20]。Penza 等[23]发现甲状腺功能减退患者通过外源性补充甲状腺激素,可以改善神经病变,促进神经修复、再生。
本研究发现,DPN 组患者FT3显著低于NDPN组患者,回归分析显示FT3是DPN 的影响因素,与既往研究结果一致。分析原因可能是甲状腺激素在神经修复、再生过程中起促进作用,甲状腺功能减退导致神经修复受阻,而且甲状腺功能减退会增强体内氧化应激反应,体内自由基增多,糖尿病患者清除自由基的能力减弱,这些增多的自由基会攻击、损伤神经,因而FT3对糖尿病患者的周围神经有保护作用。
综上所述,FT3是糖尿病周围神经病的影响因素,其可能是DPN 的保护因素之一。因此,糖尿病患者积极监测FT3的变化或可为DPN 的预测提供参考,积极控制甲状腺疾病,使甲状腺功能恢复正常,这或许能够保护周围神经,延缓糖尿病周围神经病变的发生和发展。但是,本研究作为回顾性横断面研究,无法确定FT3水平与DPN 之间的因果关系,且纳入的糖尿病患者为就诊于肌电图室的患者,可能存在一定的选择偏倚,要克服这些局限有赖于更大规模的、长期的循证医学研究,以验证甲状腺激素与DPN 之间的关系。

