原发性醛固酮增多症患者使用螺内酯或依普利酮有效性与安全性的meta分析*
万瑾瑾,李 娟,2,曾 辉,刘 美,2,曾梅青,2,谢亚楠,2,敖检根,张卫芳△
(1.南昌大学第二附属医院药学部,南昌 330006;2.南昌大学江西医学院,南昌 330031;3.南昌大学第一附属医院药学部,南昌 330006)
原发性醛固酮增多症(PA)是继发性高血压的常见病因之一。研究显示,有5%~15%的高血压患者同时患有PA[1-2]。大多数PA可归因于单侧醛固酮腺瘤或双侧肾上腺增生[3]。与单纯的高血压患者相比,PA患者在心律失常、心肌梗死、中风、慢性肾病等心血管/肾脏并发症方面的发生率更高[4-7]。因此,PA患者的早期诊断和治疗对降低严重心血管并发症发生率尤为重要。
目前,PA的主要治疗方法包括手术和药物治疗,两种方式均可逆转PA导致的心血管不良事件[2]。醛固酮受体拮抗剂(ARA)为PA患者首选的治疗药物。螺内酯是第一代ARA,由于结构与性激素类似,患者易发生性激素相关药物不良反应,一定程度上限制了该药的临床使用。依普利酮是基于螺内酯研发的新药物,于2002年在美国上市,目前已在欧美、日本等地区用于原发性高血压和心肌梗死后心力衰竭的治疗[8-10],但其尚未在国内上市。最近的美国PA管理指南[2]和中国PA诊断治疗专家共识[11]中,仍建议将螺内酯作为一线药物,依普利酮作为二线药物,且对依普利酮建议的评估为较弱推荐、极低质量证据。截至目前,关于依普利酮,仅有较少样本量的临床研究数据且结果不一。有研究发现依普利酮和螺内酯降压能力相当[12],而有研究则认为螺内酯降压能力更加显著[13]。由于尚缺乏两者直接比较的大型随机对照试验(RCTs)及荟萃分析,本研究拟纳入近年来国内外对比螺内酯和依普利酮在PA患者中的临床研究进行meta分析,探讨两种药物使用过程中的有效性和安全性,以期为PA患者合理选择ARA提供循证证据。
1 资料与方法
1.1 文献纳入与排除标准
纳入标准:(1)患者明确诊断PA;(2)试验组(依普利酮组)口服依普利酮与对照组(螺内酯组)口服螺内酯;(3)临床研究。排除标准:(1)文献为meta分析;(2)同一研究人群重复发表的研究;(3)无法获得有效数据且与作者联系无果的研究;(4)试验设计不严谨或不合理的研究。
1.2 文献检索与筛选
通过检索PubMed、Cochrane图书馆、Elsevier、中国知网、万方数据库。检索时间为建库至2021年12月。英文检索词包括:spironolactone、primary aldosteronism、hyperaldosteronism、PA、clinic、patient、prospective、retrospective。中文检索词包括:原发性醛固酮增多症、原醛、螺内酯、安体舒通、临床、患者、治疗、前瞻、回顾。语种限定为中文或英文。检索所得文献由两位研究者按照纳入与排除标准,通过阅读标题及摘要进行初步筛选。对于符合纳入标准的文献,进一步通过阅读全文来判断是否纳入,必要时检索参考文献进行筛选。两位研究者意见不统一时由第3位研究人员确定。
1.3 质量评价
由于纳入的文献有RCTs和队列研究,根据Cochrane风险偏倚评估工具对RCTs研究进行质量评价和分级,评价内容共包括6条。如完全满足上述标准则发生偏倚的可能性较小,为低偏倚风险;如部分满足上述标准则为中偏倚风险;如完全不满足上述标准则为高偏倚风险。采用纽卡斯尔-渥太华量表(NOS)对队列研究进行评价,≤5分为低质量研究,>5~7分为中质量研究,>7~9分为高质量研究。
1.4 结局指标
有效性指标:(1)治疗前后收缩压变化;(2)治疗前后舒张压变化;(3)治疗前后血钾变化。安全性指标:(1)总不良反应发生率;(2)男性乳房女性化发生率;(3)高钾血症发生率;(4)不同剂量螺内酯的不良反应发生率。结局指标数据提取由两位研究者独立提取,如数据不一致由第3位研究人员仲裁。其中,对于血压变化仅有图表而无直接数据的情况,使用Engauge Digitizer 10.8提取图表中的数据。
1.5 统计学处理
采用R语言软件进行meta分析,计数资料采用风险比(RR),对纳入研究的计量资料采用加权均数差(WMD)作为分析统计量,同时应用95%置信区间(95%CI)进行描述,P<0.05为差异有统计学意义。采用Cochrane Q检验进行异质性分析,并通过I2值定量评估。若P>0.05且I2<50%,表明各项研究异质性小,采用固定效应模型分析数据;若P<0.05且I2≥50%,表明各项研究存在异质性,选择随机效应模型。
2 结 果
2.1 文献检索结果及基本特征
通过检索策略初步获得相关文献1 045篇,剔除重复文献后剩余890篇文献进行初筛。通过阅读标题和摘要剔除不符合纳入标准文献881篇,对剩余的9篇进行全文阅读,排除3篇无法获得有效数据的研究,最终纳入6篇符合要求的临床研究[12-17]。各项研究的纳入、排除标准基本一致。(1)纳入标准:18岁以上高血压男性或非孕龄女性,其中舒张压≥90 mm Hg(1 mm Hg=0.133 kPa)且≤120 mm Hg,收缩压<200 mm Hg;血钾>3.0 mmol/L且<5.0 mmol/L,比较螺内酯≤50 mg/d与>50 mg/d剂量的性激素相关不良反应发生率(男性乳房发育、男性性欲下降、乳房疼痛、月经紊乱)。(2)排除标准:曾患恶性高血压;曾接受激素治疗;肝、肾功能不足;6个月内曾经历心力衰竭、心肌梗死等严重心血管疾病。纳入的研究发表于2002—2021年,患者数量为34~210例,共573例患者。研究时长多为8~16周,给予依普利酮50~300 mg/d和螺内酯25~400 mg/d。纳入研究基本特征见表1。
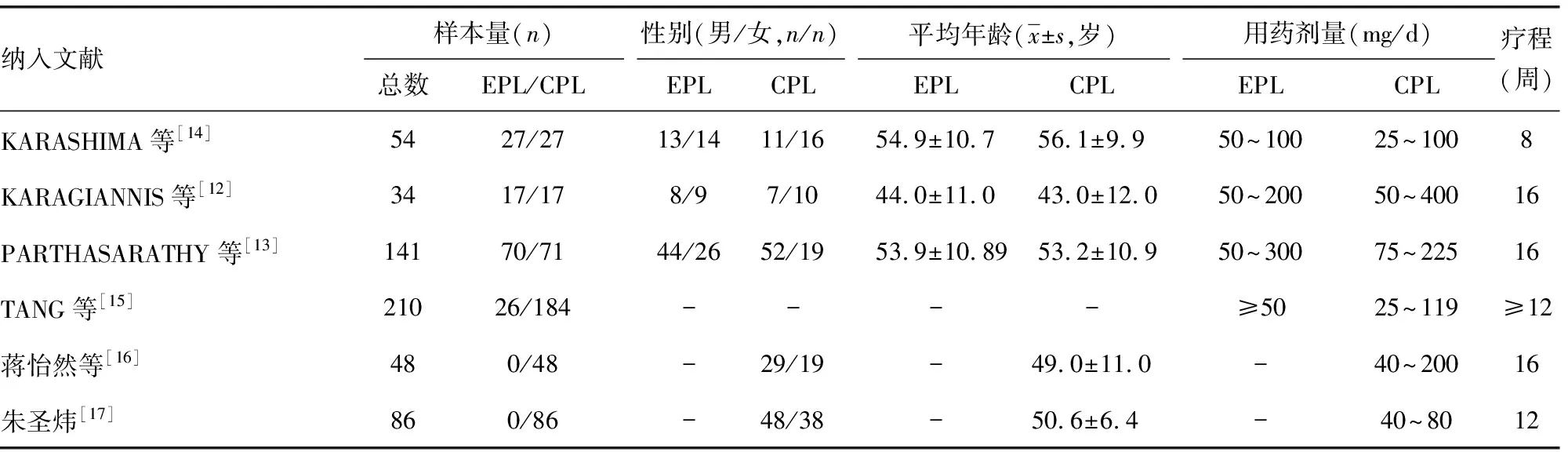
表1 纳入研究基本特征
2.2 纳入研究质量评价
纳入的6篇文献中,4篇为RCTs,2篇为队列研究。RCTs风险偏倚分析见表2,除KARASHIMA等[14]研究明确结果评估未采取盲法外,其余3个研究均无显著偏倚风险,质量较高。队列研究NOS评分≥7分,属于中高质量研究。见表3。

表2 纳入RCTs研究的风险偏倚分析
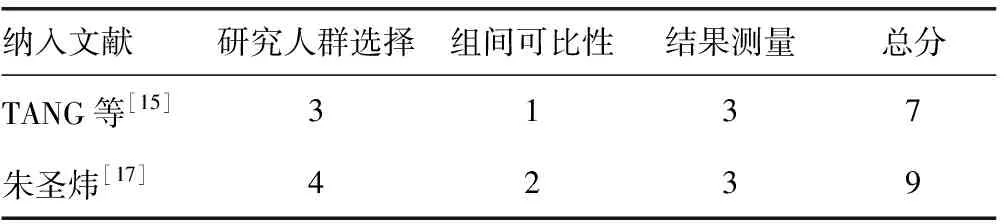
表3 纳入队列研究的NOS评分(分)
2.3 meta分析结果
2.3.1治疗前后血压变化
纳入的3项研究[12-14]异质性较大(P<0.01,I2>79%),采用随机效应模型进行分析。结果显示,螺内酯和依普利酮在降低收缩压方面比较,差异无统计学意义(MD=4.567 6,95%CI=-12.446 7~21.582 0,P=0.60);螺内酯降低舒张压效果显著高于依普利酮,差异有统计学意义(MD=4.473 4,95%CI=0.679 4~8.267 4,P=0.02)。见表4。
2.3.2治疗前后血钾水平变化
纳入的3项研究间[12-14]无异质性(P=0.94,I2=0%),采用固定效应模型进行分析。结果显示,螺内酯升高血钾的能力显著高于依普利酮(MD=-0.244 0,95%CI=-0.422 8~-0.065 1,P=0.007 5)。见表4。
2.3.3药物不良事件
药物不良事件包括总不良事件、高钾血症、男性乳房女性化及不同剂量螺内酯不良反应发生率。其中,由于各研究间[12-14]高钾血症不良反应存在较大异质性(P=0.05,I2=75%),采用随机效应模型;男性乳房女性化药物不良事件(P=0.97,I2=0%)采用固定效应模型进行分析[12-14];螺内酯的不良反应发生率(P=0.44,I2=0%)采用固定效应模型分析[15-17]。
总药物不良事件的4篇研究[12-15](P<0.01,I2=79%)存在较大异质性,其中1篇回顾性研究[15]纳入的研究对象中>50%为单侧醛固酮增多症,包括手术前用药和仅药物治疗者,其使用剂量高于双侧的醛固酮增多症患者。通常认为,>60%的PA患者为特发性醛固酮增多症(双侧醛固酮增多症),故可能存在病种亚型的异质性。该研究纳入统计的不良反应种类较多,包括低血压、低钠血症、胃肠道等,依普利酮组纳入例数明显少于螺内酯组,增加了统计数据的异质性。
两组总药物不良事件的固定效应模型存在显著性差异(RR=0.638 2,95%CI=0.492 9~0.826 2,P=0.000 7),高钾血症发生率比较差异无统计学意义(RR=0.530 7,95%CI=0.055 3~5.089 9,P=0.582 9)。使用螺内酯发生男性乳房女性化不良反应比例显著高于依普利酮,差异有统计学意义(RR=0.219 1,95%CI=0.079 3~0.605 6,P=0.003 4)。螺内酯的不良反应发生率与剂量相关,剂量≤50 mg/d时,不良反应发生率显著低于>50 mg/d,差异有统计学意义(RR=0.341 3,95%CI=0.187 2~0.622 2,P=0.000 5)。见表4。
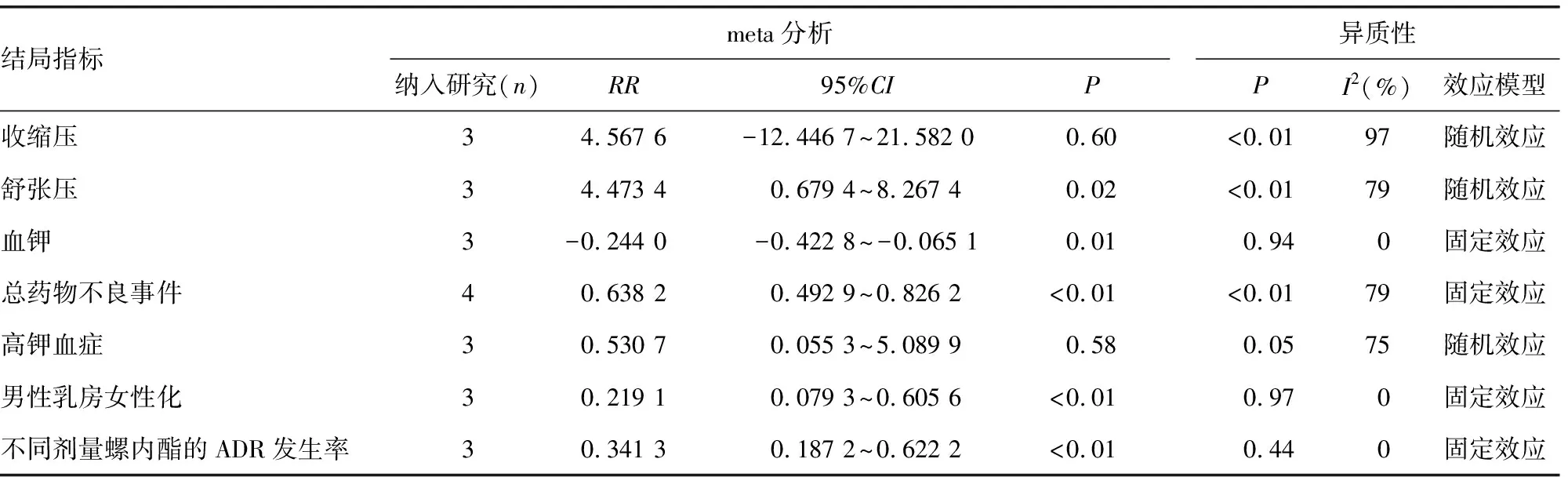
表4 依普利酮/螺内酯治疗PA的有效性和安全性meta分析
2.3.4敏感性分析和发表偏倚
通过按顺序剔除单个研究进行敏感性分析,评估降压、升高血钾及药物不良事件结果的稳定性,合并结果的方向并不随着单个研究的剔除而发生显著改变。依据Cochrane手册,由于纳入研究数量少于10项,故未对纳入的研究进行发表偏倚检测。
3 讨 论
PA是指肾上腺皮质分泌过量醛固酮,醛固酮过量导致体内代谢障碍和心脏结构异常,包括潴钠排钾、血容量增多、肾素-血管紧张素系统活性抑制,临床主要表现为高血压伴低血钾[18]。醛固酮过量也可导致心室肥厚和心脏纤维化,与原发性高血压比较,PA的预后明显不良[19]。因此,早期诊断和治疗尤为重要。指南推荐的治疗药物主要为ARA。
螺内酯是人工合成的甾体化合物,由于非选择性拮抗醛固酮受体,它在起效的同时还具有抗性激素的不良反应,导致患者体内性相关激素水平异常,男性表现为乳房发育或阳痿等,女性则表现为乳房胀痛、毛发增多、月经失调、性欲降低等。螺内酯在PA中的使用通常需要较大剂量,而大剂量的使用会增加不良反应发生率,这也使得螺内酯在这类人群中的使用受到一定限制。依普利酮是在螺内酯结构的基础上进行改造而获得的药物。经结构改造后的依普利酮可选择性抑制醛固酮受体,避免产生类似螺内酯的性激素相关不良反应[20]。但研究发现,依普利酮体内拮抗醛固酮受体的活性仅为螺内酯的50%左右[21],表明依普利酮经结构改造后,虽提高了对盐皮质激素受体的选择性,但却出现相对低的亲和力。目前,PA相关指南[2]和共识[11]虽然明确推荐优先使用螺内酯,以依普利酮作为替代治疗方案,但主要依据为仅有的2~3个直接比较且结果不一的临床研究,推荐等级和证据等级均非常低。本研究首次通过meta分析对比了螺内酯和依普利酮在PA患者中的疗效和安全性,其中纳入了3项[12-14]直接比较螺内酯与依普利酮的RCTs。结果表明,在降压方面,两种药物在降低收缩压方面的效果相当,但螺内酯降低舒张压的作用更强。螺内酯提升高血钾的作用比依普利酮更强,引起高血钾不良反应发生率与依普利酮类似,引起男性乳房女性化不良反应发生率高于依普利酮。4项研究[12-15]显示,螺内酯的总体不良反应发生率显著高于依普利酮。3项研究[15-17]对不同剂量螺内酯的不良反应发生率进行了分析,显示螺内酯的不良反应发生率与剂量相关。有研究显示,当患者不耐受螺内酯时,可选用依普利酮替代,或采用低剂量螺内酯与其他降压药物联合治疗[16]。
本研究纳入的文献全面,得出的结论可靠并具有说服力,但对于降压疗效、总不良反应结果的meta分析存在一定异质性,各纳入研究的人群特征、人群数量少,药物治疗剂量、随访终点不一致均可能是出现异质性的原因。经过筛选后,只有6篇文献符合要求,3篇对螺内酯和依普利酮的治疗结局及安全性结局进行了分析,仅其中1项研究明确指出纳入患者为特发性醛固酮增多症,其余两篇未明确细分PA亚型,导致无法进行亚组分析来降低异质性。其余3篇对不同剂量螺内酯的安全性结局及不良反应进行了分析。因此,大样本、高质量、多中心的RCTs仍然非常有必要。
目前,ARA在PA患者中的使用率仍不足。有研究表明,使用螺内酯治疗特发性醛固酮增多症可能会导致估算的肾小球滤过率相对急性下降[22],但螺内酯或依普利酮的持续使用有助于长期保存肾功能[23]。长期ARA治疗会产生心脏保护作用,降低心力衰竭相关发病率和病死率,依普利酮长期使用的耐受性优于螺内酯。因此,依普利酮可能比螺内酯更具优势,尤其是对于男性患者[23]。2021年7月,新一代ARA非奈利酮在美国上市,其在抑制醛固酮作用的同时具有心、肾双重获益,安全性良好,有望成为PA治疗的新选择。
综上所述,在PA患者中,依普利酮降压疗效不如螺内酯,但总药物不良事件发生率、男性乳房女性化发生率更低,对男性PA患者可能更具优势。螺内酯的不良反应发生率与剂量相关,但需要联合使用多种其他降压药物达到治疗目的。本研究可为PA患者个体化选择ARA提供循证证据。

