来那度胺在初诊多发性骨髓瘤患者化疗中的应用效果
蔡振杰 林武强 郑合勇 陈秀丽
多发性骨髓瘤(multiple myeloma,MM)是由浆细胞异常增殖或病理性改变引起,导致一系列组织器官损害而无法治愈的恶性血液肿瘤[1]。MM主要特征为溶骨性骨骼破坏与大量单克隆免疫球蛋白分泌,我国MM的发病率约为1/10万,发病中位年龄为69岁,随着我国人口老龄化加剧,MM患病群体日益庞大,严重影响老年人群的身心健康[2]。MM发病较为缓慢,早期并不会有特异性症状,随着病情的发展可出现相关组织或器官受损。当前对于MM尚无有效地根治性方案,一般采用化疗药物延缓病情。随着蛋白酶体抑制剂、免疫调节剂、单抗类药物与自体造血干细胞移植等手段在临床广泛应用,MM患者的预后得到了显著地提升[3]。为进一步提升初诊多发性骨髓瘤(newly diagnosed multiple myeloma,NDMM)临床疗效,延缓复发、延长生存,本研究探讨来那度胺在NDMM中的应用效果,现报道如下。
1 资料与方法
1.1 一般资料
选择福建省莆田市第一医院血液科2019年6月—2022年5月收治的NDMM患者80例,采用随机数字表法分为VTD组与VRD组,每组各40例,VTD组男29例,女11例。年龄59~77岁,平均(68.56±3.87)岁;Durie-Salmon分期:Ⅱ期13例,Ⅲ期27例。VRD组男27例,女13例;年龄61~79岁,平均(68.81±3.98)岁;Durie-Salmon分期:Ⅱ期16例,Ⅲ期24例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究患者签署知情同意书,并经医院医学伦理委员会批准开展。
1.2 纳入与排除标准
纳入标准:(1)MM诊断符合《中国多发性骨髓瘤诊治指南(2017年修订)》[4]中相关依据,且为初次确诊;(2)患者肾功能正常;(3)Durie-Salmon分期[5]Ⅱ~Ⅲ期;(4)预计生存期>6个月;(5)患者知晓病情,经与家属协商后自愿参与。排除标准[6]:(1)全身状况差,合并重大系统性疾病;(2)精神疾病、其他恶性肿瘤;(3)会造成M蛋白变化的疾病,如浆细胞白血病等;(4)已出现溶骨性病变;(5)对本研究拟用药物过敏或过敏性体质;(6)依从性差,未完成治疗的患者。
1.3 方法
VTD组化疗方案:硼替佐米(正大天晴药业集团股份有限公司,国药准字H20183261,规格:1 mg)在化疗的第1、4、8、11天静脉注射,1.3 mg/m2;沙利度胺(常州制药厂有限公司,国药准字H32026129,规格:25 mg)100 mg/d,口服;地塞米松磷酸钠注射液(河南瑞宏制药股份有限公司,国药准字H41020330,规格:5 mg)在化疗的第1、2、4、5、8、9、11、12天静脉注射,20 mg。
VRD组化疗方案:硼替佐米(正大天晴药业集团股份有限公司,国药准字H20183261,规格:1 mg)第1、4、8、11天静脉注射,1.3 mg/m2;来那度胺(正大天晴药业集团股份有限公司,国药准字H20193006,规格:25 mg)25 mg,第1~14天;地塞米松磷酸钠注射液(河南瑞宏制药股份有限公司,国药准字H41020330,规格:5 mg)在化疗的第1、2、4、5、8、9、11、12天静脉注射,20 mg。
两组治疗过程中进行血常规、心电图、免疫功能、肝肾功能等监测,给予保肝、护胃、营养神经等对症处理;疗程均为28 d,如果发生无法耐受的不良反应则需停药,待患者状况好转后继续疗程。
1.4 观察指标
比较两组临床疗效、细胞免疫指标、炎症因子水平及不良反应发生情况。(1)临床疗效[7],完全缓解(complete relief,CR):经检验,患者血清、尿免疫固定电泳结果呈阴性,软组织浆细胞瘤消失,骨髓中浆细胞低于5%;部分缓解(partial relief,PR):经检验,患者血清M蛋白下降≥50%,24 h尿M蛋白下降≥90%或水平低于200 mg;微缓解(micro-relief,MR):未达到上述标准,但无新增骨质病变或原有骨质病变未进展。临床总有效率=(CR+PR)例数/总例数×100%。(2)细胞免疫指标,治疗前后采用流式细胞仪测定外周血淋巴细胞中CD3+、CD4+、CD4+/CD8+水平。(3)炎症因子水平:治疗前后抽取静脉血5 mL,采用酶联免疫吸附试验测定IL-6、IL-17、TGF-β水平。(4)不良反应:贫血、血小板减少、周围神经病变、感染、中性粒细胞减少、恶心、呕吐,治疗过程中发生则记录。
1.5 统计学方法
本研究数据应用统计学软件SPSS 23.0处理,计量资料以(±s)表示,采用t检验;计数资料采用n(%)表示,采用χ2检验,P<0.05为差异有统计意义。
2 结果
2.1 两组临床疗效比较
VRD组临床疗效总有效率高于VTD组,差异有统计学意义(P<0.05)。具体见表1。

表1 两组临床疗效比较[例(%)]
2.2 两组化疗前后免疫功能比较
两组化疗前免疫功能比较,差异无统计学意义(P>0.05),化 疗 后VRD组CD3+、CD4+、CD4+/CD8+水 平 高于VTD组,差异有统计学意义(P<0.05);两组化疗后CD3+、CD4+、CD4+/CD8+水平高于化疗前,差异有统计学意义(P<0.05)。具体见表2。
表2 两组化疗前后免疫功能比较 (±s)

表2 两组化疗前后免疫功能比较 (±s)
注:与同组化疗前比较,aP<0.05。
组别 例数 CD3+(%) CD4+(%) CD4+/CD8+化疗前 化疗后 化疗前 化疗后 化疗前 化疗后VRD组 40 30.16±4.13 44.02±3.22a 56.62±6.18 68.19±5.11a 1.12±0.22 1.75±0.51a VTD组 40 29.94±3.96 34.71±3.20a 57.25±6.33 62.34±5.30a 1.08±0.17 1.27±0.41a t值 - 0.243 12.971 0.450 5.026 0.910 4.639 P值 - 0.809 <0.001 0.654 <0.001 0.366 <0.001
2.3 两组化疗前后炎症因子水平比较
两组化疗前炎性因子水平比较,差异无统计学意义(P>0.05),化疗后VRD组IL-6、IL-17、TGF-β水 平 低于VTD组,差异有统计学意义(P<0.05);两组化疗后IL-6、IL-17、TGF-β水平低于化疗前,差异有统计学意义(P<0.05)。具体见表3。
表3 两组化疗前后炎症因子水平比较 (pg/mL,±s)
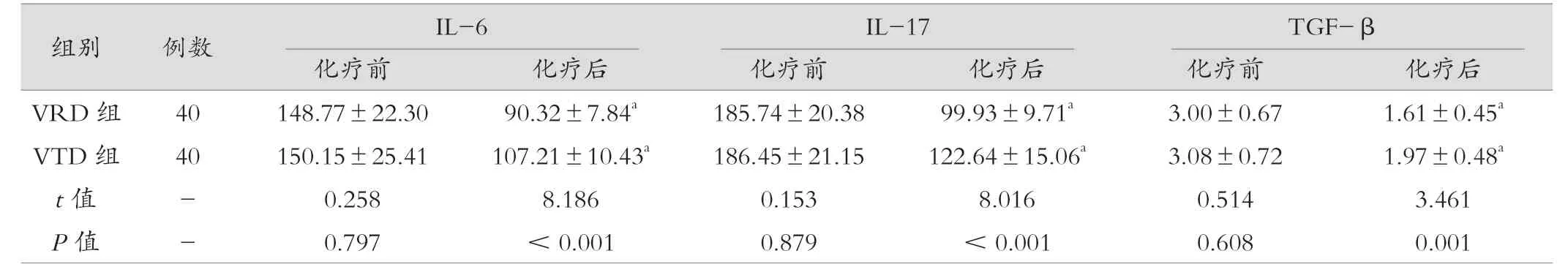
表3 两组化疗前后炎症因子水平比较 (pg/mL,±s)
注:与同组化疗前比较,aP<0.05。
组别 例数 IL-6 IL-17 TGF-β化疗前 化疗后 化疗前 化疗后 化疗前 化疗后VRD组 40 148.77±22.30 90.32±7.84a 185.74±20.38 99.93±9.71a 3.00±0.67 1.61±0.45a VTD组 40 150.15±25.41 107.21±10.43a 186.45±21.15 122.64±15.06a 3.08±0.72 1.97±0.48a t值 - 0.258 8.186 0.153 8.016 0.514 3.461 P值 - 0.797 <0.001 0.879 <0.001 0.608 0.001
2.4 两组化疗期间不良反应情况比较
VRD组不良反应发生率虽低于VTD组,但差异无统计学意义(P>0.05)。具体见表4。
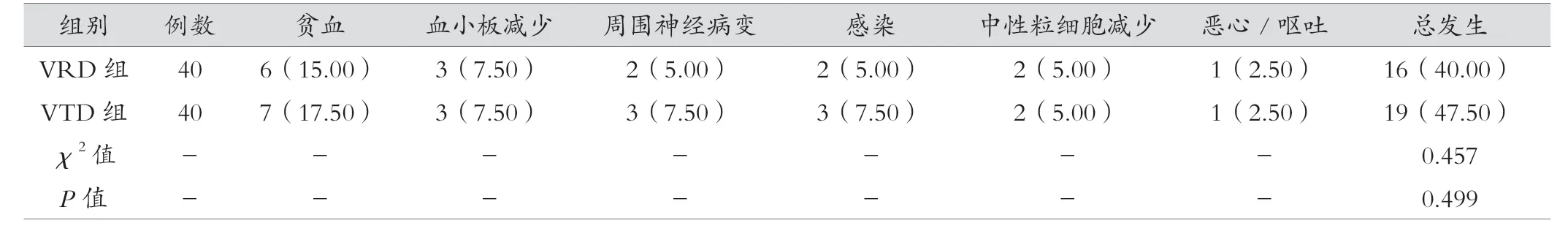
表4 两组化疗期间不良反应情况比较[例(%)]
3 讨论
MM在血液系统恶性肿瘤中发病率高达10%以上,好发于老年人群,严重影响患者生命健康与晚年生活质量。MM的早期预后较差,治疗方案有限,只能依靠化疗延缓病情。硼替佐米为哺乳动物细胞中26 s蛋白酶体类糜蛋白酶活性的可逆抑制剂,能够对泛素化蛋白质产生降解作用,而蛋白质是多种癌细胞生存与增殖的基础,硼替佐米通过抑制泛素-蛋白酶体途径抑制糜蛋白酶活性与胰蛋白酶活性,加速癌细胞的凋亡;此外,硼替佐米还可以对转录因子核因子κB通路激活产生抑制作用[8]。但近年研究[9]显示,硼替佐米单药疗效不及硼替佐米联合用药。
目前对于NDMM患者有多种联合化疗方案,其中三药联合方案中,国内外报道均发现VRD方案具有较好的临床应用效果,但由于医保政策与药物普及性等方面原因,VRD方案在NDMM患者中的应用报道较少,VRD方案与VTD方案在NDMM患者中的应用比较更少。本研究结果显示,VRD组临床疗效总有效率高于VTD组,差异有统计学意义(P<0.05),提示来那度胺在NDMM患者中应用临床疗效显著。来那度胺属第2代免疫调节剂,能够通过多靶位攻击浆细胞微环境,促进肿瘤细胞凋亡,从而发挥免疫调节和抑制血管生成的双重作用,且来那度胺的不良反应发生率较低,对神经的影响甚小。鉴于来那度胺的疗效显著及安全性,越来越多的学者将其用于MM的临床治疗中。王文秀等[10]对100例NDMM患者采用RVD连续治疗情况进行回顾性分析(随访时间2~57个月),其随访结果发现,来那度胺联合硼替佐米及地塞米松的治疗方法具有良好的疗效与安全性。马鸿雁等[11]对40例MM患者采用RVD治疗方案进行治疗2个月后发现,患者的免疫功能较硼替佐米联合地塞米松的对照组明显改善,与本研究化疗后VRD组CD3+、CD4+、CD4+/CD8+水平高于VTD组,差异有统计学意义(P<0.05)的结果基本一致。范丽等[12]开展的一项meta分析中纳入了4 007例MM患者,研究组采用来那度胺或联合地塞米松治疗,对照组采用安慰剂、地塞米松或联合治疗,研究结果显示,研究组发生严重感染风险较高,特别是呼吸道严重感染,其认为在MM患者中应用来那度胺治疗应密切关注患者的感染情况。本研究结果显示化疗后VRD组IL-6、IL-17、TGF-β水平低于VTD组,差异有统计学意义(P<0.05),提示与VTD化疗方案比较,VRD化疗方案可下调炎症因子水平。本研究结果中发生2例感染,但并非呼吸道感染,也未发生严重感染,可能与药物治疗方案、样本量、治疗周期等差异不同有关。王国苗等[13]的一项收集中国12家医院165例MM患者接受来那度胺治疗的多中心非干预性前瞻性观察研究也发现,在≥3级的副作用中白细胞减少11.5%,血小板减少12.7%,中性粒细胞减少12.7%,并未发生严重感染。罗曼等[14]研究也证实,来那度胺在MM患者长期维持性治疗中具有良好的效果与安全性。
综上所述,来那度胺在NDMM患者中应用临床疗效显著,与VTD化疗方案比较,VRD化疗方案能改善患者免疫功能与下调炎症因子水平。本研究结果为中国多发性骨髓瘤诊治指南后期标准制定提供了借鉴。

