脓毒症合并急性肾损伤生存预后列线图预测模型的构建与验证
林泽华 黎代强 陈琳
脓毒症是由明确或可疑感染引起的全身性炎症反应综合征,宿主对感染反应失调会导致多器官功能障碍,危及患者生命[1]。急性肾损伤(AKI)在脓毒症中的发病率约为20%,可使脓毒症死亡率升高[2]。脓毒症合并AKI的生存预后与血流动力学改变、炎性因子、疾病严重程度等因素有关,控制这些因素有利于改善患者预后,降低死亡风险[3]。目前临床尚缺乏一种便捷、可视化、高效率的脓毒症合并AKI预后风险评估手段[4]。列线图将logistic回归分析结果图形化,能直观描述多个预测变量之间的量变关系,使临床医生实现快速评估预后风险,对后期实施针对性干预措施并改善预后具有重要意义。基于此,本研究旨在建立可视化的脓毒症合并AKI预后列线图预测模型,为临床方便、快速识别高风险患者提供参考。
对象与方法
1.对象:回顾性纳入2016年10月~2021年4月在本院ICU治疗的192例脓毒症合并AKI患者。纳入标准:(1)符合脓毒症和AKI的诊断标准[5];(2)年龄≥18岁;(3)治疗依从性较好;(4)电子病历、随访资料完整。排除标准:(1)ICU住院时间≤24 h或入院后立即进行透析治疗;(2)合并尿毒症、代谢性疾病、血液系统疾病、恶性肿瘤;(3)由肾血管性、肾小管性、肾小球性等因素引起的AKI;(4)既往存在肾功能不全。本研究已经过我院医学伦理委员会审核批准。
2.方法:查阅患者电子病历及随访信息,收集临床资料,包括性别、年龄、BMI、AKI分期、合并低蛋白血症情况、肌酐(Cr)、血钾、急性生理学和慢性健康状况评分系统Ⅲ(APACHE Ⅲ)评分、尿量、液体平衡量、器官衰竭数量、使用血管活性药物情况、机械通气、输注血液制品、ICU住院时间、PLT计数、降钙素原(PCT)、血清白蛋白(ALB)、C反应蛋白(CRP)、国际标准化比值(INR)、乳酸(LA)、辅助性T细胞(Th)17、IL-17、可溶性髓样细胞触发受体-1(sTREM-1)、血管生成素-2(Ang-2)、B型钠尿肽(BNP)。统计患者生存预后情况,以患者入住ICU时间为观察起点,以死亡为截止事件,随访时间最长为28 d。根据随访截止时的预后情况将192例患者分为死亡组88例(45.83%)和存活组104例(54.17%)。
结 果
1.两组患者临床资料比较:死亡组AKI 3期、合并低蛋白血症、器官衰竭数量>3 个、机械通气患者比例及Cr、Th17、IL-17水平、液体平衡量、ICU住院时间均高于存活组,AKI 1期患者比例及ALB水平均低于存活组(P<0.05),两组患者其余项目比较差异均无统计学意义(P>0.05)。见表1。
表1 两组患者临床资料比较
2.脓毒症合并AKI预后的多因素logistic回归分析:多因素logistic回归分析结果显示,AKI分期(2期、3期)、ICU住院时间、Th17、IL-17水平及液体平衡量是脓毒症合并AKI预后的独立影响因素(P<0.05)。见表2。
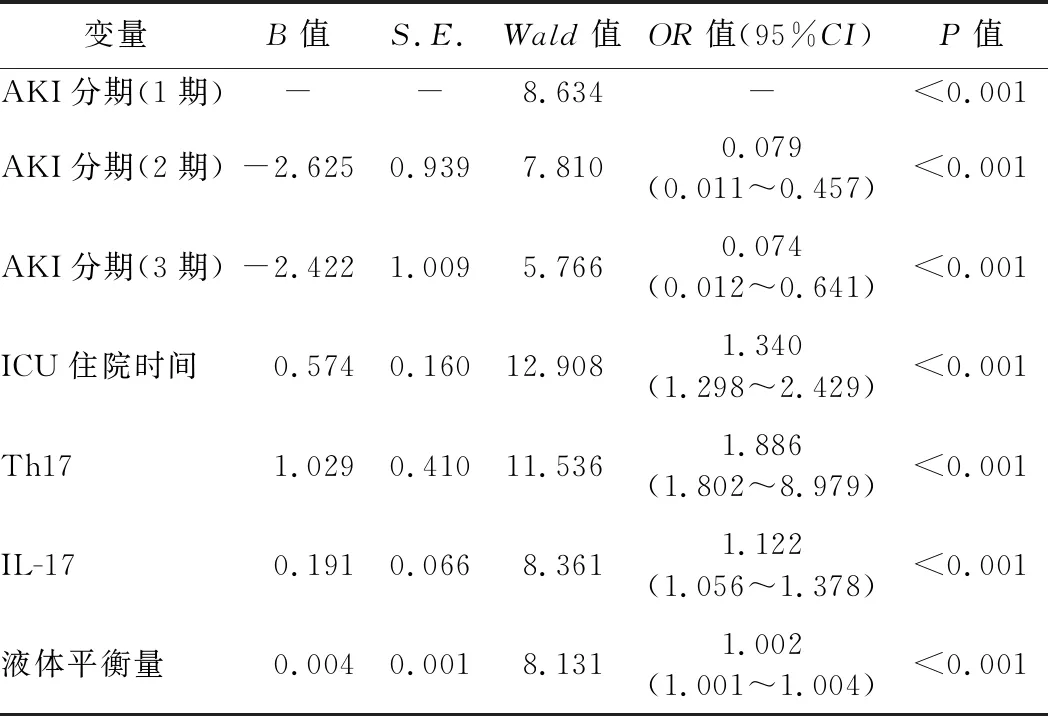
表2 脓毒症合并AKI预后的多因素logistic回归分析
3.列线图预测模型的建立及内部验证:将多因素logistic回归分析中的独立影响因素作为预测变量,建立脓毒症合并AKI预后列线图预测模型。见图1。预测模型经内部验证,CI=0.864,其预测脓毒症合并AKI预后校正曲线趋势接近理想曲线,模型内部验证前后平均绝对误差为0.031。ROC曲线分析结果显示,预测模型预测脓毒症合并AKI预后的ROC曲线下面积(AUC)、敏感度、特异度分别为0.864(95%CI0.805~0.905)、0.795、0.798。见图2。经Hosmer-Lemeshow拟合优度检验,该模型的风险预测值与实际值的χ2=11.598,P=0.170。
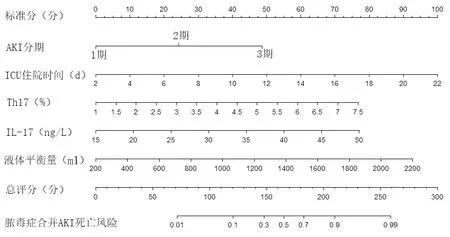
图1 脓毒症合并AKI预后的列线图预测模型

图2 脓毒症合并AKI预后的列线图预测模型预测效能的ROC曲线
讨 论
脓毒症合并AKI患者入住ICU后28 d死亡率较高,本研究结果显示,192例患者死亡率为45.83%,与张玲等[6]研究报道的46.15%相近。建立脓毒症合并AKI预后可视化列线图预测模型,对疾病早期甄别、干预及减少死亡均具有指导意义。
本研究中脓毒症合并AKI预后的独立影响因素与既往研究不同,可能与研究对象的纳入与排除标准及随访时间不同有关[7]。脓毒症发生AKI的病理基础包括肾脏微循环障碍、免疫炎性损伤、凝血级联反应激活、肾小管上皮细胞适应性反应等[8-9]。AKI分期越高,提示患者肾功能损伤越严重,死亡风险越高。临床上需加强高AKI分期诊断和治疗力度,争取治疗时机,以延缓AKI进展恶化。患者ICU住院时间延长,预示其病情加重,全身炎症反应和AKI同时侵害患者全身系统功能,升高死亡风险。此外,长期入住ICU可可使呼吸机相关性肺炎、导管相关性感染等并发症的发生率及病死风险升高[10]。脓毒症的发生和发展与淋巴细胞刺激炎症反应并调节免疫应答有关。Th17可分泌IL-17和IL-22,对抗细胞外细菌和霉菌,具有免疫防御功能。Th17在脓毒症机体中高表达,对脓毒症的早期诊断具有较高的敏感度和特异度[11]。Th17水平升高,大量炎症细胞浓集于感染区域,使炎症反应和脓毒症病情加重,增高死亡率。IL-17为致炎细胞因子,可激活T细胞,刺激内皮细胞、上皮细胞、成纤维细胞产生细胞因子,如化学增活素、IL-8、IL-6等,上述细胞及细胞因子协同介导炎症的发生和发展。可见IL-17水平偏高,炎症反应剧烈,脓毒症加重,对全身脏器造成器质性损伤,导致其功能衰退,患者死亡风险升高。本研究结果中,死亡组患者Th17及IL-17水平均明显高于存活组,与庞玉洪等[12]的研究一致。多因素logistic回归分析结果显示,Th17和IL-17是脓毒症合并AKI死亡的影响因素,因此临床应密切关注Th17和IL-17水平异常患者,及时采取干预措施控制炎症反应,降低病死风险。相关研究表明,液体复苏可减弱内毒素介导的肿瘤坏死因子-α、IL-8及IL-1β等促炎性因子合成,升高抗炎介质IL-10水平[13]。液体平衡常被应用于脓毒症合并AKI的辅助治疗,但过度液体输入可引起组织器官水肿,增大氧弥散距离,阻碍微循环,进而诱发多脏器功能障碍,提高死亡率[14]。郭妍妍等[15]研究表明,液体超负荷会提高脓毒症性AKI的病死率。因此,临床应合理控制液体平衡量,避免因液体超负荷引起组织器官损伤而导致患者死亡。
近年来,列线图预测模型表现出良好的预测效能[16]。本研究建立脓毒症合并AKI预后列线图预测模型,其预测的AUC、特异度及敏感度均较高,说明该模型具有较高的预测价值。Hosmer-Lemeshow拟合优度检验结果显示该模型的风险预测值与实际值之间比较差异无统计学意义,说明模型预测效能较好。列线图应用中运算较简单,评估过程简便、快速。临床医生可通过查阅患者一般资料、病历资料及血常规检查结果获取模型预测变量信息,无需额外增加检测或复查项目即可获得列线图应用的前期数据,能节省预测时间,实现快速评估,使更多患者受益。由于本研究样本量较小,可能导致结果存在偏倚,后续还需更大样本量的研究进一步证实。本研究中的列线图预测模型仅经过内部验证,缺乏来自外部中心数据的外部验证,故该模型在推广应用前还需更多外部证据支持。
综上所述,AKI分期、ICU住院时间、Th17、IL-17水平、液体平衡量均可影响脓毒症合并AKI的预后,基于上述指标建立的列线图预测模型预测效能较好,具有一定的临床适用性。

