细胞程序性死亡在骨质疏松症中的研究进展
海云翔 巩彦龙 宋敏* 董万涛 蒋宜伟 王凯
1.甘肃中医药大学,甘肃 兰州 730000
2.甘肃中医药大学附属医院,甘肃 兰州 730000
骨质疏松症(osteoporosis,OP)是以骨量低下,骨组织微结构损坏,骨脆性增加,易发生骨折为特征的全身代谢性骨病[1]。OP与增龄相关,随着人口老龄化进程加快,OP已成为影响我国老年人群生活质量、加重社会财政负担的重大公共卫生问题。细胞程序性死亡(programmed cell death,PCD)包括经典的凋亡(apoptosis)和新近发现的坏死性凋亡(necroptosis)、铁死亡(ferroptosis)、焦亡(pyroptosis)等。研究表明,PCD在OP的发生发展中具有重要的作用[2-3]。在某些因素作用下,PCD的失衡使骨代谢微环境的调节处于紊乱状态,进而造成骨代谢过程中骨形成与骨吸收所处的动态平衡被打破,最终导致OP发生。本文就上述细胞程序性死亡方式与OP的相关研究进行综述,为今后基础研究及临床工作提供更多的参考。
1 细胞程序性死亡概述
早期研究发现细胞受某些基因或蛋白调控造成自然死亡。1964年科学家首次使用PCD来描述昆虫在发育过程中存在细胞自然死亡现象[4],Kerr等[5]定义了凋亡、坏死多种细胞死亡方式。PCD组织内无死亡细胞溶解,无可见的炎症反应,是机体细胞通过信号转导通路主动介导的自发性、程序性死亡方式[6],能够被相应的信号通路抑制剂阻断,主要包括细胞凋亡、焦亡、铁死亡、坏死性凋亡等。其中凋亡和焦亡属PCD死亡机制中的半胱氨酸天冬氨酸蛋白酶(caspase)依赖型,坏死性凋亡、铁死亡及其他程序性坏死方式属非caspase依赖型。PCD的紊乱与心血管系统、自身免疫性疾病、肿瘤及退行性疾病的发生紧密相关。因此,细胞程序性死亡使人类对多种疾病的防治机制有了新的研究方向。
2 细胞程序性死亡与骨质疏松症
2.1 细胞凋亡与骨质疏松症
凋亡是机体在特定基因或通路调控下,为维持自身内环境稳态而有序引发的细胞死亡过程,主要包括死亡受体(TNFR、Fas等)调控的外源性凋亡途径和线粒体调控的内源性凋亡途径[7]。不同的凋亡途径都须经过caspase家族成员介导的不可逆有限水解底物的级联放大反应过程作用于底物从而诱导细胞凋亡[8]。
OP是人体在衰老过程中因增龄性氧化应激、雌激素减少引起免疫系统低度活化,从而产生大量炎症介质[9],这种机制可能诱发成骨细胞内凋亡加速,破坏骨生理平衡。肿瘤坏死因子受体1(TNFR1)作为广谱表达的细胞膜受体,可与其配体肿瘤坏死因子α(TNF-α)相互作用介导信号传递,两者结合激活下游基因及复合物Ⅱ的形成介导细胞凋亡[10]。活化成骨细胞膜上的死亡受体Fas和TNFR可使成骨细胞发生凋亡[11],雌激素可通过热休克蛋白27(HSP27)减少TNF-α诱导的成骨细胞凋亡,同时经Fas配体途径诱导破骨细胞凋亡进而保护骨骼[12-13]。
OP形成过程中涉及线粒体途径凋亡的信号通路包括PI3K/Akt、ERK5、JNK、Wnt/β-catenin、NF-κB、P38等,各信号通路间交互影响,调节线粒体途径中caspase、BcL-2家族蛋白等关键靶点,影响成骨细胞凋亡[14]。表达于成骨细胞的骨保护素(osteoprotegerin,OPG)可通过阻断核因子κB受体活化因子配体(RANKL)和RANK的结合,抑制破骨细胞的分化和活性[15]。OPG可诱导破骨细胞和破骨细胞前体细胞中细胞色素从线粒体中释放,激活caspase-3与caspase-9,使凋亡相关因子(AIF)和线粒体核酸内切酶G(GEndo G)发生核转位,从而诱导凋亡发生[16]。骨髓线粒体蛋白(OPA)是一种新发现的线粒体跨膜蛋白,OPA的下调通过诱导线粒体ATP产生和抑制P38信号通路来抑制细胞凋亡并改善OP[17]。凋亡在骨代谢微环境中受不同基因或蛋白调节,通过凋亡途径维持成骨细胞和破骨细胞供应速率,纠正细胞数量不平衡,对骨代谢稳态具有重要意义。
2.2 坏死性凋亡与骨质疏松症
坏死性凋亡是区别于凋亡和坏死的新型细胞死亡模式。既与凋亡相类似,严格遵循细胞内信号通路调控,又具备坏死的形态特征[18]。作为非caspase依赖型死亡方式,可在细胞内不存caspase信号转导因子的情况下,通过死亡受体(TNFR、Toll样受体、Fas、干扰素受体)与配体结合触发细胞死亡程序[19],目前,TNFR介导的坏死性凋亡研究最为深入。当与TNF-α结合后,死亡受体TNFR1激活并在胞质端招募下游蛋白分子受体相互作用蛋白激酶1(RIPK1)、肿瘤坏死因子受体相关因子(TRAF2)、肿瘤坏死因子受体相关死亡域蛋白(TRADD)、细胞凋亡抑制蛋白(cIAPs)等信号分子聚集,并在胞膜上形成复合物Ⅰ[20-21],复合物Ⅰ根据接收的信号刺激对RIPK1进行不同修饰,引起凋亡或坏死性凋亡[22]。Caspase-8在此过程中扮演重要的角色,当细胞内促死亡蛋白RIPK1募集pro-Caspase-8、TRADD等形成复合物Ⅱa时,Caspase-8被激活,RIPK3活化受到抑制,诱导细胞走向凋亡。当Caspase-8缺失或活性减低时,促使RIPK1去泛素化并与相关死亡结构域蛋白(RIPK3、Fas)结合形成复合物Ⅱb,招募且磷酸化MLKL执行坏死性凋亡。
细胞凋亡在骨重塑中起关键作用[23],那么坏死性凋亡是否也参与了这一过程。研究发现,去卵巢(OVX)大鼠骨细胞中RIPK1、RIPK3水平较假手术组显著增加[24],坏死性骨细胞数量与OVX大鼠中TNF-α的产生呈正相关,TNF-α通过RIPK1/RIPK3途径调节下游关键信号分子MLKL及线粒体分裂调节蛋白(Drp1),促使骨细胞发生坏死性凋亡,给予特异性坏死性凋亡抑制剂Necrostatin-1 (Nec-1)后,RIPK1和RIPK3表达显著降低,并在体外抑制 TNF-α诱导的骨细胞坏死性凋亡,延缓骨组织微结构退变[25-26]。上述表明,坏死性凋亡加速了雌激素缺乏诱导的OP大鼠骨细胞丢失,Nec-1在减轻骨质流失方面的作用可能与其在雌激素缺乏诱导的OP大鼠模型中抑制TNF-α诱导的骨细胞坏死性凋亡有关。此外,Nec-1可通过抑制RIPK1/RIPK3/MLKL信号通路中RIPK1的表达减轻糖皮质激素和乙醇诱导的成骨细胞坏死性凋亡,促进骨形成,可见坏死性凋亡在糖皮质激素诱导的OP及酒精性OP的发病机制中亦有重要作用[27-28]。目前,坏死性凋亡与OP的相关研究尚处于初始阶段,未见Caspase、PIPK3、MLKL等中下游因子激活和抑制与OP的相关报道,这为后续研究提供了新的方向。
2.3 铁死亡与骨质疏松症
铁死亡是铁离子依赖的脂质过氧化物增多导致的细胞死亡形式,Dixon等[29]报道铁死亡后,铁死亡在细胞代谢过程中的重要作用正在逐步被发掘。在机体的病理变化过程中,当细胞胱氨酸运输蛋白受到抑制(如IKE、Erastin、炎症刺激等),胞内谷胱甘肽的耗尽导致谷胱甘肽过氧化物酶(GPX4)失活,当活性氧(reactive oxygen species,ROS)积累到一定程度可诱发细胞死亡。近年来发现辅酶Q(CoQ)氧化还原酶铁死亡抑制蛋白1(FSP1)在铁死亡中可与GPX4起相似的作用[30],这一研究结果进一步丰富了对铁死亡机制的认识。铁代谢广泛参与骨的生长和生产,在OP发生的病理变化过程中,成骨细胞内铁蛋白的磷酸化过程是通过抑制GPX4和XC-系统,导致半胱氨酸代谢的破坏和脂质过氧化的增强,过度活跃的Fenton反应产生大量ROS,导致成骨细胞死亡,进而造成骨代谢过程中骨形成与骨吸收动态平衡被破坏,最终形成OP(图1)[31]。
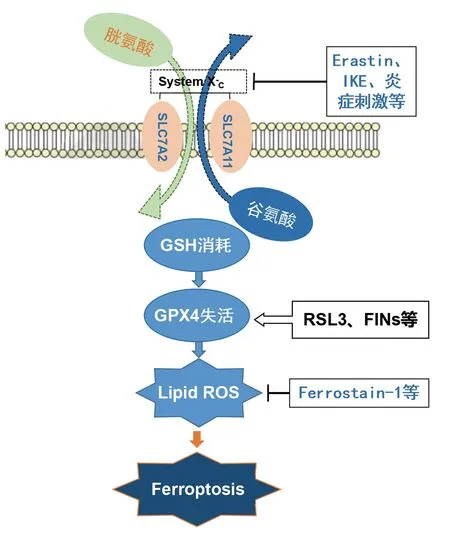
图1 GPX4依赖的细胞内铁死亡示意图Fig.1 Schematic diagram of GPX4-dependent intracellular ferroptosis
众所周知,长期大剂量类固醇治疗会改变抗氧化能力,降低成骨细胞的活力和功能,导致骨质疏松和骨坏死发生。研究表明,在大剂量糖皮质激素诱导的股骨头坏死过程中,糖皮质激素可能参与了破坏GPX4,引起成骨细胞、破骨细胞、软骨细胞和骨髓间充质干细胞中氧化应激的变化,推测类固醇激素可能诱发骨重建相关细胞的铁依赖性或激活铁依赖性信号通路,若能逆转铁依赖性通路的激活,可防止这些细胞遭受死亡或损伤[32]。由血管内皮细胞分泌的外泌体(EC-Exos)可通过抑制铁蛋白吞噬依赖性铁死亡,逆转糖皮质激素诱导的成骨细胞成骨抑制以拮抗OP的发生[33]。线粒体铁蛋白(FtMt)是一种在线粒体中储存铁离子并拦截有毒亚铁离子的蛋白质,Wang等[34]通过慢病毒沉默及过表达FtMt,观察了其对铁死亡和成骨细胞功能的影响,结果表明FtMt的过表达降低了高糖条件下成骨细胞的铁死亡,而沉默的FtMt通过ROS/PINK1/Parkin通路诱导线粒体自噬,进一步激活并增加成骨细胞中铁死亡,由此发现了FtMt通过减少过量亚铁离子引起的氧化应激来抑制成骨细胞中铁死亡的发生。铁死亡作为一种重要的细胞代谢过程,在代谢微环境中受不同信号及物质的精细调节,GPX4是其经典的调节途径,在OP低度氧化应激、雌激素减少病理变化过程中,成骨细胞内GPX4参与铁代谢途径调节铁死亡,进而保持成骨细胞内环境的稳态平衡,减少成骨细胞的死亡,对骨代谢平衡具有重要的作用。
2.4 细胞焦亡与骨质疏松症
细胞焦亡是由Gasdermin介导的以细胞胀大至膜破裂,导致内容物释放引起强烈的炎症反应。当机体发生病变时,促使炎症小体形成,被激活的Caspase切割GSDMs蛋白释放出其N端结构域,GSDMD-N通过成孔活性介导细胞焦亡[35](图2)。Shi等[36]研究发现GSDMD只存在于细胞焦亡的途径中,GSDME在Caspase-3的切割下能将TNF-α诱导的细胞凋亡转向细胞焦亡[37]。由Gasdermin介导的细胞焦亡对于年龄因素、雌激素缺乏、高血糖、免疫等引发的骨质疏松症的骨重建有不利影响[38],其对成骨细胞的分化及增殖的详细机制尚不清楚,但在此过程中均有炎症因子的参与[39],炎症因子被细胞识别后,能被Caspase-1介导并活化,通过复杂的调控机制发生细胞焦亡过程,细胞焦亡反过来亦会触发炎症小体,通过促进受损伤的免疫细胞死亡来调节骨细胞稳态[40]。
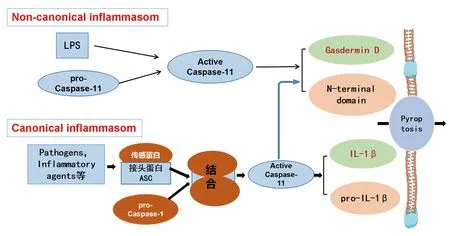
图2 GSDMD依赖的细胞焦亡示意图Fig.2 Schematic diagram of GSDMD dependent pyroptosis
阿仑膦酸盐(ALN)是一种含氮双膦酸盐(NBP)的抗骨质疏松药物,其在抗OP的同时,又有引起颌骨坏死的不良反应,Tamai等[41]在研究中发现,NBP在体内外均能诱导成骨细胞、破骨细胞死亡,这种死亡是细胞内Nod样受体家族NLRP3被激活并表达,而NLRP3炎症小体的异常激活不仅会产生炎症,同时通过上调Caspase-1和gasdermin D(GSDMD)的表达导致成骨细胞的焦亡和功能障碍,活化的Caspase-1将底物蛋白GSDMD切割为GSDMD-N,进而介导了颌骨中成骨细胞焦亡。Cheng等[42]在研究急性根尖牙周炎(AP)时发现,服用VX-765后牙槽骨的骨丢失减少,这是VX765通过抑制Caspase-1、IL-1β、单核细胞趋化蛋白-1(MCP-1)、IL-6和IL-8等的表达,从而降低了GSDMD的表达,最终抑制了牙槽骨中成骨细胞的焦亡。Yang 等[43]研究发现,高糖可通过Caspase-1/GSDMD/IL-1β途径激活糖尿病患者牙槽骨的成骨细胞焦亡,进而抑制牙槽骨成骨细胞的增殖和分化,这为糖尿病患者牙槽骨疾病的临床治疗及骨代谢提供理论依据。在OP引起骨代谢失衡的低度氧化应激、雌激素减少病理过程中,通过Caspase-1细胞焦亡通路和Caspase-4/5/11细胞焦亡通路对底物蛋白GSDMD进行激活,进而调控成骨细胞焦亡,对骨代谢平衡具有重要的作用。
3 细胞程序性死亡交互影响与骨质疏松症
尽管凋亡、坏死性凋亡、铁死亡及焦亡之间的信号转导通路不同,但它们并非是平行、没有重叠的,这些不同细胞死亡途径间紧密联系且相互调节,存在着“crosstalk”的物质基础。如细胞在TNF及氧化因子的作用下促使线粒体释放凋亡因子诱导细胞发生凋亡,当Caspase-8被抑制又可引发细胞坏死性凋亡[44],细胞中存在的GSDME蛋白又会使细胞从凋亡迅速转向焦亡[45]。凋亡还能转换为铁死亡,Yuan等[46]研究发现,铁积累可抑制骨髓间充质干细胞(MSCs)的数量,提高MSCs细胞ROS水平和氧化酶4(NOX4)蛋白表达,通过Caspase-3诱导MSCs凋亡导致骨质流失,Liu等[47]发现铁积累通过XIST/miR-758-3p/caspase 3轴调节成骨细胞凋亡。Tian等[48]发现ROS在调节成骨细胞中铁过载诱导的坏死性凋亡中起关键作用,RIPK1/RIPK3/MLKL是铁超载在体外诱导成骨细胞坏死性凋亡的关键通路。
此外,铁离子介导的铁死亡参与细胞焦亡的诱导过程。Zhou等[49]研究显示,铁离子和ROS诱导药物羰基氰-间-氯苯肼共同处理黑色素瘤细胞引起细胞ROS水平显著升高,通过ROS-Tom20-Caspase 3-GSDME信号通路导致细胞发生焦亡。Tian等[50]用不同浓度的铁离子处理MC3T3-E1成骨细胞后,检测到成骨细胞内不稳定铁水平的升高并伴随有ROS的产生及Caspase-3的活化,而Caspase-3的活化可切割GSDME将TNF-α诱导的细胞凋亡转换为细胞焦亡[51]。铁离子不仅介导铁死亡,还能诱导细胞焦亡,GPX4信号与GSDMD信号分别是引发铁死亡和细胞焦亡的重要物质基础,那么在OP病程中,也必然存在着过度的成骨细胞铁死亡和焦亡,进而引起成骨细胞功能异常或死亡,而这种影响关系可能是由GPX4与GSDMD信号“crosstalk”引起的细胞焦亡所致。目前,本课题组正在研究GPX4与GSDMD信号“crosstalk”调控成骨细胞焦亡及其对OP发生发展的影响,以期可以提供更多证据。
4 小结与展望
在机体正常的生理过程中,细胞程序性死亡的发生处于适度的平衡状态,从而维持细胞内微环境稳态。在OP发生的病理过程中,各程序性死亡处于失衡状态,可能通过某种机制相互影响而调节OP的发生发展。PCD作为可调控的细胞死亡方式存在于某些特殊细胞体系中,在促进机体发育、维持内环境稳态、免疫调节和生理病理过程中具有重要意义。尽管科学家在PCD关键分子及信号通路的识别方面已取得突破性进展,但有关这些程序性死亡信号通路调控OP发生发展的相关机制了解甚少。未来有关PCD与OP的研究应更多侧重于程序性死亡间交互影响与OP的联系方面,力求将凋亡、坏死性凋亡、铁死亡及焦亡涵盖在一个统一体系中,进一步探究PCD的信号转导与调节机制将为OP发病机制研究及治疗策略提供更多的实验依据和支撑。

