腹膜透析患者骨代谢与骨质疏松、腹主动脉钙化的相关性
汤静 陈蕴 王冬雪 陈安珉 黄建槐 夏文亚 冯锦红
徐州医科大学附属医院,江苏 徐州 221006
慢性肾脏病-矿物质骨代谢异常(chronic kidney disease-mineral and bone disorder,CKD-MBD)是一种全身性综合征,临床表现主要是钙、磷、甲状旁腺激素(parathyroid hormone,PTH)和成纤维细胞生长因子(FGF-23)代谢紊乱,如不及时诊治,将会导致骨代谢异常、血管钙化(vascular calcification,VC)或其他软组织钙化的发生[1],更有甚者可能会增加患者的心血管事件和死亡率。近年来,“骨-血管轴”理论的提出表明VC与异常的骨转换有关,其共同的病理生理机制驱动骨丢失、血管钙化的发生[2]。临床中肾性骨病特指CKD-MBD中的骨异常,其诊断的金标准是骨活检,但因其是有创性检查,不适用于日常临床诊疗,使得检测骨代谢标志物(bone turnover biomarkers,BTMs)成为临床诊断肾性骨病的重要方法[3]。本研究旨在探讨腹膜透析患者的血清BTMs水平与骨质疏松(osteoporosis,OP)、腹主动脉钙化(abdominal aortic calcification,AAC)之间的关系,这可为临床防治腹膜透析患者合并骨质疏松和监测VC严重程度提供更多理论依据。
1 资料与方法
1.1 研究对象
选取自2021年6月至2022年4月在我院进行规律腹膜透析治疗≥3个月的患者80例。男45例,女35例,年龄19~78岁,记录所有患者的临床资料。排除以下患者:①既往行甲状旁腺切除手术或有甲状旁腺瘤患者;②近半年有服用类固醇糖皮质激素药物的患者;③有骨肿瘤和(或)恶性肿瘤骨转移病史者;④近12个月有骨折病史者;⑤合并有严重感染或心肺疾病者。患者对本研究均知情并签署知情同意书。
1.2 方法
1.2.1血标本收集:清晨空腹、PD治疗前留取血标本,检测各项血生化指标:C反应蛋白(CRP)、白蛋白(ALB)、血清肌酐(Scr)、尿素氮(BUN)、脑钠肽(BNP)、血磷 (P)、血钙(Ca)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)等,计算钙磷乘积(CPP)。
1.2.2骨代谢指标:Ⅰ型胶原氨基酸延长肽(TPINP)、骨碱性磷酸酶(BALP)、骨钙素(OC)、β-胶原特殊序列(β-CTX)、甲状旁腺激素(PTH)、25(OH)D。检测方法:TPINP、β-CTX、OC、25(OH)D的测定采用电化学发光(ECL)(仪器为:罗氏Cobas e602)检测。BALP、PTH的测定采用化学发光免疫测定(CLIA)(仪器为:贝克曼DXI 800)检测。
1.2.3AAC评分测定:采用腰椎侧位X线片评估患者的AAC。AACS是由两位放射科医生使用Kauppila等[4]钙化积分法计算,取其平均值。根据AACS结果将患者分为3组:无钙化组(AACS=0)、轻度钙化组(AACS=1~4)和中重度钙化组(AACS≥5)。
1.2.4骨质疏松诊断:使用GE双能X线骨度仪(型号:DPX BRAVO)测定腰椎(L1-L4)、髋关节骨密度值(g/cm2)。采用WHO推荐的骨质疏松诊断标准[5]:①绝经女性和年龄50岁以上的男性根据T值诊断:若T值≤-2.5,则为骨质疏松;②绝经前女性和年龄50岁以下的男性根据Z值诊断:若Z值≤-2,则为低于预期年龄范围,BMD低于预期年龄范围的患者纳入骨质疏松组[6]。
1.3 统计学处理
2 结果
80例腹膜透析患者年龄为50(36.25~59)岁;透析龄为25(12.75~41.75)个月。OP组腰椎骨密度、全髋骨密度明显低于非OP组(P<0.01);OP组血清AACS、血P、CRP、β-CTX较非OP组明显升高(P<0.05)。见表1。
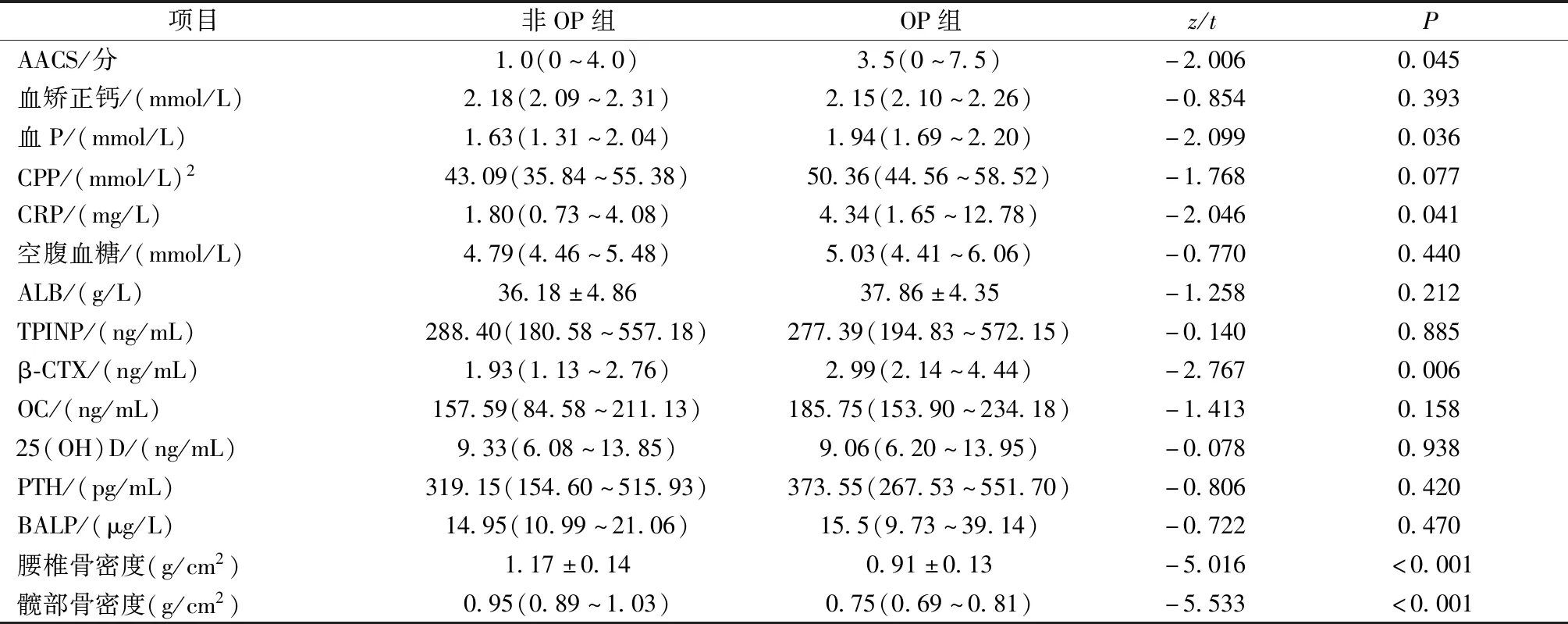
表1 腹膜透析患者骨质疏松与非骨质疏松组比较Table 1 Comparison between osteoporosis and non-osteoporosis groups in peritoneal dialysis patients
按AACS分组,无钙化组30例、轻度钙化组29例、中重度钙化组21例,三组患者的年龄、CRP、BNP、血P、CPP、β-CTX、PTH、腰椎骨密度比较,差异具有统计学意义(P<0.05)。其余生化指标比较差异均无统计学意义(P>0.05)。见表2。
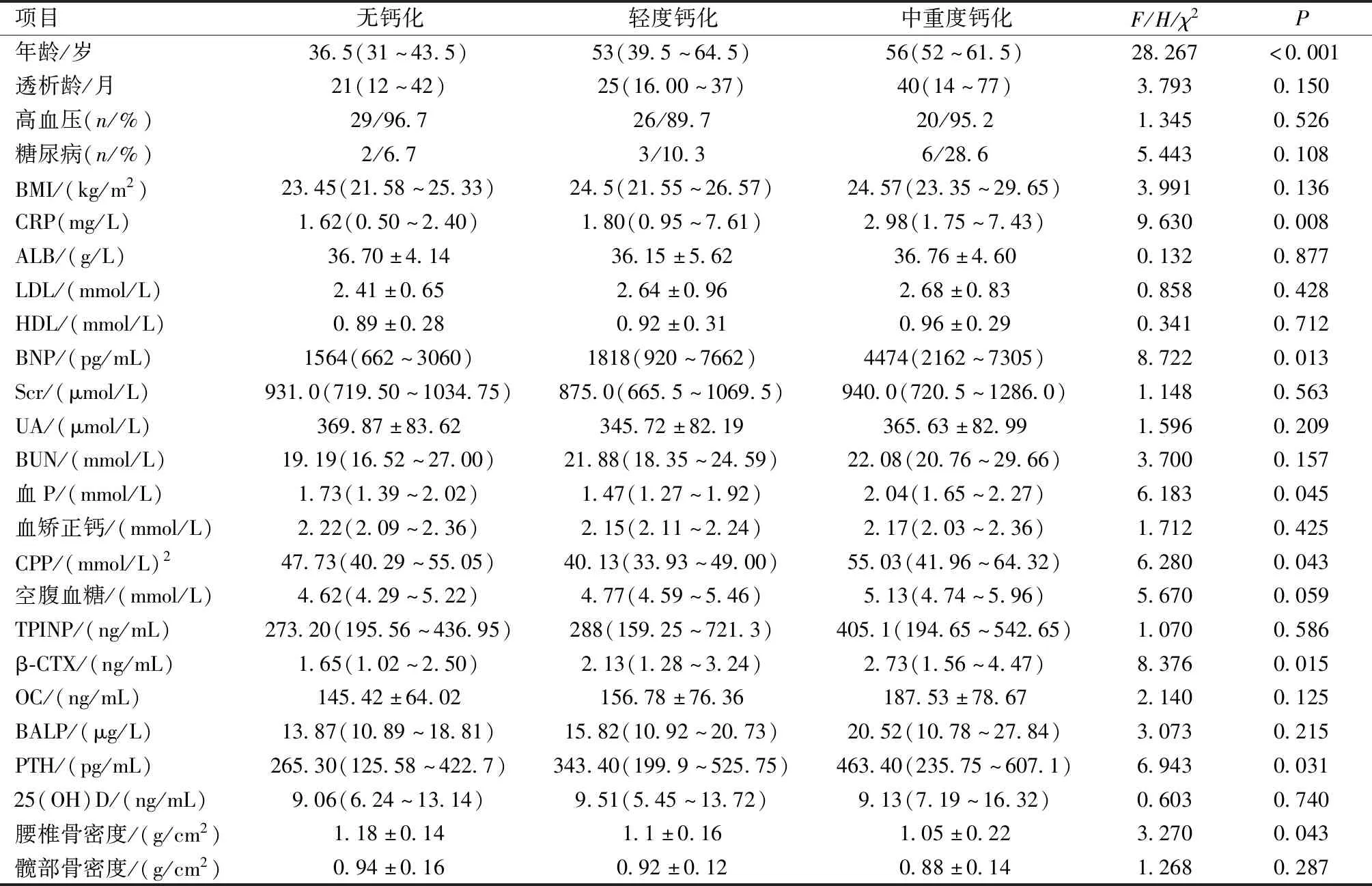
表2 AACS不同程度组临床及实验室数据比较Table 2 Comparison of clinical and laboratory data among different groups with AACS
在Spearman相关性分析中,PD患者AACS与腰椎骨密度呈负相关(r=-0.294,P=0.008),AACS与全髋骨密度无相关性。AAC与年龄、透析龄、BMI、CRP、BNP、空腹血糖、β-CTX、PTH呈正相关(P<0.05)。见表3。
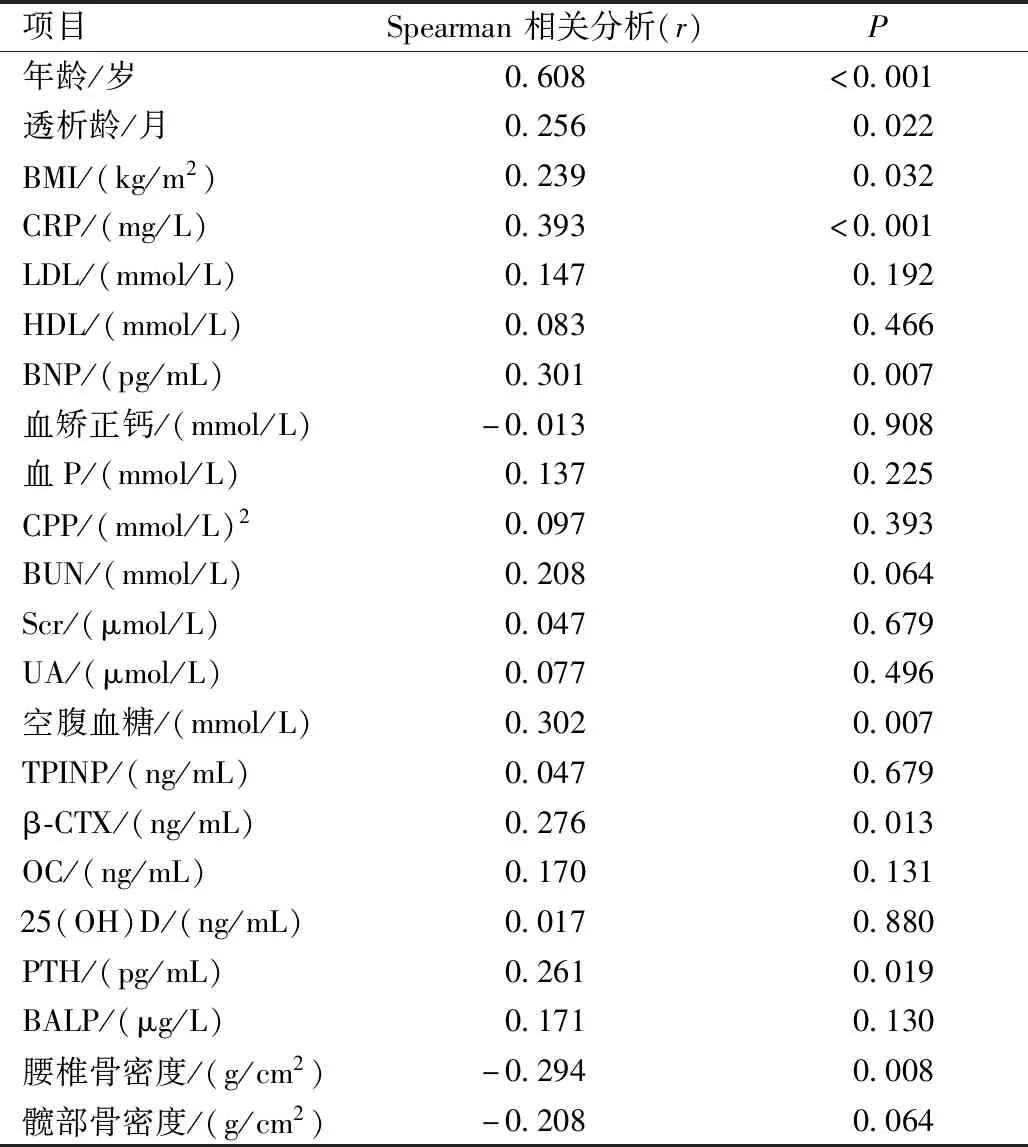
表3 腹膜透析患者AACS与各参数间的相关性Table 3 Correlation between AACS and various parameters in peritoneal dialysis patients
以PD患者是否AACS≥5为因变量,调整透析龄、PTH后,二元Logistic回归分析显示年龄、CPP、β-CTX为AACS≥5分的独立危险因素。见表4。
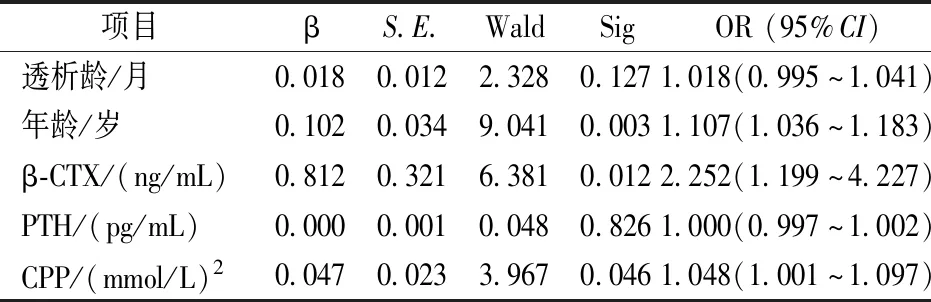
表4 腹膜透析患者AACS≥5 的多因素 Logistic 回归分析Table 4 Multi-factor logistic regression analysis of AACS≥5 in peritoneal dialysis patients
以PD患者是否发生骨质疏松为因变量,二元Logistic多因素回归分析发现β-CTX是其独立危险因素(P=0.046,OR=1.689,95%CI:1.009~2.825),BALP差异无统计学意义(P>0.05)。见表5。

表5 腹膜透析患者并发骨质疏松的Logistic 回归分析Table 5 Logistic regression analysis of peritoneal dialysis patients complicating osteoporosis
3 讨论
血管钙化和骨质疏松在ESRD患者中很常见,与普通人群相比,ESRD患者的骨骼代谢状态、血管钙化程度和早发的心血管事件有着更为紧密的联系[7]。本研究发现骨代谢标志物β-CTX与AAC和OP有相关性。近年来大量研究表明VC是一种类似于骨重建的复杂生物学过程,其中血管平滑肌细胞(vascular smooth muscle cell,VSMC)向成骨样细胞的转分化被认为是最重要的病理生理因素[8]。而且血管钙化和成骨过程有许多相似之处,骨骼通过旁分泌和内分泌因子与血管系统相互作用,途径包括Wnt信号、骨保护素(OPG)/核因子JB受体激活剂(RANK)/RANK配体系统和Galectin-3/晚期糖基化终产物受体轴。由此可以看出VC不是被动矿化过程,而是细胞介导的主动矿化过程[7]。钙化的血管释放影响骨代谢的循环因子,骨代谢因子紊乱进而导致骨质疏松[9]。本研究还发现CRP与AAC呈正相关,与骨密度呈负相关。有研究表明VC和OP的共同发病机制是炎症因子[2]。炎性因子可以通过激活Msx2-Wnt/β-catenin信号促进VSMC的钙化,也可促进内皮细胞向间充质细胞转变,此外炎症也可能会抑制重要的钙化抑制物胎球蛋白A。而且血管钙化还会增加全身炎症负担,促进RANKL、M-CSF和单核细胞趋化蛋白-1的增加,并下调OPG的表达,导致骨吸收增加,骨重建障碍。进而触发一种恶性循环,加速血管钙化和骨质疏松进程[9-10]。
骨质疏松症是一种以骨量和骨质量受损为特征的肌肉骨骼疾病,易增加骨折的风险。正在进行透析的患者骨折发生的风险是无慢性肾脏病患者的4倍以上[11]。骨质疏松的诊断以 BMD为基础,但BMD无法反映患者短期内骨代谢情况,完全依赖BMD预测骨折可能会有滞后的风险,BTMs可反映短期内患者骨代谢状况,有助于指导临床治疗[12]。BTMs包括骨吸收指标(β-CTX、TRACP-5b等)和骨形成指标(TPINP、BALP、OC等)[13-14]。本研究在Logistic多因素回归分析时发现β-CTX是骨质疏松的独立危险因素。这一结论可为腹膜透析患者提供除影像学以外的血清学指标来判断骨损伤的程度。β-CTX是破骨细胞通过分泌蛋白酶降解I型胶原蛋白,释放出N端和C端片段(分别为NTX和CTX)。CTX又分为α-CTX和β-CTX。其中β-CTX是骨吸收的重要血清学指标[15]。TPINP 是从Ⅰ型前胶原中去除产生Ⅰ型胶原的前肽之一,标志着形成新的骨基质[16]。骨碱性磷酸酶(BALP)是一种锚定在成骨细胞和基质小泡膜上的同源二聚体,由肝脏降解,其水平不受肾功能的影响。它参与了羟基焦磷酸盐矿化为羟基磷灰石,继而羟基磷灰石沉积在新形成的骨胶原纤维之间,它可促进体内血管钙化的发生,是骨形成的敏感和特异性指标[17-18]。本研究同时发现β-CTX、BALP是腹膜透析患者发生OP的危险因素,提示腹膜透析合并OP患者体内破骨细胞活性较强,骨吸收亢进,这可能是因为腹膜透析患者长期处于微炎症状态和钙磷代谢紊乱中所致。国外Nguyen等[19]报道骨质疏松患者的 PINP、β-CTX 水平升高,在多元线性回归分析中调整性别、年龄和体重后,β-CTX与股骨颈和腰椎骨密度有相关性。Yan等[20]在一项对绝经女性的前瞻性队列研究显示PINP和β-CTX的升高可增加髋部骨折风险。结合本研究的结果,早期监测β-CTX对预测骨折具有重要价值[21]。
本研究发现β-CTX、年龄、CPP是AACS≥5分的独立危险因素。当AACS>5.5分时,终末期肾脏病患者新发冠状动脉疾病的几率将大大增加[22]。Liu等[23]对中国1 023例老年患者研究发现骨密度、护骨素、骨钙素和I型胶原的C端交联末端肽(CTX)与VC进展有关。熊琳等[24]在慢性肾脏病大鼠身上研究发现血P、CPP升高和骨转换异常会促进VC的发生和进展。高P会上调成骨细胞转录因子Osterix和Runx2,进而刺激VSMC向成骨细胞转分化,推动VC的进程[25]。本研究显示随着β-CTX、CPP水平的增加,VC的程度会增加。这是因为骨代谢加快将会导致骨质释放更多的钙和磷,而且骨骼矿物受阻也会引起血中钙磷增加。本研究同时发现在腹膜透析患者中腰椎骨密度与AAC呈负相关,与髋部骨密度无相关性。目前AAC与不同部位骨密度的关联强度仍存在争议,尚需进一步的研究[7]。
综上所述,腹膜透析患者的β-CTX水平与AAC、骨密度密切相关,因此监测β-CTX有助于判断腹膜透析患者心血管疾病、骨质疏松发生的风险。此外,本研究的样本量有限,且属于横断面研究,无法确定腹膜透析患者BTMs与OP、VC之间的因果关系,具有一定的局限性,易受其他混杂因素的影响,仍需大样本的前瞻性研究来进一步证实。

