中美欧食源性细菌耐药性监测系统比较研究及启示
李 宁,白 莉
(国家食品安全风险评估中心 国家卫生健康委员会食品安全风险评估重点实验室, 北京 100022)
抗微生物药物耐药性(antimicrobial resistance,AMR)被世界卫生组织认定为21世纪威胁人类健康的最大挑战之一。最新研究表明,仅2019年就有495万人的死亡与细菌耐药性有关,其中127万人的死亡是直接相关,中低收入国家尤为严重,预计到2050年,将有1 000万人死于细菌耐药性[1]。
抗微生物药物主要用于治疗或预防人类和动物疾病,促进食品动物的生长(促生长剂),但同时抗微生物药物的使用可导致耐药细菌的产生。20世纪90年代,欧美等发达国家和地区便开始系统搭建细菌耐药性监测网,基于相关的流行病学数据和抗微生物药物使用情况,分析抗微生物药物耐药性流行趋势及新的耐药机制,为限制耐药细菌传播的干预措施的评估、抗微生物药物使用标准制定及新的抗微生物药物的研发和评审等提供科学支撑[2]。
我国是全球最大的抗微生物药物生产和消费国,其中约60%的抗微生物药物被用于养殖业。由于其在养殖业的广泛使用甚至滥用,导致大量耐药细菌的出现和迅速传播,使得食品动物的生产加工场所(养殖场、屠宰厂等)及其产品(肉、蛋、奶)成为耐药细菌的“贮存库”和“散播机”,存在经动物性食品向人群传播的风险,已有研究显示约20%人类细菌耐药性感染是由食源性途径获得的[3]。特别是近些年如质粒介导的多黏菌素耐药基因mcr- 1,替加环素耐药基因tet(X3/X4)和tmexCD1-toprJ1等抵抗临床“最后一道防线”药物的重要耐药基因的快速传播,使部分疾病难以得到有效治疗[4-6]。2021年我国颁布的《中华人民共和国生物安全法》(以下简称《生物安全法》)已将“应对微生物耐药”作为生物安全的8项主要内容之一[7]。为加快实施健康中国战略,贯彻落实《生物安全法》,遏制微生物耐药,国家卫生健康委员会(简称“国家卫健委”)在总结评估前期工作《遏制细菌耐药国家行动计划(2016—2020年)》基础上,于2022年10月颁布了《遏制微生物耐药国家行动计划(2022—2025年)》,计划中强调要完善监测评价体系,为科学决策提供依据[8]。
本研究重点比较中美欧食源性细菌耐药性监测系统的发展和特点,同时分析目前中国食源性细菌耐药性监测工作中的现状,进而探讨美欧的经验对我国食源性耐药监测体系发展的启发和借鉴作用,包括逐步完善耐药监测系统、建立多部门协同共治机制及加快新技术在数据挖掘中的运用等,从而综合提升遏制细菌耐药性的能力,保障人民健康。
1 欧洲食源性细菌耐药性监测系统及现状
据估计,欧洲每年约每10万人中131人感染耐药细菌,每10万人中有6.44人因其死亡[9]。欧洲抗细菌耐药性工作主要由欧洲疾病预防控制中心(European Centre for Disease Prevention and Control,ECDC)、欧洲食品安全局(European Food Safety Authority,EFSA)和欧洲药品管理局(European Medicines Agency,EMA)联合开展,协调相关监测网络AMR数据并进行分析。
1.1 人群食源性细菌耐药性监测
ECDC负责协调欧洲食源性、水源性疾病与人畜共患病网络(Food- and Waterborne Diseases and Zoonoses Network,FWD- Net)和欧洲抗微生物药物耐药性监测网络(European Antimicrobial Resistance Surveillance Network,EARS- Net),收集和分析欧洲各国医疗机构上报的AMR数据,并对欧洲AMR有关的健康安全问题提供咨询[10]。
FWD- Net监测人类通过动物性食品、水及与动物接触感染的18种疾病,其中对分离的沙门菌和弯曲杆菌开展AMR分析,该监测网络同时协助评估食源性、水源性疾病及人畜共患病对人群的负担并提出针对性预防措施。2022年3月,EFSA发布的2019—2020年人畜共患病细菌耐药性报告显示,大多食源性致病菌对多种抗微生物药物的耐药率仍呈上升趋势。从临床患者中分离到的沙门菌多重耐药性(multidrug resistance,MDR)总体较高(25.4%),对氨苄西林、磺胺类和四环素类药物的耐药率分别为29.8%、30.1%和31.2%。对临床一线用药环丙沙星的耐药率为14.1%,在报告了最低抑菌浓度(minimum inhibitory concentration,MIC)的沙门菌中,有1.4%对环丙沙星表现出极高的耐药性(MIC>4 μg/mL);而对三代头孢菌素类药物的耐药性总体非常低,仅为0.8%。环丙沙星和红霉素是临床治疗弯曲杆菌病的关键抗微生物药物,但空肠弯曲杆菌和结肠弯曲杆菌分离株均对环丙沙星有较高的耐药率(61.2%和65.8%),对环丙沙星和红霉素都耐的情况较少(0.5%和8.9%)。此外2种亚种对四环素的耐药较高(43.7%和74.0%),且易对环丙沙星和四环素2种药物出现联合耐药(38.1%和45.9%)[11]。
1.2 食品动物和相关食品细菌耐药性监测
EFSA负责监测和分析欧洲各国健康食品动物和动物性食品来源的AMR数据。欧盟最新发布的AMR监测执行标准中指出,监测范围应包括养殖和屠宰过程中的肉鸡、蛋鸡、肉牛和肉猪等食品动物及相关食品;监测指标应重点关注2种致病菌(沙门菌、弯曲杆菌)和一种指示菌(大肠埃希菌)[12]。食品动物携带产超广谱β-内酰胺酶、产AmpC酶或产碳青霉烯细菌可能导致耐药细菌从动物性食品传播给人类,同时这些耐药基因可能会转移到其他细菌中,包括食源性人畜共患病菌。随着多重耐药细菌的不断出现,根据欧盟委员会2013/652/EU规定增加超广谱头孢菌素(extended spectrum cephalosporins,ESC)抗性的选择性培养基筛选大肠埃希菌和沙门菌。ECDC和EFSA每年发布一次欧洲关于源自人类、动物和食品的沙门菌、弯曲杆菌及大肠埃希菌AMR的报告,用于了解AMR流行趋势及评价饲料中抗微生物药物的使用情况。
从食品动物样本(肉鸡)中分离到的沙门菌MDR较高(53.6%),对氨苄西林(18.8%)、磺胺类药物(51.0%)、四环素(50.3%)、环丙沙星(65.3%)、萘啶酸(61.4%)和黏菌素(1.5%)等抗微生物药物均出现不同程度的耐药。空肠弯曲杆菌和结肠弯曲杆菌对环丙沙星和萘啶酸的耐药率较高(71.0%~84.8%),其次为四环素(57.6%~67.7%),未发现对庆大霉素的耐药性,不同国家不同来源的弯曲杆菌对环丙沙星和红霉素也出现不同水平的联合耐药性。指示菌大肠埃希菌分离株耐药性与从临床病例报告的沙门菌分离株中观察到的结果相似。来自食品动物样本(肉鸡)的沙门菌中耐ESC沙门菌为2.1%;分离到的耐ESC指示性大肠埃希菌比例为7.1%[11]。
1.3 人医抗微生物药物使用量监测
ECDC协调欧洲抗微生物药物使用量监测网(European Surveillance of Antimicrobial Consumption Network,ESAC- Net),收集人医抗微生物药物使用量(antimicrobial consumption,AMC)数据,用于评价抗微生物药物合理使用情况[13]。连续监测数据显示,重要的人用抗微生物药物的销量在2011年至2020年期间显著下降,在2020年仅占总销售额的6%。特别是三代和四代头孢菌素、黏菌素、氟喹诺酮类药物和其他喹诺酮类药物的销量分别下降了33%、76%、13%和85%[14]。
1.4 食品动物抗微生物药物使用量监测
EMA协调欧洲兽用抗微生物药物使用量监测(European Surveillance of Veterinary Antimicrobial Consumption,ESVAC)项目收集分析兽用抗微生物药物产品总体销售数据[15],规范兽用抗微生物药物的合理使用并提供科学建议。最新发布的抗微生物药物消费和耐药性分析报告显示,目前部分抗微生物药物在食品动物中的使用量已有所减少并低于人类用量。如氨基青霉素类(氨苄西林和阿莫西林)、三代和四代头孢菌素类、喹诺酮类药物在食品动物中用量已低于人类;多黏菌素在食品动物中的用量虽高于人用量,但已减少近一半[16]。目前,欧洲不同动物来源的沙门菌对几种极为重要的临床治疗用抗微生物药物(环丙沙星、三代头孢、阿奇霉素)的MDR水平较高,弯曲杆菌的MDR水平较低[11]。但在欧洲几个成员国中,家禽中细菌的整体耐药性水平已有所降低,这表明欧洲的耐药监测工作在减少食品动物AMR方面取得了重大进展[11]。
1.5 其他内容的监测
尽管欧洲现有的耐药监测系统包涵了对食品动物来源的AMR监测,但是并未将患病的食品动物和伴侣动物纳入监测范围。为完善欧洲AMR的“One Health”战略,2021年欧盟EU- JAMRAI(European Union-Joint Action on Antimicrobial Resistance and Healthcare Associated Infections)建议建立欧洲兽医抗微生物药物耐药性监测网络(European Antimicrobial Resistance Surveillance network in Veterinary medicine,EARS- Vet),以监测兽医在对包括伴侣动物在内的所有动物进行临床治疗时,抗微生物药物的使用情况[17]。EARS- Vet将评估耐药细菌通过非食源性途径传播给人类的风险和在动物健康方面的负担,帮助兽医在临床治疗过程中规范使用兽用抗微生物药物。同时将与欧洲现有监测机构及网络相结合,补充和完善现有的欧洲 AMR监测体系。
2 美国食源性细菌耐药性监测系统及现状
耐药细菌感染在美国每年约造成超过280万人患病和35 000人死亡[18]。美国国家抗微生物药物耐药性监测系统(National Antimicrobial Resistance Monitoring System,NARMS)成立于1996年,由美国疾病预防控制中心(Centers for Disease Control and Prevention,CDC)、美国农业部(U.S. Department of Agriculture,USDA)、美国食品和药物管理局(Food and Drug Administration,FDA)共同合作成立,旨在监测病人、食品动物及动物性食品中分离的食源性细菌的耐药性[19]。NARMS于2017年和2018年分别与FDA的兽医实验室调查及响应网络(Veterinary Laboratory Investigation and Response Network,Vet- LIRN)和USDA的国家动物健康实验室网络(National Animal Health Laboratory Network,NAHLN)合作监测患病动物(食品动物和伴侣动物)中AMR情况;基于“One Health”理念,于2022年开始与美国环境保护部(Environmental Protection Agency,EPA)合作监测水中细菌耐药性。NARMS通过发布最新耐药趋势信息,以便各机构进行数据交流及研究,促进美国公共卫生安全。
2.1 人群食源性细菌耐药性监测
美国CDC下属食源、水源及环境源疾病部门(Division of Foodborne,Waterborne,and Environmental Diseases,DFWED)与各州卫生健康部门合作,重点监测腹泻病人沙门菌、弯曲杆菌、产志贺毒素大肠埃希菌O157、弧菌及志贺菌AMR情况,提供有关散发和暴发食源性疾病感染病例的细菌耐药性数据[20]。
沙门菌感染可致幼儿、老年人和免疫能力低下人群患严重疾病。据估计,沙门菌在美国每年导致超过135万人患病、26 500人住院和420人死亡,其中有21.2万人感染耐药沙门菌,导致70人死亡[21]。根据2022年NARMS发布的最新报告显示[22],人群来源的沙门菌中MDR菌株约有10%,其中26%的血清型为单相鼠伤寒沙门菌;对环丙沙星、氨苄西林、头孢曲松和阿奇霉素的耐药率分别为11%、9%、3%和1%(主要是纽波特沙门菌)。弯曲杆菌导致超过150万人患病、19 500人住院和240人死亡[21]。NARMS报告显示,空肠弯曲杆菌和结肠弯曲杆菌对大环内酯(阿奇霉素和红霉素)的耐药率分别为3%和8%,对环丙沙星的耐药率分别为34%和45%[22]。
2.2 食品动物和相关食品细菌耐药性监测
USDA下属的食品安全检验局(Food Safety and Inspection Service,FSIS)和农业科学研究院(Agricultural Research Service,ARS)负责监测食品动物(肉鸡、火鸡、牛及猪)肠内容物中分离的沙门菌、弯曲杆菌、大肠埃希菌和屎肠球菌的耐药情况。USDA同时负责监测动物性食品及其生产加工过程中的耐药细菌和抗微生物药物残留情况,为减少农业环境及食品中细菌AMR、确保动物性食品的卫生安全以及对相关食源性疾病展开调查并研究改进管理办法提供技术支撑[23-24]。
大肠埃希菌主要通过食品动物和零售肉制品感染人类,人们通常将其作为指示菌。零售猪肉中大肠埃希菌MDR为22%,动物性食品来源的大肠埃希菌对头孢曲松耐药率为7%,对环丙沙星耐药率低于8%,对碳青霉烯药物敏感。食品动物及加工操作不当的肉制品和奶制品极易污染肠球菌,NARMS使用肠球菌作为指示菌来追踪细菌耐药性。牛肉盲肠内容物来源的肠球菌对红霉素的耐药率为12%,火鸡和肉鸡来源的粪肠球菌对耐庆大霉素耐药率分别为5%和16%,2019年仅在鸡盲肠中分离出3株耐卑霉素肠球菌[22]。
2.3 人用抗微生物药物使用量监测
2014年,美国CDC发布了《医院抗微生物药物管理计划核心要素》,建议当地所有医院2015年起用其指导院内抗微生物药物的使用。到2018年,已有85%的急症护理医院具备了全部7项要素(投入、问责制、药学专业知识、行动、跟踪、报告和教育),较2014年增长44%。最新数据显示,医院中超过一半的抗微生物药物的处方与推荐的处方做法不一致[25]。医院处方医师和药剂师在诊断检测结果是否可用时,可重新评估和优化抗微生物药物治疗处方。
2.4 食品动物抗微生物药物使用量监测
FDA下属兽药中心(Center for Veterinary Medicine,CVM)负责收集食品动物抗微生物药物的销售数据[26],虽其不一定反映抗微生物药物的实际使用情况,但长时期观察到的销售量可成为与这些产品相关的市场趋势的指标。在评估合理使用抗微生物药物时,还需考虑其他重要信息来源,如实际使用数据、动物数量统计数据、动物健康数据和抗微生物药物耐药性数据。2021年发布的食品动物兽药抗微生物药物最新销量报告显示,2020年销售量较2015年和2011年分别下降了38%和27%。其中用于牛的药物占比约41%,用于猪、火鸡和肉鸡的比例分别为41%、12%和2%,有4%用于其他或未知物种[27]。
CVM出台文件计划在2019—2023年分阶段实施临床重要抗微生物药物的管理,实现以下3个目标:1)抗微生物药物的使用与管理原则保持一致;2)促进动物治疗机构抗微生物药物的管理;3)加强对兽用抗微生物药物的耐药性和使用监测。该机构的目标不仅仅是减少抗微生物药物的销量,还包括通过优化这些产品的使用,并将其使用限制在动物的治疗、控制或预防疾病所需的范围内,从而建立良好的抗微生物药物管理实践[28]。最终减缓抗微生物药物耐药性的发展,保持抗微生物药物在食品动物和人类中对抗疾病的有效性。
2.5 患病动物细菌耐药性监测
Vet- LIRN和NAHLN联合20个州的兽医诊断实验室开展伴侣动物(犬、猫)和患病食品动物(鸡、猪及牛)细菌耐药性监测,监测范围包括沙门菌、伪中间葡萄球菌及大肠埃希菌。
FDA发布的2019年动物病原体AMR数据报告显示[29],Vet- LIRN收集的从犬中分离的大肠埃希菌对阿莫西林(100%)、头孢唑林(99%)和头孢氨苄(78%)表现出极高的耐药性,对亚胺培南(0)和阿米卡星(1%)极为敏感;NAHLN收集到的患病食品动物来源大肠埃希菌呈现同样的耐药趋势。
3 中国食源性细菌耐药性监测体系及现状
中国是世界上最大的抗微生物药物生产和消费国。2016年国家卫健委(National Health Commission of the People’s Republic of China, NHC)联合其他14个部委发布的《遏制细菌耐药国家行动计划(2016—2020年)》,建立一整套系统的抗微生物药物管理体系以减少抗微生物药物的使用。至2020年,我国人用抗微生物药物产量为22.3万t,需求量为13.8万t;兽用抗微生物药物使用量为3.3亿t,约99.3%兽用抗微生物药物为本国生产[30-31]。为了更好地应对微生物耐药带来的挑战,贯彻落实《生物安全法》,国家卫健委于2022年10月发布了《遏制微生物耐药国家行动计划(2022—2025年)》以解决日趋复杂的耐药问题。
3.1 人群食源性细菌耐药性监测
NHC会同工业和信息化部、商务部、海关总署、国家市场监管总局、国家粮食和物资储备局等部门,制定和实施国家食品安全风险监测计划。NHC下属国家食品安全风险评估中心(China National Center for Food Safety Risk Assessment,CFSA)负责组织我国食源性细菌耐药性监测工作的实施,确定监测范围及对监测结果进行汇总分析。2014年我国全面启动食源性细菌耐药监测工作,监测对象为食源性疾病暴发监测和食源性疾病主动监测中腹泻病人的沙门菌、致泻大肠埃希菌分离株。由全国3 000多家地方各级疾病预防控制中心和700多家主动监测哨点医院进行采样和菌株分离工作[32],32家省级疾病预防控制中心按照统一的药敏测试方法、质量控制措施和判定标准完成药敏测试,并按照报告要求向CFSA报告药敏测试结果。
3.2 食品动物和相关食品细菌耐药性监测
中华人民共和国农业农村部(Ministry of Agriculture and Rural Affairs,MARA)每年下发畜禽及畜禽产品兽药残留监控计划和动物源细菌耐药性监测计划[33]。MARA直属事业单位中国兽医药品监察所(China Institute of Veterinary Drug Control,IVDC)于2008年起主要负责组织开展我国动物源细菌耐药性监测工作,确定监测项目及对监测结果汇总分析,并于每年发布上一年度中国兽用抗微生物药物使用情况报告。2022年监测项目对全国食品动物(鸡、鸭、猪、羊及奶牛)养殖和屠宰加工过程及部分动物医疗机构进行采样,收集分析大肠埃希菌、沙门菌、弯曲杆菌、肠球菌、金黄色葡萄球菌、副嗜血杆菌、魏氏梭菌等细菌的耐药性[34]。
此外,NHC牵头制定全国食品中微生物的监测计划,由CFSA食品污染物监测网负责监测受污染的禽畜水产品中的沙门菌、空肠弯曲杆菌和致泻性大肠埃希菌等[35]。
3.3 人群抗微生物药物使用量监测
NHC负责监测我国临床抗微生物药物使用情况,于2006年成立全国抗微生物药物临床应用监测网,对全国各级各类医疗机构抗微生物药物的使用情况进行监控[36]。截至2021年,已经有6 744家医院加入监测网,其中综合医院占比63%,为推动全国抗微生物药物合理应用工作发挥了重要作用。据2020年监测数据显示,门诊处方抗微生物药物使用率为6.5%、住院患者抗微生物药物使用率为34.08%、住院患者围手术期预防用抗微生物药物使用率为34.6%(Ⅰ类手术切口)、住院患者抗菌药物使用强度为44.12 DDDs·100/(人·d)[用药频度(defined daily doses,DDDs)];药物监测数据结果显示,头孢菌素含酶抑制剂类复方制剂使用强度为5.87 DDDs·100/(人·d)、碳青霉烯类药物为2.92 DDDs·100/(人·d)、替加环素51.92 DDDs·100/(人·d)、喹诺酮类药物6.22 DDDs·100/(人·d)[37]。
3.4 食品动物抗微生物药物使用量监测
我国于2017年发布了《全国遏制动物源细菌耐药行动计划(2017—2020年)》,依据计划由中国兽药协会负责收集全国兽用抗微生物药物销售量,IVDC负责统计分析,并于2019年发布了第一份情况报告。同时,IVDC负责汇总有关兽药残留和抗微生物药物耐药性等信息,以完成风险评估工作并提供风险管理和政策建议。数据显示,2020年我国境内兽用抗微生物药物生产销售量为32 544 t,与2017年相比下降了21.9%,每吨动物产品的兽用抗微生物药物使用量为165 g,好于欧盟部分国家。在总抗生素使用量中,促生长用途占比为28.69%[38]。根据农业农村部公告第194号,自2020年1月1日起,停止使用除中药外的所有促生长类药物饲料添加剂。
4 对我国食源性细菌耐药性监测系统的启示
相较欧美国家,我国食源性细菌耐药性监测体系起步较晚,通过近20年的努力,初步形成了涵盖病人、食品动物及相关食品中分离的食源性细菌耐药性监测网络(中美欧食源性细菌耐药监测内容见表1),取得了较大的进步,但与发达国家相比仍有较大的提升空间。
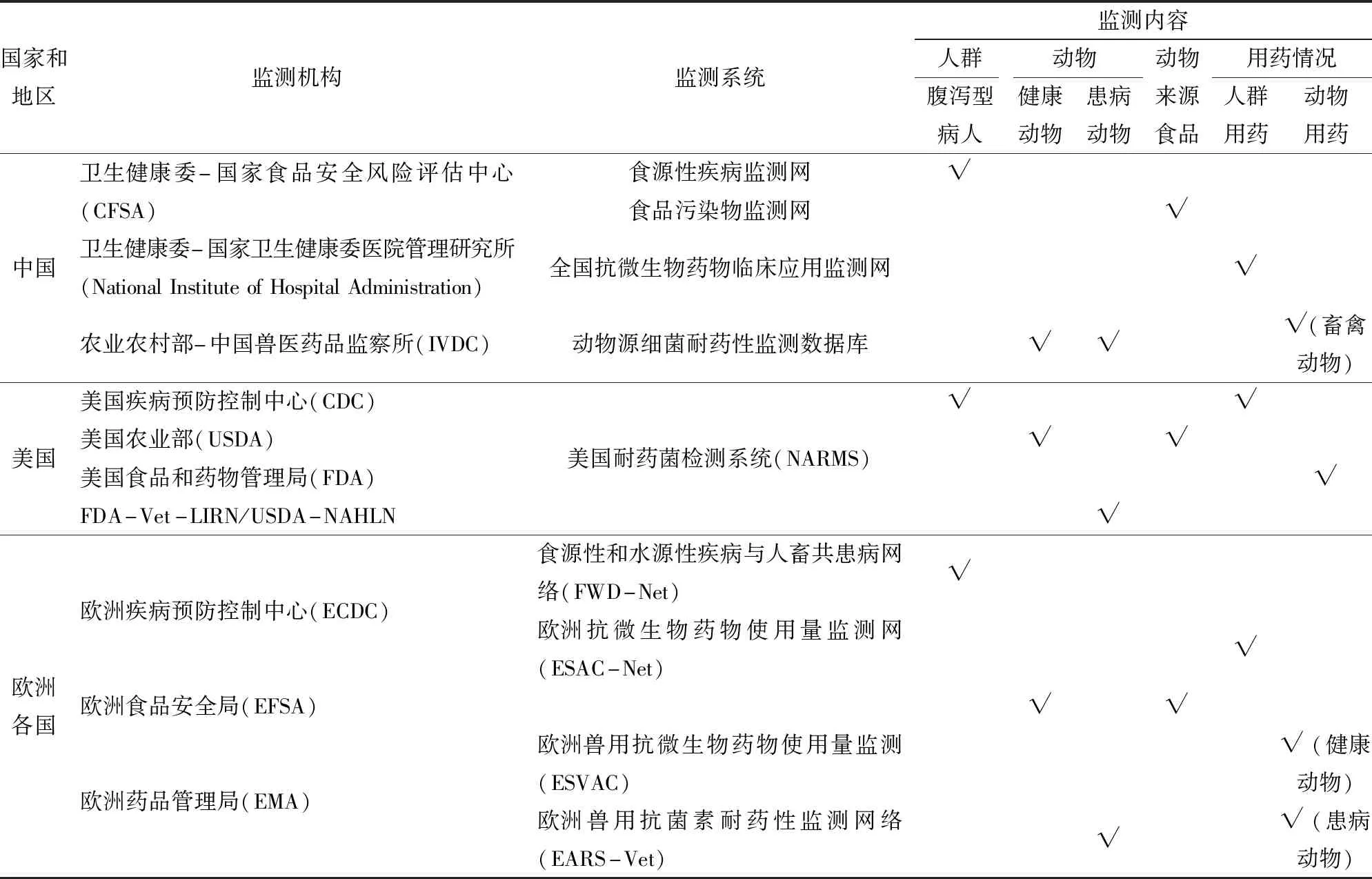
表1 中美欧食源性细菌耐药监测内容Tab.1 Surveillance of antimicrobial resistance of foodborne bacteria in China, the United States and Europe
4.1 逐渐完善监测系统
我国畜禽集约化养殖迅猛发展,抗微生物药物的不合理使用导致的细菌耐药性问题与我国现阶段的监测体系不匹配。同时新业态的发展,如我国宠物市场的快速崛起,也成为人群感染耐药细菌的一个新的“风险点”。对此我国需加强顶层设计,明确各部门职能并细化监测范围及指标体系。此外,2022年美国基于“One Health”框架已将水环境中细菌耐药性纳入NARMS的监测范畴。我国食源性细菌耐药性监测体系也应随着监测目标的扩充,分阶段分步骤逐步完善与目标相匹配的监测系统。
4.2 加强跨部门协作机制
人群中食源性耐药菌的感染主要来自养殖动物、食品供应链,也包括生活环境污染甚至宠物等,目前不同部门或机构在数据采集时各有侧重,缺少衔接,形成养殖、屠宰、运输、零售、消费等各环节的数据“烟囱”,给细菌性耐药的风险评估中的模型构建、验证以及关键控制点识别带来困难,也不利于制定基于风险评估结果的控制措施。因此,在国家层面,积极探索建立多部门(农业兽医、食品供应、环境监测、海关检疫、医疗机构、食品安全监测监督机构等密切联合)共同参与的合作平台和工作机制,在数据共享共用的基础上建立食源性细菌耐药性的全链条收集和整合协作机制。2022年10月,FAO、WHO、联合国环境规划署(United Nations Environment Programme,UNEP)和世界动物卫生组织(World Organization for Animal Health,WOAH)联合发起“同一健康联合行动计划(2022—2026年)”,侧重在包括抗微生物药物耐药等六个领域上,创建一个整合系统和能力框架,加强负责在人- 动物- 植物- 环境界面上解决健康问题的所有部门的协作、沟通、能力建设和协调。提供上游政策、立法咨询和技术援助,以帮助制定国家目标和优先事项;促进多国家、多部门、多学科合作、知识、解决方案和技术的学习和交流。
4.3 加强多学科合作创新
随着前沿分析技术不断发展,科学家对细菌耐药性的产生和传播机制的认知不断深入,但仍有较多不确定性需要解答,如细菌耐药性受到内在因素(宿主、移动元件)及外在因素(人类生产活动、气候)的影响。新技术的发展,特别是组学技术和生物信息学技术在细菌耐药性方面的运用,将支持向更精简、自动化的监测方式过渡。2014年美国已将全基因组测序(whole genome sequencing,WGS)技术运用到NARMS沙门菌耐药性监测和预测,我国“十三五”期间也已建立食源性疾病分子溯源网络(TraNet),积累大量WGS数据,应运用计算机学和生物统计学等交叉学科挖掘更多信息,有效合理利用数据,为政策转化提供更加科学的支撑。

