舒更葡糖钠注射液与罗库溴铵的体外结合与释放
唐 朝 孟芳 邓汉生
舒更葡糖钠为特异性结合性神经肌肉阻滞拮抗药物[1]。其是一种经修饰的γ-环糊精,通过与神经肌肉阻滞药物罗库溴铵或维库溴铵在血浆中形成复合物,进而降低在神经肌肉接头处与烟碱受体相结合的神经肌肉阻滞药物的数量,由此拮抗由罗库溴铵或维库溴铵诱导的神经肌肉阻滞[2-3]。
本研究采用等温滴定量热法(ITC)[4-5]和高效液相色谱法(HPLC)[6]开展不同厂家舒更葡糖钠注射液与罗库溴铵的体外结合及其释放行为研究,评价不同厂家舒更葡糖钠注射液与罗库溴铵结合及释放特征,以期为临床合理用药提供参考和依据。
1 仪器、试剂与方法
1.1 仪器、试剂
仪器:MicroCal PEAQ-ITC等温滴定量热仪(Malvern),1260 Infinity Ⅱ高效液相色谱仪(Agilent)。
试剂:舒更葡糖钠注射液(含量:100 mg/ml,批号:U035232,布瑞亭,A制剂,默沙东(中国)投资有限公司),舒更葡糖钠注射液(含量:100 mg/ml,仿制药,B制剂,扬子江药业集团有限公司),罗库溴铵对照品(含量:>98%,大连博格林生物科技有限公司),罗库溴铵注射液(含量:10 mg/ml,浙江仙琚制药股份有限公司),四甲基氢氧化铵(分析纯,上海阿达玛斯试剂有限公司),乙腈(≥99.9%,西格玛奥德里奇(上海)有限公司),磷酸(分析纯),实验用水为超纯水。
1.2 方法
1.2.1 ITC测定罗库溴铵的结合常数
1.2.1.1 受试化合物溶液的制备室温条件下受试化合物溶液的制备:用超纯水稀释舒更葡糖钠注射液及罗库溴铵注射液,分别配制舒更葡糖钠最终浓度为0.1 mmol/L,罗库溴铵为1.0 mmol/L。高温条件下受试化合物溶液的制备:将舒更葡糖钠注射液置于60 ℃条件下10 d后进行测定,用超纯水分别稀释舒更葡糖钠注射液及罗库溴铵注射液,分别配制舒更葡糖钠最终浓度为0.1 mmol/L,罗库溴铵为1.0 mmol/L。光照条件下受试化合物溶液的制备:将舒更葡糖钠注射液置于4 500 Lx,25 ℃,60%相对湿度(RH)条件下放置10 d后进行测定,用超纯水稀释舒更葡糖钠注射液及罗库溴铵注射液,分别配制舒更葡糖钠最终浓度为0.1 mmol/L,罗库溴铵为1.0 mmol/L。1%血清白蛋白(BSA)受试化合物溶液的制备:用含1%BSA的超纯水溶液稀释舒更葡糖钠注射液及罗库溴铵注射液,配制舒更葡糖钠最终浓度为0.1 mmol/L,罗库溴铵为1.0 mmol/L。
1.2.1.2 样品测定样品池注入280 μl待滴定的舒更葡糖钠溶液,40 μl罗库溴铵溶液装入注射器,恒温至25 ℃,控制搅拌速率为750 r/min,待仪器自动平衡后,记录60 s后开始滴定,连续滴定19滴,首滴0.4 μl,后18滴2 μl,间隔时间为150 s。
1.2.2 罗库溴铵HPLC的建立色谱柱:C18柱(250 mm×4.6 mm,5.0 μm);流动相:乙腈-4.53 g/L四甲基氢氧化铵溶液(体积比为90∶10,用磷酸调节pH至7.4);检测波长:210 nm;流速:1.0 ml/min;柱温:30 ℃;进样量:10 μl。
1.2.3 罗库溴铵与不同厂家舒更葡糖的结合速率评价5 ml 2.0 mg/ml的罗库溴铵溶液分别与不同厂家5 ml 6.6 mg/ml舒更葡糖钠溶液混合均匀后37 ℃孵育,分别在10 min、20 min、30 min时用1 000 Da超滤管超滤分离游离药物。过滤样品溶液采用HPLC测定游离罗库溴铵的浓度,根据游离药物与加入药物的浓度计算药物结合率。
1.2.4 罗库溴铵与不同厂家舒更葡糖结合后的释放行为评价1 ml 10.0 mg/ml罗库溴铵溶液与1 ml 33.3 mg/ml舒更葡糖钠溶液在37 ℃混合孵育20 min后,将其分别置于100 ml 磷酸盐缓冲液(PBS)和100 ml含有1%BSA的PBS中(37 ℃摇床,75转/min),分别在5 min、10 min、20 min、30 min时取液2 ml(取液后立即补液2 ml),立即用超滤管(1 000 Da)高速离心。过滤液采用HPLC测定释放的游离罗库溴铵浓度。
1.2.5 数据处理采用MicroCal PEAQ-ITC Analysis Software软件中one binding site model对每组滴定数据分别进行拟合,得到每组滴定反应的结合常数及相关热力学常数。数据分析和比较采用GraphPad Prism 8(GraphPad Software Inc.,La Jolla,CA,USA)和Excel软件。两组之间的统计比较采用双尾Studentt检验。多个(两个以上)组之间的统计比较采用单因素方差分析(ANOVA)和Tukey事后检验。P<0.05为差异有统计学意义。
2 结果
2.1 舒更葡糖钠与罗库溴铵结合的ITC结果
表1结果表明,舒更葡糖钠与罗库溴铵具有极强的药物结合能力,其结合常数KD均小于10-5mol/L。在常温条件下,B制剂的舒更葡糖钠KD值显著高于A制剂(P<0.05)。光照与高温条件对各制剂与罗库溴铵的结合常数KD值未有显著影响(P>0.05)。加入1%BSA后,B制剂的KD值高于A制剂,但差异无统计学意义(P>0.05),各制剂的KD值均显著增大(P<0.05),提示在血清存在条件下,罗库溴铵可能和血清蛋白存在竞争性结合舒更葡糖钠。

表1 舒更葡糖钠和罗库溴铵结合相关热力学参数(n=6)
2.2 罗库溴铵与不同厂家舒更葡糖钠的结合率与结合速率
罗库溴铵与不同厂家舒更葡糖钠的结合率结果如图1~2所示。罗库溴铵与不同厂家舒更葡糖钠的结合率结果表明:舒更葡糖与罗库溴铵以近似1∶1的分子比例(质量比1∶3.3)结合,且超滤可将游离罗库溴铵与舒更葡糖罗库溴铵结合物有效分离。在10 min时大部分罗库溴铵与舒更葡糖快速结合,在20 min已基本全部结合。B制剂在5 min时的结合率和结合速率均显著低于A制剂(P<0.05)。
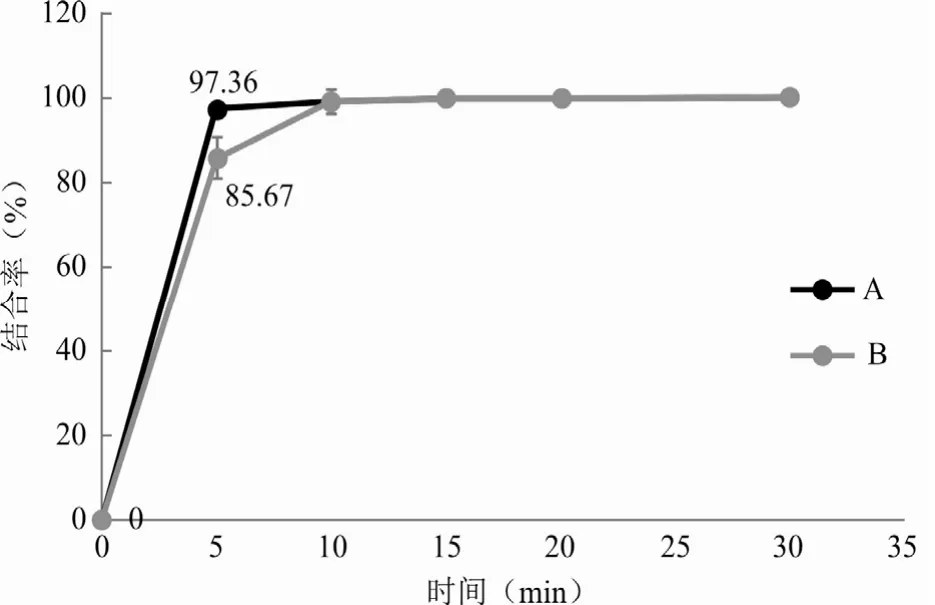
图1 罗库溴铵与不同厂家舒更葡糖钠的结合速率(n=6)
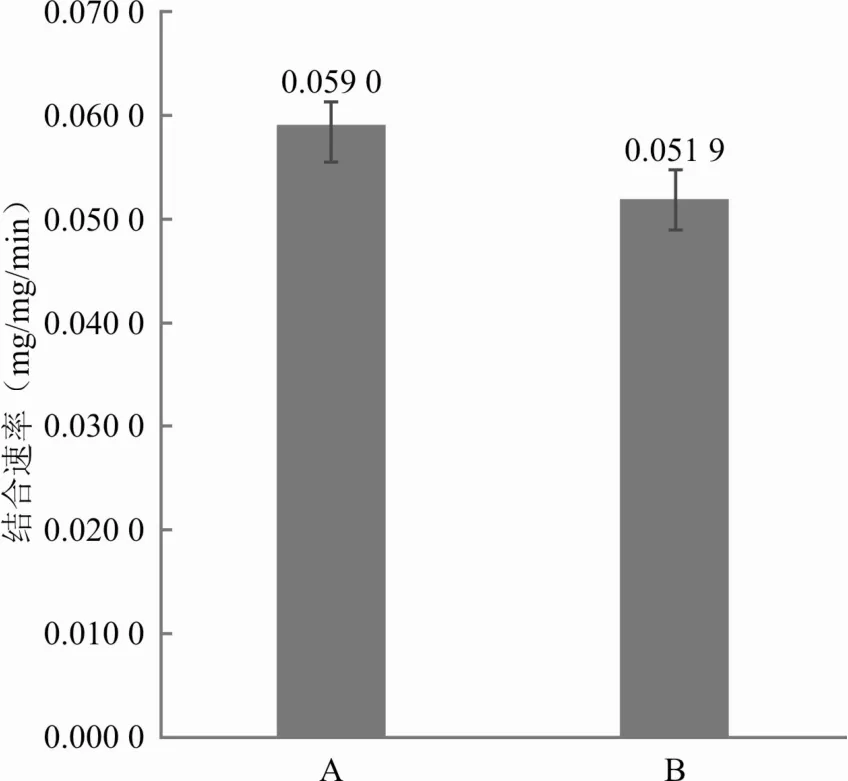
图2 罗库溴铵与不同厂家舒更葡糖钠混合5 min时的结合速率比较(n=6)
2.3 罗库溴铵与不同厂家舒更葡糖结合后的释放行为
罗库溴铵与不同厂家舒更葡糖结合后的释放结果表明:罗库溴铵与舒更葡糖结合物在PBS(pH 7.4)释放介质中各时间点均未测到游离的罗库溴铵,表明罗库溴铵与舒更葡糖均能以结合物的形式存在,结合物稳定性较强。当释放介质中存在BSA时,仅B制剂在5 min时测得极少量游离药物释放,而在其他时间点和A制剂各时间点均未测到游离药物。
3 讨论
本研究采用ITC测定了舒更葡糖钠与罗库溴铵的结合力,该方法灵敏度高,专属性较好。实验结果也确证舒更葡糖钠与罗库溴铵的结合常数KD均小于10-5mol/L,呈现出极强的罗库溴铵结合能力。两个厂家的舒更葡糖钠制剂与罗库溴铵结合力具有一定的差异性,其中与A制剂(原研药)的KD值相比B制剂显著降低,约为原研药的58%,提示其体内拮抗罗库溴铵的能力可能弱于A制剂。加入1%BSA后,罗库溴铵的KD值与正常条件下相比均显著增大,提示在血清存在条件下,罗库溴铵可能和血清蛋白存在竞争性结合舒更葡糖。
罗库溴铵与舒更葡糖钠结合与释放行为的评价结果进一步验证了罗库溴铵与舒更葡糖钠具有极强的结合力[7],在PBS(pH7.4)释放介质中均能以药物-环糊精结合物的形式存在,并且结合物的稳定性较好[8],而当释放介质中存在BSA时,仅发现B制剂在早期时(5 min)有极少游离药物释放,而A制剂未测到游离药物,提示在血清竞争性结合下可能导致弱结合药物从环糊精上快速释放。据该药品说明书,舒更葡糖钠注射液中含有单-羟基舒更葡糖,而单-羟基舒更葡糖与罗库溴铵和维库溴铵之间的亲和力约为舒更葡糖的50%。因此,引起不同厂家舒葡糖钠与罗库溴铵结合力和早期释放特性差异的原因可能是不同制剂中单-羟基舒更葡糖含量存在差异。

