成年朗格汉斯细胞组织细胞增生症误诊为肺癌1例报告
叶春雨,吴玉枝
(1山西医科大学第五临床医学院呼吸与危重症医学科,太原 030012;2山西省人民医院呼吸与危重症医学科;*通讯作者,E-mail:wuyuzhi1966@126.com)
朗格汉斯细胞组织细胞增生症(Langerhans cell histiocytosis,LCH)是一组原因不明、局部或全身组织内异常组织细胞增生性疾病,增殖的组织细胞形成大小不同的结节性病变,浸润邻近组织并破坏其结构,几乎可以发生在任何器官系统,但只有肝、脾、骨髓系统等造血组织的受累和功能障碍会影响生存期[1]。研究表明,LCH对骨骼、皮肤、肺和垂体有特殊的亲和性[2]。肺朗格汉斯细胞组织细胞增生症(pulmonary Langerhans cell histiocytosis,PLCH )是LCH累及肺的表现形式,主要影响有吸烟史的年轻男性。PLCH的组织学特征是由激活的朗格汉斯细胞、巨噬细胞、浆细胞和纤维母细胞对肺实质的浸润,这些细胞主要位于肺实质末端和呼吸性细支气管。常见的临床表现如咳嗽、咳痰、气短出现较晚,仅约10%~20%的患者有早期严重表现,包括反复气胸或慢性肺心病进行性呼吸衰竭[3]。LCH常由于临床症状的非特异性,再加上该病常累及婴幼儿,成年人发病并不多见,易误诊为其他疾病[4]。本文报告1例误诊为肺癌的成年男性LCH患者,根据该病例诊治过程中观察到的临床、实验室和影像学表现,期望帮助医生更快地识别和诊断LCH,避免误诊。
1 病例报告
患者,男,44岁,主因“左侧胸痛20 d,加重4 d”于2020年7月2日入院。患者20 d前无明显诱因出现左侧胸痛,为左后背部持续针刺样疼痛,部位局限,无放射痛,与活动及体位变化无关,无咳嗽、咳痰、气短、胸憋、咳血、发热等症状,未予重视。4 d前胸痛症状明显加重,就诊于朔州市人民医院呼吸科门诊行胸部CT,结果示双肺多发转移灶并左侧肋骨破坏(见图1)。当地医院考虑肺癌伴骨转移可能性大,建议住院进一步详细检查,患者拒绝。为求进一步治疗,就诊于我院呼吸科,患者自发病以来,精神、食欲、睡眠可,大小便正常,体重未见明显变化。既往有吸烟史30年,平均20~30支/d,未戒烟。20年前发现乙型病毒性肝炎,自诉规律治疗后好转(具体不详)。入院专科查体:体温36.2 ℃,P 66次/min,R 21次/min,血压134/68 mmHg。无皮疹,口唇无发绀,球结膜无水肿,颈静脉无充盈,咽部无充血,浅表淋巴结未触及肿大,左背部第10肋压痛阳性,双肺呼吸音清,未闻及明显干湿啰音,心律齐,各瓣膜听诊区未闻及病理性杂音。
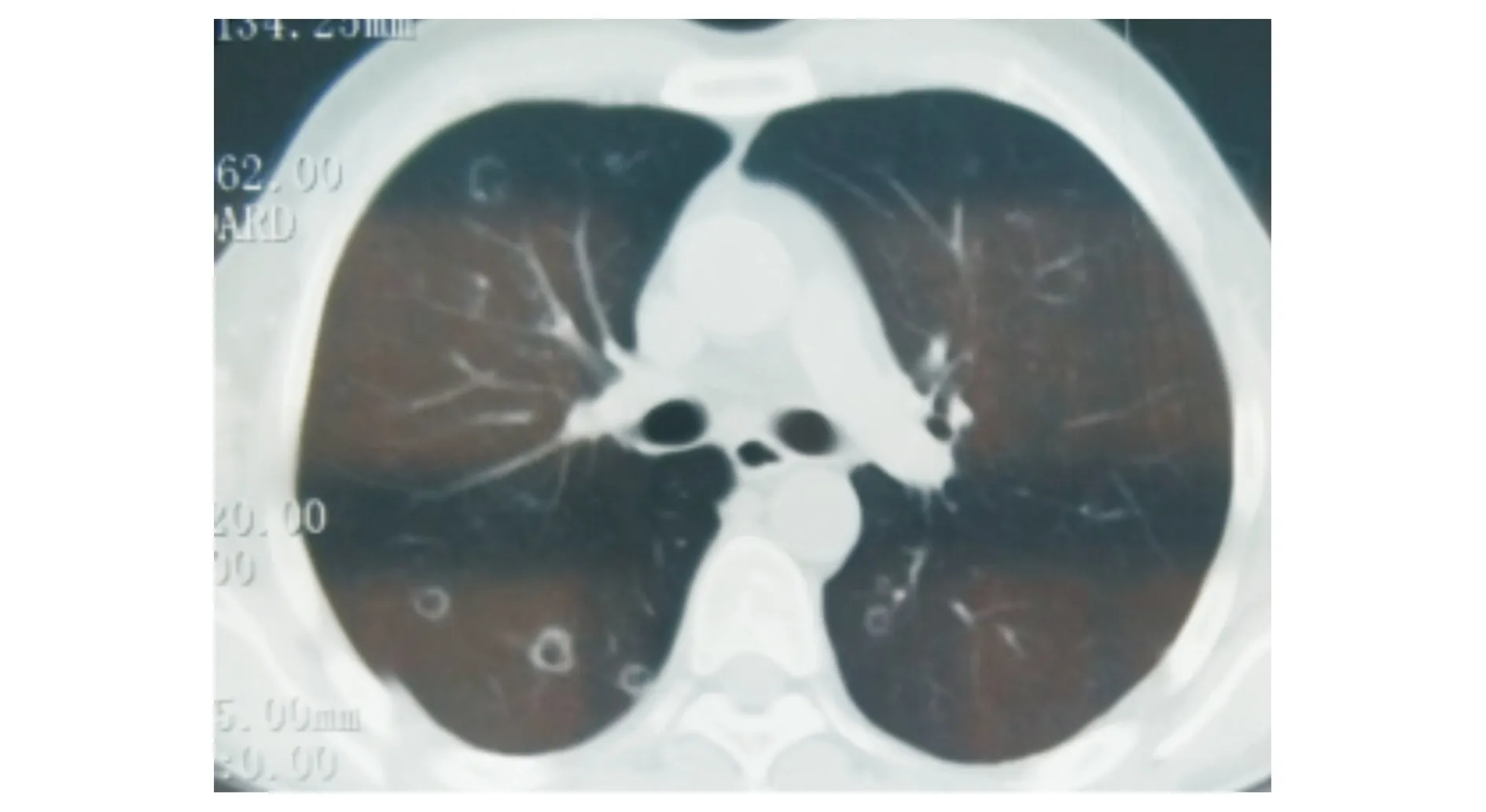
双肺散在多发空泡样结节,也可见1~2 mm磨玻璃结节,边界清,集中于中上肺野图1 入本院前患者胸部CT
初步考虑双肺多发结节伴空洞性质待查,病因可能是肺癌或肺结核。入院后化验血常规、肝肾功、电解质、凝血检查、风湿免疫、传染病系列、血气分析、尿液检查均无异常。反复痰培养、痰找抗酸杆菌、血G试验、GM试验均无异常发现。7月4日再次完善胸部增强CT提示左肺上叶软组织密度结节影、可见毛刺及分叶征、伴空洞形成,双肺多发结节伴空洞(见图2)。考虑左肺上叶Ca,伴双肺转移不除外,左侧第10肋骨骨质破坏,建议结合骨扫描。患者无明显呼吸系统疾病临床表现及体征,左侧胸部疼痛考虑左侧肋骨溶骨性病变所致,给与经验性抗感染、氯芬待因对症止痛治疗,同时进一步分析病因。
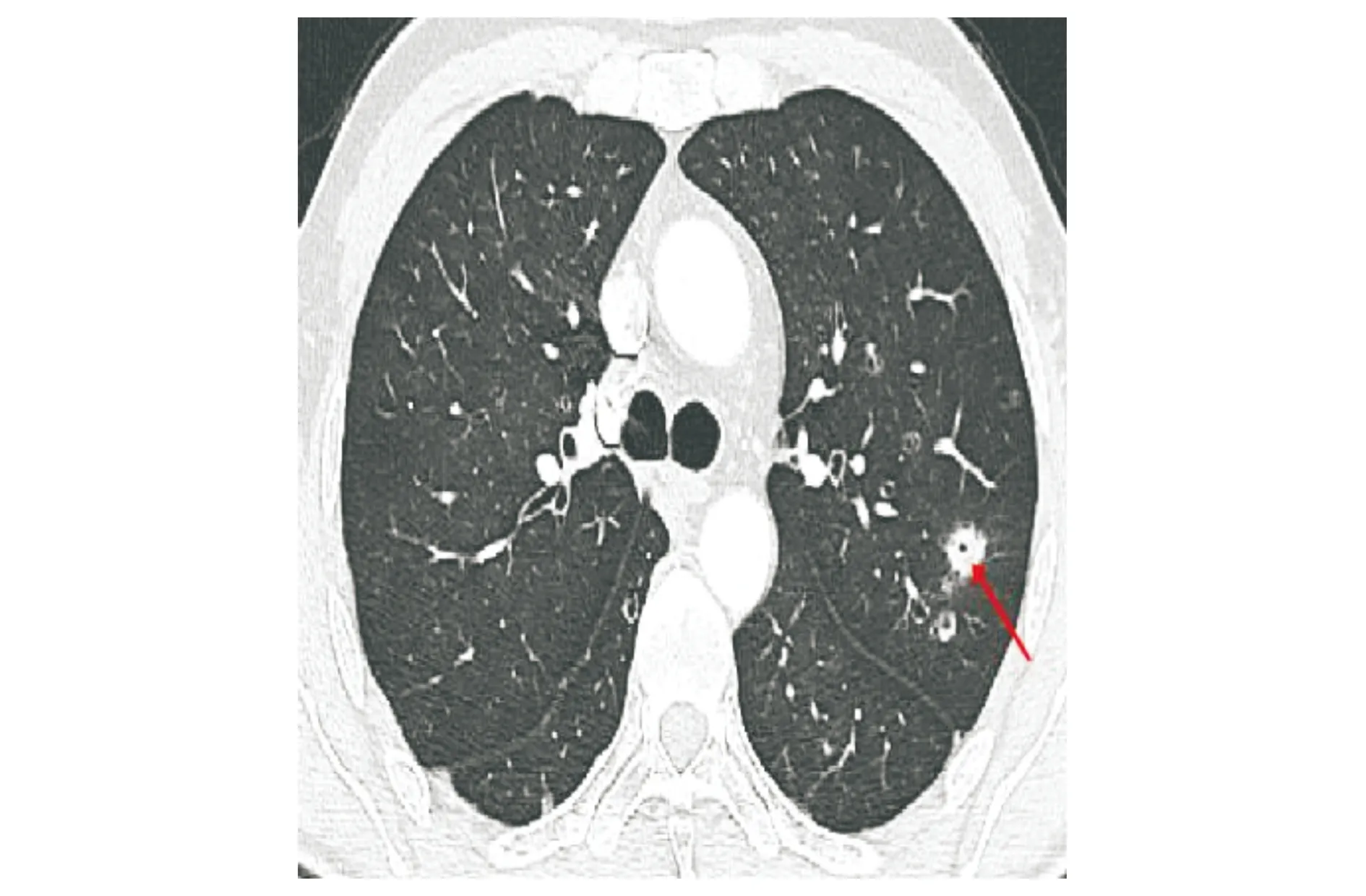
双肺多发大小不等类圆形结节影,大部分病灶内可见空洞形成影;左肺上叶(如箭头所指)最大结节为1.3 cm,可见毛刺征及分叶征图2 入院后患者胸部增强CT
根据辅助检查结果回报,认为胸部影像学表现为如此特点的多为腺癌,考虑肺腺癌可能性较大,但仍需除外身体其他部位腺癌(例如甲状腺、前列腺、肝脏)转移。完善甲状腺、腹部超声并无异常。化验:肿瘤标记物(前列腺特异性抗原、癌胚抗原、CA125、CA199、鳞状角蛋白19片段、神经元特异性烯醇化酶)均正常。行支气管镜检查可见各支气管管口通畅、未见新生物形成、散在脓性分泌物予以吸出。7月3日全身骨扫描:左侧第10后肋放射性核素分布增高,其余全身各骨未见明显放射性核素分布异常浓聚或稀疏缺损区(见图3)。结果表明:左侧第10后肋骨质破坏,伴周围骨质代谢性增高,性质待定。全身浅表淋巴结彩超:左锁骨上窝可见多发低回声结节,较大的约0.8 cm×0.4 cm,淋巴结结构欠清。
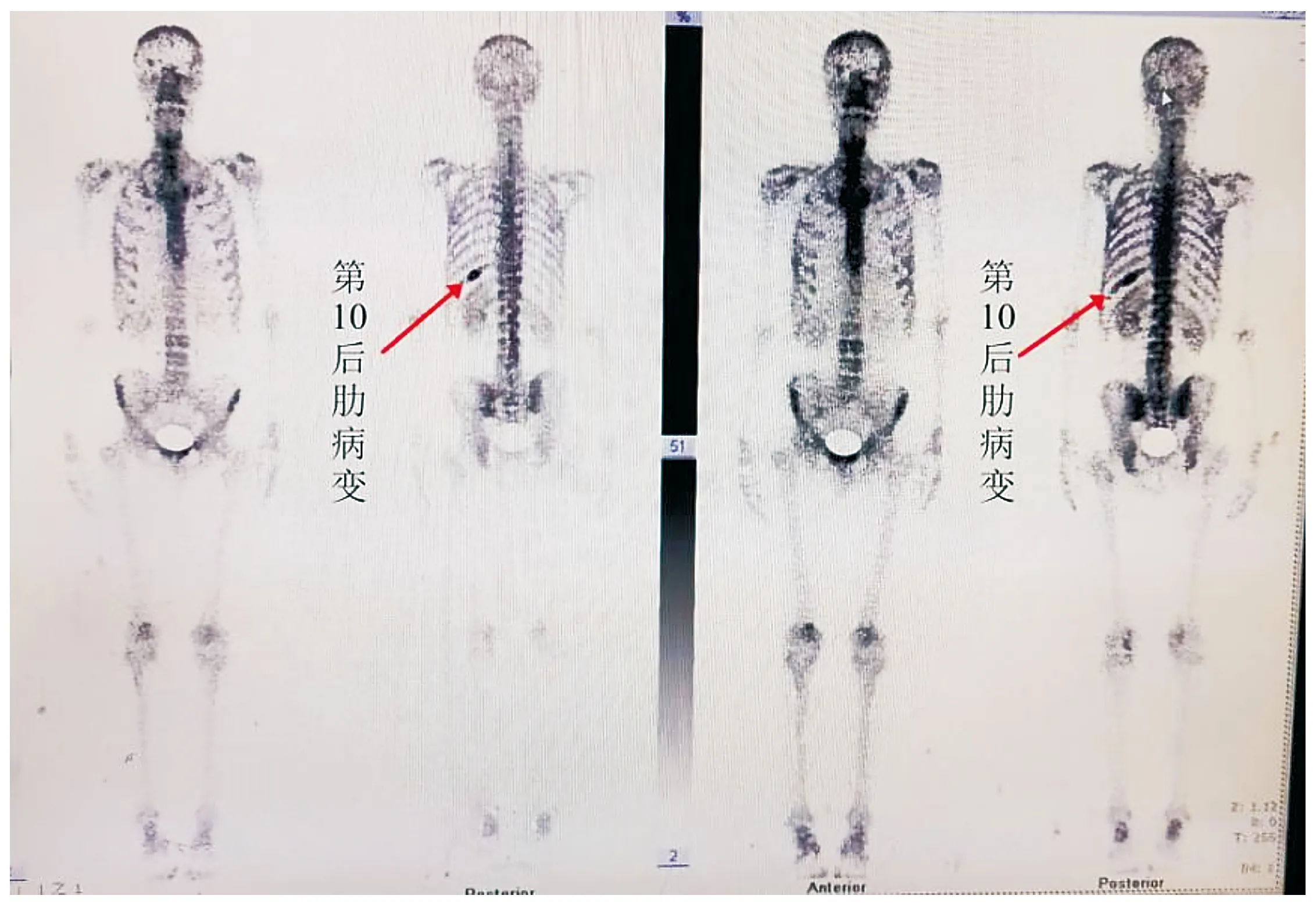
左侧第10后肋放射性核素摄取增加,伴周围骨质代谢增高,其余全身各骨放射性核素基本均匀图3 入院后全身骨扫描
考虑到近4 d症状有所加重,影像学病灶短期内增大与肿瘤不完全相符,仍需要除外感染等可引起胸部影像学迅速改变的因素。支气管镜检查结果回报:灌洗液及刷片找抗酸杆菌均为阴性;双肺灌洗液一般细菌培养、真菌培养均无菌生长;灌洗液G试验、GM试验均阴性;PPD试验阴性;结核抗体阴性。综上,进一步化验检查并未明确病因,仍需更深入分析。考虑到经皮肺穿刺活检双肺病灶均较小,淋巴结也偏小,穿刺难度大,与骨科医师会诊后,除外活检禁忌证,于2020年7月7日行CT引导下左后第10肋骨病灶处取活检,术后患者无特殊不适。组织病理学结果回报:骨病理活检形态结合免疫组化结果符合LCH(见图4),请结合临床。免疫组化:TTF-1(-),CK5/6(-),CK7(-),Ki-67(热点区约50%),CD38(-),CD138(-),MCK(-),LCA(少量+),CD68(散在+),CD163(散在+),D1 α(+),Langerin(+),S-100(+),最终确定为LCH。
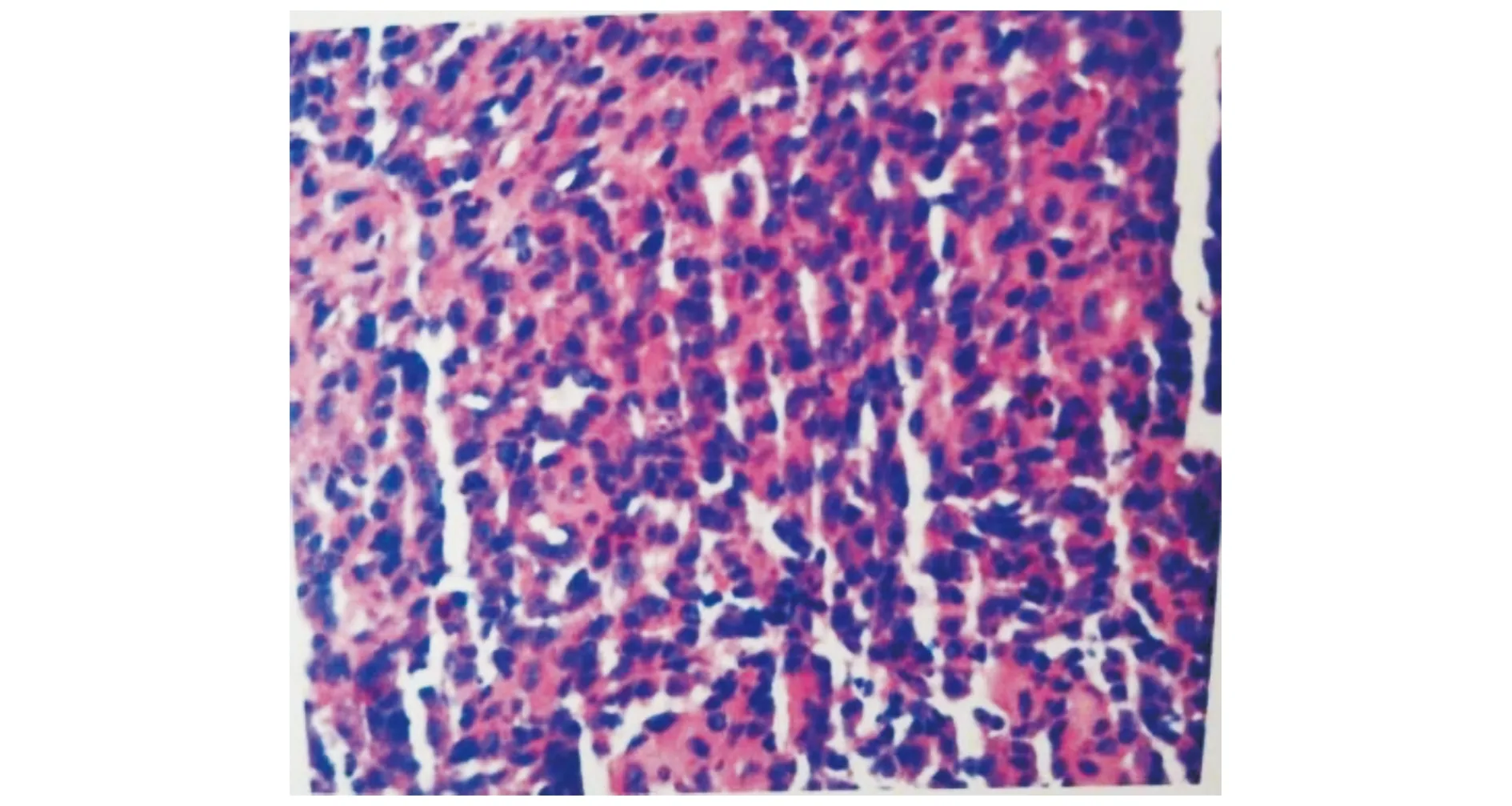
大量朗格汉斯细胞、少量嗜酸性粒细胞浸润图4 骨病理组织HE染色 (×100)
确诊后嘱其严格戒烟,后患者就诊于我院血液科,血液科给与甲氨蝶呤和阿糖胞苷化疗4个周期,随后患者就诊于山西省肿瘤医院,继续给与原方案化疗。8个月后随访患者胸痛缓解,无特殊不适,胸部CT表现见图5,可见左侧软组织密度结节影明显减小,其余多发类圆形结节伴空洞影消失,肺纹理清晰,病灶较前明显吸收。
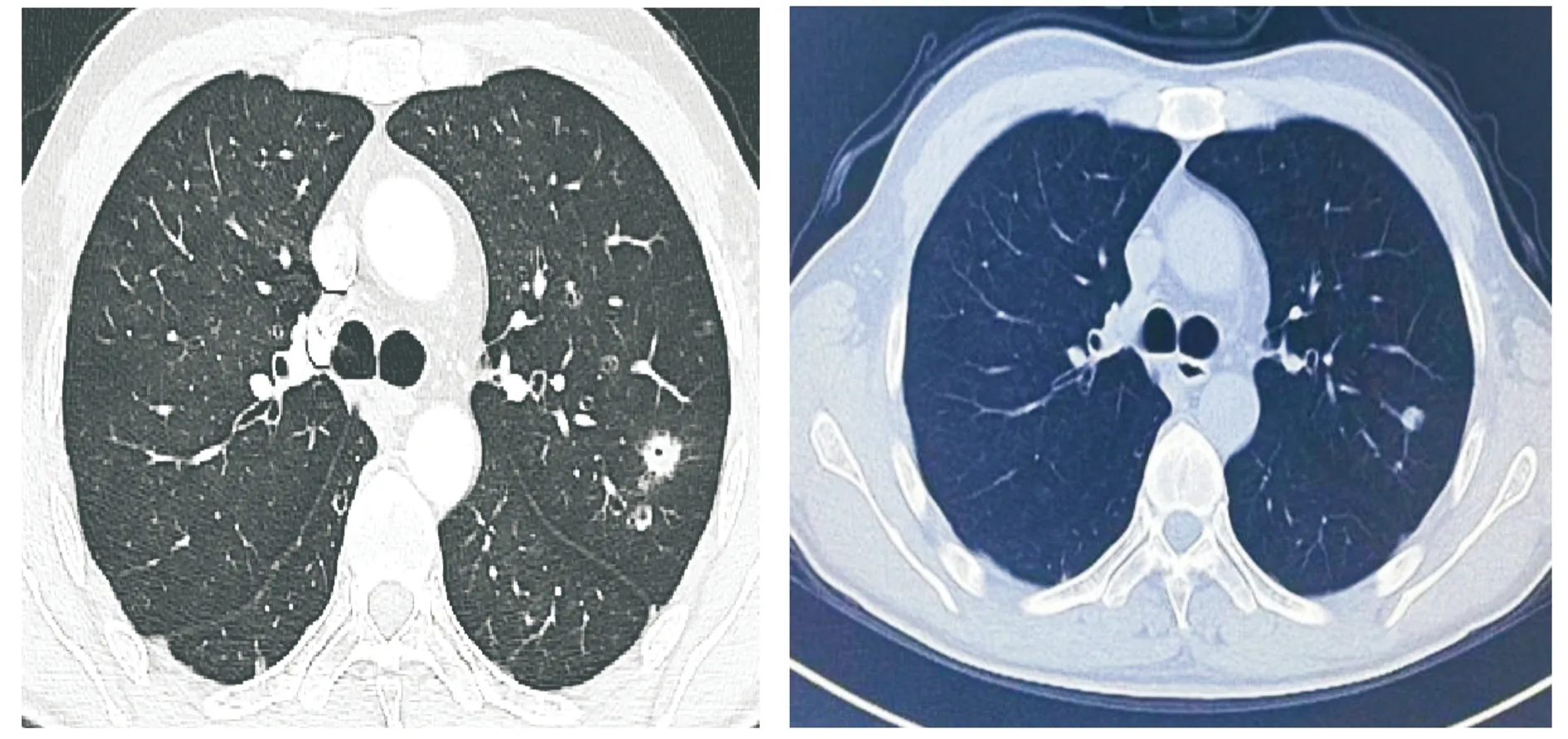
A.治疗前(2020年7月4日)B.治疗后(2021年3月21日)图5 患者治疗前后胸部CT对比
2 讨论
LCH是一种罕见的组织细胞疾病,在2016年修订的组织细胞学会分类中,LCH被定义为一种炎性髓系肿瘤[5]。由骨髓来源细胞的异常增殖引起的LCH在儿科人群中更为常见,成人LCH的确切发病率尚不明确,估计为每年每百万人中1~1.5例确诊此病[6]。
目前临床上基于诊断时涉及的病变范围将LCH分为单系统LCH(SS-LCH)和多系统LCH(MS-LCH),在SS-LCH中,病变只涉及一个器官或系统,比较常见的有骨骼(约80%)、皮肤(33%)、脑垂体(25%)和肺(15%),其他器官诸如淋巴结(不是另一个LCH病变的引流淋巴结)、甲状腺和胸腺等也会被LCH累及[7]。在MS-LCH中,有两个或两个以上的器官或系统被累及。本报告病例以此被分为LCH多系统病变,具体累及肺和骨。LCH累及肺病变主要发生在年轻吸烟者中,在男女中均无优势,典型的临床表现包括咳嗽、呼吸困难和胸痛等,需要注意的是多数患者的肺部病变是在胸部影像学检查中偶然发现的。在本报告中该病例长期抽烟,以胸痛起病,并无典型的咳嗽、咳痰、呼吸困难等临床表现,查体除左后背肋骨压痛外,无明显阳性体征,肺部病变是在患者因胸痛完善胸部CT时发现的。由于本例发现较早,肺功能包括一秒用力呼气容积(FEV1)、用力肺活量(FVC)和一氧化碳弥散量(DLCO)尚未受影响。肺受累损伤主要发生于肺的中上部,其形态学进展通常以一个非常有特点的顺序发展,开始形成小结节,称为中央小叶结节,接着是结节内空化,发展成厚壁囊肿,甚至生长成薄壁囊肿。囊肿的持续生长最终破坏了囊壁,导致形成形状奇异的大囊肿[8]。本例中胸部影像学表现为多发结节伴空洞形成、多发厚壁囊肿。需要注意的是,这种影像学病变特征呼吸科很多疾病,如肺结核、肺脓肿、支气管扩张、肺癌等都会表现,需进行鉴别诊断,否则容易误诊,本病例在前期被误诊为肺癌。后经支气管镜检查未能发现新生物以及未识别到肿瘤细胞或病原体,使用抗生素治疗后影像学病灶并未见变化,考虑既往判断有所偏差,及时进行的病变肋骨病灶病理活检,最终明确诊断为LCH。在2019年进行的组织细胞学年度会议上[9],国际专家首要推荐:即使临床和影像学特征高度提示的情况下,也建议对病变组织进行活检,以确认LCH诊断。LCH的病理特点为:细胞核核大而有凹槽,富含嗜酸性细胞质,反应性炎症细胞背景常见,且常有嗜酸性粒细胞浸润。免疫组化可见CD207和CD1 α(+),S-100(+),电镜检查可见朗格汉斯巨细胞。本病例光镜下可见大量朗格汉斯细胞、嗜酸性粒细胞等组织细胞密集浸润,免疫组化结果证实LCA(少量+)、CD68(散在+)、CD163(散在+)、CD1 α(+)、Langerin(+)、S-100(+),LCH诊断证据充分。
至今还没有针对成人LCH患者的明确治疗方法。LCH的治疗因其异质性表现而异,成人LCH高度强调个体化治疗,建议基于疾病程度及风险分层制定治疗方案。2019年组织细胞学会年会得出的共识建议[10]:单灶LCH通常只需局部治疗,一般预后良好,局部治疗无效的单灶性疾病(垂体、中枢神经系统和心脏)应考虑全身治疗。单系统PLCH应结合呼吸道症状、肺部影像学病变、肺功能损害的程度而决定治疗用药,晚期单系统PLCH患者肺移植可能是唯一的治疗选择。对于有症状且病变数量有限的纯骨疾病,放射治疗是一种有效的选择。而多灶单系统LCH及多系统LCH多采用化疗、靶向治疗、造血干细胞移植方案,免疫治疗成为当前治疗新的研究方向。甲氨蝶呤+阿糖胞苷已被推荐用于多系统受累的成人LCH患者[11]。本例患者病变累及多系统,后血液科给与甲氨蝶呤、阿糖胞苷方案化疗,8月后再次复查,胸痛已完全缓解,胸部影像学提示病灶已大部分消除。
综上所述,由于PLCH发病较为罕见、临床症状呈现非特异性、实验室大部分结果正常、胸部影像学难以鉴别等原因,导致该病容易被误诊。典型的影像学表现为小叶内小结节、空化结节、薄壁和厚壁囊肿,常合并,早期的病灶活检及组织病理诊断能够对LCH在临床治疗及疗效评估方面发挥重要作用。本文的报道将有助于进一步提高临床医生对该病的认识及诊疗水平。

