非诺贝特联合熊去氧胆酸治疗难治性原发性胆汁性胆管炎的Meta分析
王学昌, 宣乐乐, 尚 鑫, 王勤三, 宋子瑞, 宣国云, 刘 宁, 许 昂, 孙 昊, 李 萍
1.聊城市人民医院消化内科,山东 聊城 252000;2.东海县人民医院神经内科;3.南部战区空军医院卫勤处;4.空军军医大学基础医学院;5.空军军医大学西京医院消化内科
原发性胆汁性胆管炎(primary biliary cholangitis,PBC)是一种慢性自身免疫性肝内胆汁淤积疾病,其病因与发病机制目前尚未完全清楚,有研究报道与遗传因素及环境因素相互作用所导致的免疫紊乱有关[1]。PBC多见于中老年女性,最常见的临床表现为乏力和皮肤瘙痒,其血生物化学指标的主要特点是ALP、GGT、IgM升高,病理学特点是非化脓性破坏性小胆管炎[2]。
熊去氧胆酸(Ursodeoxycholic acid,UDCA)是经FDA批准治疗PBC的一线治疗药物,UDCA的治疗效果十分显著,可以很好地提高患者生活质量,延长其生存期,延缓组织病理学进展,并且具有很高的安全性[3]。然而仍有约40%的PBC患者对UDCA单药治疗存在不良应答现象,相关临床指标并未明显下降,甚至还有部分患者病情会进一步发展为死亡或需要肝移植,治疗效果并不理想[4]。
非诺贝特属于一类通过激活过氧化物酶体增殖物激活受体α (peroxisome proliferators-activated receptor α, PPARα) 发挥作用的药物,临床上常用于治疗高胆固醇血症和高甘油三脂血症[5]。但近些年有部分研究表明,非诺贝特在治疗难治性PBC的试验中可通过抑制胆汁酸的生成,进而较好地改善患者的生化和免疫学指标,并且未发生更多的不良反应事件[6]。因此,本文采用Meta分析方法来评估UDCA和非诺贝特联用治疗与UDCA单药治疗的疗效,并通过对比PBC患者各项指标的变化来分析UDCA联用非诺贝特方案在治疗难治性PBC的优越性。
1 资料与方法
1.1 文献检索纳入的文献均通过计算机检索PubMed、Embase、The Cochrane Library等英文数据库,及中国知网、万方、维普、中国生物医学文献数据库等中文数据库,检索自建库至2021年12月公开发表的相关文献,并结合手动搜索相关文献,根据检索结果中所参考的文献进一步查找文献,防止漏查。
1.2 纳入及排除标准
1.2.1 纳入标准:(1)单用UDCA治疗与UDCA联合非诺贝特治疗比较的随机对照试验或临床对照试验。(2)满足以下3条标准中的2条即可诊断为PBC:①存在胆汁淤积的生物化学证据(主要是ALP和GGT升高),且影像学检查排除了肝外或肝内大胆管梗阻;② AMAs/AMA M2阳性,或其他PBC特异性自身抗体(抗gp210抗体、抗sp100抗体)阳性;③ 组织学上有非化脓性破坏性胆管炎和小胆管破坏的证据[7]。(3)所有患者均未使用其他肝病治疗药物。(4)研究报道至少包括评价疗效的指标如生化指标和(或)免疫学指标、生存率等中的一项。(5)对于同一团队的研究,取病例最多,数据最全的结果。
1.2.2 排除标准:(1)重复的文献。(2)无数据可提取的文献。(3)随机对照试验以外的其他试验形式。
1.3 数据提取提取所有纳入研究的第一作者姓名、发表年份、患者性别、年龄、例数、治疗剂量及疗程、生物化学指标、临床症状、不良反应、生存率等。
1.4 纳入研究的偏倚风险评估由研究者根据Cochrane评价手册对纳入的文献进行评价,主要根据以下6个方面进行评价:(1)随机分配方法。(2)分配方案的隐藏。(3)盲法的使用。(4)结果数据的完整性。(5)选择性报告的结果报道。(6)其他偏倚来源。同时由研究员独立检查偏倚风险,低偏倚风险用“是”表示,不确定偏倚风险用“不确定”表示,高偏倚风险则用“否”表示。
1.5 统计学方法对提取的资料采用Cochrane系统评价软件RevMan 5.4进行Meta分析。对于二分类计数资料计算各文献的OR值及95%CI。对于连续性变量资料使用均数差(MD)及95%CI。我们主要使用Q检验和I2检验来检验异质性,当P<0.10或I2>50%被认为具有显著异质性,此时采用随机效应模型分析。当P≥0.10且I2≤50%时使用固定效应模型。必要时使用亚组及敏感性分析,并制作漏斗图评估发表偏倚。
2 结果
2.1 文献筛选结果该Meta分析包括16篇文献[1-16]。其中6篇为中文文献[7,10,12-14,16],10篇为英文文献[1-6,8-9,11,15],发表时间为2002年至2021年,共纳入850例患者,文献筛选流程如图1所示,年龄41~61岁,随访时间3个月~8年。非诺贝特的常用剂量为200 mg/d。16篇研究的一般资料如表1所示,纳入研究中临床事件和生化参数变化如表2所示。
2.2 质量评价与偏倚风险评估对最终纳入的16篇研究进行质量评价。图2为风险偏倚图,显示了所有纳入文献相对于每个偏倚风险项目的评估。图3为偏倚风险总结图,即对所有纳入文献产生的偏倚风险项目所占百分比的评估。图4为该Meta分析的漏斗图,即对所有纳入文献的GGT、不良事件、瘙痒症状和ALT进行发表偏倚评估。
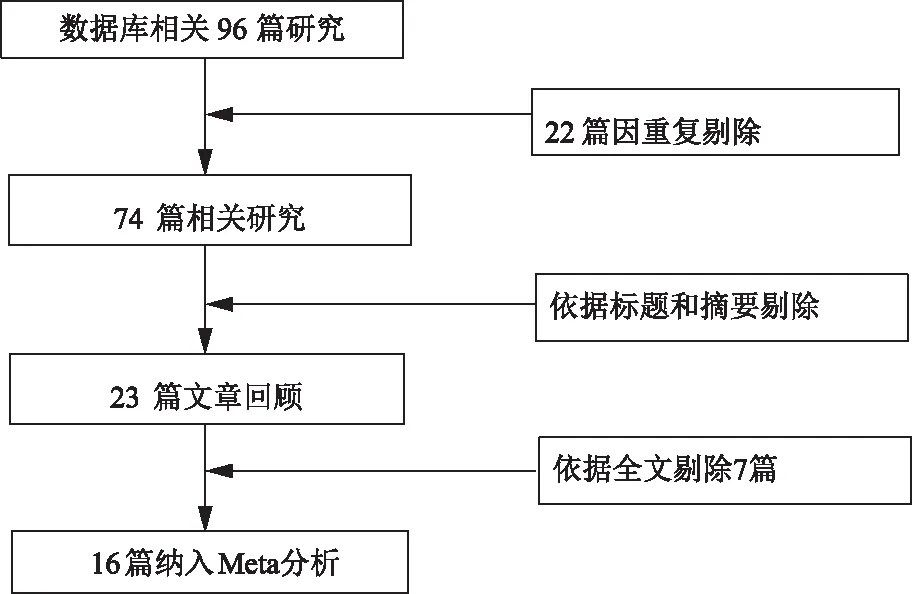
图1 文献筛选流程
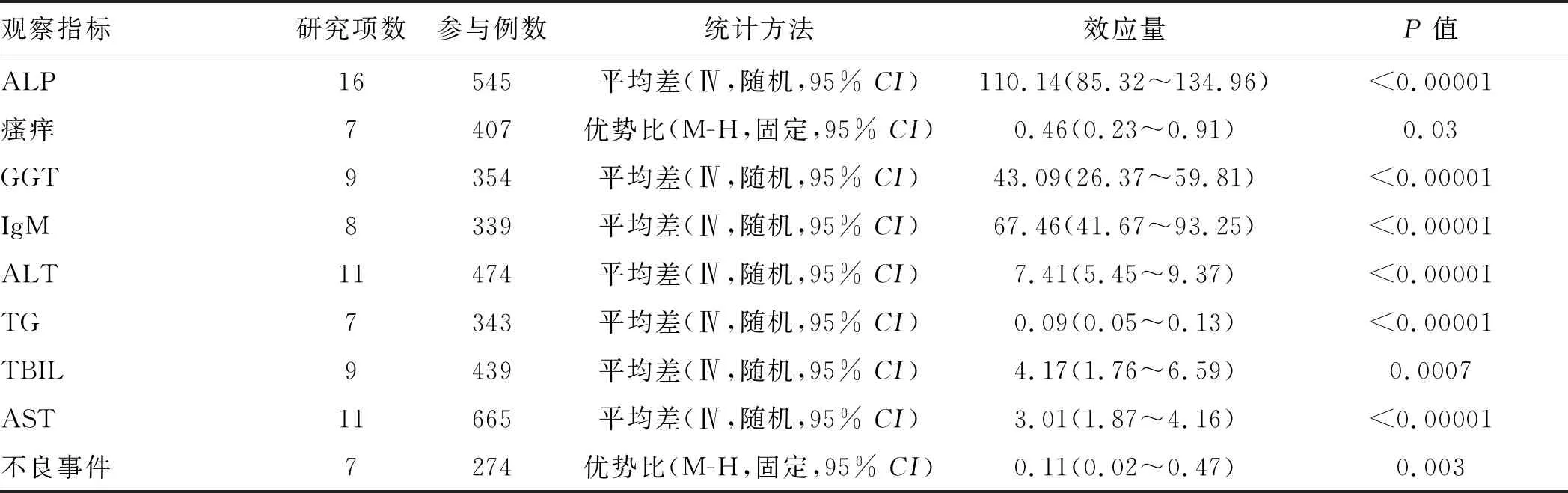
表2 纳入研究中临床事件和生化参数变化Tab 2 Changes in clinical events and biochmical parameters in included studies

图2 偏倚风险图:对所有纳入研究中每个偏倚风险项目的判断
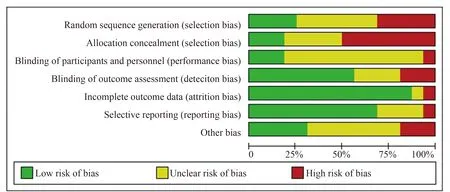
图3 偏倚风险图:对所有纳入研究中每个偏倚风险项目的判断,以百分比形式呈现
2.3 结局指标16项研究[1-16]报告了两种治疗方式对患者症状的临床结果,并发现联合治疗显著改善了肝功能并降低了相应血生化指标。也有研究[1,2,4-8]报告了发生不良事件,但发生率并未明显提高,研究中未报告死亡事件。
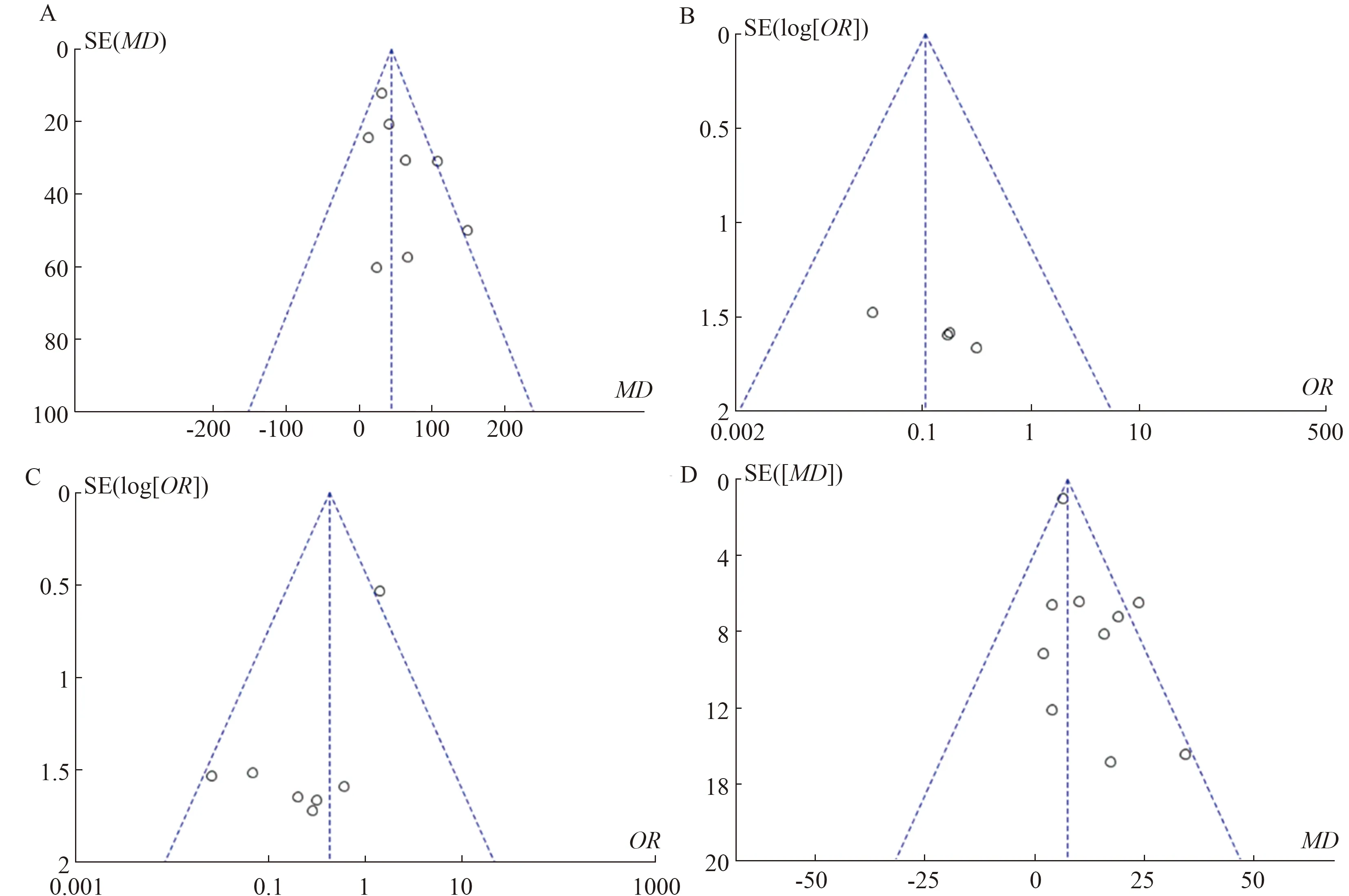
注:A:GGT;B:不良事件;C:瘙痒症状;D:ALT。
2.4 Meta分析结果
2.4.1 ALP水平:有16篇文献[1-16]报道了ALP水平的变化,但由于其I2>50%,对其进行敏感性分析后,得到可用文献13篇[1-12, 14],其中UDCA单药治疗298例,联合治疗247例,结果显示,MD=110.14 U/L;95%CI:85.32~134.96,表明UDCA联用非诺贝特在改善ALP效果上具有明显优势,差异有统计学意义(P<0.00001)(见图5)。
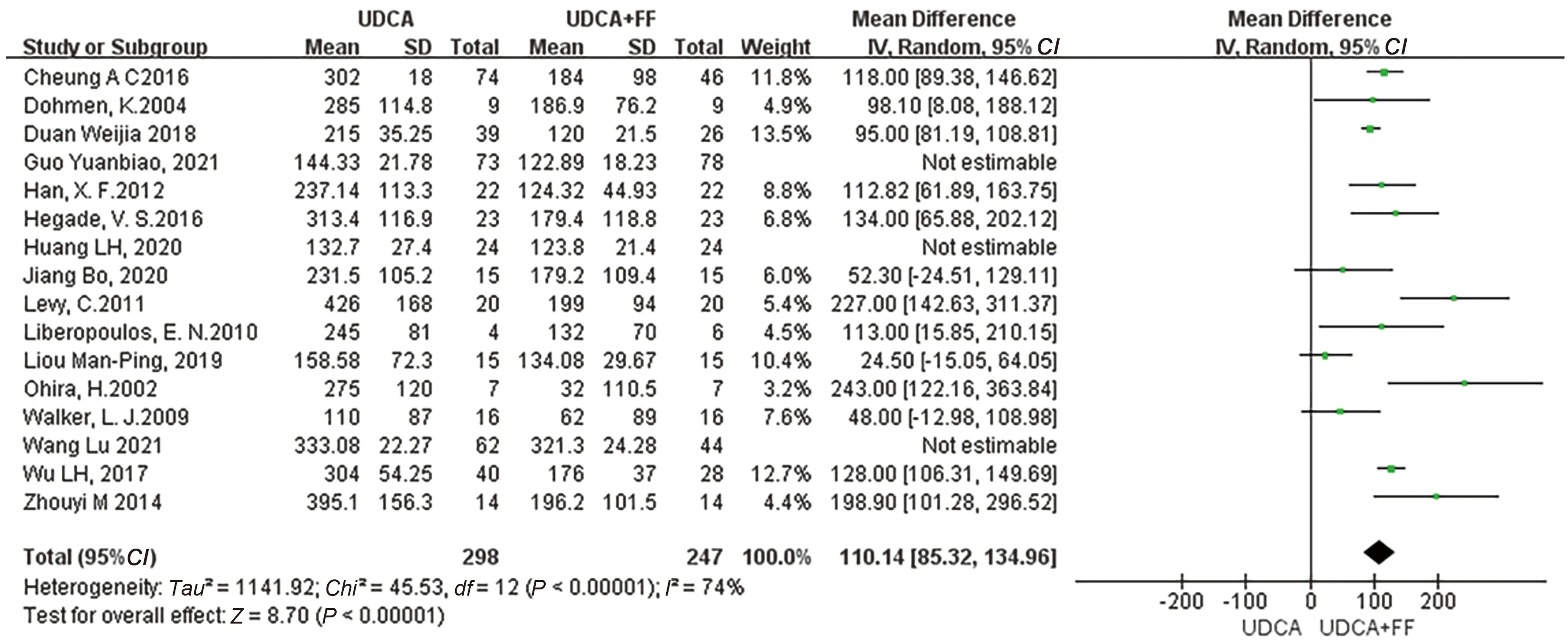
图5 治疗组与对照组的PBC患者的ALP水平
2.4.2 GGT水平:有9篇文献[2,4,6-7,10,12-15]报道了GGT水平的变化,通过敏感性分析之后,得到可用研究8篇[2,4,6,10,12-15],其中UDCA单药治疗191例,联合治疗163例,结果显示MD=43.09 U/L,95%CI:26.37~59.81,表明UDCA联用非诺贝特在改善GGT效果上具有明显优势,差异有统计学意义(P<0.00001)(见图6)。
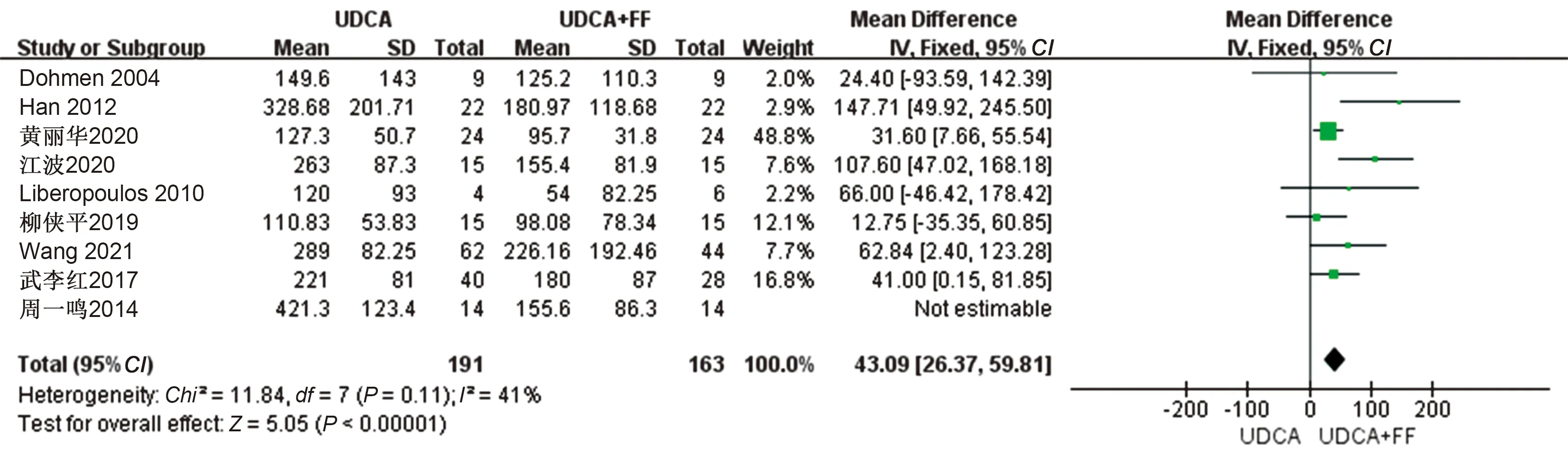
图6 治疗组与对照组的PBC患者的GGT水平
2.4.3 ALT水平:有11篇研究[2,4,12-15]报告了ALT的水平变化,通过敏感性分析,得到可用研究10篇[2,4-8,12-15],其中UDCA单药治疗259例,联合治疗215例,结果显示MD=7.41 U/L,95%CI:5.45~9.37,表明UDCA联用非诺贝特在改善ALT效果上具有明显优势,差异有统计学意义(P<0.00001)(见图7)。
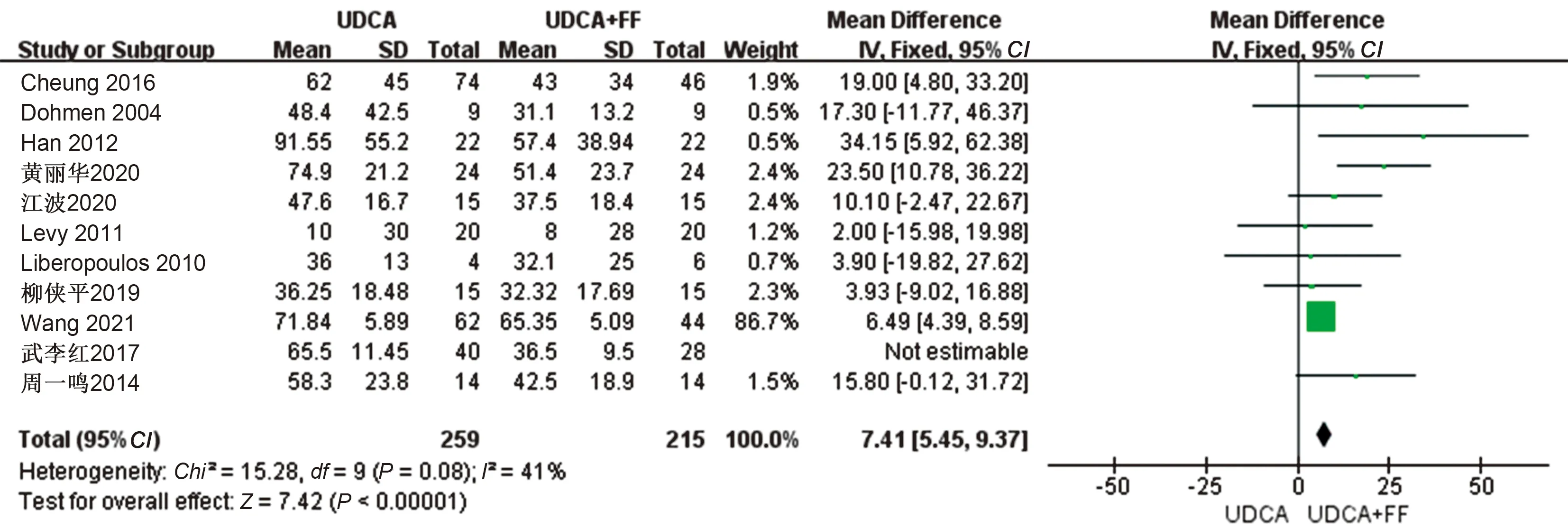
图7 治疗组与对照组的PBC患者的ALT水平
2.4.4 AST水平:有10篇研究[5-8,10,12-16]报告了AST的水平变化,其中UDCA单药治疗359例,联合治疗306例,结果显示MD=3.01 U/L,95%CI:1.87~4.16,表明UDCA联用非诺贝特在改善ALT效果上具有明显优势,差异有统计学意义(P<0.00001)(见图8)。

图8 治疗组与对照组的PBC患者的AST水平
2.4.5 IgM水平:有8篇研究[2-3,5,10,12-13,15-16]报道了IgM的水平变化,通过敏感性分析之后,得到可用研究7篇[2-3, 5,10,12-13,15],其中UDCA单药治疗186例,联合治疗153例,结果显示MD=67.46 U/L;95%CI:41.67~93.25,表明UDCA联用非诺贝特在改善IgM效果上具有明显优势,差异有统计学意义(P<0.00001)(见图9)。
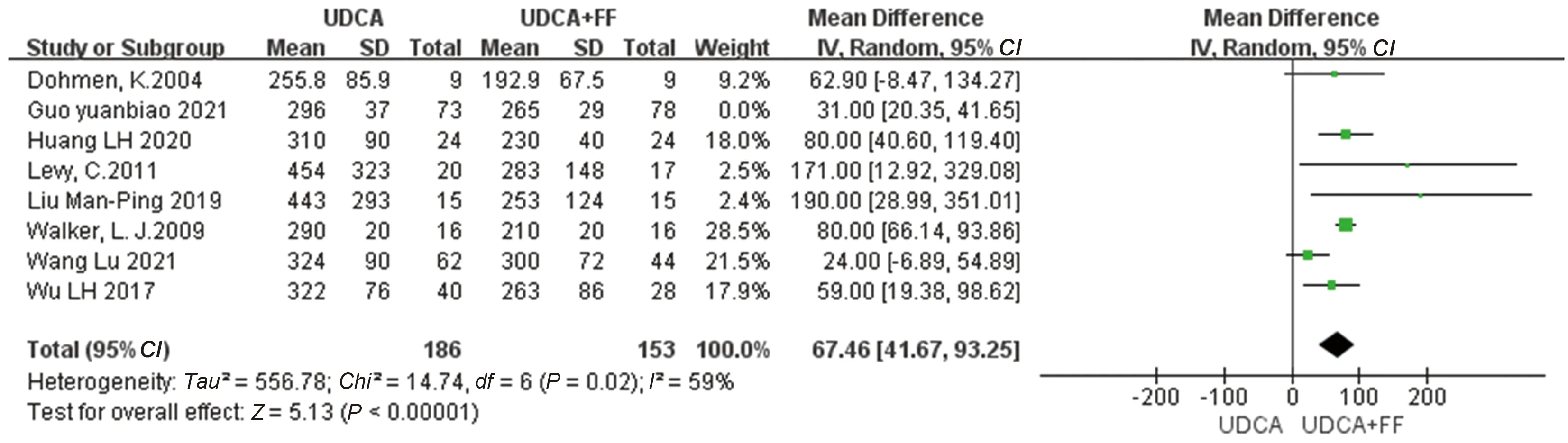
图9 治疗组与对照组的PBC患者的IgM水平
2.4.6 TG水平:有7篇研究[2,4-6,10,12,16]报道了TG的水平变化,通过敏感性分析之后,得到可用研究6篇[4-6,10,12,16],其中UDCA单药治疗174例,联合治疗169例,结果显示MD=0.09 U/L;95%CI:0.05~0.13,表明UDCA联用非诺贝特在改善IgM效果上具有明显优势,差异有统计学意义(P<0.00001)(见图10)。
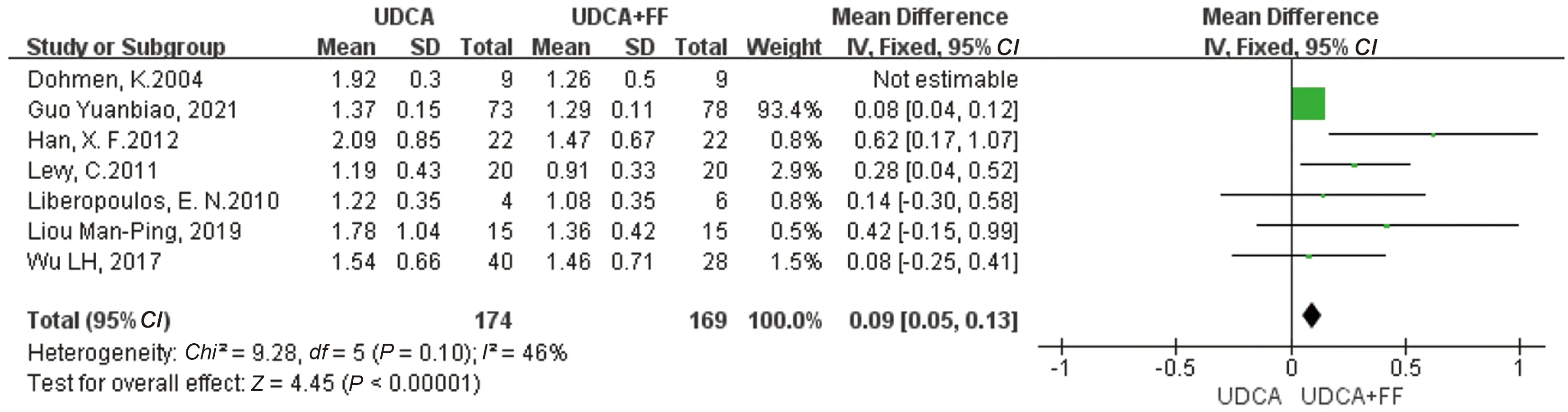
图10 治疗组与对照组的PBC患者的TG水平
2.4.7 TBIL水平:有9篇研究[5-7,10,12-16]报道了TBIL的水平变化,通过敏感性分析之后,得到可用研究8篇[5-7,10,12-14,16],其中UDCA单药治疗223例,联合治疗216例,结果显示MD=4.17 U/L;95%CI:1.76~6.59,表明UDCA联用非诺贝特在改善TBIL效果上具有明显优势,差异有统计学意义(P=0.0007)(见图11)。

注:文献[15]Wang 2021数据未纳入最终的分析。图11 治疗组与对照组的PBC患者的TBIL水平
2.4.8 瘙痒水平:有7篇研究[1,4-8,16]报道了瘙痒,其中联合治疗组193例中有24例瘙痒症状得到改善,UDCA单药治疗组214例中有10例瘙痒症状得到改善,异质性检验提示P=0.10,I2=44%,采用固定效应模型。结果显示在改善瘙痒症状方面联合非诺贝特治疗比单用UDCA治疗稍有优势,但并不显著,差异有统计学意义(OR=0.46,95%CI:0.23~0.91,P=0.03)(见图12)。
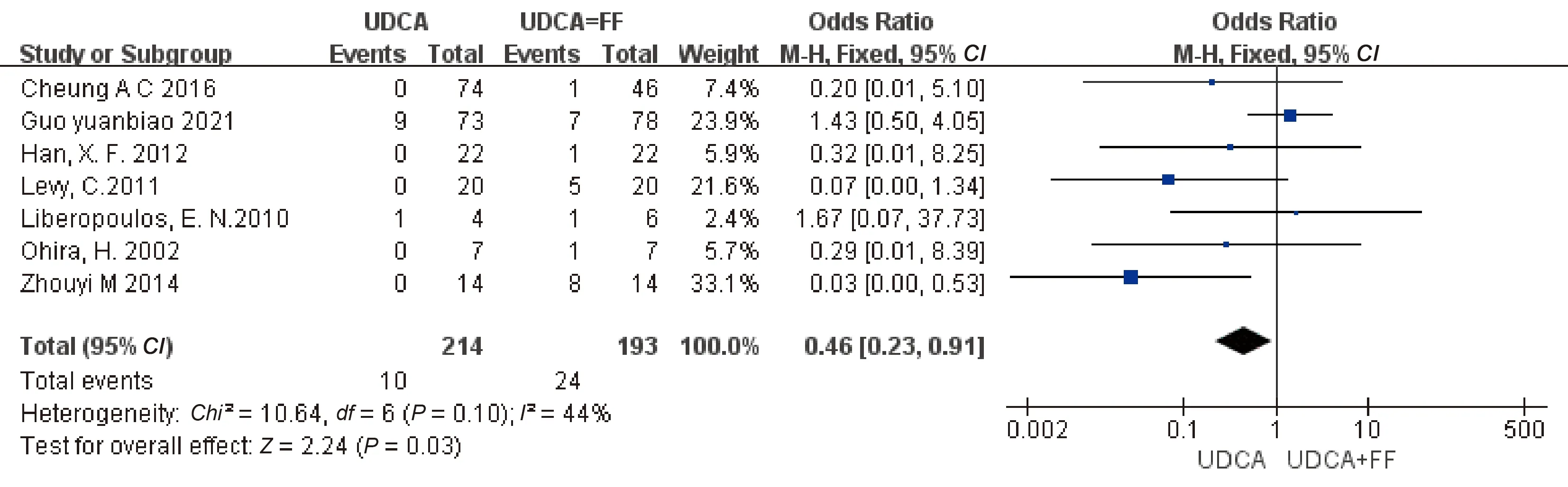
图12 治疗组与对照组的PBC患者的瘙痒水平
2.4.9 不良事件水平:有7篇研究[8-9,11-15]报道了发生不良事件,其中UDCA单药治疗150例中未发生不良事件,联合治疗124例中有12例发生了不良事件,异质性检验提示P=0.75,I2=0,采用固定效应模型。结果显示在发生不良事件方面联合非诺贝特治疗比单用UDCA治疗出现了更多的不良事件,但不良事件的增加数量上并不显著,差异有统计学意义(OR=0.11,95%CI:0.02~0.47,P=0.003)(见图13)。
3 讨论
PBC又称原发性胆汁性肝硬化,是一种慢性肝内胆汁淤积性疾病,主要以肝内胆管进行性非化脓性炎性反应为特征,可发展为肝纤维化和肝硬化[17]。UDCA目前是治疗PBC的一线用药,目前国际上有多种评价UDCA治疗后生物化学应答的标准,其中巴黎Ⅰ和巴黎Ⅱ标准应用较多,分别用于评价晚期PBC(Ⅲ~Ⅳ期)和早期PBC(Ⅰ~Ⅱ期)患者生化应答[18]。生物化学应答良好的患者可以极大地提高生存率,然而有部分患者对UDCA的治疗效果并不明显,对于这部分患者的长期生存率有明显的降低[19],这是目前临床治疗的难点。
近年来有研究报道,贝特类药物在临床上可用于治疗高甘油三酯血症和混合性高脂血症,也有抗炎、抗纤维化、降低胆汁淤积的效果,可以降低PBC患者的生化指标,然而对瘙痒症状改变不明显[20]。尽管已经发表了许多观察性研究,但贝特类药物降低胆汁淤积生物化学标志物的机制以及应用贝特类药物治疗是否能提高这些疾病患者的生存率仍不清楚,并且相关报道研究样本量小,随访时间差异大,不能很好地反映出联合用药的疗效和安全性,以及长期治疗是否可以改善生存率[21]。
研究认为,PPAR-MDR3-PL可能是非诺贝特主要的抗胆汁淤积机制,来自于肝细胞胆管膜侧的多药耐药蛋白3(multiple drug resistance 3, MDR3)是磷脂分泌的主要决定因素,PPAR激动剂(而非诺贝特是特异性PPARα激动剂)可通过上调MDR3促进胆汁中磷脂酰胆碱的排泄,使胆汁盐细胞毒性降低,同时还可以抑制胆汁酸形成[22]。对于抗炎作用机制,研究认为 PPARα可能是通过反调节干扰促炎性转录因子如核因子κB(nuclear factor κ-B, NF-κB)、信号转导和激活因子等转录因子通路,抑制 mRNA 及蛋白表达,从而减少p65介导的基因激活促炎细胞因子从而发挥抗炎作用[23]。然而,UDCA的作用机制是不同的。UDCA的主要作用是改善有毒和无毒疏水胆汁酸之间的平衡,激活胆汁酸、磷脂和胆固醇的分泌[24]。因此,它与贝特类发挥作用的方面并不重叠,非诺贝特和UDCA的联合治疗可能比UDCA单药治疗更有效。为此本文通过Meta分析方法系统地研究联合治疗对UDCA反应不佳的患者的疗效与安全性,意义是十分重要的。
本研究也有一定的局限性。尽管我们纳入了16篇文献,但由于检索策略局限性以及数据库覆盖范围有限,可能存在遗漏应该纳入的高质量文献,导致对本次研究的结果有所影响。除此之外我们只纳入了已发表的文章,对一些尚未发表的文章并未进行评价。再有本文纳入的随机对照试验的样本量有限。在方法上我们主要评估了联合治疗和单药治疗对于生物化学指标的治疗差异,缺乏对组织学的评估,无法研究是否可以延缓组织学进展。并且由于随访时间不同,无法统计死亡率,所以对于是否可以改善长期存活率还有待进一步的证实。如果样本量更大,随访时间更长统计结果才更有说服力。所以希望可以有更大的样本量,多中心的随机对照试验来进一步评价UDCA联用非诺贝特治疗的长期疗效和生存率,以此来指导临床上治疗难治性PBC的用药。
最后,UDCA联用非诺贝特对于治疗难治性PBC取得了良好的临床结果,这将是对UDCA反应不佳的患者临床治疗很好的替代方案。但联合用药在改善瘙痒方面和降低TBIL上不明显,联合治疗也可能会引起一些不良反应事件的增加。最后还需要更大的样本量和更长随访时间来评估疗效,还要观察是否可以改善患者的组织学情况。

