电沉积制备铜基催化剂及其对CO2电还原的催化性能
楚萌恩,陈春俊,吴海虹,何鸣元,韩布兴,
(1.华东师范大学 化学与分子工程学院 上海市绿色化学和化工过程绿色化重点实验室,上海 200062;2.崇明生态研究院,上海 202162;3.中国科学院 化学研究所 胶体、界面与化学热力学重点实验室,北京 100190)
0 引 言
二氧化碳(CO2)是温室气体的主要成分,同时也是一种重要的C1资源,利用可再生的电能将CO2转化为高附加值的化学品具有环境保护和碳资源合理利用的双重意义[1-3].CO2作为碳的最高氧化物,化学性质稳定且极难活化,因此在电化学转化过程中通常需要较高的过电位以驱动电子转移过程[4-5].此外,CO2的还原路径极为复杂,且相较于低碳中间体的加氢速率而言,C–C键的形成速率较慢,因而C2+产物的选择性和活性通常较低[6].在各类金属中,铜是已知的能高效电还原CO2为C2+产物的最有前景的催化剂之一[7-8].为了提高铜基催化剂的催化性能,近年来,通过水热法[9]、湿化学法[10]和热退火[11]等方式制备开发了单晶铜[12]、铜合金[13]、氧化物衍生铜[14]以及单原子铜[15]等电催化剂.然而,目前大多数铜基催化剂的制备过程较为复杂,能耗大且耗时长.开发制备工艺简单且性能优异的铜基催化剂,对推动电催化CO2还原技术具有重大意义.
相较于其他制备方法,电沉积法无须经过高温煅烧过程,耗时短且无须添加导电性较差的粘结剂(nafion)即可将所制备的纳米材料固定于支撑电极(如碳纸)上,能够降低金属催化剂与基底之间的接触电阻且有利于提高电极的稳定性[16-17].此外,电沉积法制备的金属颗粒微观表面通常呈现多维结构,有利于催化活性中心的充分暴露[18].
为调整催化剂的形貌和结构,在电沉积过程中往往采用添加剂辅助控制金属沉积过程.例如,Hoang 等[19]以3,5-二氨基-1,2,4-三氮唑(3,5-diamino-1,2,4-triazole,DAT)为添加剂制备了不同形貌的铜基催化剂,其中线状结构的Cu催化剂电还原CO2制备C2+的法拉第效率(faradaic efficiency,FE)可达到40%.以乙二胺四乙酸二钠(ethylenediaminetetraacetic acid disodium salt,EDTA-2Na)作为添加剂时,不仅能够调整金属催化剂的形貌,还可以吸附于Cu的表面调节催化剂的电子分布,显著提高C2+产物的选择性[20].总之,添加剂对电沉积过程的影响十分巨大,决定着催化剂性能的优劣.但目前被开发和利用的添加剂种类相对较少,限制了电沉积制备金属催化剂在CO2电还原中的应用.
在电沉积过程中,添加剂通过络合金属离子调控催化剂形貌[20-21].氮三乙酸(nitrilotriacetic acid,NTA)同时含有氨基和羧基,具有较强的络合能力.因此,本文采用NTA作为添加剂,通过电沉积法制备了含有丰富金属空位且具有三维结构的铜基催化剂.并通过X射线衍射仪(X-ray diffraction,XRD)、透射电子显微镜(transmission electron microscope,TEM)以及同步辐射等表征分析了NTA对铜基催化剂形貌结构和配位环境的影响,同时,研究了该方法制备的铜基催化剂电还原CO2制备C2+产物的性能.
1 实验部分
1.1 试剂与原料
本研究所用的无水氯化铜、氯化锌、硝酸钾、氯化钾均购买自国药集团化学试剂有限公司,硝酸钯、氮三乙酸购买自阿尔发埃萨尔(中国)有限公司,碘化铯购买于北京伊诺凯科技有限公司,型号为TGP-H-60的碳纸购买于阿尔发埃萨尔(中国)有限公司.
1.2 电极制备
1.2.1 原位合成Cu-X/CP电极
电极的制备采用恒电流沉积法,将疏水碳纸裁剪成1 cm ×1 cm的正方形,并依次在蒸馏水和丙酮中超声清洗,经过烘干后备用.Cu-0.5/CP电极的详细制备过程如下:0.1 mol·L−1CuCl2和0.5 mmol·L−1NTA充分超声混合后作为电沉积液,Pt网作为对电极,Ag/AgCl电极(饱和氯化钾)作为参比电极,夹有疏水碳纸的电极为工作电极(图1).在CHI 6081E电化学工作站的控制电流模式下沉积,沉积后的碳纸用去离子水反复冲洗,干燥后直接作为电极使用.此外,改变沉积时间,制备出Cu-0.5/CP-200和Cu-0.5/CP-600电极;改变沉积电流,制备出Cu-0.5/CP-8和Cu-0.5/CP-15电极.
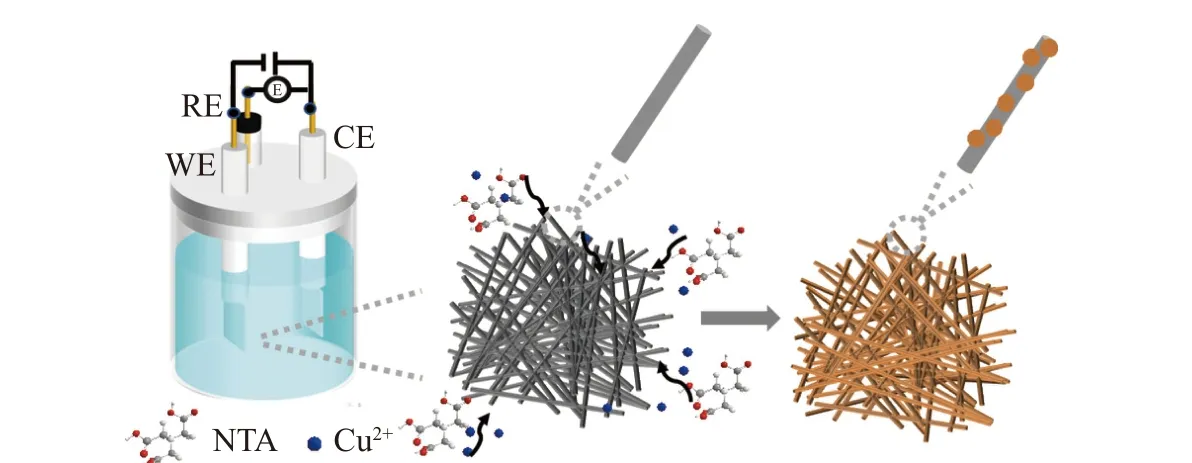
图1 Cu-X/CP材料的制备流程Fig.1 Synthesis pathway for a Cu-X/CP catalyst
1.2.2 原位合成M-X/CP电极
Zn电极的制备与Cu电极相似,Zn镀液中NTA的浓度为0.5 mmol·L−1,制备出的Zn电极命名为Zn-0.5/CP.制备Pd镀液时,加入适量酸促进钯盐溶解,并调整NTA的浓度为1 mmol·L−1,所制备的Pd电极命名为Pd-1/CP电极.
1.3 材料表征
利用X射线衍射仪(XRD,Ultima VI,Cu靶Kα射线)对沉积制备的催化电极进行晶体结构表征.利用AXIS SUPRATM型X射线光电子能谱(X-ray photoelectron spectroscopy,XPS,Al Kα射线为辐射源)分析反应前后催化剂的组成和价态,获取的数据根据碳在284.6 eV处的C 1s峰进行荷电校正.使用扫描电子显微镜(scanning electron microscope,SEM,Hitachi S-4800,加速电压10 kV)和透射电子显微镜(TEM,JEM-2100F,加速电压200 kV)观测M-X/CP电极的形貌和结构.在北京同步辐射装置1W1B、1W2B束上进行X射线吸收精细结构(X-ray absorption fine structure,XAFS)实验,所收集的光谱使用Ifeffit包中的Athena和Artemis程序进行分析.
1.4 实验过程
CO2电解实验在含有三电极系统的H型电池中进行,Nafion N-117质子交换膜用于分离阴极室和阳极室.在电化学工作站(CHI 6081E,上海辰华)上选用恒电位模式进行CO2电解还原,阳极电解液为0.1 mol·L−1K2SO4,阴极电解液为0.1 mol·L−1CsI.CO2的流速由质量流量控制器(SevenStar D07-19B,北京七星华创)控制并以15 sccm的流速持续通入电解液中.电解实验前,向阴极电解液通入N2或CO2至少30 min,形成N2或CO2饱和电解质溶液.本文所有施加电位均按照如下公式转换为可逆氢电极:

式中:ERHE为可逆氢电极的电极电势,EAg/AgCl为相对Ag/AgCl参比电极的电极电势.
2 结果与结论
2.1 Cu-X/CP电极的形貌结构表征
图2为Cu-X/CP的扫描电镜和透射电镜图.NTA辅助制备的Cu-0.5/CP表面呈现多面体的形貌特征(图2(a)—(b)),而Cu-0/CP则表现出颗粒堆积的球状形貌(图2(c)).NTA是一种络合能力极强的氨羧络合剂,能与溶液中的金属Cu2+离子络合,控制其还原过程中的成核动力学,并最终影响铜基催化剂的形貌结构[22].由Cu-0.5/CP的HR-TEM图可观察到0.21 nm和0.249 nm的晶格间距(图2(f)),分别对应于Cu的(111)面和Cu2O的(111)面[23].此外,在HR-TEM图中还观察到大量的晶格空位(图2(e)),表明Cu-0.5/CP内存在金属空位型缺陷[24].这些金属空位可以作为CO2吸附和加氢的活性位点,对CO2电还原反应极为有利.

图2 Cu-X/CP的SEM(a—c)、TEM(d)、HR-TEM(e)图及从红线标记处(Ⅰ和Ⅱ)测量的强度分布Fig.2 SEM(a—c),TEM(d),and HR-TEM(e)images of Cu-X/CP and intensity distribution measured based on the areas outlined in red
2.2 元素价态分析
图3是Cu-X/CP的X射线衍射图谱.由图可知,Cu-0/CP与Cu-0.5/CP的衍射图谱无明显差异,两者表现出相似的多晶结构,这说明NTA的加入对Cu的晶体取向无明显改变.其中,位于26.10°和54.21°处的强衍射峰归属于碳纸基底,在43.10°、50.10°和74.01°处的衍射峰分别归属于单质Cu的(111)、(100)、(110)晶面,位于36.40°处的弱衍射峰则归属于氧化亚铜(Cu2O)的(111)晶面[24].

图3 Cu-X/CP的XRD图谱Fig.3 XRD pattern of Cu-X/CP
通过XPS技术,对Cu-X/CP的元素种类和元素价态展开分析.如图4所示,Cu-0/CP和Cu-0.5/CP在932.6 eV和952.0 eV处均出现与Cu0或者Cu+物种相关的结合能峰,这表明Cu-X/CP中Cu以低价态为主.Cu-0.5/CP的Cu俄歇能谱(Cu LMM(linear mixed model))进一步验证了这一结果[25].同时,Cu-0/CP在942.0 eV和952.6 eV处出现明显的卫星峰,表明Cu-0/CP中部分Cu2O被氧化.

图4 Cu-X/CP的XPS图谱Fig.4 XPSspectra of Cu-X/CP
进一步利用同步辐射技术对Cu-X/CP中Cu的化学状态和电子结构进行分析.如图5所示,Cu的k边XANES光谱中Cu-X/CP展现出Cu0和Cu+的特征,这与XPS的结果一致[24].同时,Cu-X/CP在2.24 Å(1Å=1×10–10m)处均出现Cu-Cu配位峰,且Cu-0.5/CP中Cu-Cu配位峰强度明显低于Cu-0/CP和铜箔,这说明Cu-0.5/CP中Cu的配位数更小,其含有更多的缺陷位点[24].从图5(c)的波变换数据可知,Cu-0/CP和Cu-0.5/CP的能量强度最大值出现在更宽的6~10Å–1范围内,同样表明Cu-0.5/CP中存在一定的Cu-O结构.除此之外,相较于Cu-0/CP而言,Cu-0.5/CP的最强能量密度偏移至更小的k值区域内,进一步证明Cu-0.5/CP中存在缺陷结构[26].因此,添加NTA制备的Cu-0.5/CP中含有丰富的Cu0/Cu+和大量的金属空位,这会使得催化剂具有更高的表面能和丰富的活性位点.
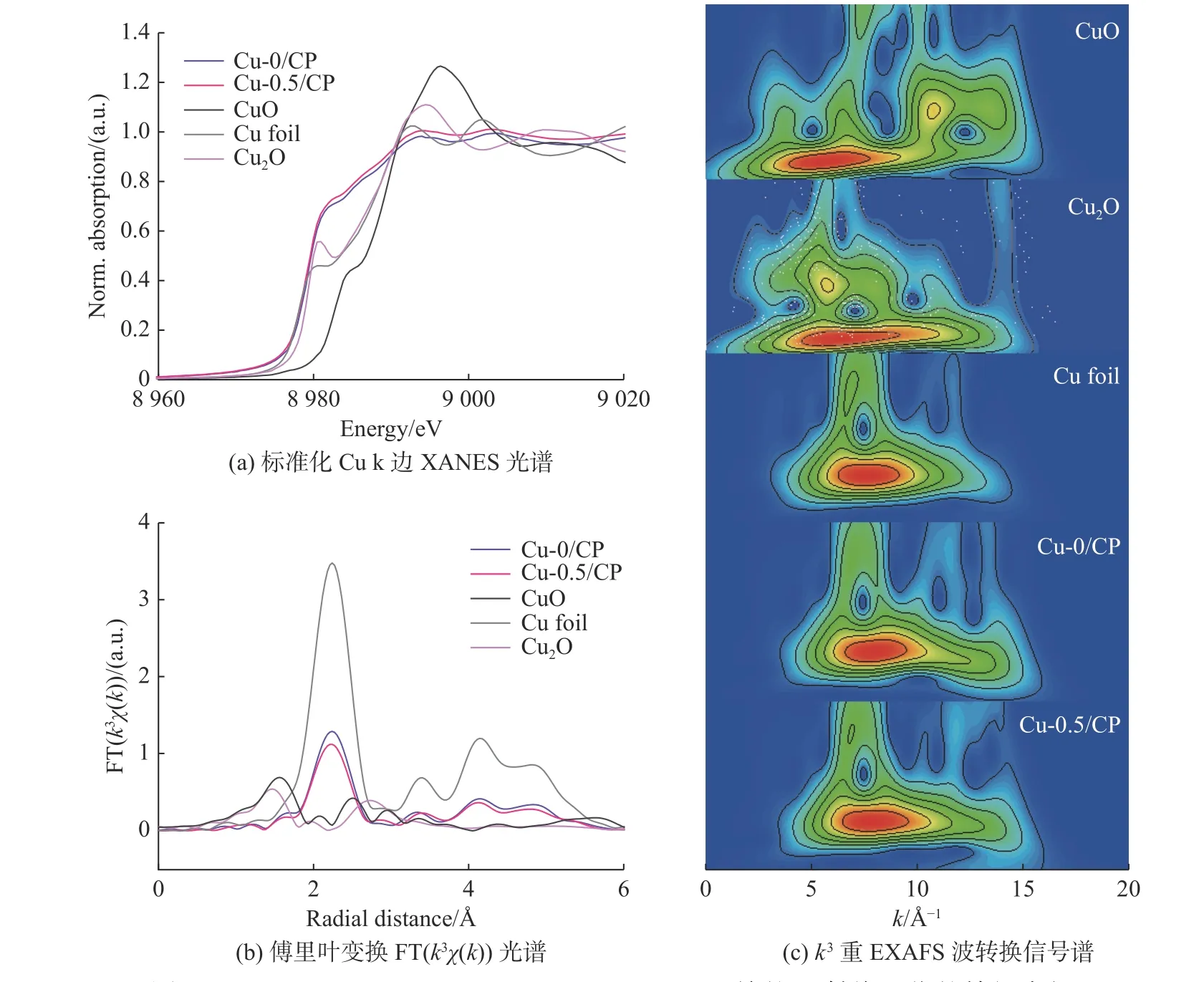
图5 Cu-0.5/CP、Cu-0/CP、CuO、Cu2O和Cu箔的X射线吸收的精细表征Fig.5 X-ray absorption characterization of Cu-0.5/CP,Cu-0/CP,CuO,Cu2O,and Cu foils
2.3 电催化性能研究
2.3.1 NTA对催化性能的影响
首先利用线性扫描伏安法(linear sweep voltammetry,LSV)分别在N2或CO2饱和的CsI电解液中对Cu-X/CP电极进行测试.如图6(a)所示,Cu-0.5/CP相较于Cu-0/CP电极而言具有更高的电流密度,表明Cu-0.5/CP电极更有利于CO2的活化.同时,Cu-0.5/CP电极在CO2氛围下的电流密度更高,这说明电极上优先发生CO2还原反应[27-28].
采用控制电位法对催化性能进行进一步分析,电解结束后收集气相和液相产物,并分别用气相色谱(gas chromatography,GC)和核磁共振(nuclear magnetic resonance,NMR)检测.产物主要包含C2H4、CH3CH2OH、C3H7OH等C2+产物以及CH4、CO、HCOOH等C1产物.如图6(c)所示,在电位为–1.26 Vvs.RHE(reversible hydrogen electrode)时,Cu-0.5/CP电极上C2H4的法拉第效率可达到44.0%,C2+产物的总法拉第效率达到61.6%.将Cu-0.5/CP和Cu-0/CP在不同电位下的产物按照H2、C2+、C1分类,并将分布情况汇总于图7中,可以看出不同电位下Cu-0.5/CP对于C2+产物的选择性均明显高于Cu-0/CP电极.与文献中报道的其他Cu基催化剂相比,本文通过简单的电沉积法制备的Cu-0.5/CP电极在H型电解池中展现出良好的C2+产物选择性和电流密度[29-30].

图6 Cu-0/CP和Cu-0.5/CP在不同电解电位下的催化性能对比Fig.6 Comparison of the catalytic performance of Cu-0/CP and Cu-0.5/CP at different electrolysis potentials

图7 Cu-0.5/CP和Cu-0/CP上C2+、C1及H2的法拉第效率对比Fig.7 Comparison of the FE of C2+,C1,and H2 for the Cu-0.5/CP and Cu-0/CP electrodes
2.3.2 电沉积时间和电流的影响
进一步对不同沉积时间和沉积电流下制备的Cu基催化剂进行电解实验,结果如图8所示.当沉积电流增大时,C2H4的选择性下降,而HCOOH的法拉第效率略有提升.图8(b)对比了沉积时间对产物选择性的影响,当沉积时间减少至200 s时,产物中出现少量的CH4,而增加沉积时间至600 s时,HCOOH和CH3COOH的法拉第效率略有上升.即当沉积时间为400 s、沉积电流为5 mA时,催化材料具有最佳的CO2电还原制备C2+产物性能.

图8 沉积条件对催化性能的影响Fig.8 Effects of deposition current and time on catalytic performance
2.3.3 电极的稳定性
为评价Cu-0.5/CP电极的稳定性,在–1.26 Vvs.RHE电位下进行4 h的恒电位电解实验.如图9(a)所示,Cu-0.5/CP电极的总电流密度未出现衰减现象,说明其具有良好的使用寿命.由图9(b)的XRD图谱可知,反应前后Cu-0.5/CP的晶体结构未发生明显改变,Cu(111)和Cu (200)晶面仍然存在.XPS和Cu的俄歇电子能谱显示,反应后Cu-0.5/CP中Cu仍然以低价态为主,Cu0和Cu+的含量分别为65.1%和34.9%.与反应前的XPS结果对比,Cu-0.5/CP在反应后Cu0含量略有升高,这表明在催化反应中部分Cu+被还原.总之,这种原位制备的自支撑Cu-0.5/CP电极能有效避免剥离脱落问题而大大提高电极的稳定性.

图9 Cu-0.5/CP电极的稳定性Fig.9 Stability of the Cu-0.5/CP electrode
2.4 机理研究
为探究Cu-0.5/CP优异性能的原因,首先对两种电极的电化学表面积展开研究.如图10(a)所示,与Cu-0/CP(1.7 mF·cm–2)相比,Cu-0.5/CP(2.7 mF·cm–2)具有更大的双层电容值(double-layer capacitance,Cdl),即Cu-0.5/CP具有更大的电化学表面积,这表明缺陷更多的Cu-0.5/CP电极在CO2还原反应中能够提供更多的催化活性位点,能够促进CO2还原反应的进行[31-32].为研究两电极上的电子转移能力,进行电化学阻抗测试并通过Zview软件对数据进行拟合.图10(b)的拟合结果显示,Cu-0.5/CP的电荷转移阻抗(charge transfer resistance,Rct)和接界阻抗(film resistance,Rf)均比Cu-0/CP小.Cu-0.5/CP较低的电阻值对电化学反应中电荷转移极为有利,这可能是其显示高催化活性的重要原因之一[10].

图10 Cu-0/CP和Cu-0.5/CP电极的电化学表征结果Fig.10 Characterization results of the Cu-0/CP and Cu-0.5/CP electrodes
2.5 普适性研究
为验证该策略的普适性,以NTA为添加剂,通过电沉积法制备了Pd和Zn基金属催化剂.对所制备的Pd-0/CP和Pd-1/CP、Zn-0/CP和Zn-0.5/CP共4种电极进行SEM表征,发现加入NTA后金属Pd和Zn的形貌产生较大变化.如图11所示,Pd-0/CP主要是片状结构,而Pd-1/CP呈现出海绵状的结构;Zn-0/CP电极表现出片状堆叠的不规则形貌,而Zn-0.5/CP电极呈现出堆叠的簇状形貌.在–1.26 Vvs.RHE下测试了4种电极的CO2电还原性能,结果如图12所示.Pd-0/CP和Zn-0/CP电极CO的法拉第效率分别为15.7%和76.6%,而Pd-1/CP和Zn-0.5/CP电极CO的选择性均有明显提高,CO的法拉第效率分别可达到70.0%和81.5%,其中Pd电极上CO选择性提升最明显.这些结果表明,NTA是一种调节金属催化剂性能的有效添加剂.

图11 Pd-0/CP、Pd-1/CP、Zn-0/CP和Zn-0.5/CP的SEM图Fig.11 SEM images of Pd-0/CP,Pd-1/CP,Zn-0/CP,and Zn-0.5/CP
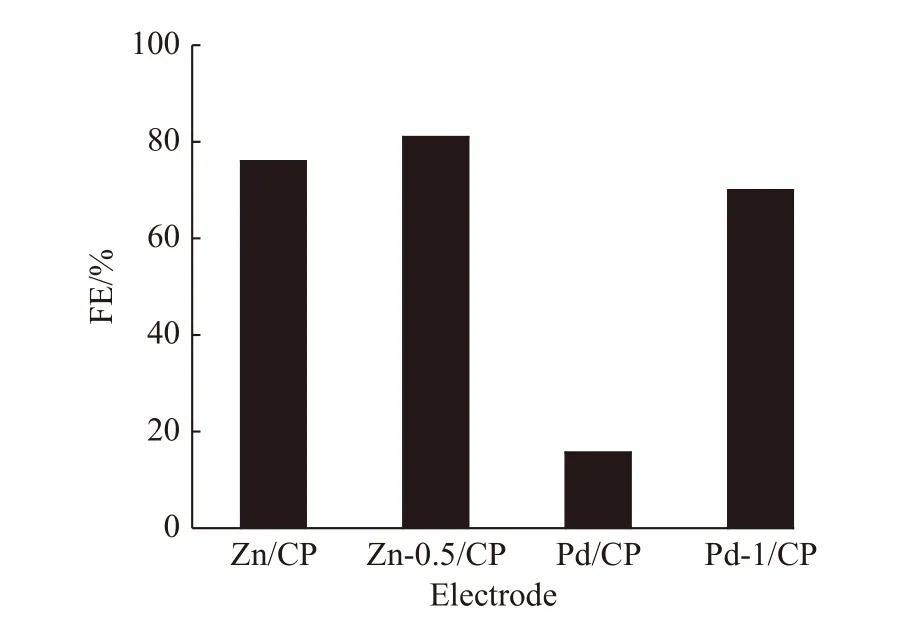
图12 Pd-0/CP、Pd-1/CP、Zn-0/CP和Zn-0.5/CP电极上CO的法拉第效率Fig.12 FE of CO for Pd-0/CP,Pd-1/CP,Zn-0/CP,and Zn-0.5/CP electrodes
3 结 论
本文以氮三乙酸(NTA)作为添加剂,通过电沉积法制备了具有三维结构的铜基催化剂.利用TEM、XAFS等技术证实了NTA的添加能够增加铜基催化剂的金属空位,有利于提高铜基催化剂电还原CO2制备C2+产物的性能.所合成的Cu-0.5/CP电极在–1.26 Vvs.RHE时,C2H4和C2+产物的法拉第效率分别能达到44.0%和61.6%,此时总电流密度为12.3 mA·cm–2.Pd和Zn基金属催化剂的制备和电催化实验证明该策略具有一定的普适性.

