多巴胺表面修饰在医疗领域的研究进展
刘雨晗,刘德,王意,王虎鸣,曹攀
多巴胺表面修饰在医疗领域的研究进展
刘雨晗,刘德,王意,王虎鸣,曹攀
(扬州大学 机械工程学院 表面工程研究所,江苏 扬州 225127)
多巴胺(DA)及其聚合物聚多巴胺(PDA)含有邻苯二酚基团、氨基等大量活性官能团,使其具有良好的黏附性、生物相容性、反应活性和还原性,被广泛用于医疗器械材料、船舶材料、传感器件材料、药物运输等材料表面的改性,其中对医疗器械材料表面的修饰研究前景尤为广阔。分析了多巴胺的理化特性及相关功能,归纳了多巴胺在生物工程材料上的应用,包括增强材料的骨组织再生能力和提高材料表面细胞的黏附、增殖等。在此基础上,重点综述了近年来多巴胺在医疗领域的改性研究进展,其中多巴胺对骨修复及骨移植材料的修饰包括复合材料和高分子材料等,多巴胺对牙种植体及牙修复材料的修饰包括纳米金属材料和合金材料等,多巴胺对新型医疗材料的修饰包括人工血管、人工韧带材料和医用膜材料等。阐述了改性材料的优缺点和作用,以及多巴胺如何对材料表面进行改性来弥补材料的缺陷。针对不同材料的多巴胺改性,分别从制备方法、实验对比结果等方面进行归纳。最后展望了多巴胺表面修饰技术的发展方向。
多巴胺;聚多巴胺;表面修饰;医疗器械;人体植入材料
全球医疗器械市场迅猛发展,随着我国人口平均寿命增加,老龄化日益严重,促进了对医疗器械尤其是心脑血管、骨科和美容等植入物的需求,但是医疗器械和人体植入物的表面会与人的体液、血液和组织等发生接触,它们的表面易于被细菌黏附,从而形成生物膜,危害人类健康。多巴胺含有大量的邻苯二酚基团、氨基等活性官能团,使其具有极佳的黏附性和化学反应活性,可以借助共价键或非共价键作用将骨修复材料和生长因子结合,两者的结合力会显著提升,从而使骨组织的再生能力增强[1]。多巴胺可作为连接工程支架与细胞的桥梁,有效促进支架材料表面细胞的黏附与增殖,提高骨修复材料表面细胞黏附[2];DA氧化聚合可形成PDA,利用PDA改性基底,可显著改善细胞的贴附能力[3],而且有利于固定成骨因子,使得细胞的增殖、分化以及成骨基因表达功能得到改善[4-5]。DA以及其聚合物PDA在医疗器械表面改性领域具有广阔前景,因此,本文对多巴胺表面修饰在医疗领域的研究进展进行综述。
1 多巴胺在改性骨修复及骨移植材料中的研究进展
1.1 多巴胺改性骨科修复材料
聚多巴胺富含—OH、—NH2等基团,拥有极佳的亲水性、生物活性和稳定性[6]。杨晓玲等[7]以碳/碳(C/C)复合材料为基底材料,将PDA涂层沉积在材料表面,然后与不同浓度的精氨酸-甘氨酸-天冬氨酸(RGD)共价偶联。结果(图1)显示,RGD-PDA涂层成功改善了基底材料的亲水性和生物活性。聚乳酸(PLA)是医用高分子材料,生物可降解性、力学性能、生物相容性等性能良好,被广泛用于骨组织修复材料。但其亲水性和细胞相容性较差,且存在缺乏成骨、成血管化功能等缺陷。对材料表面进行生物学修饰可有效改善PLA材料的功能。多巴胺是贻贝黏附蛋白的关键成分,它几乎可以黏附在任何材料的表面,能够有效改善材料表面的亲水性和细胞相容性。此外,多巴胺自聚形成的聚多巴胺层可以作为二级反应平台,在基体材料表面进一步修饰生物活性分子,赋予基体材料优异的生物学性能。李慧华[8]用聚(D、L-乳酸)(PDLLA)材料制备膜,并用PDA对其表面进行改性,得到一系列不同浓度的PDLLAP/PDA-x复合膜。研究发现:经PDA改性后,PDLLA膜的亲水性得到显著改善,其表面粗糙度和表面能明显增大。

图1 接种于C/C复合材料上MC3T3-E1细胞的增殖情况(空白组:原始C/C复合材料;PDA涂层组:表面有PDA涂层的C/C复合材料;35RGD-PDA涂层组:表面有RGD-PDA涂层的C/C复合材料,其中RGD质量浓度为35 μg/mL;50RGD-PDA涂层组:表面有RGD-PDA涂层的C/C复合材料,其中RGD质量浓度为50 μg/mL)(*p<0.05表明存在显著差异)[7]
聚己内酯(PCL)生物相容性、可加工性、生物可降解性、机械性能、物理性能等良好,被广泛用于骨组织修复工程。但PCL存在亲水性差、生物活性不理想等缺陷,国内外学者常借助DA改性提升PCL的性能。闫欢欢[1]以苯胺四聚体、多巴胺和聚乙二醇为原料,通过自由基加成反应合成了具有黏附性的导电无规共聚物poly(PAT)。测试表明:此材料不仅保持一定的导电性和电活性,还具有良好的亲水性和生物相容性。栗可心等[9]复合了羟基磷灰石(HA)和聚己内酯(PCL),制备出PCL-HA骨组织工程多孔支架,该支架材料具有良好的生物相容性和生物活性,但难以实现生物活性因子在材料底物上的固定化附着。徐燕等[10]利用DA的黏附性,将软骨源性形态发生蛋白1(CDMP-1)引入至 PCL-HA三维多孔支架材料表面,并将其与成人骨髓间充质干细胞(hBMSCs)体外培养。实验表明:经多巴胺改性修饰后,支架材料的亲水性能得到改善,且对细胞的黏附、增殖及成软骨分化有显著促进作用。Xu等[11]通过3D打印制备了聚多巴胺涂层的聚-(乳酸-共-乙醇酸)/β-磷酸三钙复合支架,并进行了一系列表征和生物相容性测试。结果表明,PDA涂层含量越高的支架对新骨形成的效果越好。Chen等[12]使用PDA涂层的仿生工艺处理3D聚乳酸-羟基乙酸共聚物(PLGA)多孔支架,加强了人骨形态发生蛋白-2(BMP-2)和ponericin G1在3D PLGA多孔支架上的固定。BMP-2/ponericin G1固定后,MC3T3-E1细胞在3D PLGA 支架上的附着、增殖与成骨分化显著提高。
1.2 多巴胺改性骨科移植材料
生物陶瓷材料可通过PDA改性来改善表面活性,从而促进成骨细胞在陶瓷表面的黏附、增殖和分化,以达成骨整合[13]。PDA具有一定程度的弱还原性,能够实现各种材料表面的无电金属化。Tan等[14]以钛为基底材料,将PDA进行表面改性后的钛片浸泡在硝酸银溶液中,成功制备出表面载银的钛片。结果表明,经PDA改性后的钛片抗菌性、细胞相容性良好。
纳米银被视为一种良好的抗菌试剂。王勇[15]利用PDA涂层将吸附的[Ag(NH3)2]+原位还原为Ag纳米粒子,成功在聚醚醚酮(PEEK)材料表面制备出Ag纳米粒子涂层。实验结果显示,PEEK-PDA-Ag材料的抗菌性能良好。张维波[16]在微纳米多孔及光滑的钛表面成功制备了聚多巴胺-纳米银修饰涂层,得出结论:构建的修饰涂层解决了多孔表面易发生感染的问题,DA介导的矿化有效改善了表面成骨细胞相容性。
镁合金具有极佳的生物相容性和独特的机械性能,而且它能减小甚至消除“应力遮挡”,被用作生物医学领域可降解骨科植入材料。但是临床应用中发现:医用镁合金在生理体液环境中释放氢气以及降解速度具有不可控性。王邓莉[17]利用PDA涂层修饰医用镁合金(AZ31)表面,然后将经PDA改性的AZ31浸入仿生矿化液中以形成HA涂层,并对镁和镁合金的改性方法进行了初步研究。研究表明,经PDA改性的HA涂层能够成功降低医用镁合金在人体的降解速率。
钛合金的物理性能优异、机械性能良好、耐腐蚀性较强、生物相容性极佳,常用作骨移植材料。但是医用钛合金表面疏水,耐腐蚀性能还需加强,且它与人骨间并未完成化学骨性结合。张松营[18]采用PDA改性医用钛合金(SA)材料表面。实验表明,PDA涂层完全均匀的覆盖在SA基底表面,材料基底形貌和粗糙度未改变,表面亲水性、细胞相容性良好,能促进成骨细胞的早期黏附、增殖。尤莹[19]以金属纯钛材料为基体材料,经热碱处理后材料形成微观多孔网状结构。利用PDA在此结构上黏附羟基磷灰石形成复合涂层。研究表明,碱热处理后的多孔钛表面形成的PDA生物活性复合涂层能够显著促进骨髓间充质干细胞(BMSCs)的黏附和早期增殖,见图2。

图2 BMSCs在材料表面培养24 h后SEM观察固定在各种材料表面的细胞[19]
2 多巴胺在改性牙种植体及牙修复材料中的研究进展
2.1 多巴胺改性牙植入材料
牙种植体植入后首先与人体血液相接触。在骨整合中,种植体与血液间血凝块的形成起重要作用。采用共价键结合的方法可以将生物分子连接到材料表面。多巴胺仅通过简单浸泡的方式即可在几乎任何无机和有机材料表面形成聚多巴胺涂层,且形成的聚多巴胺涂层还可通过邻苯二酚结构与含有氨基、巯基等基团的化合物发生一系列反应,形成牢固稳定的化学键[20-21]。张冉冉等[22]利用PDA的特性将具有促血小板聚集作用的二磷酸腺苷(Adenosine Di-phosphate,ADP)接枝到材料表面(细胞爬片)。实验表明,通过PDA偶联作用将二磷酸腺苷接枝到材料表面后仍能保持其生物活性,材料表面经改性后能够促进血小板的黏附、聚集与激活,见图3。
金属钛中,六铝四矾钛的生物相容性和抗腐蚀性良好,力学性能如拉伸强度和弹性模量等较低,且相关机械参数非常接近骨皮质,常被用作口腔种植体。钛作为生物惰性材料,存在骨结合时间较长、骨结合强度不足等缺陷。周田园等[23]利用DA偶联在纯钛(Ti)表面构建Ti陶瓷生物膜-多巴胺-Arg-Gly-Asp(RGD)环肽活性层。实验结果显示,纯钛-微弧氧化-多巴胺-环肽活性涂层能促进成骨细胞的早期黏附和增殖,并能有效促进成骨细胞扩散。Guo等[24]为使钛材料表面获得良好的抗菌性能,利用DA涂层螯合Ag+并将它们还原成Ag的特性,在多孔钛表面成功制备了聚电解质(poly-L-lysine/sodium alginate/poly- L-lysine,PSP)、多巴胺和银纳米颗粒(AgNPs)的复合涂层。结果表明:pTi/PSP/DA/Ag可以防止细菌黏附和定植,且该涂层在模拟体液(SBF)中培养时可诱导表面矿化,表现出了良好的细胞相容性。Choi等[25]研究了经PDA涂层和Ag改性Ti材料对变形链球菌和牙龈卟啉菌的抗菌特性,结果表明,与未经表面处理的Ti相比,经PDA涂层和Ag改性的Ti抗菌性能明显更好。Marinas等[26]优化了Ti-6Al-6V合金表面的聚多巴胺薄膜涂层,使用氧化剂KMnO4来减少PDA的沉积时间,并扩大了DA实现其氧化优势的pH范围。

图3 细胞体外增殖评价hBMSCs在材料表面增殖检测(P>0.05)[22]
2.2 多巴胺改性人体牙质
牙体硬组织缺乏完善的自我修复功能,国内外学者就促进牙本质再生的方法展开了研究。邱滢等[27]研究发现载BMP-2多巴胺-肝素-透明质酸支架能够促进牙髓干细胞在牙本质表面的黏附、增殖、分化、迁移并形成牙本质。Liu等[28]将DA修饰的透明质酸(DA-HA)涂层处理牙本质表面,成功将牙髓干细胞(DPSC)稳定黏附在牙本质上,且制备的涂层进一步促进了DPSCs的增殖,有效提高牙本质的再生能力。
牙本质的再矿化和黏结修复一直是临床医学关注的重点问题,材料领域学者也对此展开了研究。Zhou等[29]研究了PDA涂层对牙本质再矿化的影响,使用亚稳定的钙磷溶液来实现牙本质的再矿化。实验对比发现,经PDA涂层的牙本质再矿化功能得到极大改善。在Zhou等的研究基础上,De Lima等[30]采用PDA和具有胶原蛋白及钙结合结构域的合成多巴肽等材料进行原位制备。用制备出的聚(儿茶酚)仿生药物处理牙本质样品,在体外测试样品矿化能力。结果表明:牙本质经药物处理后,表面特性改变、矿物质形成能力增加。曾玲等[31]研究了DA溶液对牙本质黏结力的影响,得出结论:使用适宜浓度的DA溶液对牙本质进行处理,可以增强牙本质黏结强度,DA溶液的质量浓度为2 mg/mL时效果最佳。
3 多巴胺改性在其他医疗材料中的研究进展
3.1 多巴胺改性人工血管、人工韧带材料
临床常用的小口径(直径<6 mm)人工血管生物相容性较差,移植后效果不佳,易形成血栓。鉴于对DA改善材料生物相容性的研究,Luo等[32]发现在聚合物材料表面,DA会发生自氧化和自聚合。自聚合后,肝素接枝到多巴胺氨基位置后,材料表面血液相容性优良。Davoudi等[33]利用DA的自聚合特性,将肝素和血管内皮生长因子(VEGF)固定在聚氨酯(PU)纳米纤维血管支架上,抗血栓性能良好,同时促进了内皮的单层生长和融合。研究发现,模仿贻贝黏附蛋白的PDA技术可以在聚四氟乙烯(PTFE)材料表面自聚合形成膜[34-35],可在引入活性基团邻苯二酚的同时提高材料表面的亲水性,从而实现带有氨基或巯基功能物质的单层改性,这项技术可以固定能够选择性黏附在聚四氟乙烯血管表面上的内皮细胞的活性肽,并构建出特定结构来促进内皮细胞的选择性生长,成功使人工血管的内皮化快速有效地进行[36]。汪涛等[37]利用DA修饰聚四氟乙烯人工血管,并用MTT比色法检测血管对内皮细胞的毒性。检测发现,聚四氟乙烯人工血管经处理后对内皮细胞的生长无毒性作用,且细胞亲和性、细胞相容性良好,见图4。贾山山[38]利用DA自聚合的特点,使其在膨体聚四氟乙烯上形成自聚成膜,并与聚乙烯亚胺共混以增加氨基的数量。人工血管经多巴胺/聚乙烯亚胺覆盖处理后,成功将肝素固定在表面,人工血管表面的血液相容性得到显著提升。Mi等[39]为了同时提高PTFE材料对内皮细胞的亲和力和抗血栓形成能力,使用包括DA、RGD和肝素在内的生物活性分子对PTFE进行功能化。实验表明,PTFE材料经修饰后生物相容性和细胞亲和力显著改善。

图4 与经多巴胺预处理后聚四氟乙烯人工血管共培养后内皮细胞的形态学变化(40×)[37]
人工韧带移植物材料Polyethylene terephthalate(PET)的疏水性很强,因而造成细胞在其上的黏附和生长困难,导致与骨骼之间的黏附力弱,植入后难以和人体骨形成骨整合,易导致重建失败[40]。俞斌等[41]在基于PET材料骨隧道部分预涂DA改性上,引入了纳米Fe3O4材料。研究发现,PET人工韧带材料经DA修饰过的四氧化三铁涂层处理后,小鼠胚胎成骨细胞前体细胞(MC3T3-E1)的黏附、增殖和分化显著增强,见图5。Yu等[42]用PDA修饰Mesoporous Bioactive glass(MBG),人工韧带经PDA-MBG涂层处理后生物相容性和生物活性显著提升,动物试验表明,改良的PET移植物可以加速与骨的愈合。Wu等[43]在弱氧化性弱碱性水溶液中,用PDA修饰PET人工韧带表面,然后以PDA为黏合层,在PET表面改性nano-hydroxyapatite(nHA),利用DA的还原性和nHA中所含的磷酸盐成功将银原子吸附在PET表面。抗菌试验结果表明,经修饰的PET表面具有显著的抗菌性能。生物活性试验结果表明,PDA能显著促进细胞增殖。
3.2 多巴胺修饰医用膜材料
聚砜(PSf)膜的机械强度高、热稳定性好、化学惰性强,可用作医用血液透析膜,在临床应用中具有广阔的前景,但聚砜膜与血液的相容性较差。研究表明,蛋白质或多肽固定在膜表面能够明显抑制蛋白质在界面处的吸附,因此将蛋白固定在膜表面可以用作开发高性能血液净化膜的有效方式。吉明波[44]利用DA在聚砜膜上分别黏附牛血清白蛋白(BSA)和具有抗凝血生物活性的纳豆激酶和蚓激酶分子。结果表明,PDA涂层和BSA分子固定化可以降低膜表面孔隙率,并使膜表面的孔径分布更窄。PSf/PDA-BSA膜的亲水性高于PSf膜。修饰后的膜减少了非特异性蛋白质的吸附和血小板黏附,抗污性能、生物相容性提高。DA涂覆时间短时,辅助BSA固定有利于改善膜渗透性能。Xie等[45]利用PDA层作为反应平台,将heparin(Hep)和BSA共价固定在聚砜膜表面,Hep和BSA同时固定后,所得膜具有良好的血液相容性且在细胞黏附、生长和增殖方面表现出优异的细胞相容性。
蚕丝蛋白因抗氧化、抗菌能力较强和生物相容性良好等特性,能够提升人体创伤组织的再生能力。目前,理想的创伤敷料通常需要具备透气性、保湿性、抗菌性以及优良的生物相容性和生物降解性,改善蚕丝蛋白材料的细胞相容性是优化其在组织工程中应用的关键。研究表明,DA的修饰可以吸附血清蛋白并使其结构保持活性,从而有效增强材料的细胞黏附性[46]。周官山[47]以蚕丝蛋白膜为基体材料,利用DA对其表面进行修饰,由此获得了具有高细胞黏附特性的皮肤创伤修复材料,有效加速创伤的愈合,并研究出经DA改性的蚕丝蛋白膜,包括丝素纳米纤维膜和柞蚕丝素膜。Hao等[48]利用PDA纳米颗粒的光热性能,将其作为光敏剂对丝素蛋白进行功能化,成功研制出具有光热肿瘤治疗和骨组织再生的双重功能的PDA@SF组织工程支架,见图6。
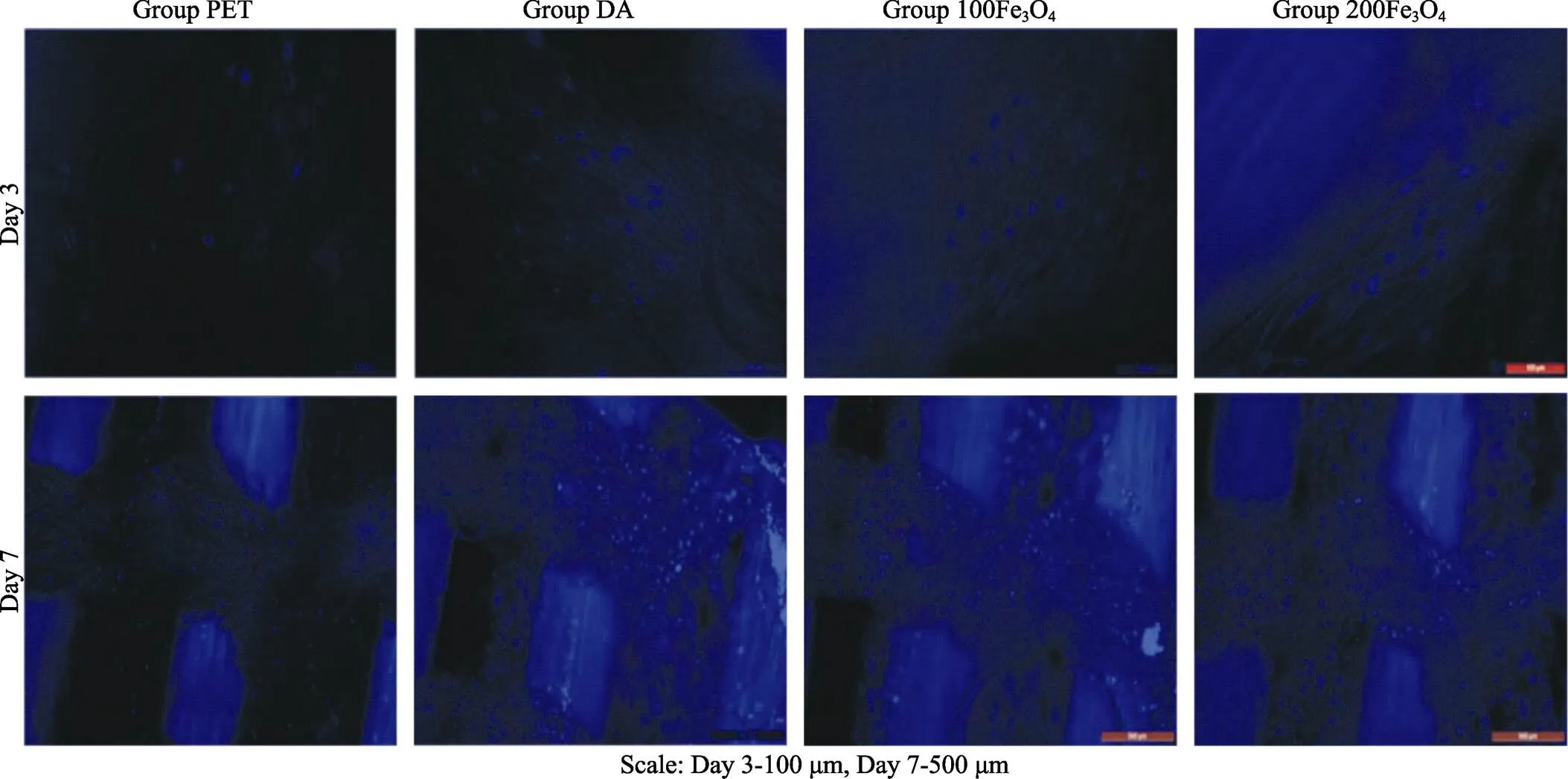
图5 PET人工韧带材料经不同方式处理后细胞接种培养第3 d和第7 d时PET组、DA组、100Fe3O4组和200Fe3O4组Hoechst 33258的染色结果[41]
有研究者利用PDA的光热效应来实现癌症额光热治疗。Jiang等[49]提出了红细胞(RBC)膜包被的PDA(PDA@RBC)作为体内癌症光热疗法(PTT)的治疗平台。PDA纳米颗粒上的RBC膜包被不仅保持了平台优异的光热性能,而且还改善了肿瘤的积累。此外,国内外学者利用PDA自身良好的生物相容性,促进细胞的黏附和增殖生长。Zhu等[50]以PDA为连接桥梁将牛血清蛋白(BSA)固定在多孔聚乙烯(PE)膜上,有效改善PE膜的亲水性,从而促进了细胞在膜表面的黏附与增殖,与PE/PDA-BSA复合膜表面相比,PE/PDPA复合膜表面更有利于细胞的黏附、增殖、分化和扩散。利用PDA层的二级反应平台,能够将目标分子接枝到膜上。An等[51]通过DA在聚偏二氟乙烯(PVDF)膜表面自聚合形成聚多巴胺层,将半胱氨酸共价接枝到该涂层上,改性后的PVDF膜被证实具有优异的亲水性、稳定的力学性能和良好的血液相容性(动态和静态抗蛋白吸附、溶血率、血浆凝固),并且这些特性随着聚多巴胺和半胱氨酸的加入而增加。
4 结论
将多巴胺加入Tris-HCl缓冲液中,再用溶液浸泡材料,即可使多巴胺在材料表面形成膜。多巴胺涂层可以增强材料表面抗菌性能、亲水性和细胞相容性等。此外,它可以通过共价键的结合方式将生物分子连接到材料表面。聚多巴胺涂层可通过邻苯二酚结构与含有氨基、巯基等基团的化合物发生一系列反应,形成牢固稳定的化学结合,通过聚多巴胺偶联法可以向材料表面接枝抗生素类药物。
多巴胺可以在有溶解氧的弱碱性条件下进行氧化自聚合反应,在材料表面形成生物相容性较强的聚多巴胺涂层,广泛应用于医疗器械表面改性研究中。本文从多巴胺改性骨修复及骨移植材料、牙种植体及牙修复材料、新型医疗材料3个方面阐述多巴胺表面改性在医疗领域的研究进展,指出了多巴胺改性医疗器械表面存在的黏附力、耐摩擦、抗菌广谱性和时效性不足的缺点。为了克服以上缺点,需要从多巴胺聚合、黏附机制出发,提高多巴胺修饰涂层的时效性,在不影响其生物相容性的基础上掺入抗菌防污有机物,提高其抗生物膜广谱性、黏附力等特性,为多巴胺在医疗领域的应用提供理论基础。
[1] 闫欢欢. 贻贝仿生导电性苯胺齐聚物生物材料的制备及在组织工程中的应用[D]. 合肥: 中国科学技术大学, 2020.
YAN Huan-huan. Preparation of Mussel-Inspired Conductive Oligoaniline Biomaterials for Tissue Engineering Applications[D]. Hefei: University of Science and Technology of China, 2020.
[2] 秦泽昭. 高强度可注射水凝胶的设计与制备[D]. 合肥: 中国科学技术大学, 2019.
QIN Ze-zhao. Design Andpreparationof Injectable Hydrogel with High Mechanical Strength[D]. Hefei: University of Science and Technology of China, 2019.
[3] 韩璐. 仿贻贝多功能水凝胶及其生物医学应用的研究[D]. 成都: 西南交通大学, 2017.
HAN Lu. Mussel-Inspired Hydrogel with Multi-Functions for Biomedical Applications[D]. Chengdu: Southwest Jiaotong University, 2017.
[4] WU Jiu-ping, LIU Yan-ting, CAO Qi-dong, et al. Growth Factors Enhanced Angiogenesis and Osteogenesis on Polydopamine Coated Titanium Surface for Bone Regeneration[J]. Materials & Design, 2020, 196: 109162.
[5] PACELLI S, CHAKRAVARTI A R, MODARESI S, et al. Investigation of Human Adipose-Derived Stem-Cell Behavior Using a Cell-Instructive Polydopamine-Coated Gelatin-Alginate Hydrogel[J]. Journal of Biomedical Materials Research Part A, 2021, 109(12): 2597-2610.
[6] YAN Ji, WU Ruo-yin, LIAO Si-si, et al. Applications of Polydopamine-Modified Scaffolds in the Peripheral Nerve Tissue Engineering[J]. Frontiers in Bioengineering and Biotechnology, 2020, 8: 590998.
[7] YANG Xiao-ling, LIU Xue, WU Qian-qian, et al. Dopamine-Assisted Immobilization of Peptide Arginine-Glycine-Aspartic Acid to Enhance the Cellular Performances of MC3T3-E1 Cells of Carbon-Carbon Composites[J]. Journal of Biomaterials Applications, 2019, 34(2): 284- 296.
[8] 李慧华. 基于聚多巴胺黏附层生物学修饰聚乳酸及其细胞相容性研究[D]. 广州: 暨南大学, 2016.
LI Hui-hua. Biological Modification of Polylactide Membrane Based on Polydopamine Adhesive Coating and the Study of Cytocompatibility[D]. Guangzhou: Jinan University, 2016.
[9] 栗可心, 钟聚婧, 郭华超, 等. PCL/HA骨组织工程多孔支架的制备及其理化性能研究[J]. 高分子通报, 2021(5): 88-95.
LI Ke-xin, ZHONG Ju-jing, GUO Hua-chao, et al. Preparation and Physicochemical Properties of PCL/HA Bone Tissue Engineering Porous Scaffold[J]. Polymer Bulletin, 2021(5): 88-95.
[10] 徐燕, 魏波, 周进, 等. 多巴胺表面修饰/负载软骨源性形态发生蛋白1的3D打印聚己内酯-羟基磷灰石三维多孔支架促进人BMSCs成软骨分化的实验研究[J]. 中国修复重建外科杂志, 2018, 32(2): 215-222.
XU Yan, WEI Bo, ZHOU Jin, et al. Dopamine Modified and Cartilage Derived Morphogenetic Protein 1 Laden Polycaprolactone-Hydroxyapatite Composite Scaffolds Fabricated by Three-Dimensional Printing Improve Chondrogenic Differentiation of Human Bone Marrow Mesenchymal Stem Cells[J]. Chinese Journal of Reparative and Reconstructive Surgery, 2018, 32(2): 215-222.
[11] XU Zhi-min, WANG Ning-ning, LIU Peng, et al. Poly (Dopamine) Coating on 3D-Printed Poly-Lactic-Co-Glycolic Acid/β-Tricalcium Phosphate Scaffolds for Bone Tissue Engineering[J]. Molecules, 2019, 24(23): 4397.
[12] CHEN Lei, SHAO Li-ping, WANG Feng-ping, et al. Enhancement in Sustained Release of Antimicrobial Peptide and BMP-2 from Degradable Three Dimensional-Printed PLGA Scaffold for Bone Regeneration[J]. RSC Advances, 2019, 9(19): 10494-10507.
[13] ZHANG Meng, ZHANG Ji-ting, BAN Li-na, et al. Polydopamine Regulated Hydroxyapatite Microspheres Grown in the Three-Dimensional Honeycomb-Like Mollusk Shell- Derived Organic Template for Osteogenesis[J]. Biofabrication, 2020, 12(3): 035022.
[14] 谭英, 谭帼馨, 宁成云, 等. 聚多巴胺修饰钛表面纳米载银及其抗菌和细胞相容性[J]. 无机材料学报, 2014, 29(12): 1320-1326.
TAN Ying, TAN Guo-xin, NING Cheng-yun, et al. Bioinspired Polydopamine Functionalization of Titanium Surface for Silver Nanoparticles Immobilization with Antibacterial Property[J]. Journal of Inorganic Materials, 2014, 29(12): 1320-1326.
[15] 王勇. 基于聚多巴胺辅助表面沉积含银涂层的聚醚醚酮的制备及抗菌性能与生物相容性研究[D]. 苏州: 苏州大学, 2016.
WANG Yong. Preparation and Antibacterial Property and Biocompatibility of Silver-Coated PEEK Using Polydopamine-Assisted Deposition Technique[D]. Suzhou: Soochow University, 2016.
[16] 张维波. 多巴胺介导钛表面纳米银涂层的构建及其抗菌和成骨活性评价[D]. 济南: 山东大学, 2019.
ZHANG Wei-bo. Construction of Dopamine-Mediated Nano-Silver Coating on Titanium Surface and Its Antibacterial and Osteogenic Activity Evaluation[D]. Jinan: Shandong University, 2019.
[17] 王邓莉. 多巴胺诱导AZ31医用镁合金仿生矿化HA涂层的体内研究[D]. 兰州: 兰州大学, 2017.
WANG Deng-li. In Vivo Study of AZ31 Medical Magnesium Coated with Hydroxyapatite by Polydopamine- Assisted Biomimetic Technique[D]. Lanzhou: Lanzhou University, 2017.
[18] 张松营. 医用钛合金表面不同粒度Al2O3喷砂酸蚀及多巴胺涂层研究[D]. 兰州: 兰州大学, 2014.
ZHANG Song-ying. Surface Treatments of Medical Titanium Alloy by Al2O3Blasting with Different Sizes and Acid Etching and Dopamine Coating[D]. Lanzhou: Lanzhou University, 2014.
[19] 尤莹. 多孔钛表面聚多巴胺黏附羟基磷灰石的复合涂层制备及对细胞黏附和增殖的研究[D]. 南京: 南京医科大学, 2018.
YOU Ying. Preparation of Poly Dopamine-Hydroxyapatite Composite Coating on Porous Titanium and Study on Cell Adhesion and Proliferation[D]. Nanjing: Nanjing Medical University, 2018.
[20] MULYATI S, MUCHTAR S, ARAHMAN N, et al. Two- Step Dopamine-to-Polydopamine Modification of Polyethersulfone Ultrafiltration Membrane for Enhancing Anti- Fouling and Ultraviolet Resistant Properties[J]. Polymers, 2020, 12(9): 2051.
[21] TIAN Jin, XU Ting, ZHANG Zhong-wei, et al. Study on the Construction of Polyethyleneimine/Nano-Silica Multilayer Film on the Carbon Fiber Surfaces to Improve the Interfacial Properties of Carbon Fiber/Epoxy Composites[J]. Composite Interfaces, 2022, 29(4): 361-381.
[22] 张冉冉, 韩慧, 魏世成, 等. 基于聚多巴胺的材料表面修饰对二磷酸腺苷促血小板聚集功能的影响[J]. 口腔颌面修复学杂志, 2016, 17(4): 202-206.
ZHANG Ran-ran, HAN Hui, WEI Shi-cheng, et al. The Effects of Polydopamine Surface Modification on Platelet Aggregation Activated by Adenosine Diphosphate[J]. Chinese Journal of Prosthodontics, 2016, 17(4): 202-206.
[23] 周田园, 李德超, 李慕勤, 等. 纯钛微弧氧化-多巴胺-环型多肽涂层的细胞相容性研究[J]. 口腔医学研究, 2017, 33(7): 703-706.
ZHOU Tian-yuan, LI De-chao, LI Mu-qin, et al. Cytocompatibility of Ultrasonic Micro-Arc Oxidation-Dopamine-Cyclo(RGD)Coating on Pure Titanium[J]. Journal of Oral Science Research, 2017, 33(7): 703-706.
[24] GUO Chu-chu, CUI Wen-di, WANG Xiao-wei, et al. Poly-l-Lysine/Sodium Alginate Coating Loading Nanosilver for Improving the Antibacterial Effect and Inducing Mineralization of Dental Implants[J]. ACS Omega, 2020, 5(18): 10562-10571.
[25] CHOI S H, JANG Y S, JANG J H, et al. Enhanced Antibacterial Activity of Titanium by Surface Modification with Polydopamine and Silver for Dental Implant Application[J]. Journal of Applied Biomaterials & Functional Materials, 2019, 17(3): 2280800019847067.
[26] MARINAS I C, TIHAUAN B M, DIACONU A G, et al. Polydopamine-Assisted Surface Modification of Ti-6Al- 4V Alloy with Anti-Biofilm Activity for Dental Implantology Applications[J]. Coatings, 2021, 11(11): 1385.
[27] 邱滢, 李祥伟, 刘亚楠, 等. 载BMP-2多巴胺-肝素-透明质酸促进牙本质形成的研究[C]//中华口腔医学会第十一次全国牙体牙髓病学学术大会论文汇编. 长沙: 中华口腔医学会, 2018: 205-206.
QIU Ying, LI Xiang-wei, LIU Ya-nan, et al. Dopamine- Heparin-Hyaluronic Acid Loaded with BMP-2 Promotes Dentin Formation[C]//Dissertation Compile of the 11th National Conference on Endodontics and Endodontics of the Chinese Association of Stomatology. Professional Committee of odontology and endodontics of Chinese Stomatological Association: Chinese Stomatological Association,2018:205-206.
[28] LIU Ya-nan, QIU Ying, NI Shi-lei, et al. Mussel‐Inspired Biocoating for Improving the Adhesion of Dental Pulp Stem Cells in Dental Pulp Regeneration[J]. Macromolecular Rapid Communications, 2020, 41(24): 2000102.
[29] ZHOU Yun-zhi, CAO Ying, LIU Wei, et al. Polydopamine-Induced Tooth Remineralization[J]. ACS Applied Materials & Interfaces, 2012, 4(12): 6901-6910.
[30] FIGUEIREDO MACEDO DE LIMA J, AGUIAR JORDÃO MAINARDI M D C, PUPPIN-RONTANI R M, et al. Bioinspired Catechol Chemistry for Dentin Remineralization: A New Approach for the Treatment of Dentin Hypersensitivity[J]. Dental Materials, 2020, 36(4): 501-511.
[31] 曾玲, 董波, 仲琪, 等. 多巴胺对牙本质黏结强度的实验研究[J]. 微量元素与健康研究, 2019, 36(6): 4-6.
ZENG Ling, DONG Bo, ZHONG Qi, et al. Experimental Study on the Bonding Strength of Dopamine to Dentin[J]. Studies of Trace Elements and Health, 2019, 36(6): 4-6.
[32] LUO Ri-fang, WANG Xin, DENG Jin-chuan, et al. Dopamine-Assisted Deposition of Poly(ethylene imine) for Efficient Heparinization[J]. Colloids and Surfaces B: Biointerfaces, 2016, 144: 90-98.
[33] DAVOUDI P, ASSADPOUR S, DERAKHSHAN M A, et al. Biomimetic Modification of Polyurethane-Based Nanofibrous Vascular Grafts: A Promising Approach towards Stable Endothelial Lining[J]. Materials Science and Engineering: C, 2017, 80: 213-221.
[34] GREWAL M S, ABE H, MATSUO Y, et al. Aqueous Dispersion and Tuning Surface Charges of Polytetrafluoroethylene Particles by Bioinspired Polydopamine-Polyethyleneimine Coating via One-Step Method[J]. Royal Society Open Science, 2021, 8(8): 210582.
[35] 朱利平, 徐又一, 奚振宇, 等. DOPA在聚乙烯微孔膜上的自聚合及肝素固定化[J]. 高分子学报, 2009(4): 394-397.
ZHU Li-ping, XU You-yi, XI Zhen-yu, et al. self-Polymerization of Dopa on Polyethylene Porous Membranes and Immobilization of Heparin[J]. Acta Polymerica Sinica, 2009(4): 394-397.
[36] 肖琳琳, 魏雨, 计剑. 基于聚多巴胺辅助自组装单分子层技术的PTFE表面修饰及其内皮细胞选择性黏附研究[J]. 高分子学报, 2010(4): 479-483.
XIAO Lin-lin, WEI Yu, JI Jian. Surface Tailoring of Ptfe for Endotheleal Cells Selectivity Based on polydopamine-Assisted self-Assembly Monolayer Technique[J]. Acta Polymerica Sinica, 2010(4): 479-483.
[37] 汪涛, 赵珺, 张健, 等. 多巴胺处理聚四氟乙烯人工血管对体外种植内皮细胞的影响[J]. 中国现代普通外科进展, 2016, 19(1): 11-15.
WANG Tao, ZHAO Jun, ZHANG Jian, et al. Influence of Growth of Cultivatable Endothelial Cells by Polytetrafluoroethylene Artificial Blood Vessels Processed with Dopamine in Vitro[J]. Chinese Journal of Current Advances in General Surgery, 2016, 19(1): 11-15.
[38] 贾山山. 多巴胺共混聚乙烯亚胺并接枝肝素对膨体聚四氟乙烯人工小血管表面改性的研究[D]. 广州: 南方医科大学, 2018.
JIA Shan-shan. Study on the Surface Modification of Expanded Polytetrafluoroethylene Artificial Small Blood Vessel with Dopamine Blend Polyethylene Imine and Graft Heparin[D]. Guangzhou: Southern Medical University, 2018.
[39] MI Hao-yang, JING Xin, THOMSOM J A, et al. Promoting Endothelial Cell Affinity and Antithrombogenicity of Polytetrafluoroethylene (PTFE) by Mussel-Inspired Modification and RGD/Heparin Grafting[J]. Journal of Materials Chemistry B, 2018, 6(21): 3475-3485.
[40] 李亚民. 生物活性人工韧带移植物的构建及促进移植物-骨整合的实验研究[D]. 上海: 上海交通大学, 2020.
LI Ya-min. Optimal Construction of Bioactive Engineered Ligament for Enhancing Graft—Bone Osseointegration[D]. Shanghai: Shanghai Jiao Tong University, 2020.
[41] 俞斌, 丁惠锋, 杨超华, 等. Fe3O4涂层多巴胺修饰PET人工韧带对MC3T3-E1细胞黏附、增殖和分化影响的实验研究[J]. 中国运动医学杂志, 2016, 35(5): 438-444.
YU Bin, DING Hui-feng, YANG Chao-hua, et al. Fe3O4and Dopamine Coating Improves the Adhesion, Proliferation and Differentiation of MC3T3-E1 Cells on the Surface of PET[J]. Chinese Journal of Sports Medicine, 2016, 35(5): 438-444.
[42] YU Bin, PEI Peng, YU Bao-qing, et al. Enhance the Bioactivity and Osseointegration of the Polyethylene- Terephthalate-Based Artificial Ligament via Poly(Dopamine) Coating with Mesoporous Bioactive Glass[J]. Advanced Engineering Materials, 2017, 19(5): 1600708.
[43] WU Yang, ZHANG Yu-han, ZHANG Ren, et al. Preparation and Properties of Antibacterial Polydopamine and Nano-Hydroxyapatite Modified Polyethylene Terephthalate Artificial Ligament[J]. Frontiers in Bioengineering and Biotechnology, 2021, 9: 630745.
[44] 吉明波. 聚砜超滤膜仿生改性及其在血液净化中的应用[D]. 北京: 中国科学院大学(中国科学院过程工程研究所), 2017.
JI Ming-bo. Biomimetic Modification of Polysulfone Ultrafiltration Membrane and Its Application in Blood Purification[D]. Beijing: Institute of Process Engineering, Chinese Academy of Sciences, 2017.
[45] XIE Bing-wu, ZHANG Ran-ran, ZHANG Huan, et al. Decoration of Heparin and Bovine Serum Albumin on Polysulfone Membrane Assisted via Polydopamine Strategy for Hemodialysis[J]. Journal of Biomaterials Science, Polymer Edition, 2016, 27(9): 880-897.
[46] KU S H, RYU J, HONG S K, et al. General Functionalization Route for Cell Adhesion on Non-Wetting Surfaces[J]. Biomaterials, 2010, 31(9): 2535-2541.
[47] 周官山. 多巴胺改性丝蛋白膜皮肤创伤修复功能的研究[D]. 杭州: 浙江大学, 2018.
ZHOU Guan-shan. Silk Fibroin Film Modified by Dopamine and Its Application in Skin Wound Repair[D]. Hangzhou: Zhejiang University, 2018.
[48] MIAO Hao, SHEN Run-qing, ZHANG Wen-hai, et al. Near-Infrared Light Triggered Silk Fibroin Scaffold for Photothermal Therapy and Tissue Repair of Bone Tumors[J]. Advanced Functional Materials, 2021, 31(10): 2007188.
[49] JIANG Qin, LUO Zi-miao, MEN Yong-zhi, et al. Red Blood Cell Membrane-Camouflaged Melanin Nanoparticles for Enhanced Photothermal Therapy[J]. Biomaterials, 2017, 143: 29-45.
[50] ZHU Li-ping, JIANG Jin-hong, ZHU Bao-ku, et al. Immobilization of Bovine Serum Albumin Onto Porous Polyethylene Membranes Using Strongly Attached Polydopamine as a Spacer[J]. Colloids and Surfaces B: Biointerfaces, 2011, 86(1): 111-118.
[51] AN Zi-han, DAI Feng-ying, WEI Chen-jie, et al. Polydopamine/Cysteine Surface Modified Hemocompatible Poly (vinylidene fluoride) Hollow Fiber Membranes for Hemodialysis[J]. Journal of Biomedical Materials Research Part B, Applied Biomaterials, 2018, 106(8): 2869-2877.
Research Progress of the Surface Modification by Dopamine in Medical Field
,,,,
(Institute of Surface Engineering, School of Mechanical Engineering, Yangzhou University, Jiangsu Yangzhou 225127, China)
Dopamine (DA) and polydopamine (PDA) contain a large number of active and hydrophilic functional groups like catechol groups and amino groups. Therefore, they possess many properties such as strong adhesive property, good biocompatibility, outstanding reactivity and reducibility and they are widely used for surface modification of medical device materials, ship materials, sensor materials, drug transportation materials, etc. Among them, the research prospects for the surface modification of medical device materials are particularly broad. materials.
This article analyzes the various properties and functions of dopamine, and summarizes the specific application of dopamine in bioengineering materials such as enhancing the bone tissue regeneration ability of the material and improving the adhesion and proliferation of cells on the surface of the material. On this basis, the manuscript focuses on the research progress of dopamine modification in the medical field in recent years. Explains the advantages, disadvantages and functions of each material, and how dopamine's characteristics modify the surface of the material to make up for the defects of the material. In view of the dopamine modification of different materials, the preparation methods and experimental comparison results were summarized. The future perspectives of dopamine surface modification technology are discussed rationally at the end.
The modification of dopamine on bone repair and bone graft materials includes composite materials and polymer materials, etc.; Dopamine on dental implants and dental restoration materials Modifications include nano-metal materials and alloy materials; the modification of new medical materials by dopamine includes artificial blood vessels, artificial ligament materials and medical membrane materials. In most articles, dopamine coatings are prepared in much the same way. Dopamine is added to Tris-HCl buffer, and then the material is soaked in solution to form a film of dopamine on the surface of the material. Due to its excellent adhesion and chemical reaction activity, dopamine can be used as a bridge between engineered scaffolds and cells, effectively promoting the adhesion and proliferation of cells on the surface of scaffolds and improving the adhesion of cells on the surface of bone repair materials. Due to the large number of active functional groups, such as catechol groups and amino groups, dopamine can combine bone repair materials with growth factors through covalent bond or non-covalent bond, and the binding force of the two is significantly improved, thus enhancing the regeneration ability of bone tissue. Due to its good adhesion, dopamine can improve the regeneration ability of the bone tissue by guiding the surface mineralization of the scaffold material, so as to slow down the occurrence of the stress shielding phenomenon of the scaffold. Dopamine contains a large number of amino, hydroxyl and other hydrophilic groups. By adding hydrophilic groups on the hydrophobic surface of the material, dopamine can improve the hydrophilic properties of the material, thus improving cell adhesion and proliferation, making artificial blood vessels, artificial ligaments and other materials more suitable for medical applications. Dopamine can undergo oxidation self-polymerization under weak alkaline conditions with dissolved oxygen, forming a biocompatible polydopamine coating on the surface of the material. Polydopamine coatings can react with compounds containing groups such as amino groups and thiols through the structure of phthalol to form a strong and stable chemical bond, and antibiotic drugs can be grafted to the surface of the material by polydopamine coupling. The surface of dopamine-modified medical devices has the disadvantages of adhesion, friction resistance, antibacterial broad spectrum and insufficient timeliness. In order to overcome the above shortcomings, it is necessary to improve the timeliness of dopamine modification coatings from the dopamine polymerization and adhesion mechanism, and incorporate antibacterial and antifouling organic matter on the basis of not affecting its biocompatibility, so as to improve the broad spectrum and adhesion of the anti-biofilm.
dopamine; polydopamine; surface modification; medical apparatus; medical implant materials
TB34
A
1001-3660(2022)11-0164-10
10.16490/j.cnki.issn.1001-3660.2022.11.014
2021–09–13;
2022–03–17
2021-09-13;
2022-03-17
国家自然科学基金项目(51905468);江苏省自然科学基金项目(BK20190916)
The National Natural Science Foundation of China (51905468); the Natural Science Foundation of Jiangsu Province (BK20190916)
刘雨晗(2000—),女,硕士生,主要研究方向为表面与界面工程。
LIU Yu-han (2000-), Female, Postgraduate, Research focus: surface and interface engineering.
曹攀(1989—),男,博士,讲师,主要研究方向为船体绿色防污新技术。
CAO Pan (1989-), Male, Doctor, Lecturer, Research focus: new technology of hull green antifouling.
刘雨晗, 刘德, 王意, 等. 多巴胺表面修饰在医疗领域的研究进展[J]. 表面技术, 2022, 51(11): 164-173.
LIU Yu-han, LIU De, WANG Yi, et al. Research Progress of the Surface Modification by Dopamine in Medical Field[J]. Surface Technology, 2022, 51(11): 164-173.
责任编辑:万长清

