紫杉醇脂质体联合顺铂治疗晚期卵巢癌患者的疗效及血清肿瘤标志物水平分析
刘锦 张敏 王卉 国晓 尹春霞
聊城市第三人民医院妇产科,聊城 252000
卵巢癌是女性生殖系统常见恶性肿瘤,临床卵巢癌患者采用手术切除、放化疗等治疗,但患者的预后不佳[1-5]。有研究显示,顺铂在卵巢癌患者治疗中,有利于降低对肿瘤细胞的毒性作用[6]。紫杉醇脂质体属于细胞毒类的抗肿瘤药。它能够促进微管双聚体装配并且阻止其解聚。还有研究显示,紫杉醇脂质体在卵巢癌患者治疗中,效果较好,且不良反应较少[7]。然而,卵巢癌患者应用紫杉醇脂质体联合顺铂治疗的效果尚不清楚,鉴于此,本研究选取患者,探讨联合用药的效果,详情如下。
资料与方法
1、临床资料
经医学伦理委员会批准选取2018年12月至2021年12月聊城市第三人民医院收治的82例晚期卵巢癌患者,随机数字表法分为研究组和对照组,各41例。研究组年龄36~68(51.85±5.19)岁,体 质 量 指 数(BMI)22.47~25.98(22.85±1.54)kg/m2。对照组年龄35~59(50.89±5.58)岁,BMI 21.65~25.96(23.68±1.61)kg/m2。两组基本资料可比(均P>0.05)。
纳入标准:符合卵巢癌诊断标准[8];患者均行手术治疗;患者生存期>6个月;>18岁;患者均签订知情同意书。
排除标准:其他恶性肿瘤;化疗禁忌证患者;主要器官功能异常;化疗前血尿粪常规、血凝异常;同时进行其他抗肿瘤治疗者。
2、方法
对照组采用TP(紫杉醇+顺铂),每周期第1天给予顺铂(德州德药制药有限公司生产,国药准字H37020524)30 mg/m2。21 d为1个周期,每周期第1天给予260 mg/m2白蛋白结合型紫杉醇,初始量400 ml/min,30 min后患者无不适症状可调整至600 ml/min。
研究组采用紫杉醇脂质体联合顺铂静脉给药治疗,顺铂参照对照组,紫杉醇脂质体(包装规格30 mg/瓶,南京绿叶制药有限公司,批准文号H2003.357),常用剂量为135~175 mg/m2,使用前先向瓶内加入10 ml 5%葡萄糖溶液,置振荡器上振摇5 min,待完全溶解后,注入250~500 ml 5%葡萄糖溶液中,治疗2个月。
3、研究指标
⑴比较两组患者临床疗效[9]。完全缓解:症状消失;部分缓解:症状明显减轻;疾病稳定:临床症状未见减轻;疾病进展:临床症状加重。客观缓解率=(完全缓解人数+部分缓解人数)/总人数×100.00%。⑵患者T细胞亚群水平。空腹采集静脉血5 ml于抗凝管中,离心分离血浆,采用流式细胞仪测定患者CD3+、CD4+。⑶比较两组患者血清肿瘤标志物水平。癌胚抗原(CEA)及人附睾分泌蛋白4(HE4)检测方法:采集卵巢癌患者首次化疗前(健康者于体检当天)静脉血3 ml(肝素抗凝),分离血清后采用酶联免疫吸附法测定血清CEA、HE4水平(试剂盒均购于上海雅培公司)。⑷不良反应。
4、统计学分析
采用SPSS 25.0软件进行统计学分析,以(±s)表示符合正态分布的计量资料,组内比较采用配对t检验,组间比较采用独立样本t检验;以例(%)表示计数资料,行χ2检验。P<0.05为差异有统计学意义。
结 果
1、临床疗效
研究组客观缓解率高于对照组(P<0.05)。见表1。

表1 两组晚期卵巢癌患者临床疗效比较[例(%)]
2、T细胞亚群水平
与治疗前相比,两组CD3+、CD4+均呈现升高趋势,且研究组高于对照组(均P<0.05)。见表2。
表2 两组晚期卵巢癌患者T细胞亚群水平比较(%,±s)
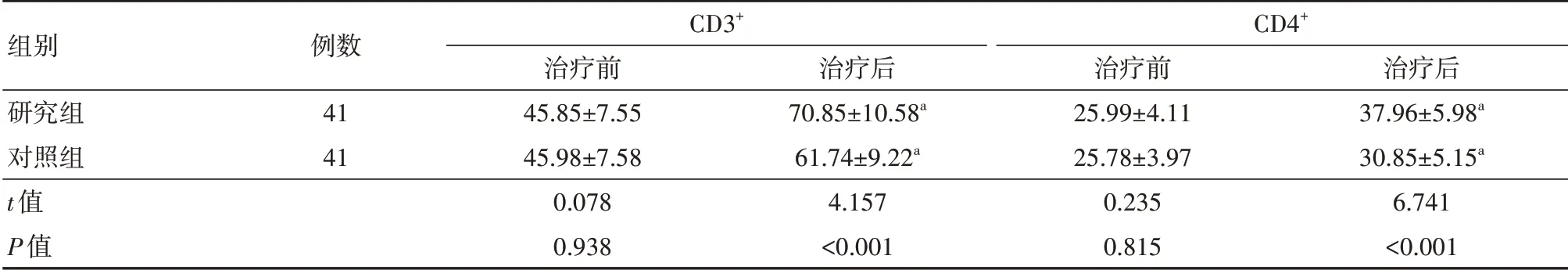
表2 两组晚期卵巢癌患者T细胞亚群水平比较(%,±s)
注:对照组采用TP方案(紫杉醇+顺铂),研究组采用紫杉醇脂质体联合顺铂治疗。与治疗前比较,aP<0.05
组别研究组对照组t值P值例数41 41 CD3+治疗前45.85±7.55 45.98±7.58 0.078 0.938治疗后70.85±10.58a 61.74±9.22a 4.157<0.001 CD4+治疗前25.99±4.11 25.78±3.97 0.235 0.815治疗后37.96±5.98a 30.85±5.15a 6.741<0.001
3、血清肿瘤标志物
与治疗前相比,两组患者治疗后CEA、HE4水平均降低,且研究组低于对照组(均P<0.05)。见表3。
表3 两组晚期卵巢癌患者治疗前后血清肿瘤标志物水平比较(±s)
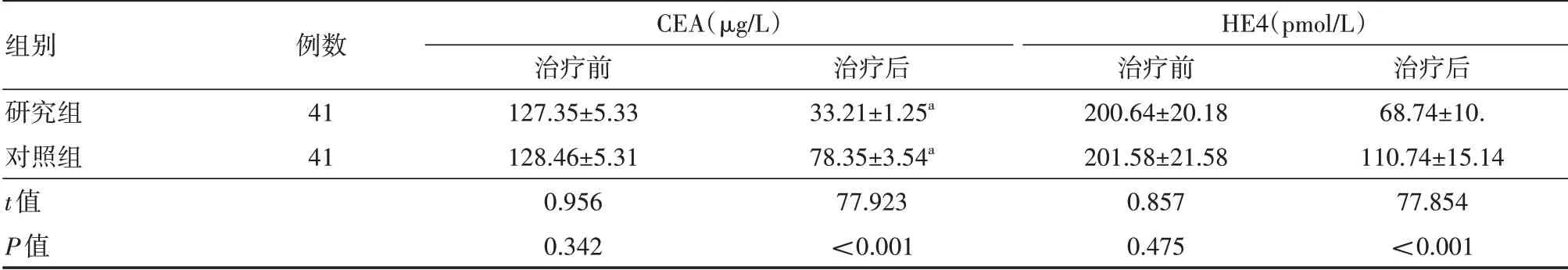
表3 两组晚期卵巢癌患者治疗前后血清肿瘤标志物水平比较(±s)
注:对照组采用TP方案(紫杉醇+顺铂),研究组采用紫杉醇脂质体联合顺铂治疗。CEA为癌胚抗原,HE4为人附睾分泌蛋白4
组别研究组对照组t值P值例数41 41 CEA(µg/L)治疗前127.35±5.33 128.46±5.31 0.956 0.342治疗后33.21±1.25a 78.35±3.54a 77.923<0.001 HE4(pmol/L)治疗前200.64±20.18 201.58±21.58 0.857 0.475治疗后68.74±10.110.74±15.14 77.854<0.001
4、不良反应
研究组不良反应发生率低于对照组(P<0.05)。见表4。

表4 两组晚期卵巢癌患者不良反应发生情况比较[例(%)]
讨 论
卵巢癌是临床中较为常见的妇科恶性肿瘤。研究指出,对于晚期卵巢癌患者治疗应采取多种方案,改善患者预后,提高患者的生存期[11-15]。临床中卵巢癌的治疗方案多采用手术联合化疗,有患者治疗后复发率较高,临床转归情况较差,影响患者预后[16-18]。常规化疗方案由于周期长等,对于部分患者来说难以忍受,对患者产生不良影响[19-21]。
本研究发现,研究组客观缓解率高于对照组,提示本研究治疗方案疗效显著。紫杉醇脂质体可用于卵巢癌的一线化疗以及以后卵巢转移性癌的治疗[22-23]。研究指出,紫杉醇脂质体也可与顺铂联合应用,紫杉醇脂质体可用于过含阿霉素标准化疗的乳腺癌患者的后续治疗,或复发患者的治疗,而达到抑制癌细胞增殖的目的,起到抗肿瘤的效果[24-26]。此外,治疗后研究组CD3+、CD4+高于对照组,提示紫杉醇脂质体联合顺铂治疗能够改善患者免疫功能。研究指出,成熟T淋巴细胞表示人体细胞免疫功能状态[27-18]。CD3细胞正常值参考范围955~2 860/µl。紫杉醇脂质体治疗卵巢癌患者,可改善患者机体免疫功能。
本研究还发现,治疗后,研究组CEA、HE4水平低于对照组,提示紫杉醇脂质体联合顺铂治疗卵巢癌患者,可以促进患者康复。有研究指出,CEA为一种具有人类胚胎抗原特性的酸性糖蛋白,其水平异常升高可能会影响肿瘤的分化,致使浸润、转移的发生风险升高,进而可能影响卵巢癌患者的临床转归[15];HE4可促进卵巢癌的早期浸润转移,可致使疾病进展恶化,其表达水平升高可能是影响卵巢癌临床转归不良的信号,可在一定程度上反映卵巢癌患者的临床进展、预后[29]。研究组不良反应发生率低于对照组,提示紫杉醇脂质体联合顺铂治疗卵巢癌,可降低患者不良反应发生率。有研究指出,紫杉醇脂质体是常用的一种化疗药物,在治疗中,患者不良反应低,说明紫杉醇脂质体较为安全[30]。
卵巢癌患者应用紫杉醇脂质体联合顺铂治疗可提高疗效,改善患者免疫功能,降低不良反应发生率。
利益冲突所有作者均声明不存在利益冲突

