地骨皮药材饮片和标准汤剂的定量检测及UPLC特征图谱的建立
史紫娟,曾杉,林碧珊,高永坚,刘勇,梁思韵,区淑蕴
国药集团 广东环球制药有限公司,广东 佛山 528305
地骨皮为茄科植物枸杞Lycium chinenseMill.或宁夏枸杞L.barbarumL.的干燥根皮,具有凉血除蒸、清肺降火之功效,用于阴虚潮热、骨蒸盗汗、肺热咳嗽等症[1]。地骨皮含有生物碱、黄酮、蒽醌及有机酸等多种化学成分,其中生物碱类主要有地骨皮甲素和地骨皮乙素等[2-3]。地骨皮甲素和地骨皮乙素属于酚酰胺类,是地骨皮中的特有成分,也是其主要的药效成分。现代药理学研究表明,地骨皮具有降血压、调血脂、降血糖、抑菌抗炎、免疫调节、解热镇痛等作用[4-5]。本研究参考《香港中药材标准》中地骨皮的质量标准[6],以地骨皮乙素为定量指标,采用超高效液相色谱法(UPLC)测定地骨皮药材、饮片和标准汤剂中地骨皮乙素的含量,对地骨皮药材进行质量控制。
中药饮片标准汤剂作为中药配方颗粒临床疗效的标准参照物,在《中药配方颗粒质量控制与标准制定技术要求》等文件中明确要求有关中药配方颗粒的所有研究均应与标准汤剂进行对比研究[7-9]。因此,本研究建立地骨皮药材-饮片-标准汤剂的UPLC特征图谱及有效成分的定量检测方法,深入开展药材-饮片-标准汤剂的相关性分析,为地骨皮的质量控制及中药配方颗粒和经典名方的研究提供参考。
1 材料
1.1 仪器
H-Class型UPLC仪(美国Waters公司);XPR105 DR 型天平、AL104 型天平(瑞士Mettler-Toledo 公司);KQ5200DA型数控超声波清洗器(昆山市超声仪器有限公司);FTS-40F 型陶瓷保健壶(潮州市一壶百饮电器实业有限公司);TRL-0.5 型真空冷冻干燥机(大连双瑞科技有限公司);Synergy UV 型超纯水仪(美国Millipore公司)。
1.2 试药
对照品地骨皮甲素(批号:DST170724-101,纯度≥96%)、地骨皮乙素(批号:DST170724-105,纯度≥98%)均购自成都德思特生物技术有限公司;甲醇和乙腈(美国BCR 公司,色谱纯);甲酸、磷酸、三氟乙酸(Aladdin 公司,色谱纯);水为超纯水。
18 批地骨皮药材分别产自陕西、河南、山西、宁夏等地,经广东一方制药有限公司魏梅主任药师鉴定为茄科植物枸杞Lycium chinenseMill.的干燥根皮,按《中华人民共和国药典》(以下简称《中国药典》)2020 年版标准检验全部合格,并参考其地骨皮项下炮制方法制成地骨皮饮片[1]。具体炮制方法:除去泥沙、异物及残留木心等杂质,喷淋10 s,于烘箱60 ℃干燥2 h。药材产地分别为陕西省渭南市(S1~S3)、河南省洛阳市(S4~S6)、山西省运城市(S7~S12)、宁夏固原市(S13~S15)、宁夏银川市(S16~S18)。
2 方法与结果
2.1 地骨皮标准汤剂的制备
取地骨皮饮片100 g,加水煎煮2 次,一煎加10 倍量水浸泡30 min,加热25 min,用350 目筛趁热滤过;二煎药渣再加8 倍量水,加热20 min,趁热滤过,合并2 次滤液。减压浓缩至150 g 左右的浸膏,即得地骨皮标准汤剂。浸膏加水稀释至含固率约15%,再进行冷冻干燥,即得地骨皮标准汤剂冻干粉。
2.2 UPLC特征图谱
2.2.1 色谱条件与系统适用性试验 Waters BEH C18色谱柱(100 mm×2.1 mm,1.7 μm),流动相为甲醇(A)-0.15%三氟乙酸水溶液(B),洗脱梯度(0~5 min,8%~14%A;5~14 min,14%~25%A;14~23 min,25%~50%A;23~26 min,50%~90%A);检测波长为280 nm;柱温为40 ℃;流速为0.25mL·min-1,进样量为1µL。理论板数按地骨皮乙素峰计算应不低于10 000。
2.2.3 药材和饮片供试品溶液的制备 取本品粉末约0.2 g,精密称定,置25 mL 量瓶中,加入甲醇-0.5%乙酸溶液(1∶1)的混合溶液适量,超声处理(500 W,40 kHz)30 min,放冷,用甲醇-0.5%乙酸溶液(1∶1)的混合溶液定容至刻度,摇匀,滤过,取续滤液,即得。
2.2.4 标准汤剂供试品溶液的制备 取本品冻干粉约0.1 g,精密称定,与2.2.3 项下“置25 mL 量瓶中”后相同操作,取续滤液,即得。
2.2.5 方法学考察 精密度试验:取地骨皮标准汤剂供试品溶液,连续进样6 次,结果各特征峰的相对保留时间和相对峰面积的RSD 均小于2%,表明仪器精密度良好。
重复性试验:取地骨皮标准汤剂冻干粉,平行制备6 份供试品溶液进样测定,结果各特征峰的相对保留时间和相对峰面积的RSD 均小于3%,表明该方法重复性良好。
稳定性试验:取地骨皮标准汤剂供试品溶液,分别于0、2、4、6、8、12、24 h进样测定,结果各特征峰的相对保留时间和相对峰面积的RSD 均小于3%,表明供试品溶液在24 h 内稳定。
2.2.6 样品测定 按2.2.3 和2.2.4 项下方法制备供试品溶液,按2.2.1 项下色谱条件分别对18 批地骨皮药材、饮片和标准汤剂进行测定,记录色谱图,见图1~3。

图1 18批地骨皮药材UPLC特征图谱

图2 18批地骨皮饮片UPLC特征图谱

图3 18批地骨皮标准汤剂UPLC特征图谱
2.2.7 共有峰的标定 将各批地骨皮药材、饮片及标准汤剂所得结果分别导入“中药色谱指纹图谱相似度评价系统”(2012版),设参照图谱、对色谱图进行多点校正、峰匹配,采用平均数法生成多批样品的特征图谱与对照特征图谱。选择分离度较好、峰面积稳定的色谱峰作为共有峰,最终药材、饮片和标准汤剂分别各确定了5个共有峰,见图1~3。通过对照品指认了2 个特征峰,其中2 号峰为地骨皮乙素、3 号峰为地骨皮甲素,见图4。地骨皮药材、饮片与标准汤剂对照特征图谱见图5。以峰2(地骨皮乙素)为参照峰,分别计算地骨皮药材、饮片和标准汤剂中各共有峰的相对保留时间和相对峰面积,结果见表1。结果表明,不同产地的药材物质群接近,炮制不会对物质群造成太大改变。
表1 地骨皮药材、饮片、标准汤剂UPLC特征图谱分析(, n=18)

表1 地骨皮药材、饮片、标准汤剂UPLC特征图谱分析(, n=18)

图4 地骨皮乙素、地骨皮甲素对照品溶液的UPLC图
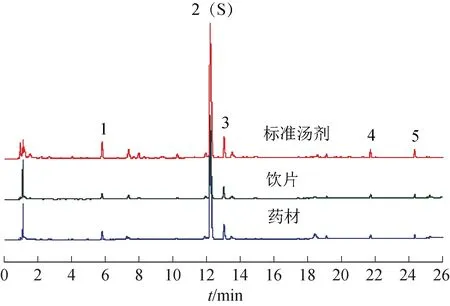
图5 地骨皮药材、饮片与标准汤剂对照特征图谱
2.2.8 相关性分析 采用“中药色谱指纹图谱相似度评价系统”(2012 版),对各批供试品特征图谱与对照图谱进行比较,分别计算18 批地骨皮药材、饮片、标准汤剂的相似度,结果见表2。18 批地骨皮药材与对照特征图谱的相似度为0.951~0.994,饮片相似度为0.942~0.991,标准汤剂相似度为0.978~0.999。说明不同来源的地骨皮药材和饮片主成分具有较好的一致性。所标定5 个共有特征峰经多批次产品验证,各峰均可在标准汤剂、药材和饮片特征图谱中得到追踪,表明地骨皮从药材到标准汤剂过程中各成分得到了有效的转移。
从各元素的沸点可知,由铁到砷挥发率越来越大,所以控制适当的真空度和温度,铅、铋、砷、锑能以气态挥发出来,而铁、铜则留在锡液中。

表2 18批地骨皮药材、饮片、标准汤剂的相似度
2.3 地骨皮药材、饮片和标准汤剂中有效成分的定量测定
《中国药典》2020 年版地骨皮药材及饮片均没有相应的含量测定项,本研究参考《香港中药材标准》中地骨皮的含量测定项方法[6],采用UPLC 同时建立了地骨皮药材、饮片和标准汤剂中地骨皮乙素的含量测定方法,可为制定地骨皮配方颗粒的质量控制标准提供参考。
2.3.1 色谱条件与系统适用性试验 同2.2.1项下方法。
2.3.2 对照品溶液的制备 取地骨皮乙素对照品适量,精密称定,加甲醇-0.5%乙酸溶液(1∶1)的混合水溶液制成质量浓度为120 μg·mL-1的对照品溶液。
2.3.3 供试品溶液的制备 地骨皮药材和饮片供试品溶液的制备同2.2.3 项下方法,标准汤剂供试品溶液的制备同2.2.4项下方法。
2.3.4 方法学考察
2.3.4.1 线性关系考察 精密称取地骨皮乙素对照品20.03 mg,置25 mL量瓶中,加甲醇-0.5%乙酸溶液(1∶1)的混合水溶液溶解并定容至刻度,作为对照品储备溶液。分别精密量取上述储备液稀释成质量浓度分别为25.04、50.08、100.15、200.30、400.60、801.20 μg·mL-1的对照溶液,按2.3.1项下色谱条件进行测定,记录色谱峰面积。以地骨皮乙素的峰面积为纵坐标(Y),质量浓度为横坐标(X),绘制标准曲线,得回归方程:Y=1 480.247X+4 499.614(r=1.000),表明25.04~801.20 μg·mL-1时,地骨皮乙素质量浓度与峰面积线性关系良好。
2.3.4.2 精密度试验 取地骨皮乙素对照品溶液,按2.3.1项下色谱条件连续进样6次,计算地骨皮乙素峰面积的RSD为0.2%,表明仪器精密度良好。
2.3.4.3 稳定性试验 取地骨皮标准汤剂约0.1 g,精密称定,按2.3.3 项下方法制备供试品溶液,精密吸取供试品溶液,按2.3.1 项下色谱条件,分别在0、2、4、6、8、12、16、20、24 h进样,计算地骨皮乙素峰面积的RSD 为0.4%,表明供试品溶液在24 h内稳定。
2.3.4.4 重复性试验 取地骨皮标准汤剂约0.1 g,精密称定,按2.3.3项下方法平行制备6份供试品溶液,精密吸取供试品溶液,按2.3.1 项下色谱条件测定,测定供试品溶液中地骨皮乙素含量并计算RSD为0.9%,表明该方法重复性良好。
2.3.4.5 加样回收率试验 取同一批已知含量的地骨皮标准汤剂约50 mg,平行称取6 份,精密称定,置25 mL 具塞锥形瓶中,分别按1∶1 加入地骨皮乙素对照溶液,按2.3.3 项下方法制备供试品溶液,精密吸取供试品溶液,按2.3.1 项下色谱条件测定,结果地骨皮乙素的平均回收率为101.6%,RSD 为0.8%。
2.3.5 地骨皮标准汤剂出膏率测定 将18 批地骨皮饮片按2.1 项下方法制备成标准汤剂,测定样品的出膏率,按公式(1)计算出膏率。

2.3.6 地骨皮药材、饮片和标准汤剂样品测定根据已建立的含量测定方法对18 批地骨皮药材、饮片及标准汤剂进行定量测定并计算饮片到标准汤剂的转移率,结果见表3。结果表明18 批地骨皮标准汤剂出膏率为10.22%~14.34%,均值为12.89%,地骨皮乙素的转移率为33.63%~56.82%,均值为44.84%;按照均值的70%~130%计算地骨皮乙素的转移率为31.39%~58.29%,18 批地骨皮标准汤剂的转移率均在此范围内,未出现离散数据。

表3 地骨皮药材、饮片及标准汤剂测定结果 %

3 讨论
本研究参考《香港中药材标准》中地骨皮药材的特征图谱方法[6],对检测波长、流动相、色谱柱、柱温、流速等系统适应性条件进行优化,通过全波长扫描确定280 nm 下色谱图基线平稳、分离度较好,色谱峰信息更多且响应值较高,故选择280 nm 作为特征图谱的检测波长。考察了不同体系流动相甲醇-0.15%三氟乙酸水溶液、乙腈-0.15%三氟乙酸水溶液、甲醇-0.1%甲酸水溶液、甲醇-0.1%磷酸水溶液对特征图谱的影响,结合分离度和峰形选择甲醇-0.15%三氟乙酸水溶液作为流动相体系。比较了3种不同类型色谱柱Waters BEH C18(100 mm×2.1 mm,1.7 μm)、YMC Triart C18(100 mm×2.1 mm,1.9 μm)、WatersCSH C18(100 mm×2.1 mm,1.7 μm)的分离效果,最终选择Waters BEH C18色谱柱。考虑到柱温和流速会影响分离度,所以考察了20、30、40 ℃的柱温,确认40 ℃柱温时分离度最佳。考察了0.20、0.25、0.30 mL·min-1的流速,结果流速为0.25 mL·min-1时,各特征峰的分离度及峰形更优。
本研究考察了不同溶剂[甲醇、50%甲醇、甲醇-0.5%乙酸溶液(1∶1)的混合水溶液、水]、提取方法(回流、超声)、提取时间(20、30、40 min)对地骨皮标准汤剂特征图谱提取效果的影响,结果显示,用甲醇-0.5%乙酸溶液(1∶1)的混合水溶液超声提取30 min 时提取效果最好,特征峰的数量和响应值最优。
4 结论
本研究制备的18 批地骨皮标准汤剂的出膏率为10.22%~14.34%,平均出膏率为12.89%。测定标准汤剂中地骨皮乙素的质量分数为7.47%~14.35%,平均质量分数为10.95%;地骨皮乙素从饮片到标准汤剂的转移率为33.63%~56.82%,平均转移率为44.84%。本研究利用UPLC 特征图谱、出膏率、含量测定及转移率,对地骨皮药材、饮片和标准汤剂进行了质量传递性研究,是经典名方及中药配方颗粒所倡导的研究方法,具有良好的科学性和合理性[10]。18 批地骨皮药材、饮片和标准汤剂的特征图谱通过拟合共确定了5 个特征峰,通过对照品指认了地骨皮甲素和地骨皮乙素,将多批结果导入“中药色谱指纹图谱相似度评价系统”(2012 版)进行计算,结果18 批地骨皮药材、饮片和标准汤剂的相似度均大于0.90,说明三者特征图谱具有良好的相关性。地骨皮标准汤剂特征图谱与地骨皮药材和饮片特征图谱化学成分基本一致,能够准确地反映药材-饮片-标准汤剂之间化学成分的可追溯性。通过标准化工艺得到的地骨皮标准汤剂质量稳定,建立的特征图谱方法和指标性成分的定量检测方法可同时用于地骨皮药材、饮片和标准汤剂的分析测定,研究结果可为地骨皮配方颗粒的质量标准研究及后期经典名方的研究提供参考。

