不同施氮水平对农田黑土净氮转化速率和温室气体排放的影响
郎 漫,袁晓航,李 平
(1南京信息工程大学江苏省农业气象重点实验室,南京 210044;2南京信息工程大学应用气象学院,南京 210044;3南京信息工程大学长望学院,南京 210044)
0 引言
氮是陆地生态系统中限制植物生长的重要养分元素之一,对农田生态系统生产力和生态环境过程具有重要影响[1]。土壤中的氮主要以有机氮形态存在,占土壤全氮含量的85%~90%。有机氮不能被植物直接吸收利用,必须经微生物作用转化为无机氮才能被植物吸收。研究指出,即使在大量施用氮肥的情况下,作物吸收的氮素仍然有50%以上来自土壤有机氮矿化产生的无机氮[2]。有机氮矿化作用的速率和强度决定了土壤中可利用氮素有效性的大小,是表征土壤基础供氮能力和供氮水平的重要指标,对于外源氮肥的吸收利用具有重要影响[3]。好气条件下,土壤铵态氮经硝化作用转化为硝态氮,当土壤含水量较高时,硝态氮可能发生反硝化作用转化为气态氮或经淋溶损失。因此,土壤氮转化速率大小对氮肥利用率和生态环境具有重要影响。
土壤有机氮矿化过程和硝化过程受众多因素影响,施用外源氮肥是其中一个重要影响因素。铵态氮肥的施用直接改变了土壤有机氮矿化作用产物和硝化作用底物的数量,进而对氮矿化和硝化过程产生重要影响。一般情况下,施用外源氮肥可以提高土壤脲酶和蛋白酶活性,促进矿化作用形成铵态氮,从而增加净氮矿化量[4-5]。王晓维等[6]研究报道,在0~120 mg N/kg施氮范围内,红壤净氮矿化量随施氮量的增加而增加。田冬等[7]研究表明,添加250 mg N/kg的外源氮显著提高了紫色耕作土壤净氮矿化量和净氮矿化速率。然而,罗亲普等[8]研究报道,低施用量[<10 g N/(m2·a)]条件下外源氮不影响草地土壤有机氮矿化,但施用高量外源氮[10、25 g N/(m2·a)]则显著提高了土壤无机氮含量。有研究指出,在0~80 mg N/kg施氮范围内,施氮抑制了农田土壤有机氮的矿化,使得净氮矿化速率为负值[9-10]。施用氮肥通常能增加土壤氨氧化古菌(AOA)和氨氧化细菌(AOB)的丰度和活性[11-12],使得净硝化速率随着施氮量的增加而显著增加,但是氮肥用量过多反而会抑制硝化作用的进行。王晓维等[6]研究发现,施用60 mg N/kg的氮肥显著增加了红壤净硝化速率,而当氮肥用量增加至120 mg N/kg时,土壤净硝化速率反而有所降低。佟得利和徐仁扣[13]的研究也表明,在0~150 mg N/kg施氮范围内,施氮量越大,土壤净硝化速率越高;但当施氮量进一步增加到200、300 mg N/kg时,土壤净硝化速率反而下降到与50 mg N/kg时相当。这可能是因为高施氮量会导致土壤微生物性状和生化功能减退,微生物活性下降,进而抑制硝化作用的进行[14]。由此可见,土壤中有机氮矿化作用和硝化作用对氮肥施用的响应可能因土壤类型和施氮水平而异,具体机制还需进行深入研究。
N2O是一种重要的温室气体,其在大气中滞留时间长,辐射潜力大,大气中的N2O能破坏平流层中的臭氧,增加地球的紫外线辐射强度,百年尺度上N2O的增温效应是CO2的310倍[15]。土壤通过硝化过程和反硝化过程排放N2O[16],据估计,农田土壤排放的N2O占大气中N2O总量的80%~90%[17]。研究表明,土壤排放的N2O主要来自反硝化过程[16]。然而中国旱作农田土壤资源丰富,铵态氮肥施用基数大,硝化过程对N2O排放的贡献也不容忽视[18-19]。研究表明,氮肥施用量对旱作农田土壤N2O排放的影响与土壤类型和施氮水平有关,两者间可能呈线性[20]、米氏[21]或指数函数关系[22]。此外,氮肥施用会影响土壤微生物活性,进而影响微生物控制的CO2排放过程[23]。因此,有必要针对土壤温室气体排放对不同施氮水平的响应开展深入研究。
目前,有关氮肥施用水平对土壤有机氮矿化和硝化过程的影响研究主要针对热带、亚热带森林土壤[24-25]和温带草原、农田土壤[6,8,22]开展,对于寒温带农田土壤氮转化过程对氮肥施用水平的响应研究鲜有报道。因此,本研究以寒温带农田土壤为对象,采用室内培养试验研究不同施氮水平下土壤净氮矿化速率、净硝化速率、温室气体排放的动态变化,以期深入理解东北黑土区农田生态系统的氮素转化规律,为黑土区旱地农田土壤的合理施肥及可持续发展提供科学指导。
1 材料与方法
1.1 土样采集
供试农田土壤采自黑龙江省哈尔滨市阿城区。采样区农田主要种植玉米,年均施氮量120 kg N/hm2。于玉米收获后多点采集表层土壤(0~20 cm),一部分新鲜土壤混匀过2 mm筛后用于室内培养试验,另将一部分土样风干后用于土壤理化性质的测定,具体为:土壤pH 5.98,田间持水量(WHC)为61.9%,有机碳和全氮含量分别为21.5、1.95 g/kg,C/N比为11.02,水溶性有机碳和水溶性有机氮含量分别为265、23.4 mg N/kg,铵态氮和硝态氮含量分别为4.23、16.8 mg N/kg,砂粒、粉粒、粘粒含量分别为16.8%、65.3%、17.9%。
1.2 培养方法
称取相当于30 g烘干土重的新鲜土样于60个250 mL三角瓶中,将三角瓶平均分为4组,每组15个。用移液管向其中3组三角瓶中加入2 mL(NH4)2SO4溶液,使添加氮浓度分别达到40、60、80 mg N/kg(N40、N60、N80),另外1组加入等量去离子水作为对照(N0),每个处理3个重复。用去离子水调节土壤水分含量至60%WHC,用扎有小孔的锡箔封口,然后将所有三角瓶置于恒温培养箱中25℃下黑暗培养7天。培养期间每天去除锡箔通气30 min,蒸发损失的水分通过称重法补足。分别在培养后的0、1、3、5、7天采集培养瓶上部空间气体,每次采气前将三角瓶用带取气孔的硅胶塞塞紧,用真空泵抽真空后注入空气,如此反复3次使得所有培养瓶内初始气体浓度与室内空气相同,将三角瓶密闭6 h后抽取20 mL气体至真空瓶中用于测定N2O和CO2气体浓度。取气完毕后,向三角瓶中加入2 mol/L KCl溶液(液土比为2.5:1),恒温震荡1 h后过滤,滤液用于测定铵态氮和硝态氮浓度。
1.3 分析方法
土壤pH用电位法测定(水土比为2.5:1);田间持水量(WHC)用漏斗法测定[26];土壤铵态氮和硝态氮用2 mol/L KCl溶液提取后利用流动分析仪测定;土壤有机碳和全氮用C/N元素分析仪测定(NA Series 2,CE Instruments,Italy);土壤水溶性有机碳和水溶性有机氮用水浸提后(液土比为5:1)用有机碳氮分析仪测定(Schimadzu Corp,Kyoto,Japan);土壤砂粒、粉粒和粘粒含量用比重计法测定;N2O和CO2气体浓度用岛津气相色谱仪测定(Shimadzu GC-14B,Japan)。
1.4 数据处理与分析
净氮矿化速率和净硝化速率计算方法如式(1)~(2)所示。

式中,m为净氮矿化速率[mg N/(kg·d)],n为净硝化速率[mg N/(kg·d)],t为培养时间,NH4+-N和NO3--N单位为mg N/kg。
N2O和CO2气体浓度计算方法如式(3)所示。

式中,F为气体平均排放速率[ng N2O-N/(kg·h),mg CO2-C/(kg·h)],ρ为标准状态下N2O和CO2的密度,dc/dt为单位时间内气体浓度增加量(×10-6/h或×10-9/h),V为培养瓶上部空间有效体积(mL),T为培养温度(℃),W为土壤干重(kg)。
气体累积排放量采用相邻2次取样气体排放速率平均值与时间乘积后加权计算得出,N2O排放比例(‰)为N2O平均排放速率与净硝化速率之比。
全文采用Excel软件作图,采用SPSS软件进行统计分析。采用单因素和Duncan法进行方差分析和多重比较(α=0.05)。
2 结果与分析
2.1 土壤无机氮含量
不同培养时间土壤铵态氮和硝态氮含量的动态变化如图1所示。各处理土壤铵态氮含量都随着培养时间的推进逐渐下降,N0、N40、N60和N80处理土壤铵态氮含量分别从0天时的3.28、43.5、62.9、84.7 mg N/kg下降到7天时的1.23、4.44、11.5、21.9 mg N/kg,各取样时间点不同处理土壤铵态氮含量均表现为N80>N60>N40>N0,不同处理间差异显著(P<0.05)(图1a)。整个培养期间,不施氮的N0处理土壤硝态氮含量(13.6~15.8 mg N/kg)没有显著变化,而各施氮处理土壤硝态氮含量随培养的进行逐渐增加。至培养结束,N40、N60和N80处理土壤硝态氮含量分别达到48.1、60.4、69.4 mg N/kg,各取样时间点不同处理土壤硝态氮含量均表现为N80>N60>N40>N0,不同处理间差异显著(P<0.05)(图1b)。
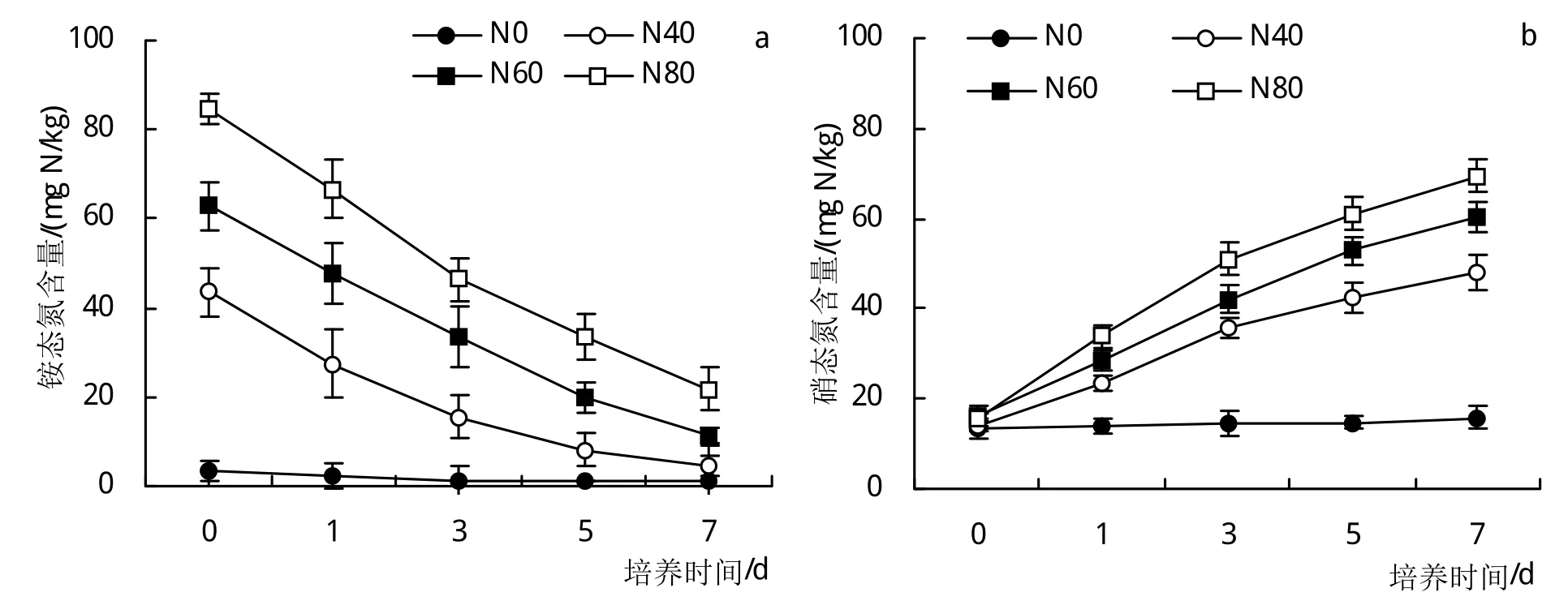
图1 不同施氮水平下土壤铵态氮和硝态氮含量的动态变化
2.2 净氮矿化速率和净硝化速率
施氮水平对于土壤有机氮矿化作用和硝化作用的影响十分显著(图2)。不施氮的N0处理土壤净氮矿化速率为0.03 mg N/(kg·d),土壤氮矿化量稍高于氮固定量,而3个施氮处理的土壤净氮矿化速率均为负值,表现为对氮的净固定。N40、N60和N80处理的土壤净氮矿化速率分别为-0.71、-1.01、-1.27 mg N/(kg·d),各处理之间差异显著(P<0.05)(图2a)。施氮显著促进了硝化作用的进行,不施氮的N0处理土壤净硝化速率为0.32 mg N/(kg·d),而N40、N60和N80处理的土壤净硝化速率分别为4.87、6.35、7.70 mg N/(kg·d),分别是N0处理的15.2、60.4、69.4倍(P<0.05)(图2b)。

图2 不同施氮水平下土壤净氮矿化速率和净硝化速率
2.2 土壤N2O排放
由图3可见,施氮水平显著影响土壤N2O排放。N0、N40和N80处理土壤N2O排放速率随培养的进行先增加后降低,N0处理的N2O排放峰值出现在培养后的第5天,N40和N80处理则在培养后的第3天就达到峰值(图3a)。与前述3个处理不同的是,N60处理的N2O排放速率在培养后的第1天就达到了峰值,随后缓慢下降至第3天后快速下降。培养期间,N0、N40、N60和N80处理的N2O平均排放速率分别为3.33、7.16、10.9、8.84 µg N2O-N/(kg·d),各处理不同取样时间点N2O排放速率表现为N60>N80>N40>N0。随着培养的进行,各处理N2O累积排放量显著增加。至培养结束,N0、N40、N60和N80处理的N2O累积排放量分别为23.3、50.1、76.1、61.9 μg N2O-N/kg(图3b),各处理间差异显著(P<0.05)。

图3 不同施氮水平下土壤N2O排放速率和累积排放量的动态变化
不施氮的N0处理N2O排放比例为8.11‰,施氮后N2O排放比例显著降低(P<0.05)(图4),N40、N60和N80处理的N2O排放比例分别为1.48‰、1.72‰和1.15‰,3个施氮水平之间没有显著差异(P>0.05)。
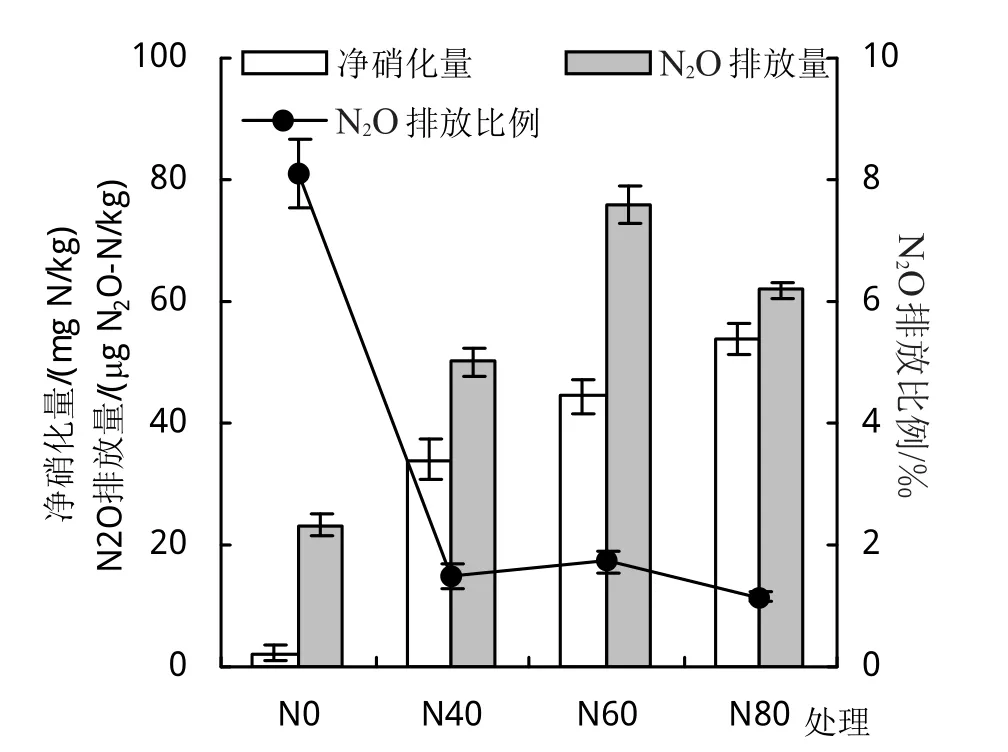
图4 不同施氮水平下土壤净硝化量、N2O排放量和N2O排放比例
2.3 土壤CO2排放
无论施氮与否,各处理土壤CO2排放速率均随着培养的进行逐渐下降,施氮显著抑制了CO2的排放(图5a)。整个培养期间N40、N60和N80处理土壤CO2平均排放速率分别为11.9、11.5、11.5 mgCO2-C/(kg·d),3个处理间没有显著差异(P>0.05),但均显著低于N0处理的13.7 mg CO2-C/(kg·d)(P<0.05)。培养期间,CO2累积排放量随着培养的推进显著增加(图5b),培养结束后N40、N60和N80处理的CO2累积排放量分别为83.2、80.3、80.7 mg CO2-C/kg,显著低于 N0处理的96.1 mg CO2-C/kg。

图5 不同施氮水平下土壤CO2排放速率和累积排放量的动态变化
3 结论
施氮水平对东北农田黑土氮素转化过程和温室气体排放具有显著影响。施氮显著抑制了农田土壤的有机氮矿化作用,土壤净氮矿化速率为负值且随施氮水平的增加而显著降低。施氮显著促进了农田土壤的硝化作用,净硝化速率随施氮水平的增加而显著增加。0~60 mg N/kg范围内土壤N2O排放量随施氮水平的增加而显著增加,当氮肥用量进一步增加到80 mg N/kg时,N2O排放量有所下降。施氮显著抑制了土壤CO2的排放,但施氮水平对CO2排放没有显著影响。本研究采用的是室内培养的试验方法,不能完全反映田间实际情况,后续还需开展原位田间试验加以验证。
4 讨论
4.1 净氮矿化速率
土壤有机氮的矿化是在微生物作用下将有机氮转化为铵态氮的过程,因此铵态氮肥的施用对有机氮矿化速率具有重要影响。研究表明,农田土壤施用一定量的氮肥能够促进土壤有机氮矿化,增加土壤净氮矿化量[9]。但当供氮水平过高时反而会抑制有机氮的矿化,甚至导致净氮矿化速率为负值,表现为对无机氮的净固定,这是因为在土壤内部存在一个控制有机氮矿化-固定的机制[27]。本研究中不施氮条件下土壤净氮矿化速率为正值,说明没有外源氮时土壤有机氮可以通过矿化释放出一部分无机氮,具备一定的基础供氮能力。而施用氮肥后土壤净氮矿化速率变为负值,且土壤净氮矿化速率随施氮水平的增加而显著降低,说明土壤中有机氮矿化作用不受氮素有效性的限制。李平等[10]也曾报道,农田土壤施用氮肥后导致净氮矿化速率显著降低,与本研究结果一致。一方面,施用外源氮肥影响了土壤中微生物的数量和活性,抑制了与含氮有机化合物分解有关的酶活性[4]。另一方面,化学氮肥的施用可能导致土壤有机质结构发生显著变化,不利于底物与酶的结合[28],进而导致胞外酶的代谢效率和分解速率降低[5],影响有机氮的矿化过程。
4.2 净硝化速率
硝化作用是在硝化微生物的作用下将铵态氮转化为硝态氮的过程,其过程速率受底物铵态氮浓度的影响。本研究结果显示,在没有外源氮肥的条件下土壤净硝化速率数值很低[0.32 mg/(kg·d)],而施用铵态氮肥后土壤净硝化速率随施氮水平的增加而显著增加,达到N0处理的15~23倍,表明土壤中硝化作用的强度受铵态氮底物浓度的限制。农业生产中氮肥的长期大量施用刺激了土壤中硝化微生物的活性,导致硝化速率受制于土壤中底物数量。很多已有的研究也表明,农田土壤施用氮肥后显著促进了硝化作用的进行,一定用量范围内土壤净硝化速率与施氮水平显著正相关[6,13-14]。研究发现,土壤硝化细菌丰度和群落多样性等微生物学性质的提高可能是施氮促进硝化作用的主要原因[12]。吕玉等[11]报道,农田土壤施用不同量氮肥后AOA的数量是不施氮处理的1.05~1.67倍,AOB的数量是不施氮处理的1.25~7.62倍,且2种硝化细菌丰度随施氮水平的增加显著增加,进而显著增加了土壤硝化势。Enwall等[29]的研究也表明,长期施用氮肥后农田土壤AOB丰度是不施氮处理的20倍,且土壤硝化速率显著提高。
4.3 N2O排放
土壤中N2O的排放主要来自硝化和反硝化过程,好气条件下硝化是N2O的主要排放途径,嫌气条件下反硝化是N2O的主要排放途径[30]。本研究中土壤含水量控制在60%WHC,培养期间处于好氧条件,N2O排放主要来自硝化过程。前人研究报道,土壤N2O排放量与施氮水平显著正相关[12,31],两者呈线性[20]或指数函数关系[22]。本研究结果显示,在0~60 mg N/kg的施氮范围内土壤N2O排放量随施氮水平的增加而增加,当施氮达到80 mg N/kg时,N2O排放量反而降低,山楠等[32]和马智勇等[33]均有类似报道。这说明适量施氮可以通过促进土壤硝化作用而促进N2O的排放,但是过高的氮肥用量反而会降低N2O排放。本研究中施氮水平为80 mg N/kg时土壤净硝化速率相对60 mg N/kg时显著增加,其显著下降的N2O排放量可能与N2O在土壤中的扩散受阻有关。马智勇等[34]报道,高施氮水平易导致土壤表面板结,抑制土壤中气体的扩散与传输,促使N2O在局部厌氧微区进行还原转化为N2,从而降低土壤N2O排放量,但具体机制还需进行深入研究。
研究指出,好氧条件下农田土壤硝化过程排放的N2O比例通常在0.02%~0.2%之间[35-37],一般都小于0.1%。但也有研究报道,硝化过程排放的N2O比例较高,介于0.16%~2.32%之间[30,38-39],这与本研究结果一致(图4)。与不施氮处理相比,施用氮肥后土壤净硝化量和N2O排放量都显著增加,但N2O排放比例却显著降低,说明氮肥施用对净硝化量和N2O排放量的促进程度并不成比例。此外,3个施氮水平处理的N2O排放比例没有显著差异,说明施氮后N2O排放比例相对稳定,不受氮肥用量影响。由于N2O排放量与净硝化量之间具有一定的相关性,因此N2O排放比例是使用计算机模型在大尺度范围内估算N2O排放清单的重要参数,但不同模型中该参数的设定值有所不同。目前广泛使用的CENTURY模型中假定N2O的排放比例为2%[30],而在Expert-N 模型[40]和 PnET-Ndc模型[41]中,这一比例分别设定为0.5%和0.06%。不同模型中N2O排放比例设定值的差异可能与模型适用的区域、土壤类型、植被类型、施肥等因素有关,本研究结果可为黑土旱地农田土壤N2O排放的估测提供科学依据。
4.4 CO2排放
实验室培养条件下,土壤中CO2的排放主要来自微生物呼吸,因此CO2排放量的高低可以代表土壤微生物活性的强弱[23]。土壤有机碳是微生物呼吸的基质,尤其是易分解有效碳的含量对CO2排放具有直接影响[42]。土壤中有机碳大部分是以腐殖质形态存在,而腐殖质通常与矿物质胶结成团聚状态形成稳定的有机质矿物质复合胶体,属于惰性有机碳,水溶性易分解有效碳的数量通常很低。本研究中CO2排放速率随培养的进行不断下降,说明易分解有效碳逐渐被消耗,呼吸强度减弱;3个施氮处理的CO2排放量显著低于不施氮处理,说明施氮抑制了土壤微生物的活性。有研究指出,大量施用硫酸铵改变了土壤碳氮比,导致局部铵离子浓度过高,土壤pH下降[7],从而降低了微生物的整体活性和对单一碳源底物的利用能力[43],土壤微生物生物量碳、多样性和丰富度也显著降低,微生物群落结构发生显著变化[14],进而影响微生物呼吸。栗方亮等[14]的研究表明,当硫酸铵施用水平大于120 mg N/kg时就可能造成红壤微生物性状和呼吸功能的衰减。本研究中硫酸铵施用水平为40 mg N/kg时土壤微生物呼吸量就显著降低,这可能与不同土壤微生物活性对外源氮肥施用量的反应不同有关。氮肥施用显著促进了土壤硝化作用的进行,硝化作用的快速发生消耗了土壤中的氧气,导致局部微域孔隙氧气含量减少[44],进而抑制土壤微生物呼吸。此外,过量施氮会改变土壤有机质形态,不利于微生物分解,利用效率降低也可能是导致土壤CO2排放量降低的原因之一[28]。

