Ni基双金属催化剂的制备及其加氢脱氧反应性能
鲁玉莹,王宗宝,肖海成,徐 华,张 鹏,吕 雉
(中国石油石油化工研究院,北京 102206)
费-托合成技术是以净化后的合成气(主要含H2和CO)为原料,在催化剂和一定的温度、压力等条件下合成各种有机化合物的工艺技术[1-2]。根据反应温度不同,分为高温费-托合成和低温费-托合成两类。低温费-托合成产物以长链正构烷烃为主,且不含硫、氮等杂质,是生产各类高端、环保的钻井液基础油和润滑油基础油等的优质原料。但是费-托合成油中含有一定量的含氧化合物,含氧化合物的存在会影响后续加工过程和最终产品质量,需要进行加工处理[3]。
费-托合成油中的含氧化合物主要是醇、醛、羧酸等[4],Ni基非贵金属催化剂是常用的加氢脱氧催化剂。加氢脱氧反应过程一般需要两种活性位,其中一种用于氢气的活化(如Pt、Ni 等[5-7]),另一种需要具有可变价态的金属位,用于活化含氧化合物中的含氧基团[8],研究认为相比单金属催化剂,双金属催化剂的加氢脱氧活性更高。目前针对费-托合成油的非硫化态加氢脱氧催化剂的研究较少,助剂的类型及助剂影响Ni基催化剂加氢脱氧性能方面的研究更少[9-10]。本研究以非贵金属Ni为活性组分,考察具有可变价态的助剂金属Mo,Co,Ce对催化剂晶态结构以及表面物性的影响,并以正丁醇为模型化合物,考察不同助剂金属催化剂对模型化合物加氢脱氧反应性能的影响。
1 实 验
1.1 原 料
拟薄水铝石,工业级,山西炬华铝业有限公司产品;田菁粉,工业级,江苏省灌南县宏图植物胶厂产品;硝酸(HNO3质量分数65.0%~68.0%)、磷酸(H3PO4质量分数不小于85.0%)、六水合硝酸镍[Ni(NO3)2·6H2O]、四水合钼酸铵[(NH4)6Mo7O24·4H2O]、六水合硝酸钴[Co(NO3)3·6H2O]、六水合硝酸铈[Ce(NO3)3·6H2O]、正丁醇(C4H10O)、正庚烷(C7H16),均为分析纯,国药集团化学试剂有限公司产品。
1.2 催化剂的制备
称取一定量的拟薄水铝石,加入田菁粉、硝酸、磷酸和去离子水,经混捏、挤条成型后,110 ℃干燥4 h、550 ℃焙烧4 h,得到含2%(w)磷酸改性的γ-Al2O3载体。
采用等体积浸渍法制备催化剂。将催化剂活性组分和助剂组分硝酸盐或相应的盐类配制成一定浓度的水溶液,等体积浸渍到经过磷酸改性的γ-Al2O3载体上。浸渍后的催化剂于110 ℃烘干,然后在马弗炉中450 ℃焙烧4 h,得到一系列负载型Ni基双金属催化剂。其中NiO质量分数为16%(相对于载体),助剂组分按照Ni/M(M=Mo,Co,Ce)原子比为8添加。
1.3 催化剂的表征
采用荷兰帕纳科公司生产的X’Pert PRO X射线粉末衍射仪进行物相测定(XRD),Cu Kα射线为辐射源,Ni滤光片,管电压45 kV,管电流40 mA,扫描范围2θ为5°~85°。
采用美国Micromeritics公司生产的ASAP 2020 Plus物理吸附仪测定孔结构,用BJH公式计算孔径分布,用BET公式计算孔体积和比表面积。
采用美国Micromeritics公司生产的AutoChem 2920型全自动程序升温化学吸附仪测定载体和催化剂的表面酸性(NH3-TPD)。称取20 mg样品置于石英反应管中,先通入高纯He并升温至500 ℃,恒温吹扫60 min,然后降温至100 ℃,吸附NH3至饱和后,以10 ℃/min的速率从100 ℃升温到800 ℃脱附,TCD在线检测尾气组成。
采用美国Micromeritics公司生产的AutoChem 2920 型全自动程序升温化学吸附仪测定催化剂的还原性能(H2-TPR)。称取10 mg样品置于石英反应管中,先通入高纯Ar在400 ℃下预处理30 min,随后冷却至室温,切换H2体积分数10% 的H2/Ar混合气,待色谱基线稳定后,以10 ℃/min的速率从100 ℃升温至900 ℃,TCD在线检测尾气组成。
采用Thermo Scientific公司生产的 ESCALab250型X射线光电子能谱仪进行催化剂的X射线光电子能谱(XPS)表征。激发源为单色化Al Kα X射线,能量为1 486.6 eV,功率为150 W。窄扫描所用通透能为30 eV。分析时的基础真空约为6.5×10-8Pa。结合能用烷基碳或污染碳的C 1s峰(284.8 eV)校正。
1.4 催化剂性能评价
采用固定床微型反应装置对催化剂活性进行评价。催化剂装填量为10 mL,进料前先在H2气氛下420 ℃还原6 h,然后降温至170 ℃进料,反应原料为含15%(w)模型化合物正丁醇的正庚烷溶液,此外在反应原料中添加与正丁醇相同质量的正辛烷作为色谱分析的内标物。进料后稳定24 h取离线样,此后每隔12 h取样并升温10 ℃,反应温度170~210 ℃,压力4 MPa,液时空速1 h-1,氢油体积比400。采用Agilent 7890B气相色谱仪对收集的液相产物进行分析,配置HP-PONA毛细管柱(50 m×0.2 mm×0.5 μm),氢火焰离子化检测器(FID)。
考虑到反应为临氢反应且反应产物里有气体,为避免反应结束后气液分离过程中气体夹带液体造成液相组分损失,因此在计算液体中含氧化合物的转化率时,引入内标物正辛烷采用内标法计算。反应以正丁醇转化率和产物选择性作为催化剂性能评价指标,二者均以物质的量为基准进行计算。
2 结果与讨论
2.1 载体和催化剂的表征
2.1.1晶相分析
图1为载体和不同助剂金属催化剂的XRD图谱。由图1可知:载体在2θ为36.93°,46.06°,66.56°处出现了Al2O3的特征衍射峰(PDF#028260);与载体相比,催化剂的衍射峰强度明显减弱且宽化,表明加入的助剂金属与氧化铝载体产生了相互作用;所有催化剂均未检测到NiO的衍射峰,表明载体表面的NiO呈高度分散状态且未呈晶型[11]。

图1 载体和不同助剂金属催化剂的XRD图谱
2.1.2结构性能
图2为载体和不同助剂金属催化剂的低温N2吸附-脱附等温线。由图2可知,载体和催化剂的N2吸附-脱附等温线均为Ⅳ型等温线,而且不同助剂金属催化剂的N2吸附-脱附等温线无明显差别,这主要是由于助剂金属添加量较低,对催化剂的孔道结构影响较小。表1列出了载体和含不同金属助剂催化剂的孔结构参数。由表1可知,相比氧化铝载体,浸渍活性组分和助剂金属后,催化剂的比表面积、孔体积和平均孔径均有不同程度降低,但添加助剂金属对表面结构影响不大。

图2 载体和不同助剂金属催化剂的N2吸附-脱附等温线 —载体; —Ni/Al2O3; —NiMo/Al2O3; —NiCo/Al2O3; —NiCe/Al2O3。图3同
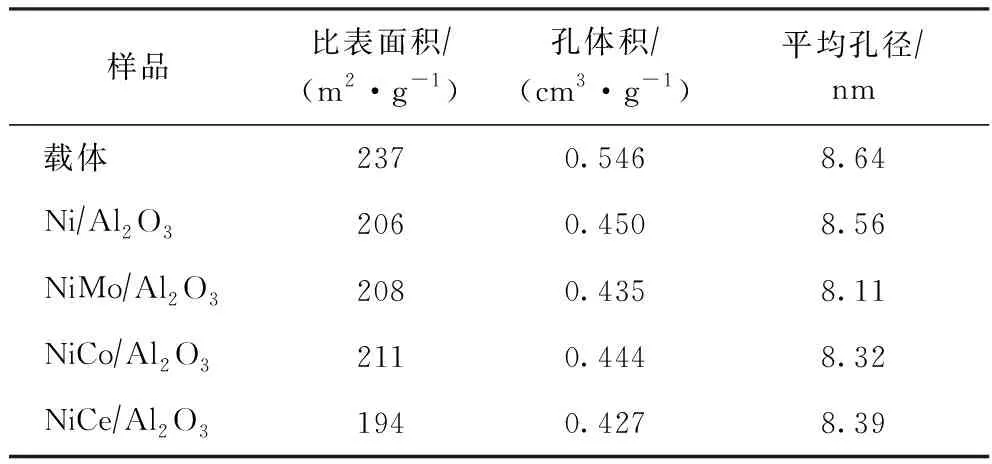
表1 载体和不同助剂金属催化剂的孔结构参数
2.1.3表面酸性
催化剂的酸性和酸量对其加氢脱氧性能有一定的影响。研究表明,酸量的增加有助于C—O键的活化[12-14]。图3为不同助剂金属催化剂的NH3-TPD曲线。由图3可知,所有样品均具有低温(200~350 ℃)和高温(600 ℃)两个NH3脱附峰。其中低温脱附峰对应弱酸中心,高温脱附峰对应强酸中心。由NH3-TPD曲线对比可以看出,活性组分和助剂金属的添加显著增加了催化剂的弱酸量,强酸量略有减少,但不同助剂金属的添加对NH3-TPD曲线影响不大,说明助剂的添加对催化剂表面酸量分布没有显著影响。
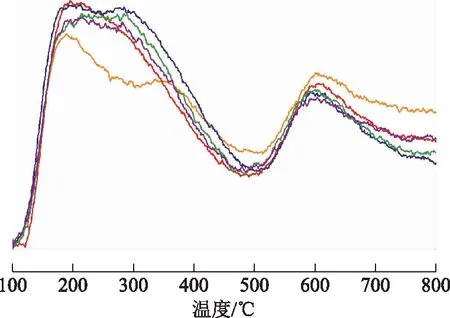
图3 载体和不同助剂金属催化剂的NH3-TPD曲线
2.1.4还原性能
图4为不同助剂金属催化剂的H2-TPR曲线。由图4可知:单金属Ni/Al2O3催化剂仅在580 ℃附近有一个还原峰,该峰归属于与载体表面具有一定强度相互作用力且分散良好的NiO的还原峰[15-16];添加助剂后,NiMo/Al2O3,NiCo/Al2O3,NiCe/Al2O3催化剂的还原峰均向低温方向移动,峰位分别为509,525,529 ℃,说明助剂金属的添加显著降低了NiO的还原温度,其中以Mo助剂的影响最大。结合XRD表征结果可知,还原峰温度向低温方向偏移主要是由于助剂金属的添加降低了NiO与氧化铝载体之间的相互作用。
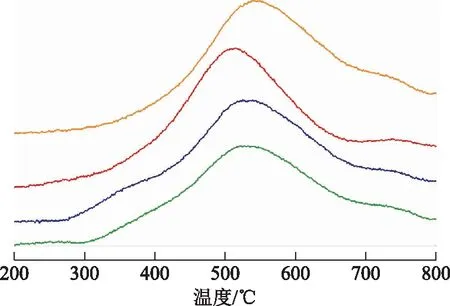
图4 不同助剂金属催化剂的H2-TPR曲线 —Ni/Al2O3; —NiMo/Al2O3; —NiCo/Al2O3; —NiCe/Al2O3
2.1.5XPS表征
表2为催化剂的XPS表征结果。由表2可知:相比Ni/Al2O3催化剂,NiCe/Al2O3催化剂的Ni 2P3/2结合能降低,表明有电子从助剂Ce转移到Ni,提高了催化剂表面Ni的电子云密度,有助于提高Ni对H2的吸附能力[17];同时,NiCe/Al2O3催化剂表面Ni原子含量以及表面Ni/Al原子比也是最高的;NiMo/Al2O3催化剂的Ni 2P3/2结合能比Ni/Al2O3催化剂的高,且在几种催化剂中是最高的,表明金属Mo的电负性较高,使得电子从金属Ni转移到金属Mo。
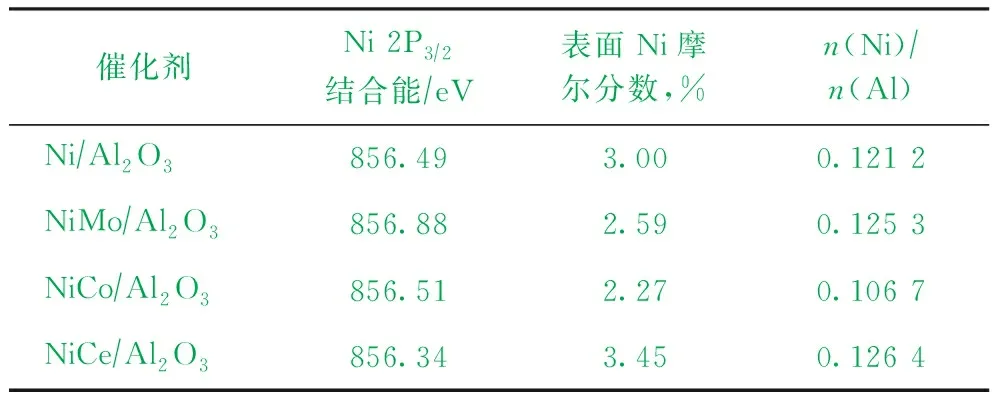
表2 不同金属助剂催化剂的XPS分析结果
2.2 催化剂加氢脱氧反应性能
在温度为170~210 ℃、压力为4 MPa、体积空速为1 h-1、氢油体积比为400的反应条件下,以含正丁醇质量分数15%的正庚烷溶液为原料,考察含不同助剂金属催化剂在不同反应温度下催化正丁醇加氢脱氧反应的性能,结果见图5。由图5可知,温度对不同催化剂加氢脱氧活性的影响规律是一致的,随着反应温度升高,正丁醇转化率均呈逐渐上升趋势。在相同反应温度、不同催化剂作用下的正丁醇转化率由高到低的顺序为:NiCe/Al2O3>Ni/Al2O3≈NiCo/Al2O3>NiMo/Al2O3,说明助剂金属Ce对Ni基催化剂加氢脱氧活性的促进作用显著。在210 ℃时正丁醇转化率接近100%,基本实现完全转化,这可能与NiCe/Al2O3催化剂表面Ni原子含量相对较高有关。

图5 不同助剂金属催化剂上正丁醇加氢脱氧反应性能■—Ni/Al2O3; ●—NiMo/Al2O3; ▲—NiCo/Al2O3;
正丁醇的加氢脱氧反应过程主要有2种方式:一种是C—O键断裂,生成正丁烷;另一种是C—C键断裂,生成丙烷。图6为不同助剂金属催化剂催化正丁醇加氢脱氧反应的产物丙烷选择性。由图6可知,不同Ni基催化剂对产物丙烷的选择性因正丁醇转化率的不同而略有差异,随着反应温度升高,产物选择性均呈现先增加后降低的趋势。初步推测:虽然随着反应温度升高,含氧化合物转化率的提高会使丙烷的含量增加,但是高温下丙烷在液相中的溶解量会降低,因此液相产物中检测到的丙烷量出现先增加后降低的现象。

图6 不同助剂金属催化剂催化正丁醇加氢脱氧反应的产物丙烷选择性■—Ni/Al2O3; ■—NiMo/Al2O3; ■—NiCo/Al2O3; ■—NiCe/Al2O3。图7同
图7为不同助剂金属催化剂催化正丁醇加氢脱氧反应的产物正丁烷选择性。由图7可知,添加Mo助剂的催化剂在不同反应温度下对正丁烷的选择性(18%~30%)明显高于其他催化剂(<0.5%)。这可能主要是由于金属Mo的亲电性较高,电负性高(XPS表征结果),因此对C—O键的活化和断裂能力强,所以脱氧产物中正丁烷的选择性较高[18],也有研究表明助剂金属Mo的氧化物在还原过程中生成不同价态的钼物种(Mo5+、Mo4+等),这些钼物种由于氧配位不饱和而吸附O原子上的孤对电子,促进C—O键的断裂[19]。此外有研究表明,Mo助剂能增强催化剂对C—O键的活化和断裂能力,在以乙酸为模型化合物的加氢脱氧反应中,因C—O键的断裂而对产物乙烷的选择性较高[9]。
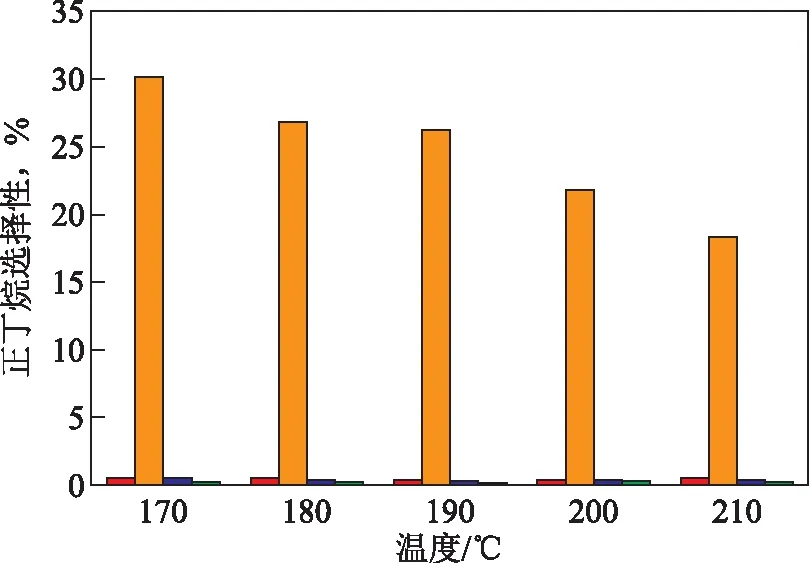
图7 不同助剂金属催化剂催化正丁醇加氢脱氧反应的产物正丁烷选择性
3 结 论
(1)采用等体积浸渍法制备了一系列负载于γ-Al2O3上的Ni基非贵金属催化剂。助剂金属的添加可显著降低催化剂的还原温度,减弱NiO与载体间的相互作用。金属活性组分的添加可调变载体酸性,主要使催化剂的弱酸量增加,强酸量减少。
(2)助剂金属Ce对Ni基催化剂加氢脱氧活性的促进作用显著,在210 ℃时基本实现正丁醇的完全转化,反应产物主要是丙烷;而助剂金属Mo因原子的电负性较高,对C—O键的活化和断裂能力强,因此对产物正丁烷的选择性明显高于其他助剂催化剂。

