PD-1抑制剂联合TACE治疗中晚期肝癌的临床研究*
江健 梁小芳 易清平 李丽华 尹卫华 邱美青
原发性肝癌是一种恶性肿瘤,在我国较为常见,现阶段,以肝动脉化疗栓塞术(TACE)为基础的联合治疗是临床治疗中晚期肝癌的主要方法。近年来,肝癌治疗中程序性死亡受体1(PD-1)抑制剂取得了重大进展,但单药治疗并不能使多数患者受益,因此免疫联合治疗势在必行。TACE 能够诱导大量肿瘤细胞,使其死亡,释放肿瘤抗原,从而启动机体免疫应答,为TACE 联合免疫治疗提供理论基础,现阶段,大部分该方面的研究仍然处于早期探索阶段,需要获取更多的数据支持[1]。本研究旨在通过对比应用分子靶向药物联合TACE,观察PD-1 抑制剂联合TACE 在中晚期肝癌患者中的疗效,为部分中晚期肝癌患者提供新的、可靠且安全的治疗方法。
1 资料与方法
1.1 一般资料 依据巴塞罗那(BCLC)肝癌临床分期标准,选取2021 年1-12 月宜春市人民医院收治的46 例原发性肝癌BCLC B 期和C 期患者。纳入标准:(1)经临床标准诊断为原发性肝癌[2];(2)无法手术或拒绝外科手术;(3)未进行干预性治疗,预计生存时间大于3 个月。排除标准:(1)ECOG体力状况评分>2 分;(2)存在严重高血压、糖尿病、肝肾疾病;(3)其他恶性肿瘤;(4)既往精神病史。依据治疗方法将患者分为试验组(卡瑞利珠单抗联合TACE)和对照组(阿帕替尼联合TACE),各23 例。本研究通过本院伦理委员会批准,患者均知情同意。
1.2 方法
1.2.1 对照组 TACE 术前开始给予甲磺酸阿帕替尼片(生产厂家:江苏恒瑞医药股份有限公司,批准文号:国药准字H20140103,规格:0.25 g)治疗,初始剂量为500 mg/d,餐后服用,1 次/d,依据受试者的不良反应进行调整,如不能耐受,将剂量调整为250 mg/d。TACE 治疗:均采用Seldinger技术经皮穿刺股动脉,对患者进行动脉造影检查,了解肿瘤部位、大小、门静脉异位血栓、血供情况,选择性将导管送至肿瘤供血之靶血管后,经导管将40 mg 洛铂(生产厂家:海南长安国际制药有限公司,批准文号:国药准字H20050308,规格:50 mg)+40 mg 吡柔比星(生产厂家:深圳万乐药业有限公司,批准文号:国药准字H10930105,规格:10 mg)注入,依据患者个体情况确定化疗药物剂量,然后依据肿瘤大小、血供注入碘化油化疗药乳剂,依据患者情况决定再次TACE 治疗的必要性,通常间隔1 个月及以上。4 周为1 个周期,共治疗1~2 个周期。
1.2.2 试验组 TACE 术前应用注射卡瑞利珠单抗(生产厂家:苏州盛迪亚生物医药有限公司,批准文号:国药准字S20190027,规格:200 mg),用法:每2 周1 次,200 mg/次。TACE 治疗方法同对照组。4 周为1 个疗程,共治疗2 个疗程。所有患者每月复查,检查内容包括血常规、肝功能、白蛋白、凝血功能、甲胎蛋白(AFP)、血肌酐和尿素氮、上腹部增强CT。
1.3 观察指标及判定标准 (1)比较两组疗效。完全缓解(CR):所有靶病灶动脉期强化消失;部分缓解(PR):所有目标病灶的长径总和减少≥30%;疾病稳定(SD):变化介于PR 和疾病进展(PD)之间;PD:所有目标病灶的长径总和增加≥20%,并且长径总和增加的绝对值≥5 mm,或出现新的病灶。疾病控制(DCR)=CR+PR+SD,客观缓解(ORR)=CR+PR[3]。(2)比较两组不良反应。采用美国国家癌症研究所常见毒性标准(NCI-CTC v4.0):感觉不舒服但没有对每天正常活动造成不良影响评定为Ⅰ度(轻微);感觉不舒服对每天正常活动造成不良影响评定为Ⅱ度(中);无法正常活动或工作评定为Ⅲ度(严重);致残或致死评定为Ⅳ度(致命)[4]。(3)比较两组生活质量。采用卡氏(Karnofsky,KPS)功能状态评分评估,总分0~100 分,评分越高生活质量越好[5]。(4)比较两组满意度。采用问卷调查,分为不满意、较满意、很满意。满意度=很满意+较满意。
1.4 统计学处理 采用SPSS 21.0,计量资料用()表示,组间比较采用独立样本t 检验,组内比较采用配对t 检验;计数资料以率(%)表示,比较采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组一般资料比较 试验组年龄29~83 岁,平均(56.68±9.14)岁;女2 例,男21 例;肿瘤最大直径:<5 cm 7 例,≥5 cm 16 例;BCLC 分期:B期10 例,C 期13 例;肝功能分级:A 级20 例,B级2 例,C 级1 例;肝病史:乙肝20 例,丙肝1 例,酒精性及其他2 例;肝外转移:有13 例,无10 例。对照组年龄30~84 岁,平均(57.42±9.36)岁;女3 例,男20 例;肿瘤最大直径:<5 cm 8 例,≥5 cm 15 例;BCLC 分期:B 期11 例,C 期12 例;肝功能分级:A 级21 例,B 级1 例,C 级1 例;肝病史:乙肝19 例,丙肝2 例,酒精性及其他2 例;肝外转移:有12 例,无11 例。两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组临床疗效比较 试验组ORR 高于对照组,差异有统计学意义(χ2=5.576,P<0.05)。两组DCR 比较,差异无统计学意义(χ2=2.681,P>0.05),见表1。

表1 两组临床疗效比较[例(%)]
2.3 两组不良反应发生情况比较 两组发热、皮疹、腹泻、乏力、甲减、高血压、声音嘶哑、消化道出血、免疫性肺炎、手足皮肤反应发生率比较,差异均无统计学意义(P>0.05),见表2。
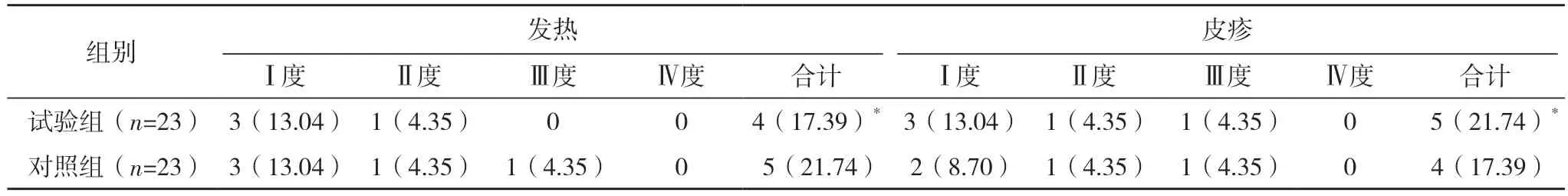
表2 两组不良反应发生情况比较[例(%)]

表2(续)

表2(续)
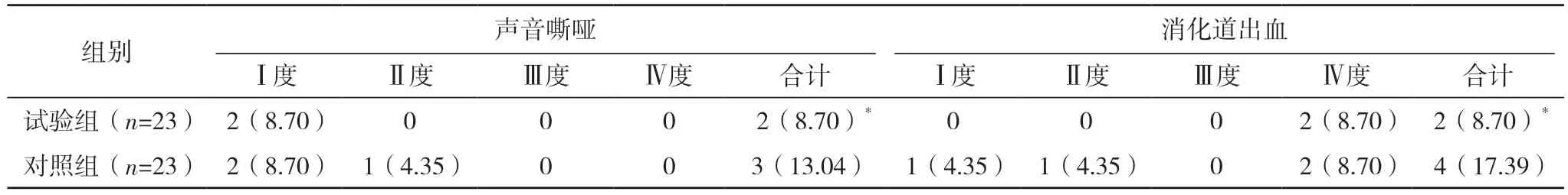
表2(续)

表2(续)
2.4 两组生活质量比较 治疗前,两组KPS 评分比较,差异无统计学意义(P>0.05);治疗后,两组KPS 评分均高于治疗前,且试验组高于对照组(P<0.05),见表3。
表3 两组生活质量比较[分,()]
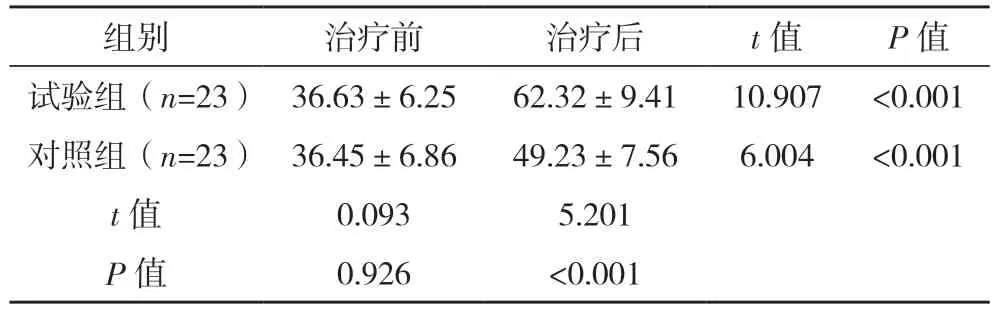
表3 两组生活质量比较[分,()]
2.5 两组满意度比较 试验组满意度为95.65%,高于对照组的65.22%,差异有统计学意义(χ2=4.973,P<0.05),见表4。

表4 两组满意度比较[例(%)]
3 讨论
原发性肝癌是一种恶性肿瘤,在我国较为常见,大部分患者在确诊时已经处于中晚期,丧失外科手术最佳时机,由于其血供主要为动脉,较为丰富,因此现阶段,在大部分中晚期原发性肝癌患者的治疗中,肝动脉栓塞化疗是首选方法。但是,晚期肝癌具有较大的肿瘤负荷,同时侵犯血管,因此放射性粒子植入、血管性介入治疗等均具有有限的局部治疗效果,具有很高的复发率及局部灭活不全的缺陷,肝内外转移常见。目前多个分子靶向药物应用于肝癌的治疗中,索拉非尼已被多个临床研究证实有效,其具有多靶点抗肿瘤活性,从而抑制肿瘤组织新血管生成,在全球范围内,在分子靶向药物中,索拉非尼被批准用于肝癌的治疗。有研究前瞻性分析了介入疗法联合索拉非尼治疗能够减少血管生成,提升介入治疗的效果,并改善肝癌患者的长期预后[6]。阿帕替尼是一种多靶点抗肿瘤药物,由我国自由研发,通过高度选择性竞争血管内皮生长因子(VEGFR-2)及其受体结合位点阻断下游信号传导,抑制肿瘤新生血管生成。有研究证实,在中晚期肝癌治疗中阿帕替尼联合TACE 具有较好的近期疗效,与TACE 联合索拉非尼临床疗效基本等同[7]。
近年来,医学界日益深入认识了肝脏肿瘤免疫微环境,在肝癌治疗领域,肝癌免疫治疗成为新趋势、新热点。免疫检查点抑制剂(ICI)治疗不可切除性肝癌近年来受到国内外研究者的充分重视,并取得重大进展。早期研究发现,与PD-L1 低表达患者相比,PD-L1 高表达患者具有较差的预后,提示在肿瘤复发预测中,PD-L1 能够作为预测因子,而PD-1/PD-L1 通路可能反映治疗靶点[8]。有研究进行了多项ICI 临床试验,发现在晚期肝癌领域,PD-1/PD-L1 抑制剂单药治疗的ORR 为10%~20%,同时具有较高的可靠性与安全性,可见单药治疗有效率不高,广大学者开始了免疫联合疗法的研究,但针对不同分期的肝癌,联合免疫最佳的方案仍需进一步探索[9]。因此,TACE 联合免疫疗法具有理论基础,能够提升肝癌治疗效果,具有极为重要的临床意义。目前,肝癌免疫疗法联合TACE 治疗仍然处于早期探索阶段。近年来,有研究表明,采用TACE 联合另一种免疫检查点CTLA4 抑制剂治疗能够发挥协同抗肿瘤作用[10]。另有临床试验评价TACE 或消融联合Tremelimumab 治疗肝癌的临床试验(NCT01853618)[11]。这些研究结果值得期待,也需更多的临床试验研究进一步佐证。
近年来,临床不断加深了解肝癌免疫逃逸中免疫检查点分子的作用,有很多研究均通过阻断这些抑制性受体获取了一系列理想的效果,基于此,肝癌治疗现状在不断创新的组合疗法作用下不断改变[12-14]。介入疗法在中晚期肝癌治疗中起着不可或缺的作用,因此,目前临床正在积极探索介入治疗联合免疫是否能够进一步提升晚期肝癌疗效[15-17]。介入疗法联合免疫检查点抑制剂治疗就有较大的潜力,能够提供新的治疗理念与方法以供参考[18-20]。本研究旨证实PD-1 抑制剂联合TACE 是一种治疗中晚期肝癌有效、可靠且安全的方案,为临床治疗提供新思路、新方法。结果表明,试验组ORR 高于对照组(P<0.05)。两组发热、皮疹、腹泻、乏力、甲减、高血压、声音嘶哑、消化道出血、免疫性肺炎、手足皮肤反应发生率比较,差异均无统计学意义(P>0.05)。治疗后,试验组KPS 评分高于对照组,试验组满意度高于对照组(P<0.05)。说明免疫联合TACE 能提高中晚期肝癌治疗效果,改善生存质量,为肝癌的治疗提供有效方案,使部分中晚期肝癌患者从中获益。本研究提供中晚期肝癌治疗的有效手段,免疫治疗及TACE 一般无严重不良反应,可缩短患者住院时间,降低患者因肿瘤控制不佳需多次住院的可能性。在保证疗效的同时,避免了多种治疗盲目联合应用,减轻了患者的经济压力,且减少了药物的副反应。通过实施本项目将促进提升本院肝癌的治疗水平,改善患者的预后,从而赢得患者及其家属的信任。
综上所述,对于中晚期肝癌,卡瑞利珠单抗联合TACE 治疗的临床效果较阿帕替尼联合TACE 治疗效果好,值得推广。

