恒温扩增荧光检测法检测结核分枝杆菌复合群的应用价值
李静 吴哲渊 杨景卉 杨丽媛 王莉莉 袁锋 沈鑫 江渊
如何在新型冠状病毒肺炎大流行的背景下做好结核病防控工作,世界卫生组织(World Health Organization, WHO)提出了一系列的建议[1],其中包括如何提高实验室病原学阳性率和快速检测能力。传统的痰涂片镜检法检测敏感度较低,培养法虽然敏感度较高但其检测时间长且需要进一步鉴定区分结核分枝杆菌复合群(Mycobacteriumtuberculosiscomplex,MTBC)和非结核分枝杆菌(nontuberculous mycobacteria,NTM),两种方法均无法满足临床早期发现和诊断结核病的需求。近年来,越来越多的以核酸扩增为基础诊断结核病的检测技术被WHO推荐[2]。恒温扩增荧光检测法是一种新型的核酸恒温扩增技术,不依赖温度循环变化,只需恒定温度就能扩增反应。其操作简便,耗时短,可直接检测临床样本中的MTBC。本研究选择上海市6家结核病定点医院为研究现场,收集疑似肺结核患者痰样本进行恒温扩增荧光检测法与传统的痰涂片、BACTEC MGIT 960 液体培养(简称“液体培养”)及GeneXpert MTB/RIF(简称“GeneXpert”)检测。以液体培养为参照标准,比较恒温扩增荧光检测法与痰涂片及GeneXpert的检测效能,评价恒温扩增荧光检测法检测痰样本中MTBC的临床应用价值。
对象和方法
一、研究对象
选择上海市6家结核病定点医院(上海市肺科医院、上海市松江区中心医院、上海市闵行区中心医院、上海市普陀区中心医院、上海市嘉定区中心医院、中国人民解放军905医院)作为研究现场,连续纳入2020年1月至2020年11月各家医院肺科门诊初诊的疑似肺结核患者。共纳入和收集2014例疑似肺结核患者痰样本,对收集到的痰样本进行痰涂片、液体培养、恒温扩增荧光检测法和GeneXpert四种方法检测。去除59例重复样本、43例无明确临床诊断者、64例培养污染等无效结果,最终1848例患者纳入研究。本研究通过上海市疾病预防控制中心伦理委员会审核批准(伦理号:2020-12 快速高通量分子诊断技术在上海示范区的验证推广研究)。
二、纳入和排除标准
1.纳入标准:(1)按照《WS 288—2017 肺结核诊断》[3]及《中国结核病防治规划实施工作指南(2008年版)》[4]中规定的咳嗽、咳痰≥2周,或痰中带血或咯血等的肺结核疑似症状者;(2)同意留取痰标本进行检测,且留取的痰标本量不少于3.0 ml者。
2.排除标准:(1)不同意参加本研究项目者;(2)未同时进行4种方法检测者;(3)检测期间,任一方法未获得有效检测结果者。
三、仪器与试剂
BACTEC MGIT 960 全自动分枝杆菌培养检测仪、MGIT 7 ml培养管和分枝杆菌培养添加试剂盒均购自于美国BD公司;GeneXpert MTB/RIF仪器及检测试剂盒均购自美国Cepheid公司;抗酸染色试剂购自珠海贝索生物技术有限公司;结核分枝杆菌MPT64抗原购自韩国Standard Diagnostics公司;Deaou-308C 恒温荧光检测仪和MTBC核酸检测试剂盒购自广州迪澳生物科技有限公司。以上试剂均由上海市疾病预防控制中心统一招标采购发放至6个研究现场。
四、方法
1.标本采集:按照《结核病实验室检验规程》[5]要求收集痰样本,每例患者收集3份痰样本(即时痰、夜间痰、晨痰),混匀后分别进行痰涂片、液体培养、GeneXpert检测、恒温扩增荧光法检测。
2.痰涂片:按照《痰涂片镜检标准化操作及质量保证手册》[6]中的标准操作程序执行,采用直接涂片法。5家结核病定点医院(上海市松江区中心医院、上海市闵行区中心医院、上海市普陀区中心医院、上海市嘉定区中心医院、中国人民解放军905医院)采用萋-尼抗酸染色;上海市肺科医院采用荧光抗酸染色。
3.液体培养:采用N-乙酰-L-半胱氨酸-NaOH法进行痰样本前处理,按照《结核病实验室检验规程》[5]进行操作。培养42 d仪器未报阳,报告液体培养阴性;对仪器报阳的培养物经涂片抗酸染色确认后,采用结核分枝杆菌抗原MPT64检测(胶体金法)进行MTBC和NTM初步鉴定。排除初步鉴定为阴性且临床诊断为非肺结核者;对于初步鉴定为阴性且临床诊断为肺结核者,进一步采用16S rRNA 测序方法进行菌种鉴定。
4.GeneXpert检测:按照操作说明书上的步骤进行,通过专用软件判读结果。
5.恒温扩增荧光检测法:采用广州迪澳生物科技有限公司生产的MTBC核酸检测试剂盒,按照操作说明书进行操作和结果判读。即以出峰时间和荧光扩增曲线显示结果。出现扩增曲线为阳性(含有 MTBC),无扩增曲线为阴性。
五、相关指标计算
敏感度=真阳性例数/(真阳性例数+假阴性例数)×100%;特异度=真阴性例数/(真阴性例数+假阳性例数)×100%;阳性预测值=真阳性例数/(真阳性例数+假阳性例数)×100%;阴性预测值=真阴性例数/(真阴性例数+假阴性例数)×100%;一致率=(真阳性例数+真阴性例数)/患者总例数×100%。
六、质量控制
为保证多中心评估质量,项目启动前上海市疾病预防控制中心对6家结核病定点医院技术人员开展了项目培训,明确病例纳入及排除标准、痰标本收集及检测要求,并对恒温扩增荧光检测法开展技术培训;项目开展期间,上海市疾病预防控制中心结核病参比实验室定期对6家结核病定点医院实验室开展质控与督导。痰涂片质量控制包括室内质控(内容包括采用标准操作规程、设备耗材、痰标本收集、涂片制备、染色、镜检、痰涂片保存等过程的内部检查和监测)和室间质控(参加上海市疾病预防控制中心结核病参比实验室组织的盲法复检及上海市临床检验中心组织的痰涂片抗酸染色室间比对),成绩均达标。培养的质量控制包括对使用的培养管及相关试剂盒质控、实验物品(标本瓶、稀释管、接种物品等)质控和污染控制等。6家结核病定点医院参加由国家结核病参比实验室组织的分子能力验证室间比对,GeneXpert和恒温扩增荧光检测法成绩均合格。
七、统计学处理
采用SPSS 17.0软件进行统计学分析。4种不同检测方法检出率的比较采用配对χ2检验,检验水准α=0.05;以液体培养为参照标准,计算恒温扩增荧光检测法、痰涂片、GeneXpert检测的敏感度、特异度、阳性预测值、阴性预测值和95%CI值;一致性分析采用Kappa检验,Kappa值≥0.75说明一致性好,Kappa值<0.40说明一致性较差,0.40≤Kappa值<0.75说明一致性一般。
结 果
一、恒温扩增荧光检测法与痰涂片、液体培养和GeneXpert的检出率结果比较
在1848例患者痰样本中,恒温扩增荧光检测法、痰涂片、液体培养和GeneXpert检测MTBC的检出率分别为16.7%(309/1848)、14.4%(266/1848)、25.4%(470/1848)和28.7%(530/1848)。恒温扩增荧光检测法检出率(16.7%)低于液体培养(25.4%),差异有统计学意义(χ2=42.16,P=0.001),也低于GeneXpert检测结果(28.7%),差异有统计学意义(χ2=75.31,P=0.001)。
二、恒温扩增荧光检测法与痰涂片、GeneXpert检测效能分析
以液体培养为参照标准,恒温扩增荧光检测法、痰涂片和GeneXpert检测的敏感度分别为58.94%(95%CI:54.33%~63.40%)、52.77%(95%CI: 48.14%~57.34%)、80.43%(95%CI: 76.49%~83.86%);特异度分别为97.68%(95%CI:96.70%~98.38%)、98.69%(95%CI:97.90%~99.20%)、88.97%(95%CI:87.17%~90.55%)。见表1。以液体培养为参照标准,恒温扩增荧光检测法、痰涂片和GeneXpert检测的一致率分别为87.82%(1623/1848)、87.01%(1608/1848)、86.80%(1604/1848),Kappa值分别为0.638、0.600、0.666,说明3种检测方法与液体培养检测结果一致性均一般。
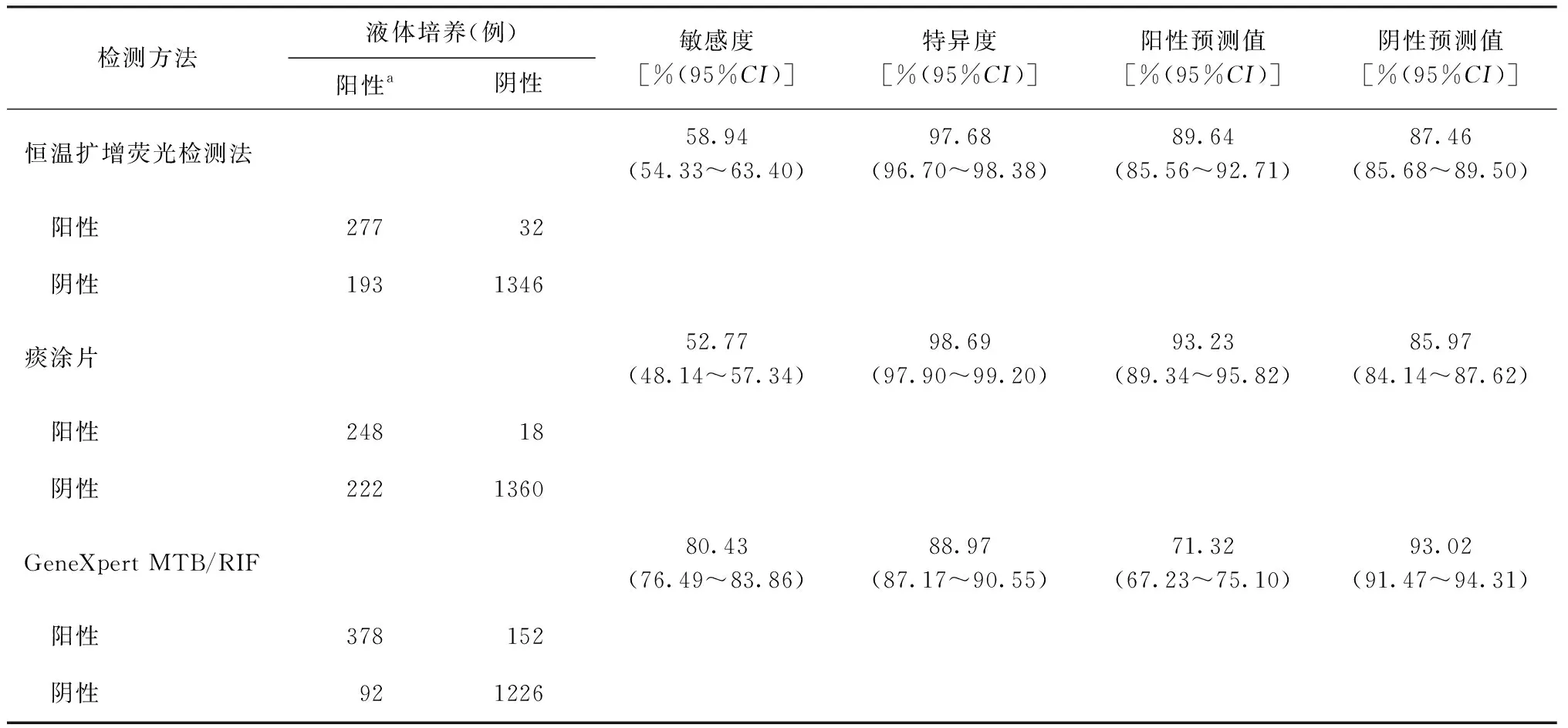
表1 以液体培养为参照标准恒温扩增荧光检测法、痰涂片和GeneXpert MTB/RIF检测效能分析
三、恒温扩增荧光检测法与痰涂片、液体培养和GeneXpert检测不同性状痰样本的结果分析
本研究对收集到的817例临床诊断肺结核患者的不同性状痰样本(黏液样痰、唾液样痰、干酪样痰和血样痰)进行4种方法检测结果比较。结果显示,采用同一种检测方法检测4种不同性状痰样本,干酪样痰的检出率均明显高于唾液样痰,除液体培养(χ2=1.700,P=0.193)差异无统计学意义,其他3种检测方法(恒温扩增荧光检测法、痰涂片和GeneXpert)差异均有统计学意义(χ2=8.140,P=0.004;χ2=5.840,P=0.016;χ2=14.950,P=0.001)。在4种不同性状痰样本中,除在唾液样痰中液体培养检出率最高[38.8%(59/152)]外,其余3种性状痰样本(黏液样痰、干酪样痰和血样痰)均为GeneXpert检出率最高,分别为51.5%(308/598)、66.7%(28/42)和64.0%(16/25)。见表2。
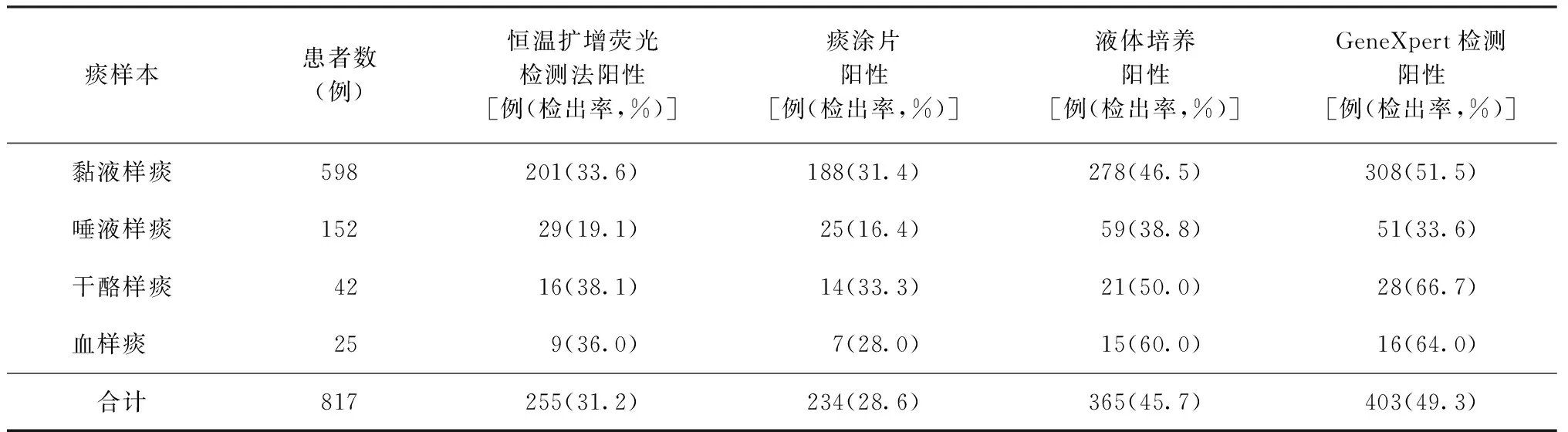
表2 对817例临床诊断肺结核患者的不同性状痰样本进行4种方法检测的结果
四、恒温扩增荧光检测法和GeneXpert检测结果与痰涂片分级的比较
根据痰涂片级别,可分为6个级别(阴性~4+)。817例临床诊断肺结核患者中,有583例(71.4%)涂阴患者。在涂阴样本中,恒温扩增荧光检测法的检出率为10.3%(60/583),低于GeneXpert检测的31.9%(186/583),差异有统计学意义(χ2=81.790,P=0.001)。各检测方法的检出率随着涂片阳性级别增高而升高;低级别阳性(条数~1+)的样本中,恒温扩增荧光检测法检出率为75.5%(105/139),GeneXpert检出率为92.1%(128/139),差异有统计学意义(χ2=14.030,P=0.001);中高级别(2+~4+)样本中的二种检测方法检出率均较高,分别为94.7%(90/95)和93.7%(89/95),差异无统计学意义(χ2=0.100,P=0.756)。在420例临床诊断肺结核患者的涂阴培阴患者中,恒温扩增荧光检测法检出率为4.5%(19/420),低于GeneXpert检出率[19.8%(83/420)],差异有统计学意义(χ2=45.710,P=0.001)。见表3。
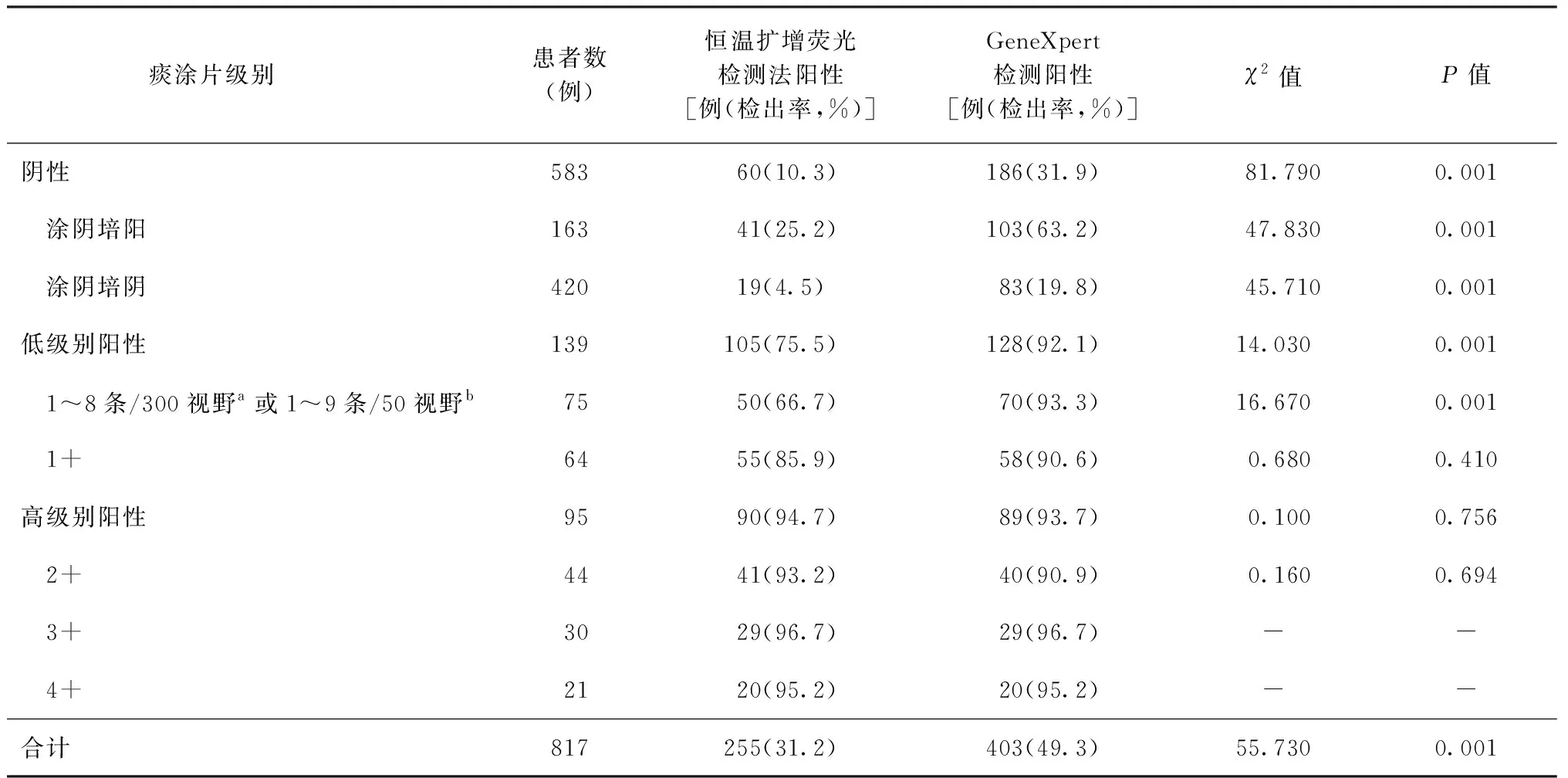
表3 817例临床诊断肺结核患者的痰涂片分级与恒温扩增荧光检测法、GeneXpert检测结果的比较
讨 论
近年来,结核病新诊断技术的研发取得了显著的进展[7]。WHO推荐了包括多色半巢式荧光定量 PCR、微流体芯片技术、环介导等温扩增法等若干新型结核病诊断新技术[8]。恒温扩增荧光检测法是一种将恒温扩增与实时荧光技术相结合的新型核酸恒温扩增技术,是“十二五”期间我国自主研发的结核病分子生物学快速诊断技术,前期已有应用该技术对结核病患者的临床样本进行快速诊断和评估的报道[9]。本研究是“十三五”期间我中心承担的该技术多中心评估项目,研究结果显示,以液体培养为参照标准,恒温扩增荧光检测法的敏感度(58.94%)高于痰涂片(52.77%),但低于GeneXpert检测(80.43%),恒温扩增荧光检测法的特异度(97.68%)与痰涂片(98.69%)相当,高于GeneXpert检测(88.97%);一致性检验结果显示,恒温扩增荧光检测法、痰涂片和GeneXpert与液体培养检测结果一致性均一般。
马晓光等[9]研究结果显示,恒温扩增荧光法检出率为17.14%,高于痰涂片(8.12%)和培养法(13.47%);杨健等[10]报道环介导等温核酸扩增技术阳性检出率(51.55%)明显高于痰涂片镜检法(31.40%)和固体培养法(39.92%)。本研究中应用恒温扩增荧光检测法检测MTBC的检出率为16.7%,相比痰涂片(14.4%)检出率略有提高,但低于液体培养检出率(25.4%),此结果与国内报道有所不同[9-11],原因可能为国内多采用固体培养法或与各实验室检测差异有关,液体培养法检测敏感度高于固体培养,尤其是在含菌量较低的涂阴患者中[12]。检测时间方面,液体培养报阳时间虽短于固体培养,但还需平均11 d左右[12],而恒温扩增荧光检测法检测时间仅需要1.5 h左右,大大缩短了临床诊断肺结核的时间;且相比传统检测方法还需进一步做菌种鉴定试验。恒温扩增荧光检测法是以MTBC种特异基因IS6110特异性区域作为检测靶标,结果阳性即为检出MTBC。李金莉等[13]报道采用该方法对NTM标准株和其他临床常见标准株检测无交叉反应,且其检测特异度高达100%。本研究中恒温扩增荧光检测法检测MTBC 的特异度(97.68%)略低,但与国内其他研究结果(93.64%~98.02%)一致[9-11],显示了其良好的检测特异度。恒温扩增荧光检测法与液体培养结果比较,一致率为87.82%,与痰涂片(87.01%)和GeneXpert(86.80%)检测一致率相当。
本研究中对817例临床诊断肺结核患者的不同性状痰样本的检出率进行比较,结果发现唾液样痰的检出率明显低于其他3种性状痰。近些年,随着肺结核知识公众知晓率的提高,以及居民健康体检的普及,新诊断肺结核患者中因典型的结核病临床表现就诊的患者比例较前减少,多数就诊的疑似肺结核患者尚处于病程早期,患者痰量少或送检唾液样痰。唾液样痰不是从肺深部咳出,含病原菌量较少而直接影响检测MTBC效能,这提示医务人员应积极向患者进行留痰宣教,讲解留痰的重要性,指导患者如何留取肺部深处咳痰,也可采用雾化诱导留痰[14]等人工干预方式获得质量较好的痰样,从而提高痰标本中MTBC检出率。有研究表明,血液中含有血红蛋白、免疫球蛋白、乳铁蛋白等成分会抑制PCR反应而可能造成分子诊断方法检测MTBC检出率降低[15]。本研究中,恒温扩增荧光检测法检测血样痰的检出率(36.0%)明显低于液体培养(60.0%)和GeneXpert(64.0%),血样痰对恒温扩增荧光检测法的检出率影响大于GeneXpert。本研究中血样痰样本量较少,无法证明是否是因两种分子检测方法采用的前处理方式或扩增方法不同所导致,可在今后工作中做进一步探讨。对恒温扩增荧光检测法和GeneXpert检测MTBC结果与痰涂片分级比较,发现2种检测方法在中高级别涂阳患者中均具有良好的敏感度,但在涂阴培阴患者中,恒温扩增荧光检测法的检出率仅4.5%,低于国内报道恒温扩增荧光检测法对涂阴培阴患者10%~20%的检出率的结果[10,13],这可能与采用液体培养提高了培养阳性率,从而减少了涂阴培阴患者比例有关,同时也表明恒温扩增荧光检测法还需进一步优化反应体系,以提高对涂阴患者及低级别涂阳患者的检出率。
恒温扩增荧光检测法是2012年前完成了试剂盒研发、成果临床转化和临床验证评估[16],该方法最初是由人工肉眼观察进行结果判读,经技术革新,现在恒温扩增荧光检测法应用荧光检测仪自动判读,实现了MTBC的快速核酸扩增和自动化结果报告,显示了该方法自动化程度的提高。本研究分别在6个研究现场开展工作,采用荧光检测仪自动判读,避免了在不同实验室环境、操作人员的技术水平和熟练度等差异而导致人工主观判读的误差,提高了检测结果的准确性和稳定性。本研究结果显示,恒温扩增荧光检测法检测MTBC效能相比痰涂片有所提高,但该方法的检测敏感度低于GeneXpert。有研究显示,采用这两种分子诊断技术检测MTBC均能提高病原学阳性率[17]。虽然恒温扩增荧光法的检测敏感度低于GeneXpert,但是,首先该方法使用的是我国自主研发的国产试剂盒,价格相较美国生产的GeneXpert试剂盒低很多,近两年GeneXpert试剂价格呈现逐年上涨趋势,也增加了政府公共卫生预算;其次,国产试剂亦不会出现因运输或者试剂报关等造成到货时间延迟而导致试剂有效期短或可能出现试剂失效等情况;第三,恒温扩增荧光检测法所使用的仪器设备均整合在一个拉杆箱中,如发生突发公共卫生事件可携带至现场开展应急检测。
恒温扩增荧光检测法操作简单、快速,相比传统PCR方法没有较复杂和严格的技术要求,但该方法仍属于分子生物学检测技术。有研究表明,该方法的实验室交叉污染较低,但仍须在四分区的标准PCR实验室进行操作[18]。随着《结核病分级诊疗和综合防治服务模式试点工作》及《遏制结核病行动计划(2019—2022年)》任务推进,我国正在大力加强对各地基层实验室能力的建设,期望结核病分子快速诊断技术能得到更广泛的应用。
综上所述,恒温扩增荧光检测法检测痰样本中MTBC具有良好的检测特异度,该方法和痰涂片及GeneXpert与液体培养检测结果一致性均一般,临床可以根据实验室硬件条件及患者情况选择开展多种方法联合检测,以提高肺结核的病原学诊断率。
本研究的不足之处:(1)本研究以液体培养为参照标准进行多种检测方法的效能分析,而其他研究大都以临床诊断为标准,因此,可能低估了恒温扩增荧光法检测MTBC的效能。(2)本研究未将免疫学检查纳入评价。近年来γ-干扰素释放试验(interferon-gamma release assay,IGRA)已逐渐成为诊断结核病的重要辅助手段,尤其对菌阴肺结核的诊断[18]。《WS 288—2017肺结核诊断》[3]也将IGRA增加到免疫学检查中,作为鉴别诊断肺结核的辅助检查之一。如进一步对病原学诊断方法联合免疫学检查进行研究,可更科学精准地评价多种检测技术联合诊断对于结核病从感染到发病的不同阶段,特别是病原学阴性肺结核、亚临床感染及结核分枝杆菌潜伏感染的检测效能。
利益冲突所有作者均声明不存在利益冲突
作者贡献李静:实验设计、实施研究、采集数据、分析/解释数据、统计分析、起草文章及审阅;吴哲渊:实验设计、实施研究、获取研究经费和行政支持;杨景卉和杨丽媛:实施研究、采集数据、分析/解释数据;王莉莉:实验设计、实施研究;袁锋:实施研究、采集数据;沈鑫:获取研究经费、行政支持和审阅;江渊:实验设计、实施研究、行政支持和技术指导及审阅

