膀胱癌患者灌注治疗过程中尿路感染危险因素分析及预测模型构建
符海能,梁培育,王声兴,符津山
(海南医学院第一附属医院泌尿外科,海南海口 570102)
膀胱癌是常见泌尿系统恶性肿瘤,常有血尿、排尿困难、膀胱刺激征等临床症状[1-2]。近年来其发病率越来越高,严重影响患者的身心健康和生活质量[3-4]。目前治疗膀胱癌的主要手段是经尿道膀胱肿瘤切除术,但治疗后容易复发,所以临床常以灌注化疗为辅助,以期降低肿瘤复发率、改善预后[5-7]。但长期灌注治疗易引起尿路感染,影响治疗进程且给患者带来痛苦[8]。研究表明,尿路感染可能与侵入性治疗、年龄、基础疾病等多种因素密切相关[9]。如能认识到影响膀胱癌患者灌注治疗过程中发生尿路感染的危险因素并及早采取干预措施从而预防和控制尿路感染的发生,则可改善患者预后。迄今为止关于膀胱癌患者进行灌注治疗过程中发生尿路感染的独立危险因素尚不明确,且缺少临床数据佐证;此外,由于缺乏有效的统计学方法,使得这些危险因素难以在临床准确、有效运用。
Nomogram模型(列线图模型)是医学中常用的评估预后的工具,通过整合不同预后相关变量,能够生成临床事件的单个数值概率,满足对生物和临床整合模型需求,推动个性化医疗,协助临床决策[10]。本研究试图确定膀胱癌患者灌注治疗过程中尿路感染发生的危险因素,旨在开发一个可以准确预测膀胱癌灌注治疗后尿路感染发生的Nomogram模型。
1 资料与方法
1.1 临床资料收集2020年2-12月于海南医学院第一附属医院接受经尿道膀胱肿瘤切除术联合术后辅助膀胱灌注化疗的160例膀胱癌患者的临床资料。所有患者资料被纳入研究之前均知情同意,且本研究经医院伦理委员会批准。纳入标准:①经尿液脱落细胞检查找到癌细胞或膀胱镜下肉眼所见或病理证实为膀胱肿瘤;②符合《膀胱癌患者诊疗指南》中膀胱癌的诊断标准[11];③具有灌注化疗的治疗指征[12];④预计生存时间超过半年;⑤灌注治疗前未有复发或感染情况。排除标准:①合并其他恶性肿瘤; ②患有其他脏器疾病;③合并有机体免疫系统疾病;④患者存在严重精神功能障碍,无法正常与别人进行语言沟通者;⑤患者肝肾功能有明显异常;⑥患有凝血障碍;⑦服用抗菌、抗感染药物。
1.2 数据收集性别、年龄、体质指数(body mass index,BMI)、病程、基础疾病(高血压、糖尿病、心血管疾病)、白蛋白水平、灌注治疗次数、是否留置导尿管、导尿管留置时间、肿瘤位点、手术时间、前列腺增生。
1.3 尿路感染定义及诊断尿路感染(urinary tract infection,UTI)指病原菌侵犯尿路任何部位引起的炎症,病原体在尿路中生长繁殖,并侵犯泌尿道黏膜或组织而引起的炎症,是细菌感染中最常见的一种感染,尿路感染分为上尿路感染和下尿路感染,按其感染部位有上尿路感染的肾盂肾炎和输尿管炎及下尿路感染的膀胱炎和尿道炎。诊断标准:参照《尿路感染诊断与治疗中国专家共识(2015版)——复杂性尿路感染》[13]评价:①出现尿路感染症状;②尿液培养检测出有病原菌;③尿液中白细胞>10个/HP。①、②、③项均符合者,即可诊断为尿路感染。
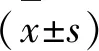
2 结 果
2.1 尿路感染组与无尿路感染组临床资料比较尿路感染组患者年龄、糖尿病比例、灌注治疗次数、留置导尿管比例、导尿管留置时间、多个肿瘤位点比例、手术时间均大于无尿路感染组(P<0.05);尿路感染组患者白蛋白水平低于无尿路感染组(P<0.05,表1)。
2.2 相关变量ROC曲线分析将表1有统计学差异的连续性变量进行ROC曲线分析。结果显示:年龄、白蛋白水平、灌注治疗次数、导尿管留置时间、手术时间的AUC分别为0.878、0.873、0.802、0.864、0.836;最佳截断值分别为66.57岁、37.60 g/L、7.26 次、8.31 d、95.87 min(表2、图1)。
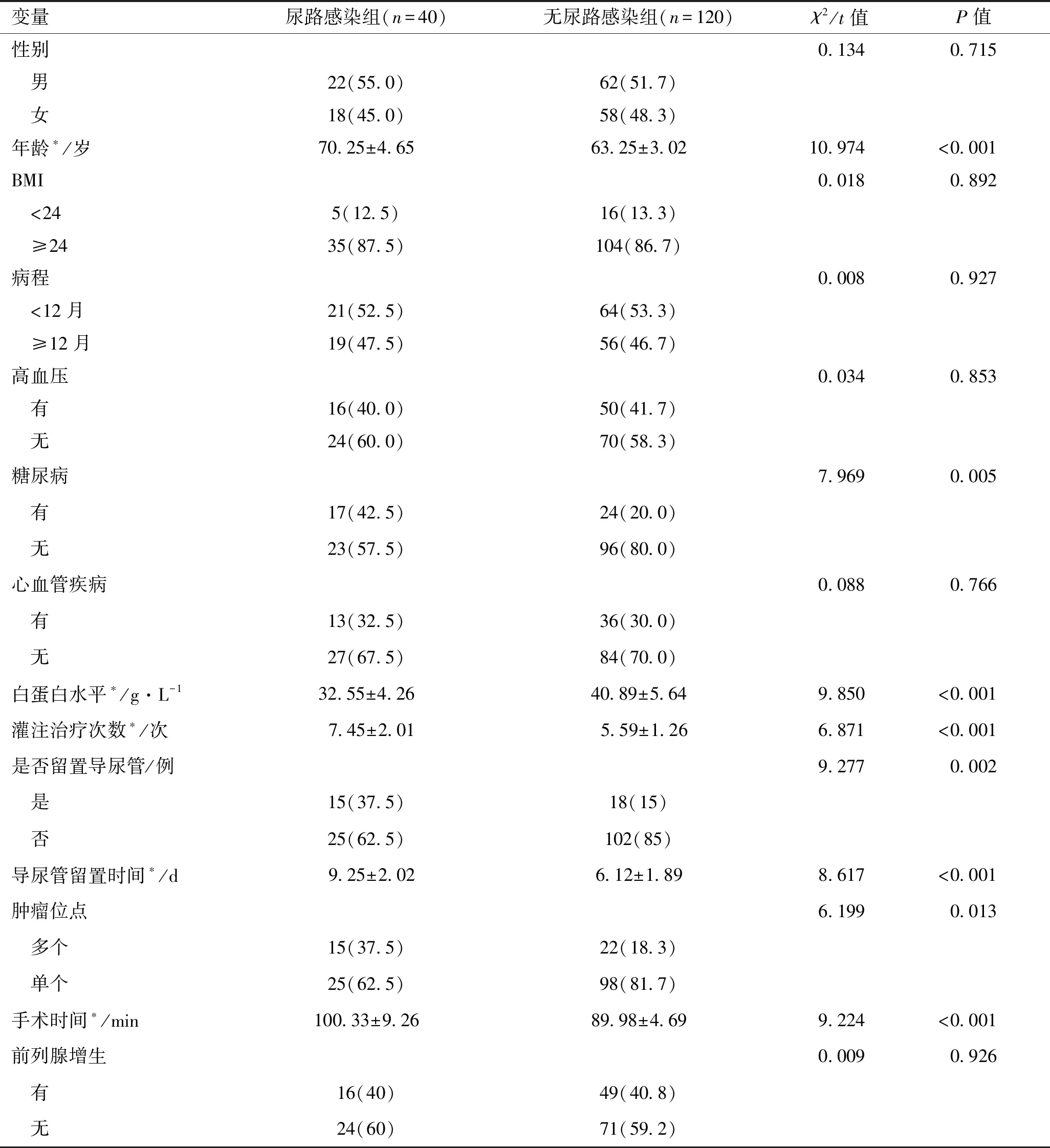
表1 尿路感染组与无尿路感染组临床资料比较 [例(%)]
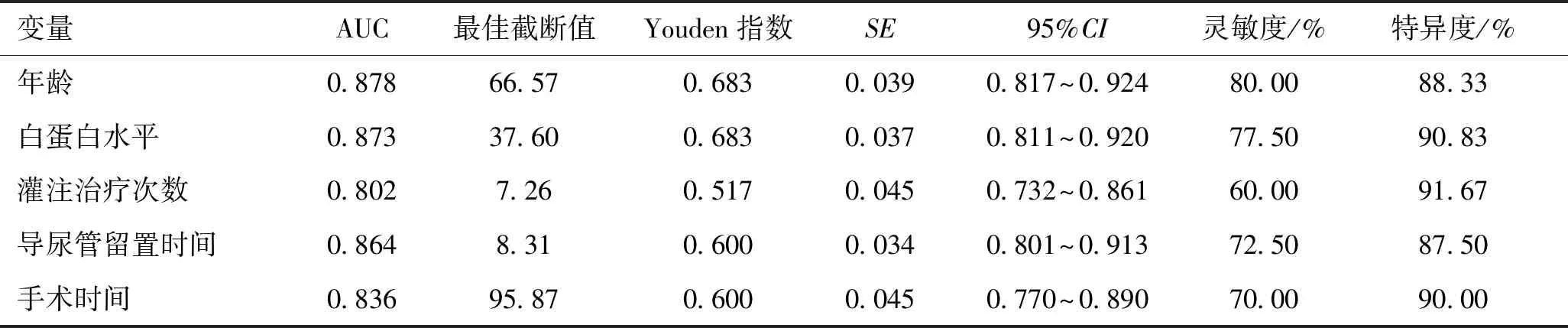
表2 相关变量ROC曲线分析结果
2.3 logistic多元回归分析将单因素分析有差异的指标纳入logistic多元回归模型中,其结果显示:有糖尿病、白蛋白水平(≤37.60 g/L)、灌注治疗次数(>7.26次)、留置导尿管、多个肿瘤位点是膀胱癌患者灌注治疗过程中尿路感染发生的独立危险因素(P<0.05,表3)。
2.4 预测膀胱癌患者灌注治疗过程中尿路感染发生的Nomogram模型将糖尿病、白蛋白水平、灌注治疗次数、留置导尿管、肿瘤位点作为预测因子构建Nomogram模型(图2)。
表3 膀胱癌患者灌注治疗过程中尿路感染发生的logistic多元回归分析
2.5 Nomogram模型校正曲线及临床净收益分析内部验证结果显示,Nomogram模型预测膀胱癌患者灌注治疗过程中尿路感染发生风险C-index 为0.723(95%CI:0.686~0.770)。校准曲线显示观测值与预测值之间保持较好一致性(图3A)。Nomogram模型预测膀胱癌患者灌注治疗过程中尿路感染发生风险阈值>0.10,Nomogram模型提供临床净收益;此外,Nomogram模型临床净收益均高于糖尿病、白蛋白水平、灌注治疗次数、留置导尿管、肿瘤位点(图3B)。
3 讨 论
膀胱癌术后灌注治疗是通过尿道进行的逆行有创治疗,和手术二者对尿道黏膜造成双重伤害,使免疫屏障功能受损,病原菌随之入侵,造成尿路感染;另外,灌注治疗所用的化疗药物虽然对疾病有治疗作用,但同时也可损伤人体免疫系统,导致机体对病原菌的抵抗力降低,因而不同程度地增加了患者并发尿路感染的风险[14-15]。研究膀胱癌患者灌注治疗过程中尿路感染发生的相关危险因素有助于规避风险、减少临床尿路感染的发生率。本研究经logistic回归分析表明,糖尿病、白蛋白水平(≤37.60 g/L)、灌注治疗次数(>7.26次)、留置导尿管、多个肿瘤位点是膀胱癌患者灌注治疗过程中尿路感染发生的独立危险因素。
Nomogram(诺莫图)列线图可以整合logistic回归分析筛选出的相关变量,用于构建预测模型,以便提供临床决策[16]。另外,Nomogram模型可以通过简单、可视化的图形代替logistic复杂的回归方程,也充分考虑每个预后因素对预后的影响,每个因素都有不同的评分,具有很好的可读性,而且使用价值较高,具有较大的临床应用价值。但目前尚鲜见膀胱癌患者灌注治疗过程中尿路感染发生风险的Nomogram预测模型,本研究整合logistic回归分析筛选的风险因素,构建出可以预测膀胱癌患者灌注治疗过程中尿路感染发生风险的Nomogram模型,并根据Nomogram模型预测结果密切关注灌注治疗患者的情况,加强干预,以减少灌注治疗过程中尿路感染发生的风险,改善预后。
探讨本研究发现的几个危险因素分析如下:①糖尿病是膀胱癌灌注治疗患者尿路感染的风险因素,合并糖尿病患者机体血糖水平不稳定,致免疫功能紊乱,且可能存在排尿功能障碍,对病原菌的抵御功能下降。这一结论在孙根喜[17]的研究中也有提到。②膀胱癌患者白蛋白水平与灌注治疗过程中尿路感染的发生密切相关。这可能是由于白蛋白的水平与机体内抗体补体含量呈正比,当白蛋白水平较低时,抗体补体含量也会相应降低,导致免疫能力下降,容易并发尿路感染[18]。③灌注治疗次数是膀胱癌灌注治疗患者尿路感染的风险因素,与刘辉等[19]研究结论一致。究其原因,可能是因为灌注治疗通过尿道进行,治疗次数越多,对尿道黏膜的侵入性损伤越严重。④留置导尿管是膀胱癌患者灌注治疗过程中尿路感染的一大风险因素,并且留置导尿管时间越长,越容易引起尿路感染。因为导尿管为体外异物,相当于细菌入侵通道,细菌附着在导尿管上,形成细菌生物膜,不易被抗生素清除,往往需拔出导尿管才能治疗彻底。⑤肿瘤位点是膀胱肿瘤患者灌注化疗后并发尿路感染的风险因素,这与简毓等[20]研究结果一致。这可能是因为治疗多个肿瘤位点的过程中,膀胱受到医疗器械及药物的损伤面积较大,因此感染的几率也随之增加。
本研究基于糖尿病、白蛋白水平、灌注治疗次数、留置导尿管、肿瘤位点构建了预测膀胱癌患者灌注治疗过程中尿路感染发生风险的Nomogram模型,该模型可用于对临床膀胱癌患者灌注治疗过程中尿路感染发生进行预测,有助于发现膀胱癌患者灌注治疗过程中尿路感染发生的高风险患者,以便尽早干预。
本研究局限性在于纳入患者样本量虽然不小,然而Nomogram模型未进行外部数据集验证;此外,膀胱癌患者灌注治疗过程中尿路感染发生的潜在影响因素较多,该Nomogram模型可能错过其他重要的危险变量;再者,因为这是一项单中心研究,该模型推广还需要进一步验证。

